题型:解答题-工业流程题
难度:0.4
引用次数:177
题号:18380160
锶(Sr)是第五周期IIA族元素。自然界中的锶存在于天青石中,天青石的主要成分为SrSO4和少量CaSO4、BaSO4。以天青石为原料制备高纯SrCO3需要两个步骤。
[步骤一]从天青石到粗SrCO3:
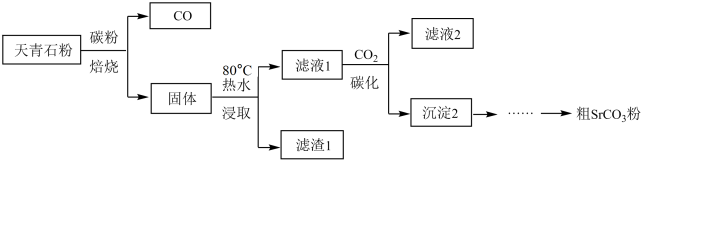
已知:i. Ca、Sr、Ba硫化物( MS)和硫氢化物[ M( HS)2]均易溶于水,
ii.20℃时,Sr(OH)2、Ba(OH)2、Ca(OH)2的溶解度(单位为g)分别为1.77、3. 89、0.173;80℃时,Sr(OH)2、 Ba(OH)2、Ca(OH)2的溶解度(单位为g)分别为20. 2、101.4、0.094。
(1)焙烧过程中SrSO4转化为SrS的化学方程式是___________ 。
(2)浸取时发生反应:2MS+2H2O M( HS)2+M(OH)2(M=Ca、Sr、Ba)。使用热水有利于提高平衡转化率,原因是
M( HS)2+M(OH)2(M=Ca、Sr、Ba)。使用热水有利于提高平衡转化率,原因是___________ 。
(3)滤渣1的主要成分是___________ (写化学式)。
[步骤二]粗SrCO3转化为高纯SrCO3:
(4)粗SrCO3中的杂质是BaCO3.有同学提出在实验室可以将粗SrCO3产物溶于酸,再加入Na2SO4溶液实现Sr和Ba的分离。设Ba2+完全沉淀时c(Ba2+)= 10-5mol·L-1,则溶液中c(Sr2+)一定不大于___________ 。该方案___________ (填“合理”或者“不合理”)。[Ksp( BaSO4)= 1.1×10-10,Ksp(SrSO4)= 3.3×10-7]
(5)实际的工业除杂和转化流程如下图所示:

已知:i.溶液中存在 +H2O
+H2O 2
2 +2H+,
+2H+, 具有强氧化性。
具有强氧化性。
ii. Cr( OH)3的性质类似Al( OH)3,Ksp[ Cr(OH)3]=1×10-31。
①若酸溶过程中H+过量太多,则除钡过程中Ba2+去除率会下降,请从化学平衡移动角度解释原因___________ 。
②还原过程中草酸(H2C2O4)发生反应的离子方程式为___________ 。
③为除铬,向溶液D中加入NH3·H2O调节pH为7~8。此过程不调节pH为13的原因是___________ 。
[步骤一]从天青石到粗SrCO3:

已知:i. Ca、Sr、Ba硫化物( MS)和硫氢化物[ M( HS)2]均易溶于水,
ii.20℃时,Sr(OH)2、Ba(OH)2、Ca(OH)2的溶解度(单位为g)分别为1.77、3. 89、0.173;80℃时,Sr(OH)2、 Ba(OH)2、Ca(OH)2的溶解度(单位为g)分别为20. 2、101.4、0.094。
(1)焙烧过程中SrSO4转化为SrS的化学方程式是
(2)浸取时发生反应:2MS+2H2O
 M( HS)2+M(OH)2(M=Ca、Sr、Ba)。使用热水有利于提高平衡转化率,原因是
M( HS)2+M(OH)2(M=Ca、Sr、Ba)。使用热水有利于提高平衡转化率,原因是(3)滤渣1的主要成分是
[步骤二]粗SrCO3转化为高纯SrCO3:
(4)粗SrCO3中的杂质是BaCO3.有同学提出在实验室可以将粗SrCO3产物溶于酸,再加入Na2SO4溶液实现Sr和Ba的分离。设Ba2+完全沉淀时c(Ba2+)= 10-5mol·L-1,则溶液中c(Sr2+)一定不大于
(5)实际的工业除杂和转化流程如下图所示:

已知:i.溶液中存在
 +H2O
+H2O 2
2 +2H+,
+2H+, 具有强氧化性。
具有强氧化性。 ii. Cr( OH)3的性质类似Al( OH)3,Ksp[ Cr(OH)3]=1×10-31。
①若酸溶过程中H+过量太多,则除钡过程中Ba2+去除率会下降,请从化学平衡移动角度解释原因
②还原过程中草酸(H2C2O4)发生反应的离子方程式为
③为除铬,向溶液D中加入NH3·H2O调节pH为7~8。此过程不调节pH为13的原因是
更新时间:2023-03-13 14:35:38
|
相似题推荐
【推荐1】我国提出2060年达“碳中和”目标,通过反应 将
将 转化为高附加值产品
转化为高附加值产品 是实现该目标的一种方式。回答下列问题:
是实现该目标的一种方式。回答下列问题:
体系中涉及两个反应:
I.主反应: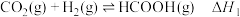
Ⅱ.副反应:
(1)测定不同温度下反应Ⅰ的平衡常数(K>0)如下表所示:
①
___________ 0(填“>”“<”或“=”)。
②已知: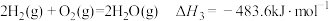 ,则
,则 的燃烧热
的燃烧热
___________ 。
③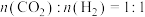 充入恒容密闭容器中反应,下列有利于提高
充入恒容密闭容器中反应,下列有利于提高 产率的措施有
产率的措施有___________ (填序号)。
A.升高反应温度 B.及时移出
C.选择 选择性高的催化剂 D.充入氮气
选择性高的催化剂 D.充入氮气
④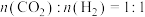 充入恒容恒温密闭容器中反应,起始压强为
充入恒容恒温密闭容器中反应,起始压强为 ,平衡时压强为
,平衡时压强为 ,
, 与
与 的浓度相等,
的浓度相等, 的转化率
的转化率
___________ (用含 和
和 的代数式表示),用各物质的平衡分压表示反应Ⅰ的平衡常数计算式
的代数式表示),用各物质的平衡分压表示反应Ⅰ的平衡常数计算式
___________  (用含
(用含 和
和 的代数式表示)。
的代数式表示)。
(2)中国科学院大学以 为电极材料,利用电化学催化还原
为电极材料,利用电化学催化还原 制备
制备 。用计算机模拟
。用计算机模拟 在电极材料表面发生还原反应的历程如图(*表示微粒与
在电极材料表面发生还原反应的历程如图(*表示微粒与 的接触位点):
的接触位点):
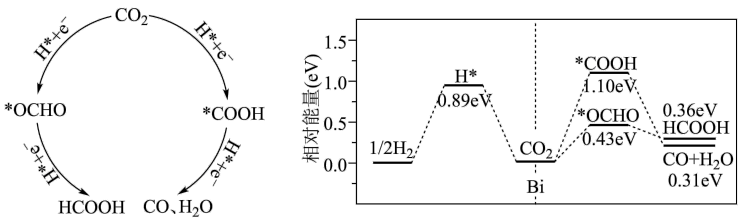
HCOOH是___________ (填“氧化”或“还原”)产物。依据反应历程图中数据,你认为电催化还原CO2生成HCOOH的选择性___________ (填“高于”或“低于”)生成CO的选择性,原因是___________ 。
 将
将 转化为高附加值产品
转化为高附加值产品 是实现该目标的一种方式。回答下列问题:
是实现该目标的一种方式。回答下列问题:体系中涉及两个反应:
I.主反应:
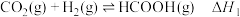
Ⅱ.副反应:

(1)测定不同温度下反应Ⅰ的平衡常数(K>0)如下表所示:
| T/K | 373 | 473 | 573 | 673 |
| 平衡常数 | 37.5K | 24.3K | 8.4K | K |

②已知:
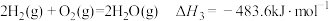 ,则
,则 的燃烧热
的燃烧热
③
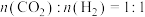 充入恒容密闭容器中反应,下列有利于提高
充入恒容密闭容器中反应,下列有利于提高 产率的措施有
产率的措施有A.升高反应温度 B.及时移出

C.选择
 选择性高的催化剂 D.充入氮气
选择性高的催化剂 D.充入氮气④
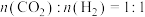 充入恒容恒温密闭容器中反应,起始压强为
充入恒容恒温密闭容器中反应,起始压强为 ,平衡时压强为
,平衡时压强为 ,
, 与
与 的浓度相等,
的浓度相等, 的转化率
的转化率
 和
和 的代数式表示),用各物质的平衡分压表示反应Ⅰ的平衡常数计算式
的代数式表示),用各物质的平衡分压表示反应Ⅰ的平衡常数计算式
 (用含
(用含 和
和 的代数式表示)。
的代数式表示)。(2)中国科学院大学以
 为电极材料,利用电化学催化还原
为电极材料,利用电化学催化还原 制备
制备 。用计算机模拟
。用计算机模拟 在电极材料表面发生还原反应的历程如图(*表示微粒与
在电极材料表面发生还原反应的历程如图(*表示微粒与 的接触位点):
的接触位点):
HCOOH是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】如图所示,根据实验室制取氯气的原理制备氯气并进行性质验证,回答下列问题:

(1)装置A的名称为___________ 。
(2)利用装置丙制取饱和氯水并测其pH。
①证明氯水已饱和的现象是___________ 。
②若撤去装置乙,直接将装置甲和丙相连,这样做对实验测定结果的影响是___________ 。
(3)在装有20mL饱和氯水试管中加入过量的块状碳酸钙,过滤,将滤液滴在有色布条上,发现其褪色速度比用饱和氯水更快(已知酸性:HCl>H2CO3>HClO),产生这一现象的原因是___________ 。
(4)制备HClO溶液,可将氯气和空气(空气中所有成分不参与反应)按体积比1:3混合后通入含水8%的Na2CO3悬浊液中制备Cl2O,并用水吸收Cl2O制备HClO溶液,实验过程如图所示(夹持装置未画出)。
已知:①Cl2O极易溶于水并与水反应生成HClO;
②Cl2O的沸点为3.8℃,42℃以上分解为Cl2和O2。
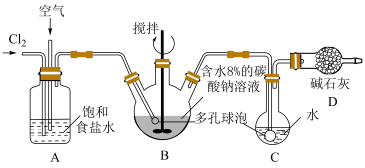
①A瓶中通入的是纯净的Cl2,写出装置A的两个作用___________ 。
②装置B中每生成1molCl2O转移的电子为___________ mol。
③有同学提出B装置外围最好加一个水浴加热装置,控制温度范围在_______ 之间,则效果会更好。
④装置C中发生的化学反应方程式为___________ 。

(1)装置A的名称为
(2)利用装置丙制取饱和氯水并测其pH。
①证明氯水已饱和的现象是
②若撤去装置乙,直接将装置甲和丙相连,这样做对实验测定结果的影响是
(3)在装有20mL饱和氯水试管中加入过量的块状碳酸钙,过滤,将滤液滴在有色布条上,发现其褪色速度比用饱和氯水更快(已知酸性:HCl>H2CO3>HClO),产生这一现象的原因是
(4)制备HClO溶液,可将氯气和空气(空气中所有成分不参与反应)按体积比1:3混合后通入含水8%的Na2CO3悬浊液中制备Cl2O,并用水吸收Cl2O制备HClO溶液,实验过程如图所示(夹持装置未画出)。
已知:①Cl2O极易溶于水并与水反应生成HClO;
②Cl2O的沸点为3.8℃,42℃以上分解为Cl2和O2。

①A瓶中通入的是纯净的Cl2,写出装置A的两个作用
②装置B中每生成1molCl2O转移的电子为
③有同学提出B装置外围最好加一个水浴加热装置,控制温度范围在
④装置C中发生的化学反应方程式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】CO2的资源化利用能有效减少CO2排放,对碳循环经济技术的发展具有重要意义。
I.利用CO2和CH4制备合成气(CO、H2),反应分两步进行:[其中C(ads)为吸附性活性炭]
反应① CH4(g) C(ads)+2H2(g)
C(ads)+2H2(g)  >0
>0
反应② C(ads)+CO2(g) 2CO(g)
2CO(g)  >0
>0
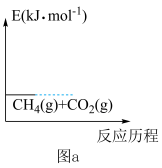
(1)研究表明,总反应速率由反应①决定,在图a上画出有关物质的相对能量与反应历程的变化(起始已给出)___________ :
(2)判断总反应CH4(g)+CO2(g) 2CO(g)+2H2(g)自发进行的条件并说明理由
2CO(g)+2H2(g)自发进行的条件并说明理由___________ 。
II.工业上可利用CO2生产燃料甲醇。该过程发生下列反应:
反应③ CO2(g)+3H2(g) CH3OH(g)+H2O
CH3OH(g)+H2O  =-49.5kJ·mol-1
=-49.5kJ·mol-1
反应④ CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)  =+41.2kJ·mol-l
=+41.2kJ·mol-l
在4MPa的恒压反应器中,按照n(CO2):n(H2)=1∶3投料,测得体系中平衡时CH3OH和CO的选择性[S(CO)= ,S(CH3OH)=
,S(CH3OH)=  ]及CO2的平衡转化率随温度的变化如图b所示。
]及CO2的平衡转化率随温度的变化如图b所示。
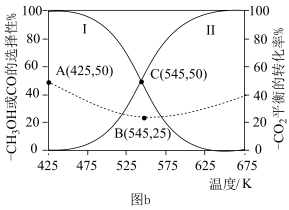
(3)研究表明,增大压强可降低CO的选择性,说明其可能的原因:___________ 。
(4)下列说法正确的是___________。
(5)反应④在545K时的平衡常数K=___________ 。
I.利用CO2和CH4制备合成气(CO、H2),反应分两步进行:[其中C(ads)为吸附性活性炭]
反应① CH4(g)
 C(ads)+2H2(g)
C(ads)+2H2(g)  >0
>0反应② C(ads)+CO2(g)
 2CO(g)
2CO(g)  >0
>0(1)研究表明,总反应速率由反应①决定,在图a上画出有关物质的相对能量与反应历程的变化(起始已给出)

(2)判断总反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)自发进行的条件并说明理由
2CO(g)+2H2(g)自发进行的条件并说明理由II.工业上可利用CO2生产燃料甲醇。该过程发生下列反应:
反应③ CO2(g)+3H2(g)
 CH3OH(g)+H2O
CH3OH(g)+H2O  =-49.5kJ·mol-1
=-49.5kJ·mol-1反应④ CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)  =+41.2kJ·mol-l
=+41.2kJ·mol-l在4MPa的恒压反应器中,按照n(CO2):n(H2)=1∶3投料,测得体系中平衡时CH3OH和CO的选择性[S(CO)=
 ,S(CH3OH)=
,S(CH3OH)=  ]及CO2的平衡转化率随温度的变化如图b所示。
]及CO2的平衡转化率随温度的变化如图b所示。
(3)研究表明,增大压强可降低CO的选择性,说明其可能的原因:
(4)下列说法正确的是___________。
| A.曲线II代表S(CO)随温度变化 |
| B.温度越低,越有利于工业生产CH3OH |
| C.上述反应条件下,CO2的平衡转化率始终高于H2的平衡转化率 |
| D.若向体系中充入惰性气体,将减慢CH3OH的生成速率并降低CH3OH的平衡产率 |
(5)反应④在545K时的平衡常数K=
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】镍(Ni)及其化合物在工业生产中具有重要地位。如图是工业精制镍的基本流程示意图:
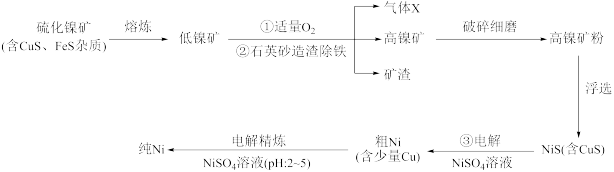
请按要求回答下列问题:
(1)写出流程图中组成气体X的元素中电负性较大的是__ (填元素符号)。气体X的中心原子的杂化轨道类型为___ ,该分子的立体构型(即空间结构)为__ 。
(2)Ni2+核外电子排布式为__ 。
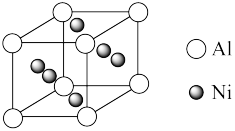
(3)向晶体Ni中掺入一定量的Al原子,会改变晶体Ni的(写一种物理性质)_ 。某种用于铸造飞机发动机叶片镍铝合金的晶胞结构如图所示,该合金的化学式为_ 。
(4)已知:常温下溶度积常数:Ksp(NiS)=1.07×10-21;Ksp(CuS)=1.27×10-36
工业生产中常用加NiS的方法除去溶液中的Cu2+,若过滤后溶液中c(Ni2+)为0.107mol·L-1,则滤液中残留的c(Cu2+)为_ 。写出流程图中③NiS在阳极参与放电的电极反应式为__ 。

请按要求回答下列问题:
(1)写出流程图中组成气体X的元素中电负性较大的是
(2)Ni2+核外电子排布式为
(3)向晶体Ni中掺入一定量的Al原子,会改变晶体Ni的(写一种物理性质)

(4)已知:常温下溶度积常数:Ksp(NiS)=1.07×10-21;Ksp(CuS)=1.27×10-36
工业生产中常用加NiS的方法除去溶液中的Cu2+,若过滤后溶液中c(Ni2+)为0.107mol·L-1,则滤液中残留的c(Cu2+)为
您最近一年使用:0次
【推荐2】以废旧玻璃粉末(主要含 )为原料可制备无水氯化铈(
)为原料可制备无水氯化铈( ),主要步骤如下:
),主要步骤如下:
(1)酸浸:用稀硫酸和双氧水的混合溶液浸取玻璃粉末,浸取液中含有 、
、 、
、 等金属阳离子。
等金属阳离子。
① 不溶于水,其发生反应的离子方程式:
不溶于水,其发生反应的离子方程式:_________ 。
②铈元素的浸出率与 、温度的关系如图所示。
、温度的关系如图所示。
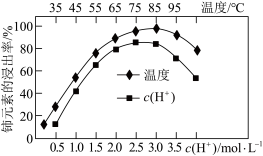
生产中 浓度最适宜控制在
浓度最适宜控制在_________ 。高于85℃时,铈元素浸出率下降的主要原因是:_________ 。
(2)除杂:向浸出液中加入NaOH调节pH除去 。已知:
。已知:
①当 时,
时, 沉淀开始溶解。
沉淀开始溶解。
② 、
、 溶度积常数分别为
溶度积常数分别为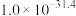 、
、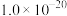 。
。
③“完全沉淀”时,金属离子浓度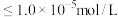
当浸出液中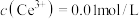 ,除杂时应控制溶液pH的范围是
,除杂时应控制溶液pH的范围是_________ (忽略体积变化)。
(3)萃取与反萃取:向除杂后的溶液中,加入有机物HT,发生反应: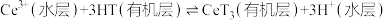 。分离后,再向所得有机层中加入
。分离后,再向所得有机层中加入_________ 能获得较纯的 溶液。
溶液。
结晶析出:将溶液蒸发浓缩、冷却结晶,过滤,得到晶体。
(4)加热脱水:将 固体和
固体和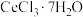 混合,存真空中加热可得无水
混合,存真空中加热可得无水 。加入
。加入 固体的作用是
固体的作用是_________ 。
 )为原料可制备无水氯化铈(
)为原料可制备无水氯化铈( ),主要步骤如下:
),主要步骤如下:(1)酸浸:用稀硫酸和双氧水的混合溶液浸取玻璃粉末,浸取液中含有
 、
、 、
、 等金属阳离子。
等金属阳离子。①
 不溶于水,其发生反应的离子方程式:
不溶于水,其发生反应的离子方程式:②铈元素的浸出率与
 、温度的关系如图所示。
、温度的关系如图所示。
生产中
 浓度最适宜控制在
浓度最适宜控制在(2)除杂:向浸出液中加入NaOH调节pH除去
 。已知:
。已知:①当
 时,
时, 沉淀开始溶解。
沉淀开始溶解。②
 、
、 溶度积常数分别为
溶度积常数分别为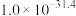 、
、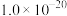 。
。③“完全沉淀”时,金属离子浓度
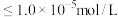
当浸出液中
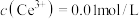 ,除杂时应控制溶液pH的范围是
,除杂时应控制溶液pH的范围是(3)萃取与反萃取:向除杂后的溶液中,加入有机物HT,发生反应:
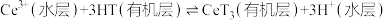 。分离后,再向所得有机层中加入
。分离后,再向所得有机层中加入 溶液。
溶液。结晶析出:将溶液蒸发浓缩、冷却结晶,过滤,得到晶体。
(4)加热脱水:将
 固体和
固体和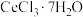 混合,存真空中加热可得无水
混合,存真空中加热可得无水 。加入
。加入 固体的作用是
固体的作用是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】Ⅰ.水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的某种方法过程如图所示:
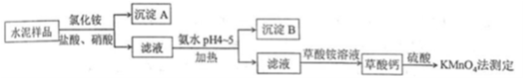
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是_____________ ,还可使用__________ 代替硝酸。
(2)沉淀A的主要成分是________ ,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为____________ 。
(3)加氨水过程中加热的目的是_____ 。沉淀B的主要成分为_______ 、_________ (填化学式)。
Ⅱ、已知25℃时草酸的电离常数为K1=5.0×10-2,K2=5.4×10-5.草酸钙的Kap=4.0×10-8.碳酸钙的Ksp=2.5×10-9.不同温度下水的离子积常数见下表:
(1)计算25℃时KHC2O4溶液的水解平衡常数Kb=_____ ;写出水溶液中草酸的电离方程式_____ ;常温下将0.2mol/L的KOH溶液10mL与0.2mol/L的草酸溶液20mL混合后溶液显________ 性。(填“酸性”“中性”或“无法确定”)
(2)25℃时向20mL草酸钙的饱和溶液中逐滴加入8.0×10-4mol/L的碳酸钾溶液10mL,能否产生沉淀,_______ (填“能”或“否”). 碳酸钙转化为草酸钙的离子方程式为______ ,列式计算该反的平衡常数K=_________ 。
(3)90℃时,将0.005mol/L的氢氧化钙溶液20mL与0.0012mol/L的草酸溶液20mL混合,则混合后溶液的pH______ 。(可能用到的对数:lg38=1.6,lg26=2.4,lg2=0.3)

(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是
(2)沉淀A的主要成分是
(3)加氨水过程中加热的目的是
Ⅱ、已知25℃时草酸的电离常数为K1=5.0×10-2,K2=5.4×10-5.草酸钙的Kap=4.0×10-8.碳酸钙的Ksp=2.5×10-9.不同温度下水的离子积常数见下表:
| t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 90 | 100 |
| Kw/10-14 | 0.134 | 0.292 | 0.681 | 1.00 | 2.92 | 5.57 | 38.0 | 55.0 |
(1)计算25℃时KHC2O4溶液的水解平衡常数Kb=
(2)25℃时向20mL草酸钙的饱和溶液中逐滴加入8.0×10-4mol/L的碳酸钾溶液10mL,能否产生沉淀,
(3)90℃时,将0.005mol/L的氢氧化钙溶液20mL与0.0012mol/L的草酸溶液20mL混合,则混合后溶液的pH
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】以铬铁矿[Fe(CrO2)2]为原料可制备K2Cr2O7和金属铬。实验流程如下:

已知:2CrO42-+2H+=Cr2O72-+H2O。pH<3.0,CrO42-含量极小。
(1)写出铬铁矿焙烧转化为Na2CrO4的化学反应方程式:_____________________ 。焙烧时不能使用陶瓷容器的原因是________________________________________ 。
(2)判断加入稀硫酸的量已经足量的标准是_______________________________________ 。
(3)操作①包括过滤和洗涤。实验室洗涤沉淀的操作是________________________________ 。
(4)Na2S的作用是调节溶液的酸碱度和_____________________ 。

(5)Fe3+在pH 为3.7时可完全转化为Fe(OH)3。在上述流程中所得Na2Cr2O7溶液中含有少量Fe3+。请结合上图有关物质的溶解度曲线,设计由Na2Cr2O7溶液制备K2Cr2O7固体的实验方案(实验中须选用的试剂:硫酸溶液、NaOH溶液、KCl固体、蒸馏水):
步骤①除杂质:__________________________________________________________________ ;
步骤②制备K2Cr2O7固体:__________________________________________________ 。

已知:2CrO42-+2H+=Cr2O72-+H2O。pH<3.0,CrO42-含量极小。
(1)写出铬铁矿焙烧转化为Na2CrO4的化学反应方程式:
(2)判断加入稀硫酸的量已经足量的标准是
(3)操作①包括过滤和洗涤。实验室洗涤沉淀的操作是
(4)Na2S的作用是调节溶液的酸碱度和

(5)Fe3+在pH 为3.7时可完全转化为Fe(OH)3。在上述流程中所得Na2Cr2O7溶液中含有少量Fe3+。请结合上图有关物质的溶解度曲线,设计由Na2Cr2O7溶液制备K2Cr2O7固体的实验方案(实验中须选用的试剂:硫酸溶液、NaOH溶液、KCl固体、蒸馏水):
步骤①除杂质:
步骤②制备K2Cr2O7固体:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】磷锌白[Zn3(PO4)2]可用于生产无毒防锈颜料和水溶性涂料。一种利用烧铸灰(主要含ZnO,还含少量Fe3O4、PbO、SnO2、CuO及SiO2等)为原料制取磷锌白的工艺流程如图:

回答下列问题:
(1)“酸溶”时,为提高锌的浸出率,可采取的措施有__________ (列举1条)。
(2)“滤渣1”的主要成分为_________ (填化学式)。
(3)“氧化”时,KMnO4与Fe2+发生反应,当消耗1molKMnO4,转移_____ mol电子。
(4)几种金属离子开始沉淀与沉淀完全的pH如下:
“调pH”为4.0的目的是除去Fe2+、Mn2+和_______ ,为检验“过滤2”后的滤液中是否含有Fe3+,可选用的化学试剂是_________ 。
(5)加锌“置换”的目的是________ 。
(6)“制备”时,加Na2HPO4至Zn2+恰好沉淀完全的化学方程式为________ 。
(7)某工厂用7吨烧铸灰(ZnO的质量分数为81%)进行上述工艺流程,最终制得Zn3(PO4)27.7吨,则产率为(保留三位有效数字)_______ 。

回答下列问题:
(1)“酸溶”时,为提高锌的浸出率,可采取的措施有
(2)“滤渣1”的主要成分为
(3)“氧化”时,KMnO4与Fe2+发生反应,当消耗1molKMnO4,转移
(4)几种金属离子开始沉淀与沉淀完全的pH如下:
金属离子 | Sn4+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀~沉淀完全的pH | 0.5~1.3 | 2.2~3.6 | 4.8~6.4 | 6.5~8.5 |
(5)加锌“置换”的目的是
(6)“制备”时,加Na2HPO4至Zn2+恰好沉淀完全的化学方程式为
(7)某工厂用7吨烧铸灰(ZnO的质量分数为81%)进行上述工艺流程,最终制得Zn3(PO4)27.7吨,则产率为(保留三位有效数字)
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】8月1日起,为了国家信息安全,我国禁止镓和锗的出口,锗是一种重要的半导体材料,工业上用精硫锗矿(主要成分为 )制取高纯度锗的工艺流程如图所示:
)制取高纯度锗的工艺流程如图所示:
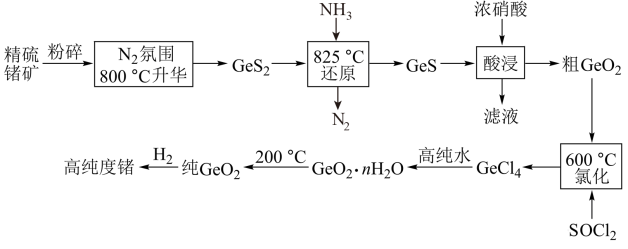
(1) 分子中各原子均达到8电子稳定结构,其结构式为
分子中各原子均达到8电子稳定结构,其结构式为___________ 。
(2)800℃升华时通入 的目的是:
的目的是:___________ 、___________ 。
(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式:___________ ,酸浸时温度不能过高的原因是___________ 。
(4) 易水解生成
易水解生成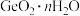 ,证明
,证明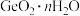 沉淀洗涤干净的方法是
沉淀洗涤干净的方法是___________ 。
(5)测定错的含量:称取0.5500g锗样品,加入双氧水溶解,再加入盐酸生成 ,以淀粉为指示剂,用
,以淀粉为指示剂,用 的碘酸钾标准溶液滴定,消耗碘酸钾的体积为24.80mL。已知:酸性条件下
的碘酸钾标准溶液滴定,消耗碘酸钾的体积为24.80mL。已知:酸性条件下 ,能将
,能将 氧化为
氧化为 ,①在滴定过程中依次发生的离子方程式为:
,①在滴定过程中依次发生的离子方程式为:___________ 、___________ ,②该样品中储的质量分数是___________ %(精确到0.01%)。
 )制取高纯度锗的工艺流程如图所示:
)制取高纯度锗的工艺流程如图所示:
(1)
 分子中各原子均达到8电子稳定结构,其结构式为
分子中各原子均达到8电子稳定结构,其结构式为(2)800℃升华时通入
 的目的是:
的目的是:(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式:
(4)
 易水解生成
易水解生成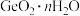 ,证明
,证明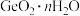 沉淀洗涤干净的方法是
沉淀洗涤干净的方法是(5)测定错的含量:称取0.5500g锗样品,加入双氧水溶解,再加入盐酸生成
 ,以淀粉为指示剂,用
,以淀粉为指示剂,用 的碘酸钾标准溶液滴定,消耗碘酸钾的体积为24.80mL。已知:酸性条件下
的碘酸钾标准溶液滴定,消耗碘酸钾的体积为24.80mL。已知:酸性条件下 ,能将
,能将 氧化为
氧化为 ,①在滴定过程中依次发生的离子方程式为:
,①在滴定过程中依次发生的离子方程式为:
您最近一年使用:0次



