下列过程中的化学反应,相应的离子方程式正确的是
| A.Fe(OH)3和HI的反应:Fe(OH)3+3H+=Fe3++3H2O |
B.惰性电极电解氯化镁溶液:2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
C.用Na2CO3溶液浸泡水垢: (aq)+CaSO4(s)=CaCO3(s)+ (aq)+CaSO4(s)=CaCO3(s)+ (aq) (aq) |
| D.Na2S水解:S2-+2H2O=H2S+2OH- |
更新时间:2023-03-19 17:33:12
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
A.向 溶液中逐滴加入 溶液中逐滴加入 溶液至刚好沉淀完全,反应的离子方程式为 溶液至刚好沉淀完全,反应的离子方程式为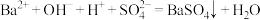 |
B.25℃时,加水稀释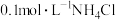 ,溶液中 ,溶液中 不断增大 不断增大 |
C.用浓盐酸分别和 、 、 反应制备 反应制备 氯气,转移的电子数均为 氯气,转移的电子数均为 ( ( 为阿伏伽德罗常数的值) 为阿伏伽德罗常数的值) |
D.相同物质的量浓度的下列溶液中,① 、② 、② 、③ 、③ 、④ 、④ 其 其 由大到小的顺序是:①>②>③>④ 由大到小的顺序是:①>②>③>④ |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列化学反应表示正确的是
A.用石墨作电极电解CuSO4溶液:2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
| B.钢铁发生吸氧腐蚀时负极反应为:Fe - 3e- = Fe3+ |
C.用惰性电极电解饱和NaCl溶液: 2H++2Cl- Cl2↑+H2↑ Cl2↑+H2↑ |
| D.Cl2通入水中:Cl2+H2O=2H+ +Cl-+ClO- |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列水解离子方程式正确的是
A.Fe3++3H2O Fe(OH)3↓+3H+ Fe(OH)3↓+3H+ |
B.Br-+H2O HBr+OH- HBr+OH- |
C.CO +H2O +H2O H2CO3+2OH- H2CO3+2OH- |
D.NH +2H2O +2H2O NH3•H2O+H3O+ NH3•H2O+H3O+ |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】油条的做法是将矾、碱、盐按比例加入温水中,再加入面粉搅拌成面团;放置,使面团产生气体,形成孔洞。放置过程发生: 。下列有关判断不正确的是
。下列有关判断不正确的是
 。下列有关判断不正确的是
。下列有关判断不正确的是| A.放置过程发生的反应中,反应物或生成物不都是电解质 |
| B.放置过程发生的反应为非氧化还原反应 |
C.反应的离子方程式为 |
| D.从物质的分类角度来看,油条配方中的“矾、碱、盐”均为盐 |
您最近半年使用:0次
【推荐1】室温下,某 溶液体系中满足
溶液体系中满足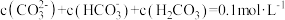 ,现利用平衡移动原理,研究
,现利用平衡移动原理,研究 在不同pH的
在不同pH的 体系中的可能产物。图1中曲线表示
体系中的可能产物。图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合
体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合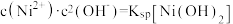 ,曲线Ⅱ的离子浓度关系符合
,曲线Ⅱ的离子浓度关系符合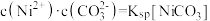 ,不同pH下
,不同pH下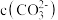 由图1得到。下列说法错误的是
由图1得到。下列说法错误的是
 溶液体系中满足
溶液体系中满足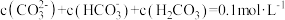 ,现利用平衡移动原理,研究
,现利用平衡移动原理,研究 在不同pH的
在不同pH的 体系中的可能产物。图1中曲线表示
体系中的可能产物。图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合
体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合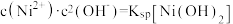 ,曲线Ⅱ的离子浓度关系符合
,曲线Ⅱ的离子浓度关系符合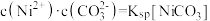 ,不同pH下
,不同pH下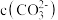 由图1得到。下列说法错误的是
由图1得到。下列说法错误的是
A.由图1, 的水解平衡常数的数量级是 的水解平衡常数的数量级是 |
B.图2中M点,溶液中存在 |
C.图2中P点,存在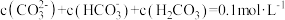 |
D.沉淀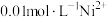 制备 制备 时,选用 时,选用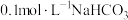 溶液比 溶液比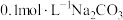 溶液效果好 溶液效果好 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】根据下列实验操作及现象能推出相应结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 在反应:2NO2(g) N2O4(g)的平衡体系中,压缩容器体积 N2O4(g)的平衡体系中,压缩容器体积 | 气体颜色加深 | 平衡向逆反应方向移动 |
| B | 用pH计分别测定一定浓度的醋酸和AlCl3溶液 | 测得两种溶液 pH均等于3.0 | 两溶液均显酸性,水的电离程度相同 |
| C | 向盛有Zn与稀盐酸的试管中滴加少量CuSO4溶液 | 产生气泡的速率加快 | 反应过程中形成了原电池 |
| D | 向1 mL0.1 mol·L-1AgNO3溶液中加入几滴0.1 mol·L-1NaCl溶液后,再向其中滴加几滴0.1 mol·L-1KI溶液 | 先产生白色沉淀,后产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
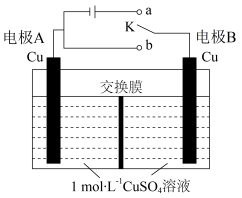
【推荐1】近期科技工作者开发了一套以乙醇为原料制备DDE( )的电解装置如图所示。下列说法不正确的是
)的电解装置如图所示。下列说法不正确的是
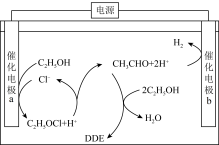
 )的电解装置如图所示。下列说法不正确的是
)的电解装置如图所示。下列说法不正确的是
| A.电极的电极电势:b<a |
B.阳极电极反应式为 |
| C.电解后溶液的pH会减小(忽略由于水的生成引起溶液体积变化) |
| D.每产生1molH2需要消耗3molC2H5OH |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】以 为原料,通过电解法制备
为原料,通过电解法制备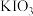 的实验装置如图所示。电解前,先将一定量的精制
的实验装置如图所示。电解前,先将一定量的精制 溶于过量KOH溶液,发生反应
溶于过量KOH溶液,发生反应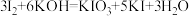 ,将反应后的溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。下列说法不正确的是( )
,将反应后的溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。下列说法不正确的是( )

 为原料,通过电解法制备
为原料,通过电解法制备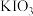 的实验装置如图所示。电解前,先将一定量的精制
的实验装置如图所示。电解前,先将一定量的精制 溶于过量KOH溶液,发生反应
溶于过量KOH溶液,发生反应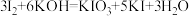 ,将反应后的溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。下列说法不正确的是( )
,将反应后的溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。下列说法不正确的是( )
A. 会穿过离子交换膜向右侧移动 会穿过离子交换膜向右侧移动 |
B.阳极发生的电极反应为: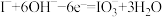 |
C.当外电路转移0.1mol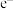 ,阴极区增重3.9g ,阴极区增重3.9g |
D.若电流利用率为100%,电解法制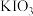 碘原子的利用率是直接歧化法的6倍 碘原子的利用率是直接歧化法的6倍 |
您最近半年使用:0次

 Cl2↑+ H2↑+ 2OH—
Cl2↑+ H2↑+ 2OH— +2H2O
+2H2O
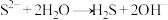
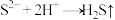

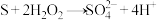

 的
的 溶液中先滴入过量
溶液中先滴入过量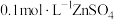 溶液有白色沉淀生成,再滴入
溶液有白色沉淀生成,再滴入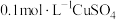 溶液,白色沉淀变为黑色沉淀
溶液,白色沉淀变为黑色沉淀 与
与 之间是可逆反应
之间是可逆反应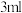 、
、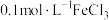 溶液中滴加
溶液中滴加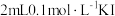 溶液,充分反应,滴加几滴
溶液,充分反应,滴加几滴 溶液后变为红色
溶液后变为红色 溶液的试管中同时加入
溶液的试管中同时加入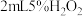 溶液,观察实验现象
溶液,观察实验现象