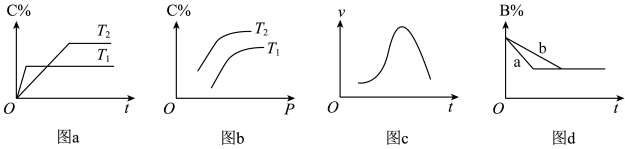
向密闭容器中充入S2Cl2、Cl2和SCl2,发生反应S2Cl2(g)+Cl2(g) 2SCl2(g),S2Cl2与SCl2的初始消耗速率(v)与温度(T)的关系如图所示(图中A、B点处于平衡状态),下列说法不正确的是
2SCl2(g),S2Cl2与SCl2的初始消耗速率(v)与温度(T)的关系如图所示(图中A、B点处于平衡状态),下列说法不正确的是

 2SCl2(g),S2Cl2与SCl2的初始消耗速率(v)与温度(T)的关系如图所示(图中A、B点处于平衡状态),下列说法不正确的是
2SCl2(g),S2Cl2与SCl2的初始消耗速率(v)与温度(T)的关系如图所示(图中A、B点处于平衡状态),下列说法不正确的是
| A.a为v(SCl2)随温度的变化曲线 |
| B.该反应正反应为放热反应 |
| C.0℃下反应一段时间,S2Cl2的物质的量增多 |
| D.反应达到平衡后向体系中充入氦气,平衡不移动 |
更新时间:2023-03-17 15:26:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某同学设计了如下一系列实验用于探究硫酸铜的量对锌与稀硫酸反应生成氢气速率的影响,该同学将表中所给的混合物分别加入6个盛有过量Zn粒的反应瓶中,记录获得 (已换算成标准状况)气体所需时间。忽略溶液体积和温度变化,下列说法错误的是
(已换算成标准状况)气体所需时间。忽略溶液体积和温度变化,下列说法错误的是
 (已换算成标准状况)气体所需时间。忽略溶液体积和温度变化,下列说法错误的是
(已换算成标准状况)气体所需时间。忽略溶液体积和温度变化,下列说法错误的是| 实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 混合物 |   溶液/mL 溶液/mL | 50 | 50 | 50 | 50 | 50 | 50 |
 固体/g 固体/g | 0 | 0.5 | 2.5 | 5 | 10 | 20 | |
| 时间/min | 30 | 25 | 23 | 22 | 23 | 35 | |
A.第②组实验从反应开始至收集到 气体,反应的平均速率 气体,反应的平均速率 |
| B.加入适量的硫酸铜,反应生成的铜与锌形成了原电池,从而加快了锌与稀硫酸的反应速率 |
| C.加入硫酸铜较多,生成的铜覆盖在锌表面,有可能会减缓锌与稀硫酸的反应速率 |
D.实验中将硫酸铜固体改为硫酸钠固体, 浓度增大,也能达到加快反应速率的效果 浓度增大,也能达到加快反应速率的效果 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验目的、实验方案以及评价正确的是( )
| 选项 | 实验目的 | 实验方案 | 评价 |
| A | 探究接触面积对化学反应速率的影响 | 相同温度下,取等质量的大理石块、大理石粉末分别投入到等体积、等浓度的盐酸中 | 该方案可行 |
| B | 证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向2 mL 1 mol·L-1 NaOH溶液中先加入3滴1 mol·L-1MgCl2溶液,再加入3滴1 mol·L-1 FeCl3溶液 | 该方案可行 |
| C | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,冷却后再向其中加入新制的银氨溶液,并水浴加热 | 该方案可行 |
| D | 测定铝箔中氧化铝的含量 | 取a g铝箔与足量稀盐酸充分反应,逸出的气体通过碱石灰后,测其体积为b L(已转化为标准状况下) | 该方案不可行 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列措施或事实不能用勒夏特列原理解释的是
| A.新制的氯水在光照下颜色变浅 |
| B.H2、I2、HI平衡混合气加压后颜色变深 |
| C.在合成氨的反应中,加压有利于氨的合成 |
| D.Fe(SCN)3溶液中加入NaOH后溶液颜色变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知反应: .按起始投料比
.按起始投料比 加入反应物,测得
加入反应物,测得 的平衡转化率和催化剂催化效率受温度的影响如下图所示.下列说法不正确的是
的平衡转化率和催化剂催化效率受温度的影响如下图所示.下列说法不正确的是
 .按起始投料比
.按起始投料比 加入反应物,测得
加入反应物,测得 的平衡转化率和催化剂催化效率受温度的影响如下图所示.下列说法不正确的是
的平衡转化率和催化剂催化效率受温度的影响如下图所示.下列说法不正确的是
A. 时,b点反应向逆反应方向进行 时,b点反应向逆反应方向进行 |
| B.生成乙烯的速率c点一定大于a点 |
C. ,催化效率降低是由于温度升高引起的 ,催化效率降低是由于温度升高引起的 |
D.a点乙烯的体积分数约为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】对于平衡体系mA(g)+nB(g)  pC(g)+qD(g) ΔH<0.下列结论中
pC(g)+qD(g) ΔH<0.下列结论中不正确 的是
 pC(g)+qD(g) ΔH<0.下列结论中
pC(g)+qD(g) ΔH<0.下列结论中| A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的1.5倍,则m+n>p+q |
B.若温度不变时,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的 要小 要小 |
| C.若平衡时,A、B 的转化率相等,说明反应开始时,A、B的物质的量之比为m∶n |
| D.若m+n>p+q,则往含有a mol气体的平衡体系中再加入a mol 的B,达到新平衡时,气体的总物质的量小于2a mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知在密闭容器里反应:mX(g)+nY(g) qZ(g)ΔH;反应物Y与反应时间t、温度T、压强p的关系曲线见右图,试通过对此曲线的分析,判断下列描述中正确的是
qZ(g)ΔH;反应物Y与反应时间t、温度T、压强p的关系曲线见右图,试通过对此曲线的分析,判断下列描述中正确的是

 qZ(g)ΔH;反应物Y与反应时间t、温度T、压强p的关系曲线见右图,试通过对此曲线的分析,判断下列描述中正确的是
qZ(g)ΔH;反应物Y与反应时间t、温度T、压强p的关系曲线见右图,试通过对此曲线的分析,判断下列描述中正确的是
| A.T1<T2、p2<p1、m+n>q、ΔH<0 |
| B.T1<T2、p2<p1、m+n>q、ΔH>0 |
| C.T1>T2、p1<p2、m+n<q、ΔH>0 |
| D.T1>T2、p1<p2、m+n<q、ΔH<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】二氧化硫的催化氧化反应:2SO2(g)+O2(g) 2SO3(g)是工业制硫酸的重要反应之一,下列说法
2SO3(g)是工业制硫酸的重要反应之一,下列说法错误 的是
 2SO3(g)是工业制硫酸的重要反应之一,下列说法
2SO3(g)是工业制硫酸的重要反应之一,下列说法| A.该反应加入催化剂是为了加快反应速率 |
| B.已知该催化氧化反应K(300 ℃)>K(350 ℃),则该反应正向是放热反应 |
| C.煅烧硫铁矿(主要成分FeS2)可获得SO2,将矿石粉碎成小颗粒可提高反应的平衡转化率 |
| D.保持温度不变,平衡后增大O2的浓度,该反应的平衡常数K不变 |
您最近一年使用:0次

 的
的 溶液
溶液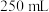 容量瓶中定容
容量瓶中定容 黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化
黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化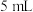 不同浓度
不同浓度 溶液的试管中同时加入
溶液的试管中同时加入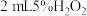 溶液,观察实验现象
溶液,观察实验现象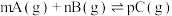 ,下列有关外界条件改变对该反应的速率和平衡的影响图像正确的是
,下列有关外界条件改变对该反应的速率和平衡的影响图像正确的是