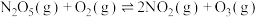对于平衡体系mA(g)+nB(g)  pC(g)+qD(g) ΔH<0.下列结论中
pC(g)+qD(g) ΔH<0.下列结论中不正确 的是
 pC(g)+qD(g) ΔH<0.下列结论中
pC(g)+qD(g) ΔH<0.下列结论中| A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的1.5倍,则m+n>p+q |
B.若温度不变时,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的 要小 要小 |
| C.若平衡时,A、B 的转化率相等,说明反应开始时,A、B的物质的量之比为m∶n |
| D.若m+n>p+q,则往含有a mol气体的平衡体系中再加入a mol 的B,达到新平衡时,气体的总物质的量小于2a mol |
更新时间:2021-09-29 22:27:34
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】工业含铬废水中含有 (溶液为橙色)和
(溶液为橙色)和 (溶液为黄色),会对水体产生很大危害,因此这种工业废水必须净化处理。一种处理含铬废水的工艺流程如下:
(溶液为黄色),会对水体产生很大危害,因此这种工业废水必须净化处理。一种处理含铬废水的工艺流程如下:
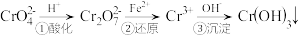
已知有反应: 。下列说法正确的是
。下列说法正确的是
 (溶液为橙色)和
(溶液为橙色)和 (溶液为黄色),会对水体产生很大危害,因此这种工业废水必须净化处理。一种处理含铬废水的工艺流程如下:
(溶液为黄色),会对水体产生很大危害,因此这种工业废水必须净化处理。一种处理含铬废水的工艺流程如下: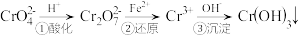
已知有反应:
 。下列说法正确的是
。下列说法正确的是| A.①中,所加酸可以是盐酸 |
| B.①中,酸化后废水黄色变浅 |
| C.②中,反应的氧化剂与还原剂的物质的量之比为1∶3 |
D.③中,该工艺流程所得 可用于制备 可用于制备 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关实验操作、现象和解释或结论都正确的组合是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 取  溶液,向其中加入 溶液,向其中加入 的硫酸,分别在20℃、30℃下,发生反应 的硫酸,分别在20℃、30℃下,发生反应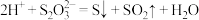 | 30℃下先出现浑浊 | 温度越高,反应速率越快 |
| B | 向 和KSCN的混合溶液中加入少量铁粉 和KSCN的混合溶液中加入少量铁粉 | 血红色溶液颜色变浅 | 铁粉与 反应,降低了 反应,降低了 的浓度,使得平衡正向移动 的浓度,使得平衡正向移动 |
| C | 两支试管中各盛有2mL 酸性高锰酸钾溶液,分别加入5mL 酸性高锰酸钾溶液,分别加入5mL 草酸溶液和5mL 草酸溶液和5mL 草酸溶液 草酸溶液 | 加入 草酸溶液的试管中,高锰酸钾溶液褪色更快 草酸溶液的试管中,高锰酸钾溶液褪色更快 | 反应物浓度越大,反应速率越快 |
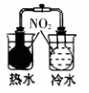
| D | 把充有 和 和 的平衡球装置分别放入热水和冷水装置中 的平衡球装置分别放入热水和冷水装置中 | 冷水中颜色更深 | 其他条件不变时,温度升高,平衡向吸热反应方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实中,不能用勒夏特列原理解释的是
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低
③实验室常用排饱和食盐水的方法收集氯气
④棕红色NO2加压后颜色先变深后变浅
⑤加入催化剂有利于合成氨的反应
⑥向MgCO3沉淀中滴加NaOH溶液可以得到Mg(OH)2沉淀
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低
③实验室常用排饱和食盐水的方法收集氯气
④棕红色NO2加压后颜色先变深后变浅
⑤加入催化剂有利于合成氨的反应
⑥向MgCO3沉淀中滴加NaOH溶液可以得到Mg(OH)2沉淀
| A.②⑤ | B.①③⑤ | C.①②⑥ | D.②③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NO2在有机化学中可用作氧化剂、硝化剂和丙烯酸酯聚合的抑制剂。已知反应:2NO2(g) N2O4(g) △H<0。在恒温条件下,将一定量的NO2充入注射器中后封口,如图表示在拉伸和压缩注射器的过程中气体透光率随时间的变化的关系图(气体颜色越深,透光率越小)。下列说法正确的是
N2O4(g) △H<0。在恒温条件下,将一定量的NO2充入注射器中后封口,如图表示在拉伸和压缩注射器的过程中气体透光率随时间的变化的关系图(气体颜色越深,透光率越小)。下列说法正确的是
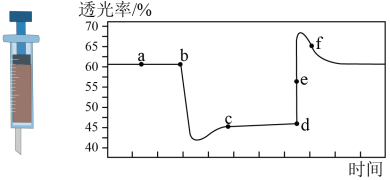
 N2O4(g) △H<0。在恒温条件下,将一定量的NO2充入注射器中后封口,如图表示在拉伸和压缩注射器的过程中气体透光率随时间的变化的关系图(气体颜色越深,透光率越小)。下列说法正确的是
N2O4(g) △H<0。在恒温条件下,将一定量的NO2充入注射器中后封口,如图表示在拉伸和压缩注射器的过程中气体透光率随时间的变化的关系图(气体颜色越深,透光率越小)。下列说法正确的是
| A.反应速率:c<a |
| B.平衡常数:K(a)>K(c) |
| C.e点到f点的过程中从环境吸收热量 |
| D.d点到e点的变化可以用勒夏特列原理解释 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】一定温度下,向2L密闭容器中加入足量C(s)并充入2molH2O(g),发生反应C(s)+H2O(g) CO(g)+H2(g),反应过程中测得如下数据,下列说法错误的是
CO(g)+H2(g),反应过程中测得如下数据,下列说法错误的是
 CO(g)+H2(g),反应过程中测得如下数据,下列说法错误的是
CO(g)+H2(g),反应过程中测得如下数据,下列说法错误的是| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| n(H2)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 | …… |
| A.6min时,反应达到平衡状态,各组分的物质的量均不再改变 |
| B.6min~8min时间段内,υ(H2)=0mol·L-1·min-1 |
| C.该条件下,无论反应多长时间,c(H2)<1mol·L-1 |
| D.保持温度和体积不变,8min时向该容器中充入少量He(g),平衡将会发生移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g) 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是
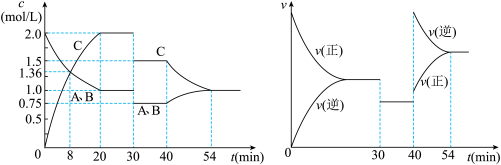
 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是
| A.第8min末 A的反应速率为0.08mol·L-1·min-1 |
| B.在0-54分钟的反应过程中该可逆反应的平衡常数始终为4 |
| C.30min时改变的条件是减小压强,40min时改变的条件是降低温度 |
| D.反应方程式中的x=1,且正反应为放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知: 在水溶液中以水合铁离子的形式存在,如
在水溶液中以水合铁离子的形式存在,如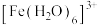 (几乎无色);
(几乎无色);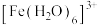 水解生成
水解生成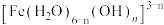 (黄色);
(黄色);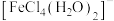 (黄色)。
(黄色)。
下列实验所得结论不正确 的是
注:加热为微热,忽略体积变化。
 在水溶液中以水合铁离子的形式存在,如
在水溶液中以水合铁离子的形式存在,如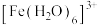 (几乎无色);
(几乎无色);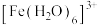 水解生成
水解生成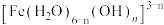 (黄色);
(黄色);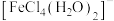 (黄色)。
(黄色)。下列实验所得结论
| ① | ② | ③ | ④ |
 0.1mol/L  溶液 溶液 |  酸化的0.1mol/L  溶液 溶液 | 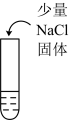 酸化的0.1mol/L  溶液 溶液 |  0.1mol/L  溶液 溶液 |
| 加热前溶液为浅黄色,加热后颜色变深 | 加热前溶液接近无色,加热后溶液颜色无明显变化 | 加入NaCl后,溶液立即变为黄色,加热后溶液颜色变深 | 加热前溶液为黄色,加热后溶液颜色变深 |
A.实验①中, 溶液显浅黄色原因是 溶液显浅黄色原因是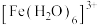 发生了水解反应 发生了水解反应 |
B.实验②中,酸化对 水解的影响程度大于温度的影响 水解的影响程度大于温度的影响 |
C.实验③中,存在可逆反应: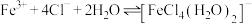 |
D.实验④,可证明升高温度, 水解平衡正向移动 水解平衡正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在恒温密闭容器中发生反应:CaCO3(s) CaO(s)+CO2(g) ∆H>0,反应达到平衡后,tl时缩小容器体积, x随时间(t)变化的关系如下图所示。x不可能是
CaO(s)+CO2(g) ∆H>0,反应达到平衡后,tl时缩小容器体积, x随时间(t)变化的关系如下图所示。x不可能是

 CaO(s)+CO2(g) ∆H>0,反应达到平衡后,tl时缩小容器体积, x随时间(t)变化的关系如下图所示。x不可能是
CaO(s)+CO2(g) ∆H>0,反应达到平衡后,tl时缩小容器体积, x随时间(t)变化的关系如下图所示。x不可能是
| A.υ逆(逆反应速率) | B.ρ(容器内气体密度) |
| C.m(容器内CaO质量) | D.p(容器压强) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
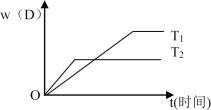
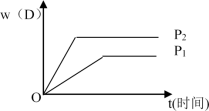
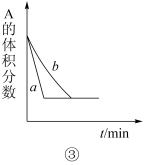
【推荐2】下图表示可逆反应 mA(g)+nB(g)  pC(g)+qD(g) 在不同温度(T)和压强(P)下生成物D的体积分数w(D)随时间的变化情况。关于上述正反应的判断正确的是
pC(g)+qD(g) 在不同温度(T)和压强(P)下生成物D的体积分数w(D)随时间的变化情况。关于上述正反应的判断正确的是
 pC(g)+qD(g) 在不同温度(T)和压强(P)下生成物D的体积分数w(D)随时间的变化情况。关于上述正反应的判断正确的是
pC(g)+qD(g) 在不同温度(T)和压强(P)下生成物D的体积分数w(D)随时间的变化情况。关于上述正反应的判断正确的是 

| A.T1>T2 ,△H<0 | B.T2>T1 ,△H>0 |
| C.P2>P1 ,m+n>p+q | D.P1>P2 ,m+n>p+q |
您最近一年使用:0次



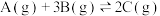



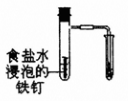
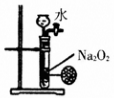
 ,该反应达到平衡后,下列说法不正确的是
,该反应达到平衡后,下列说法不正确的是 的浓度增大,则该反应的
的浓度增大,则该反应的
 的物质的量浓度减小
的物质的量浓度减小