我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、Ni、Cu等元素。回答下列问题:
(1)写出基态 的电子排布式:
的电子排布式:_______ 。
(2)P元素第一电离能大于S,原因为_______ 。
(3)镍能形成多种配合物,其中 是无色挥发性液体,
是无色挥发性液体, 是红黄色单斜晶体。
是红黄色单斜晶体。 的熔点高于
的熔点高于 的原因是
的原因是_______ 。
(4)氮化硼(BN)晶体存在如下图所示的两种结构,六方氮化硼的结构与石墨类似,可做润滑剂;立方氮化硼的结构与金刚石类似,可作研磨剂。
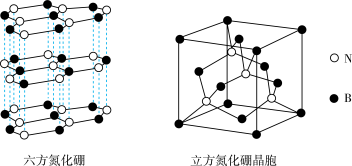
六方氮化硼的晶体类型为_______ ;立方氮化硼晶胞的密度为ρ g·cm ,晶胞的边长为acm。则阿伏加德罗常数的表达式为
,晶胞的边长为acm。则阿伏加德罗常数的表达式为_______ 。
(5)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。下列物质中,属于顺磁性物质的是_______(填标号)。
(1)写出基态
 的电子排布式:
的电子排布式:(2)P元素第一电离能大于S,原因为
(3)镍能形成多种配合物,其中
 是无色挥发性液体,
是无色挥发性液体, 是红黄色单斜晶体。
是红黄色单斜晶体。 的熔点高于
的熔点高于 的原因是
的原因是(4)氮化硼(BN)晶体存在如下图所示的两种结构,六方氮化硼的结构与石墨类似,可做润滑剂;立方氮化硼的结构与金刚石类似,可作研磨剂。

六方氮化硼的晶体类型为
 ,晶胞的边长为acm。则阿伏加德罗常数的表达式为
,晶胞的边长为acm。则阿伏加德罗常数的表达式为(5)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。下列物质中,属于顺磁性物质的是_______(填标号)。
A. | B. |
C. | D. |
更新时间:2023-03-30 16:20:21
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E是前四周期的五种元素,原子序数依次增大,只有B、C位于同一周期且位置相邻,其中C是地壳中含量最多的元素,D是其所处周期中电负性最强的元素,E为过渡元素,原子核外只有两个单电子,其余原子轨道均充满电子。回答下列问题
(1)B元素的基态原子电子的空间运动状态有_______ 种;E元素的价电子排布式_______ ,其基态原子有_______ 种能量不同的电子。
(2)B、C两种元素分别与A元素形成的两种10电子阳离子中,中心原子的杂化方式都是采用_______ 杂化,键角大的是_______ (填离子符号),原因是_______ 。
(3)D单质通入 中发生反应的离子方程式是
中发生反应的离子方程式是_______ :写出ADC的电子式_______ 。
(4) 的空间构型是
的空间构型是_______ ;第一电离能B_______ C(填“<”或“>”)。A、B、C三种元素电负性由大到小的顺序是_______ (用元素符号表示)。
(1)B元素的基态原子电子的空间运动状态有
(2)B、C两种元素分别与A元素形成的两种10电子阳离子中,中心原子的杂化方式都是采用
(3)D单质通入
 中发生反应的离子方程式是
中发生反应的离子方程式是(4)
 的空间构型是
的空间构型是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E。又知A原子的p轨道为半充满,其形成的简单氢化物的沸点是同主族非金属元素的氢化物中最高的。D原子得到一个电子后其3p轨道将全充满。B+离子比D原子形成的离子少一个电子层。C与B可形成BC型的离子化合物。E的原子序数为29。
请回答下列问题:
(1) 元素A简单氢化物中A原子的杂化类型是________ ,B、C、D的电负性由小到大的顺序为______ (用所对应的元素符号表示)。C的气态氢化物易溶于水的原因是____________________ 。
(2)E原子的基态电子排布式为________ 。元素E的单质晶体在不同温度下可有两种堆积方式,晶胞分别如图a和b所示,则其面心立方堆积的晶胞与体心立方堆积的晶胞中实际含有的E原子的个数之比为____________ 。

(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:________ 。
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是________ 。
(5)温室效应,科学家设计反应:CO2+4H2—→CH4+2H2O以减小空气中CO2。若有1 mol CH4生成,则有________ mol σ键和________ mol π键断裂。
请回答下列问题:
(1) 元素A简单氢化物中A原子的杂化类型是
(2)E原子的基态电子排布式为

(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是
(5)温室效应,科学家设计反应:CO2+4H2—→CH4+2H2O以减小空气中CO2。若有1 mol CH4生成,则有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】CuSO4和Cu(NO3)2是自然界中重要的铜盐。请回答下列问题:
(1)CuSO4和Cu(NO3)2中阳离子的核外价电子排布式为_______ ,S、O、N三种元素的第一电离能由大到小的顺序为__________ 。
(2)NO3-的立体构型是_____ ,与NO3-互为等电子体的一种非极性分子为_________ (填化学式)。
(3)CuSO4的熔点为560°C,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因是_____ 。
(4)往CuSO4溶液中加入过量NaOH能生成配合物[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为(用箭头表示出配位键的位置)_______ 。
(5)化学实验室常利用新制氢氧化铜检验醛基的存在,乙醛分子中碳原子的杂化方式为___ 。
(6)利用新制的Cu(OH)2检验醛基时,生成红色的Cu2O,其晶胞结构如下图所示。
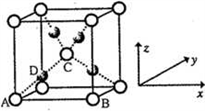
该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);C为( ,
, ,
, )。则D原子的坐标参数为
)。则D原子的坐标参数为________ ,它代表_______ 原子。
(1)CuSO4和Cu(NO3)2中阳离子的核外价电子排布式为
(2)NO3-的立体构型是
(3)CuSO4的熔点为560°C,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因是
(4)往CuSO4溶液中加入过量NaOH能生成配合物[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为(用箭头表示出配位键的位置)
(5)化学实验室常利用新制氢氧化铜检验醛基的存在,乙醛分子中碳原子的杂化方式为
(6)利用新制的Cu(OH)2检验醛基时,生成红色的Cu2O,其晶胞结构如下图所示。

该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);C为(
 ,
, ,
, )。则D原子的坐标参数为
)。则D原子的坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素原子核外有_______ 种不同运动状态的电子。

(2)如图2所示,每条折线表示周期表第ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是_______ ;判断依据是_______ 。

(3) 在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于
在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于_______ 晶体。

(4)第一电离能介于Al、P之间的第三周期元素有_______ 种。
(5)图4是碳化硅的晶胞结构。若碳化硅晶胞边长为apm,阿伏加德罗常数的值为 ,则碳化硅晶体的密度为
,则碳化硅晶体的密度为_______  (列出计算式即可)。
(列出计算式即可)。

(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素原子核外有

(2)如图2所示,每条折线表示周期表第ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(3)
 在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于
在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于
(4)第一电离能介于Al、P之间的第三周期元素有
(5)图4是碳化硅的晶胞结构。若碳化硅晶胞边长为apm,阿伏加德罗常数的值为
 ,则碳化硅晶体的密度为
,则碳化硅晶体的密度为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知A、B、C、D、E、F为元素周期表中前四周期且原子序数依次增大的六种元素.其中A、B、C、D核电荷数之和为36,A、C原子的最外层电子数之和等于B原子 的次外层电子数,D原子质子数为B原子质子数的两倍,E元素所在主族均为金属,F的价电子数与C的核电荷数相等。
(1)下列关于上述几种元素的说法正确的是_________ 。
a.B、C、D的原子半径由大到小的顺序为:D >C >B
b.E、F的最外层电子数相等
c.A、B、C、D四种元素中电负性和第一电离能最大的均为B
d.B与C形成的化合物中可能含有非极性键
e.A、C、F都位于周期表的3区
(2)B单质有两种同素异形体.其中在水中溶解度较大的是_______ (填化学式)。
(3)EA2和A2B熔点较高的是_______ (填化学式),原因是_________ 。
(4)D与B可以形成两种分子,其中DB2分子中心原子的杂化类型是____ 。下列分子或离子中与DB3结构相似的是____________ 。
a. NH3 b. SO32- c.NO3- d.PCl3
(5)已知B、F能形成两种化合物,其晶胞如下图所示.则高温时甲易转化为乙的原因为___________ 。若乙晶体密度为pg/cm3,则乙晶胞的晶胞边长a =________ nm(用含P和NA的式子表示)

(1)下列关于上述几种元素的说法正确的是
a.B、C、D的原子半径由大到小的顺序为:D >C >B
b.E、F的最外层电子数相等
c.A、B、C、D四种元素中电负性和第一电离能最大的均为B
d.B与C形成的化合物中可能含有非极性键
e.A、C、F都位于周期表的3区
(2)B单质有两种同素异形体.其中在水中溶解度较大的是
(3)EA2和A2B熔点较高的是
(4)D与B可以形成两种分子,其中DB2分子中心原子的杂化类型是
a. NH3 b. SO32- c.NO3- d.PCl3
(5)已知B、F能形成两种化合物,其晶胞如下图所示.则高温时甲易转化为乙的原因为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
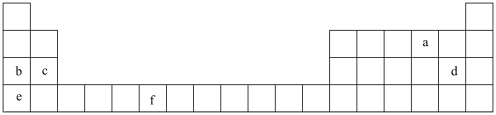
【推荐3】原子结构、元素性质、元素在周期表中的位置之间存在密切的相互关系。如图是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)a的原子结构示意图为___________ 。
(2)基态b原子核外电子占据的最高能级符号为_______ ,该能级的电子云轮廓图形状为 _______ 形。
(3)元素c位于周期表的_____ 区。
(4)元素b、d、e中电负性最大的是_______ (用元素符号表示)。
(5)基态f原子的价层电子排布式为___________ 。
(6)气态c原子失去核外不同电子所需能量如下:
①元素c的最高化合价为 _______ 。
②c原子的逐级电离能越来越大的原因是__________ 。
(1)a的原子结构示意图为
(2)基态b原子核外电子占据的最高能级符号为
(3)元素c位于周期表的
(4)元素b、d、e中电负性最大的是
(5)基态f原子的价层电子排布式为
(6)气态c原子失去核外不同电子所需能量如下:
| 电离能 | I1(第一电离能) | I2(第二电离能) | I3(第三电离能) |
| 能量/kJ•mol﹣1 | 737.7 | 1450.7 | 7732.7 |
②c原子的逐级电离能越来越大的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】臭氧(O3)在[Fe(H2O)6]2+催化下能将烟气中的SO2、NOx分别氧化为 和
和 ,NOx也可在其他条件下被还原为N2,回答下列问题:
,NOx也可在其他条件下被还原为N2,回答下列问题:
(1) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为 ___________ ; 的空间构型为
的空间构型为 ___________ (用文字描述)。
(2)Fe2+基态核外电子排布式为___________ ;[Fe(H2O)6]2+中提供孤电子对的原子是 ___________ (用元素符号表示)。
(3)N的第一电离能___________ (填“大于”或“小于”)O的第一电离能;H2SO4酸性强于H2SO3的原因是 ___________ 。
(4)①离子晶体CaC2的晶胞结构如图所示。CaC2中包含的化学键为___________ 。从钙离子看该晶体属于 ___________ 堆积,一个晶胞中含有的π键有 ___________ 个。
②图中所示晶胞中,底面边长为anm,高为bnm2晶体密度为___________ g⋅cm﹣3(NA表示阿伏加德罗常数的值,用含NA、a、b的计算式表示)。

 和
和 ,NOx也可在其他条件下被还原为N2,回答下列问题:
,NOx也可在其他条件下被还原为N2,回答下列问题:(1)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为  的空间构型为
的空间构型为 (2)Fe2+基态核外电子排布式为
(3)N的第一电离能
(4)①离子晶体CaC2的晶胞结构如图所示。CaC2中包含的化学键为
②图中所示晶胞中,底面边长为anm,高为bnm2晶体密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知可以由下列反应合成三聚氰胺:CaO+3C CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2 CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:_____ 。
CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和___ (填化学式),由此可以推知CN22-的空间构型为___ 。
(2)尿素分子中C原子采取____ 杂化。尿素分子的结构简式是____ 。
(3)三聚氰胺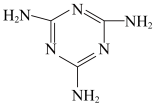 俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸
俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸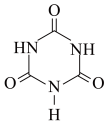 后,三聚氰酸与三聚氰胺分子相互之间通过
后,三聚氰酸与三聚氰胺分子相互之间通过____ 结合,在肾脏内易形成结石。
(4)H2与O2发生反应的过程用模型图示如下(“—”表示化学键):
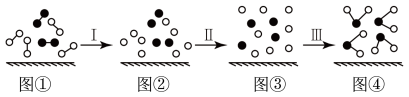
其中过程Ⅰ是___ 过程(填“吸热”、“放热”或“没有能量变化”)。图④中产生了由极性键构成的_______ 分子(填“极性”或“非极性”)。
(5)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为_____ 。
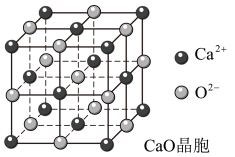
已知CaO晶体的密度为ρ,求晶胞中距离最近的两个钙离子之间的距离_____ (列出计算式)CaO晶体和NaCl晶体的晶格能分别为:CaO3401kJ·mol-1、NaCl786kJ·mol-1。导致两者晶格能差异的主要原因是________ 。
 CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2 CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:
CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和
(2)尿素分子中C原子采取
(3)三聚氰胺
 俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸
俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸 后,三聚氰酸与三聚氰胺分子相互之间通过
后,三聚氰酸与三聚氰胺分子相互之间通过(4)H2与O2发生反应的过程用模型图示如下(“—”表示化学键):

其中过程Ⅰ是
(5)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为

已知CaO晶体的密度为ρ,求晶胞中距离最近的两个钙离子之间的距离
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】稀土有“工业维生素”的美称,如今已成为极其重要的战略资源。
(1)钪(Sc)的基态原子M能层中能量不同的电子有___________ 种。
(2)铌的混合配体离子[Nd(H2O)6Cl2]+中,配体是___________ (填“微粒符号”)。
(3)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm+CH2I-CH2I→SmI2+CH2=CH2↑。CH2I-CH2I中碳原子杂化轨道类型为___________ ,1 mol CH2=CH2中含有的σ键数目为___________ 。常温下1,2-二碘乙烷为液体而乙烷为气体,其主要原因是___________ 。
(4)高温超导材料,是具有高临界转变温度,能在液氮温度条件下工作的超导材料。高温超导材料钢钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为___________ 。化合物中,稀土元素最常见的化合价是+3,但也有少数的稀土元素可以显+4价。下面四种稀土元素的电离能(单位:kJ·mol-1)数据如下表,判断最有可能显+4价的稀土元素是___________ (填元素符号)
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,则PrO2(二氧化镨)的晶胞中Pr原子的配位数为___________ 。O原子与Pr原子配位数不同,影响这一结果的是离子晶体的___________ (填“几何”“电荷”或“键性”)因素。
(6)掺杂稀土的硼化镁在39K时有超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图1是该晶体微观结构中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影。则硼化镁的化学式为___________ 。
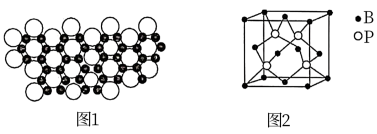
(7)磷化硼(BP)是一种有价值的超硬耐磨涂层材料,这种陶瓷材料可作为金属表面的保护薄膜。磷化硼晶胞如图2所示,在BP晶胞中B的堆积方式为___________ ,当晶胞晶格参数为478pm时,磷化硼中硼原子和磷原子之间的最近距离为___________ cm。
(1)钪(Sc)的基态原子M能层中能量不同的电子有
(2)铌的混合配体离子[Nd(H2O)6Cl2]+中,配体是
(3)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm+CH2I-CH2I→SmI2+CH2=CH2↑。CH2I-CH2I中碳原子杂化轨道类型为
(4)高温超导材料,是具有高临界转变温度,能在液氮温度条件下工作的超导材料。高温超导材料钢钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为
元素 | I1 | I2 | I3 | I4 |
Se(钪) | 633 | 1235 | 2389 | 7019 |
Y(铱) | 616 | 1181 | 1980 | 5963 |
La(镧) | 538 | 1067 | 1850 | 4819 |
Ce(铈) | 527 | 1047 | 1949 | 3547 |
(6)掺杂稀土的硼化镁在39K时有超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图1是该晶体微观结构中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影。则硼化镁的化学式为

(7)磷化硼(BP)是一种有价值的超硬耐磨涂层材料,这种陶瓷材料可作为金属表面的保护薄膜。磷化硼晶胞如图2所示,在BP晶胞中B的堆积方式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列问题
(1)四卤化硅( )的沸点和二卤化铅(
)的沸点和二卤化铅( )的熔点如图所示
)的熔点如图所示

① 的沸点依
的沸点依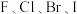 次序升高的原因是
次序升高的原因是_______ 。
②结合 的沸点和
的沸点和 的熔点变化规律,可推断:依
的熔点变化规律,可推断:依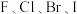 次序,
次序, 晶体中离子键百分数
晶体中离子键百分数_______ (填“增大”、“不变”或“减小”)。
(2)铍及其化合物的应用正日益被重视
①铍与相邻主族的铝元素性质相似。下列有关和铝的叙述正确的有_______ 。
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液 均小于7
均小于7
②氯化铍在气态时存在 单分子——a和二聚分子
单分子——a和二聚分子 ——b,固态时则具有如下图所示的链状结构——c
——b,固态时则具有如下图所示的链状结构——c

a属于_______ (填“极性”或“非极性”)分子,二聚分子 中
中 原子的杂化方式相同,且所有原子都在同一平面上,b的结构式为
原子的杂化方式相同,且所有原子都在同一平面上,b的结构式为_______ 。
③ 立方晶胞如下图所示。
立方晶胞如下图所示。

阿伏加德罗常数的数值为 ,若
,若 晶体的密度为
晶体的密度为 ,则
,则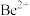 和
和 之间最近的距离为
之间最近的距离为_______  。
。
(1)四卤化硅(
 )的沸点和二卤化铅(
)的沸点和二卤化铅( )的熔点如图所示
)的熔点如图所示
①
 的沸点依
的沸点依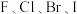 次序升高的原因是
次序升高的原因是②结合
 的沸点和
的沸点和 的熔点变化规律,可推断:依
的熔点变化规律,可推断:依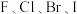 次序,
次序, 晶体中离子键百分数
晶体中离子键百分数(2)铍及其化合物的应用正日益被重视
①铍与相邻主族的铝元素性质相似。下列有关和铝的叙述正确的有
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液
 均小于7
均小于7②氯化铍在气态时存在
 单分子——a和二聚分子
单分子——a和二聚分子 ——b,固态时则具有如下图所示的链状结构——c
——b,固态时则具有如下图所示的链状结构——c
a属于
 中
中 原子的杂化方式相同,且所有原子都在同一平面上,b的结构式为
原子的杂化方式相同,且所有原子都在同一平面上,b的结构式为③
 立方晶胞如下图所示。
立方晶胞如下图所示。
阿伏加德罗常数的数值为
 ,若
,若 晶体的密度为
晶体的密度为 ,则
,则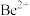 和
和 之间最近的距离为
之间最近的距离为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁元素在地壳中含量丰富,应用广泛:回答以下问题:
(1)基态Fe的价电子排布式为_____ ,其中未成对电子数目为_____ 。
(2)水溶液中Fe3+发生水解,水解过程中出现双核阳离子[Fe2(H2O)8(OH)2]4+。

①该双核阳离子中,Fe原子的配位数为_____ ,配体H2O的空间构型为_____ ,其键角_____ 109°28ˊ(填“大于”、“小于”或“等于”)。
②用KSCN可检验溶液中Fe3+的存在,lmol中SCN-中含有的π键数目为_____ NA。
(3)已知FeF3的熔点(1000℃)显著高于FeCl3的熔点(306℃),原因是_____ 。
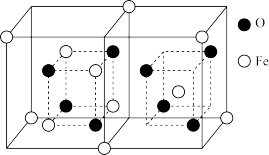
(4)铁的氧化物有多种,科研工作者常使用FexOy来表示各种铁氧化物。如图为某种铁的氧化物样品的晶胞结构,其化学式为_____ 。
(1)基态Fe的价电子排布式为
(2)水溶液中Fe3+发生水解,水解过程中出现双核阳离子[Fe2(H2O)8(OH)2]4+。

①该双核阳离子中,Fe原子的配位数为
②用KSCN可检验溶液中Fe3+的存在,lmol中SCN-中含有的π键数目为
(3)已知FeF3的熔点(1000℃)显著高于FeCl3的熔点(306℃),原因是
(4)铁的氧化物有多种,科研工作者常使用FexOy来表示各种铁氧化物。如图为某种铁的氧化物样品的晶胞结构,其化学式为

您最近一年使用:0次
【推荐3】黄铜矿(CuFeS2)是炼铜的最主要矿物。火法冶炼黄铜矿的过程中,其中一步反应是2Cu2O+Cu2S 6Cu+SO2↑。回答下列问题:
6Cu+SO2↑。回答下列问题:
(1)Cu+的价电子排布图为___________ ;Cu2O与Cu2S熔点较高的是___________ ,原因为___________ 。
(2)离子化合物CaC2的一种晶体结构如图1所示。写出该物质的电子式:___________ 。从钙离子看,属于___________ 堆积;一个晶胞含有的 键平均有
键平均有___________ 个。

(3)奥氏体是碳溶解在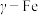 中形成的一种间隙固溶体,无磁性,其晶胞如图2所示,则该物质的化学式为
中形成的一种间隙固溶体,无磁性,其晶胞如图2所示,则该物质的化学式为___________ ,若晶体密度为 ,则晶胞中最近的两个碳原子的距离为
,则晶胞中最近的两个碳原子的距离为___________ pm (阿伏加德罗常数的值用NA表示,写出计算式即可)。
 6Cu+SO2↑。回答下列问题:
6Cu+SO2↑。回答下列问题:(1)Cu+的价电子排布图为
(2)离子化合物CaC2的一种晶体结构如图1所示。写出该物质的电子式:
 键平均有
键平均有
(3)奥氏体是碳溶解在
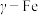 中形成的一种间隙固溶体,无磁性,其晶胞如图2所示,则该物质的化学式为
中形成的一种间隙固溶体,无磁性,其晶胞如图2所示,则该物质的化学式为 ,则晶胞中最近的两个碳原子的距离为
,则晶胞中最近的两个碳原子的距离为
您最近一年使用:0次



