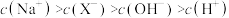25℃,用0.1 mol⋅L NaOH溶液滴定某二元弱酸
NaOH溶液滴定某二元弱酸 ,pH与粒子的分布分数δ[如
,pH与粒子的分布分数δ[如
 ],
], 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是

 NaOH溶液滴定某二元弱酸
NaOH溶液滴定某二元弱酸 ,pH与粒子的分布分数δ[如
,pH与粒子的分布分数δ[如
 ],
], 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
A. 时,应选择酚酞溶液作指示剂 时,应选择酚酞溶液作指示剂 |
B. 的数量级为 的数量级为 |
C.NaHA溶液中 |
D.Na₂A溶液中 |
2023·辽宁·三模 查看更多[4]
辽宁省农村重点高中协作校2023届高三第三次模拟考试化学试题山西省大同市2023届高三下学期三模理科综合化学试题(已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)四川省宜宾市第四中学校2023-2024学年高三上学期第二次月考理综化学试题
更新时间:2023-05-12 17:49:23
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】常温下,向20mL 0.1
 溶液中滴加0.1
溶液中滴加0.1 的NaOH溶液。有关微粒的物质的量变化如图所示(其中I表示
的NaOH溶液。有关微粒的物质的量变化如图所示(其中I表示 ,II代表
,II代表 、III代表
、III代表 ,横坐标表示加入NaOH溶液的体积)。根据图示判断下列说法不正确的是
,横坐标表示加入NaOH溶液的体积)。根据图示判断下列说法不正确的是


 溶液中滴加0.1
溶液中滴加0.1 的NaOH溶液。有关微粒的物质的量变化如图所示(其中I表示
的NaOH溶液。有关微粒的物质的量变化如图所示(其中I表示 ,II代表
,II代表 、III代表
、III代表 ,横坐标表示加入NaOH溶液的体积)。根据图示判断下列说法不正确的是
,横坐标表示加入NaOH溶液的体积)。根据图示判断下列说法不正确的是
A.滴加过程中当溶液是中性时,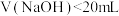 |
B.当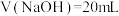 ,溶液中离子浓度的大小: ,溶液中离子浓度的大小: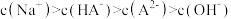 |
C. 的电离程度大于其水解程度 的电离程度大于其水解程度 |
D.当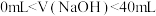 ,一定有: ,一定有: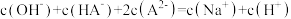 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温时,采用甲基橙和酚酞双指示剂,用盐酸滴定Na2CO3溶液,溶液中 lgc(H2CO3)、 lgc(HCO )、lgc(CO
)、lgc(CO )、lgc(H+ )、lgc(OH-)随溶液 pH 的变化及滴定曲线如图所示,下列说法不正确的是
)、lgc(H+ )、lgc(OH-)随溶液 pH 的变化及滴定曲线如图所示,下列说法不正确的是
 )、lgc(CO
)、lgc(CO )、lgc(H+ )、lgc(OH-)随溶液 pH 的变化及滴定曲线如图所示,下列说法不正确的是
)、lgc(H+ )、lgc(OH-)随溶液 pH 的变化及滴定曲线如图所示,下列说法不正确的是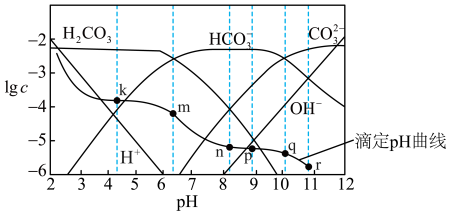
| A.整个滴定过程中可先用酚酞再用甲基橙作指示剂 |
| B.n点的pH为m点和q点pH的平均值 |
C.r点溶液中:c(OH-) = c(H+ )+c(HCO )+c(H2CO3) )+c(H2CO3) |
| D.r点到 k 点对应的变化过程中,溶液中水的电离程度一直减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】剧毒物氰化钠(NaCN)固体遇水或酸生成剧毒易燃的 HCN 气体,同时 HCN 又能与水互溶,造成水污染。已知部分弱酸的电离平衡常数如下表:
下列选项错误的是
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 |
| Ka2=5.6×10-11 |
下列选项错误的是
A.向NaCN溶液中通入少量CO2发生的离子反应为2CN-+H2O+CO2=2HCN+ |
| B.相同浓度的 HCOOH和NaCN 的溶液中,水的电离程度前者小 |
| C.中和等体积、等pH 的 HCOOH 溶液和 HCN 溶液消耗 NaOH 的物质的量前者小于后者 |
| D.等体积、等物质的量浓度的 HCOONa 和 NaCN 溶液中所含离子总数前者大于后者 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】25℃时,用HCl气体调节0.1mol/L氨水的pH,溶液中微粒浓度的对数值(lgc)、反应物的物质的量之比[ ]与pH的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法错误的是
]与pH的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法错误的是

 ]与pH的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法错误的是
]与pH的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法错误的是
A.25℃时, 的电离平衡常数为 的电离平衡常数为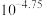 |
B.P1所示溶液: |
C.P2所示溶液: |
D.P3所示溶液: |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】室温下,向200mL 0.1 mol•L-1CH3COONa溶液中,逐渐加入0.1 mol•L-1盐酸(不考虑挥发),CH3COOH、CH3COO-物质的量随加入盐酸体积的变化关系如图所示,下列说法正确的是
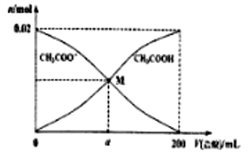
| A.随着盐酸加入,溶液中水的电离程度逐渐增大。 |
B.随着盐酸加入, 逐渐增大。 逐渐增大。 |
| C.M 点,n(H+)-n(OH-)=(a×10-4-0.01)mol |
| D.当 V(盐酸)=200mL时,c(CH3COO-)+c(CH3COOH)>c(Cl-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】向某Na2CO3、NaHCO3的混合溶液中加入少量的BaCl2,测得溶液中 与
与 的关系如图所示,下列说法正确的是
的关系如图所示,下列说法正确的是

 与
与 的关系如图所示,下列说法正确的是
的关系如图所示,下列说法正确的是
A.该溶液中 |
| B.B、D、E三点对应溶液pH的大小顺序为B>D>E |
| C.A、B、C三点对应的分散系中,A点的稳定性最差 |
| D.D点对应的溶液中一定存在2c(Ba2+ ) +c(Na+ )+c(H+ )=c(CO32- )+c(OH- )+c(Cl- ) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温下,电解质溶液中的下列关系式不正确的是
| A.已知A-+H2B(少量)==HA+HB-,则结合H+的能力: HB-<A-<B2- |
| B.在0.1mol/L的氨水中滴加0.1mol/L盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=10a-l4mol/L |
| C.将cmol/L的醋酸溶液与0.02 mol/LNaOH 溶液等体积混合后溶液恰好呈中性,用含c 的代数式表示CH3COOH 的电离常数Ka=(2×10-9)/(c-0.02) |
| D.将0.2 mol/L盐酸与0.1mol/L的KAlO2溶液等体积混合,溶液中离子浓度由大到小的顺序: c(Cl-)>c(K+)>c(Al3+ )>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】已知NaHSO3溶液呈酸性、NaHCO3溶液呈碱性。现有浓度均为0.1mol/L的的NaHSO3溶液和NaHCO3溶液,溶液中各粒子的物质的量浓度存在下列关系(R表示S或C),其中正确的是
| A.c(Na+)>c(HRO3-)>c(H+)>c(RO32-)>c(OH-) | B.c(H+)+c(H2RO3)=c(RO32-)+c(OH-) |
| C.c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-) | D.两溶液中的c(Na+)、c(HRO3-)和c(RO32-)分别相等 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温下,向1L0.1mol·L-1NH4Cl溶液中不断加入固体NaOH后,NH4+与NH3·H2O的变化趋势如右图所示(不考虑体积变化和氨的挥发),下列说法不正确的是( )

| A.M点溶液中水的电离程度比原溶液小 |
| B.在M点时,n(OH-)-n(H+)=(a-0.05)mol |
C.随着NaOH的加入,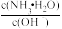 不断增大 不断增大 |
| D.当n(NaOH)=0.05mol时,溶液中有:c(Cl-)> c(NH4+)>c(Na+)>c(OH-)>c(H+) |
您最近一年使用:0次

 标准溶液滴定溶液中的
标准溶液滴定溶液中的 时,采用
时,采用 为指示剂。一定温度下,AgCl和
为指示剂。一定温度下,AgCl和 的沉淀溶解平衡曲线如图所示。下列说法不正确的是
的沉淀溶解平衡曲线如图所示。下列说法不正确的是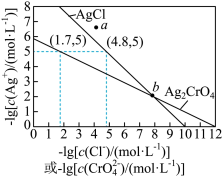
 与
与 反应生成砖红色沉淀指示滴定终点
反应生成砖红色沉淀指示滴定终点 ,
,

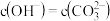
 时,
时,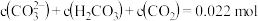
 时,溶液中不存在H2CO3分子
时,溶液中不存在H2CO3分子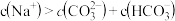
 时,用
时,用 溶液分别滴定
溶液分别滴定 、
、 、
、 三种溶液,
三种溶液, [
[ 表示负对数,
表示负对数, 表示
表示 、
、 、
、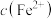 ]随
]随 的变化关系如图所示,已知:
的变化关系如图所示,已知: (不考虑二价铁被氧化)。下列说法错误的是(
(不考虑二价铁被氧化)。下列说法错误的是(
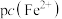 随
随 ,
, 更易溶于
更易溶于 时,可将工业废水中的
时,可将工业废水中的 沉淀完全
沉淀完全 点时,溶液中
点时,溶液中