天宫空间站有两对单翼翼展约30米的柔性太阳翼。关键部件为高性能颗粒增强铝基复合材料(SiC/Al)。请回答:
(1)基态Si的价电子轨道表示式是______ 。碳化硅的晶体类型是______ 晶体。
(2)矾土含Al3+,《诗经》言“缟衣茹蘆(茜草)”,茜草中的茜素与矾土中的Al3+、Ca2+生成的红色配合物X是最早的媒染染料。
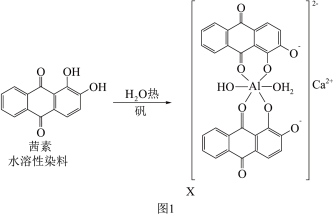
①C、N、O、Al的第一电离能从大到小的顺序为______ 。
②C的杂化轨道类型是______ 。
③茜素水溶性较好的原因是______ 。
(3)某硅、铁化合物晶胞如图2,铁有两种位置,分别用Fe1、Fe2(未画出)表示,Fe2占据硅形成的所有正四面体空隙。
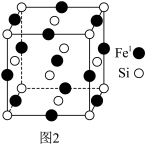
①距离Fe1最近的Fe1有______ 个。
②若将Fe1置于晶胞顶点,则位于此晶胞面心、体心的原子分别是______ 、______ (选填“Si”,“Fe1”、“Fe2”)。
③若晶胞的边长为apm,请计算该晶胞的密度为______ 。
(1)基态Si的价电子轨道表示式是
(2)矾土含Al3+,《诗经》言“缟衣茹蘆(茜草)”,茜草中的茜素与矾土中的Al3+、Ca2+生成的红色配合物X是最早的媒染染料。

①C、N、O、Al的第一电离能从大到小的顺序为
②C的杂化轨道类型是
③茜素水溶性较好的原因是
(3)某硅、铁化合物晶胞如图2,铁有两种位置,分别用Fe1、Fe2(未画出)表示,Fe2占据硅形成的所有正四面体空隙。

①距离Fe1最近的Fe1有
②若将Fe1置于晶胞顶点,则位于此晶胞面心、体心的原子分别是
③若晶胞的边长为apm,请计算该晶胞的密度为
更新时间:2023-05-22 09:10:50
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】元素周期表中所列①~⑨分别代表某种化学元素,请依据这 9 种元素回答下列问题:
(1)NA 是阿伏加德罗常数的值,下列说法正确的是___________。
(2)基态⑧原子价电子轨道表示式为___________ ,②原子和3 个⑧原子形成的分子的空间结构是___________ 。
(3)③④⑤三种元素第一电离能由大到小的排列顺序为___________ 。(用元素符号表示)
(4)关于上述 9 种元素,下列说法错误的是___________。
(5)下列相关事实内容所涉及化学知识错误的是___________。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
| ⑨ | |||||||||||||||||
(1)NA 是阿伏加德罗常数的值,下列说法正确的是___________。
| A.常温常压下,2.24L元素②形成的单质中共价键的数目为0.3NA |
| B.1mol乙醇和足量乙酸反应,生成乙酸乙酯的分子数为NA |
C.32g 环状元素⑦组成的分子(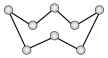 )中含有的S—S 键数为NA )中含有的S—S 键数为NA |
| D.2 mol 单质⑥中有NA个分子 |
(2)基态⑧原子价电子轨道表示式为
(3)③④⑤三种元素第一电离能由大到小的排列顺序为
(4)关于上述 9 种元素,下列说法错误的是___________。
| A.元素①属于元素周期表中 s 区元素 |
| B.元素⑦⑨组成的一种化合物可用于生产硫酸 |
| C.元素⑦的电负性大于元素⑧ |
| D.元素⑨的一种正离子可用 KSCN 溶液进行检验 |
(5)下列相关事实内容所涉及化学知识错误的是___________。
| A.医生叮嘱糖尿病患者控制白糖、红糖的摄入量——蔗糖水解能生成葡萄糖 |
| B.园艺师施肥时,草木灰和硝酸铵不混合施用——两种盐水解相互促进降低氮肥肥效 |
| C.酸雨的形成与元素②和⑦有关——形成过程都涉及了氧化还原反应 |
| D.HCl 的酸性比H2S强——元素周期律 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】铬铁合金作为钢的添加料生产多种具有高强度、耐高温、耐腐蚀等优良性能的特种钢,这类特种钢中含有碳、硅、氧、氮、磷等元素。
(1)基态Fe原子的价电子排布式为_______ 。
(2)第二周期中第一电离能介于B与N之间的元素有_______ 种。
(3)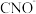 的空间构型为
的空间构型为_______ ,C的杂化方式为_______ 。
(4) 分子在独立存在时
分子在独立存在时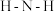 键角为
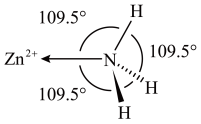
键角为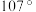 。如图是
。如图是 离子的部分结构以及
离子的部分结构以及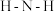 键角的测量值。解释
键角的测量值。解释 形成如图配合物后
形成如图配合物后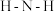 键角变大的原因:
键角变大的原因:_______ 。
(5)有机铁肥 中不存在的化学键有
中不存在的化学键有_______ 。(填字母)
A.离子键 B.金属键 C.配位键 D. 键 E.氢键
键 E.氢键
(6)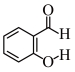 和
和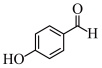 两种物质中,沸点更高的是
两种物质中,沸点更高的是 _______ (填名称)
(7)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成红色,该反应中有时用Fe(SCN)3表示形成的配合物,经研究表明Fe3+与SCN-不仅能以1:3的个数比配合,还可以以其他个数比配合。
请按要求填空:
①Fe3+与SCN-反应时,Fe3+提供_______ ,SCN-提供_______ ,二者通过配位键结合。
②所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合,所得离子显红色,含该离子的配合物化学式是_______ 。
(1)基态Fe原子的价电子排布式为
(2)第二周期中第一电离能介于B与N之间的元素有
(3)
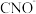 的空间构型为
的空间构型为(4)
 分子在独立存在时
分子在独立存在时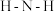 键角为
键角为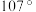 。如图是
。如图是 离子的部分结构以及
离子的部分结构以及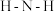 键角的测量值。解释
键角的测量值。解释 形成如图配合物后
形成如图配合物后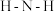 键角变大的原因:
键角变大的原因:
(5)有机铁肥
 中不存在的化学键有
中不存在的化学键有A.离子键 B.金属键 C.配位键 D.
 键 E.氢键
键 E.氢键(6)
 和
和 两种物质中,沸点更高的是
两种物质中,沸点更高的是 (7)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成红色,该反应中有时用Fe(SCN)3表示形成的配合物,经研究表明Fe3+与SCN-不仅能以1:3的个数比配合,还可以以其他个数比配合。
请按要求填空:
①Fe3+与SCN-反应时,Fe3+提供
②所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合,所得离子显红色,含该离子的配合物化学式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
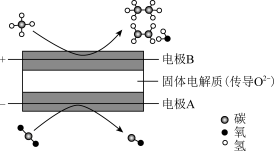
(1)C、N、O三种元素的第一电离能由大到小的顺序是_______ (填元素符号)。
(2)已知相同条件下生成乙烯和乙烷的体积比为2∶1,消耗CH4和CO2的体积比为6∶5,则生成的CO和H2O的物质的量之比为_______ 。
(3)①已知碳和硅的有关化学键键能如表所示:
简要分析乙烷的稳定性大于 的原因:
的原因:_______ 。
②如图表示碳、硅和磷三种元素的四级电离能的变化趋势,其中表示硅的曲线是_______ (填字母),判断的依据是_______ 。

(4)①通常情况下,与乙烯的沸点(-103.7℃)相比,氯乙烯(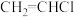 )的沸点更高(-13.9℃),其原因是
)的沸点更高(-13.9℃),其原因是_______ 。
②在乙烯中碳碳双键的键长为134pm,而在氯乙烯中碳碳双键的键长为138pm,请解释原因:____ 。

(1)C、N、O三种元素的第一电离能由大到小的顺序是
(2)已知相同条件下生成乙烯和乙烷的体积比为2∶1,消耗CH4和CO2的体积比为6∶5,则生成的CO和H2O的物质的量之比为
(3)①已知碳和硅的有关化学键键能如表所示:
| 化学键 |  |  |  | 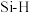 |
键能/( ) ) | 356 | 413 | 226 | 318 |
简要分析乙烷的稳定性大于
 的原因:
的原因:②如图表示碳、硅和磷三种元素的四级电离能的变化趋势,其中表示硅的曲线是

(4)①通常情况下,与乙烯的沸点(-103.7℃)相比,氯乙烯(
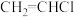 )的沸点更高(-13.9℃),其原因是
)的沸点更高(-13.9℃),其原因是②在乙烯中碳碳双键的键长为134pm,而在氯乙烯中碳碳双键的键长为138pm,请解释原因:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】近年来,我国半导体材料市场发展迅速,其中以氮化嫁、碳化硅、氧化锌、金刚石等为主的材料备受关注。回答下列问题:
(1)基态Ga原子的价电子轨道表示式为___________ ,基态N原子核外电子有___________ 种空间运动状态。Zn在元素周期表中位于___________ 区。
(2)C,N、O的第一电离能由大到小的顺序为___________ 。 的空间结构为
的空间结构为___________ 。
(3)SiC的立方晶胞结构如图1所示,已知;1号C原子的坐标参数为( ,
, ,
, ),晶胞参数为apm。则晶胞中2号C原子的坐标参数为
),晶胞参数为apm。则晶胞中2号C原子的坐标参数为___________ ,C和Si原子的最短距离为___________ pm。
①GaN晶体中N原子的杂化轨道类型为___________ 。
②GaN晶体的密度为___________ g/cm3(列出计算式,用含b、c、NA的代数式表示)。
(1)基态Ga原子的价电子轨道表示式为
(2)C,N、O的第一电离能由大到小的顺序为
 的空间结构为
的空间结构为(3)SiC的立方晶胞结构如图1所示,已知;1号C原子的坐标参数为(
 ,
, ,
, ),晶胞参数为apm。则晶胞中2号C原子的坐标参数为
),晶胞参数为apm。则晶胞中2号C原子的坐标参数为
①GaN晶体中N原子的杂化轨道类型为
②GaN晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】石墨插层化合物在电池材料、超导性等方面具有广泛的应用前景。回答下列问题:
I.某种锂离子电池以石墨(平面结构如图1所示)做负极材料,LiNiO2做正极材料。
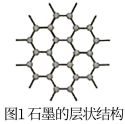
(1)石墨中碳的杂化类型是_______ ,在层中碳原子的配位数为_______ 。
(2)LiNiO2中电负性最大的元素是_______ 。
(3)基态Ni3+核外电子排布式为_______ ,其未成对电子数为_______ 。
II.下表列举了部分碳族晶体的熔点、硬度数据:
(4)请解释金刚石、碳化硅、晶体硅的硬度逐渐变小的原因是_______ 。
III.钾(K)的石墨插层化合物具有超导性,图甲为其晶胞图。其中K层平行于石墨层,该晶胞垂直于石墨层方向的原子投影如图乙所示。

(5)该插层化合物的化学式是_______ ,判断K层与石墨层之间的化学键类型为_______ (选填“离子键”“共价键”);若晶胞参数分别为a nm、a nm、b nm,则该石墨插层化合物的晶胞密度为_______  。(用含a、b、NA的代数式表示)
。(用含a、b、NA的代数式表示)
I.某种锂离子电池以石墨(平面结构如图1所示)做负极材料,LiNiO2做正极材料。

(1)石墨中碳的杂化类型是
(2)LiNiO2中电负性最大的元素是
(3)基态Ni3+核外电子排布式为
II.下表列举了部分碳族晶体的熔点、硬度数据:
| 晶体 | 熔点/℃ | 硬度(数值越大,晶体的硬度越大) |
| 金刚石(C) | 大于3500 | 10 |
| 碳化硅(SiC) | 2830 | 9 |
| 晶体硅(Si) | 1412 | 7 |
(4)请解释金刚石、碳化硅、晶体硅的硬度逐渐变小的原因是
III.钾(K)的石墨插层化合物具有超导性,图甲为其晶胞图。其中K层平行于石墨层,该晶胞垂直于石墨层方向的原子投影如图乙所示。

(5)该插层化合物的化学式是
 。(用含a、b、NA的代数式表示)
。(用含a、b、NA的代数式表示)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】有机—无机复合钙钛矿( )型材料在太阳能电池及发光二极管等方面具有很好的应用前景,一种复合材料和
)型材料在太阳能电池及发光二极管等方面具有很好的应用前景,一种复合材料和 (立方晶系)的晶胞结构如图所示。
(立方晶系)的晶胞结构如图所示。
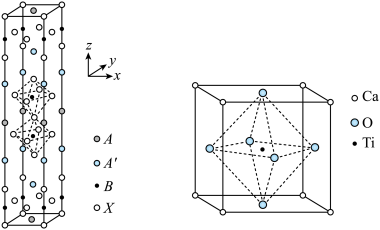
已知:A为间隔的阳离子,例如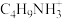 、
、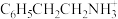 等;A'为单一组分钙钛阳离子,例如
等;A'为单一组分钙钛阳离子,例如 、
、 、
、 等;B为单一组分钙钛矿中心离子
等;B为单一组分钙钛矿中心离子 、
、 等,X为单一组分钙钛矿的阴离子,例如
等,X为单一组分钙钛矿的阴离子,例如 、
、 或
或 等卤素离子。
等卤素离子。
回答下列问题:
(1)基态Ti原子的价电子排布式为___________ 。
(2)H、C、N、O四种元素电负性由大到小的顺序为___________ ;第一电离能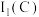 、
、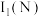 、
、 由大到小的顺序为
由大到小的顺序为___________ 。
(3) 中C的杂化方式为
中C的杂化方式为___________ ;正丁胺(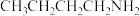 )的沸点为77.8℃,正丁醇(
)的沸点为77.8℃,正丁醇( )的沸点为117.6℃,正丁胺沸点低的原因是
)的沸点为117.6℃,正丁胺沸点低的原因是___________ 。
(4) 中Ca的配位数为
中Ca的配位数为___________ ;A为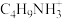 ,A'为
,A'为 ,B为
,B为 ,X为
,X为 ,晶胞参数为a nm和c nm,该晶体的密度为
,晶胞参数为a nm和c nm,该晶体的密度为___________  。
。
 )型材料在太阳能电池及发光二极管等方面具有很好的应用前景,一种复合材料和
)型材料在太阳能电池及发光二极管等方面具有很好的应用前景,一种复合材料和 (立方晶系)的晶胞结构如图所示。
(立方晶系)的晶胞结构如图所示。
已知:A为间隔的阳离子,例如
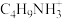 、
、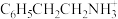 等;A'为单一组分钙钛阳离子,例如
等;A'为单一组分钙钛阳离子,例如 、
、 、
、 等;B为单一组分钙钛矿中心离子
等;B为单一组分钙钛矿中心离子 、
、 等,X为单一组分钙钛矿的阴离子,例如
等,X为单一组分钙钛矿的阴离子,例如 、
、 或
或 等卤素离子。
等卤素离子。回答下列问题:
(1)基态Ti原子的价电子排布式为
(2)H、C、N、O四种元素电负性由大到小的顺序为
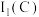 、
、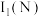 、
、 由大到小的顺序为
由大到小的顺序为(3)
 中C的杂化方式为
中C的杂化方式为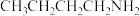 )的沸点为77.8℃,正丁醇(
)的沸点为77.8℃,正丁醇( )的沸点为117.6℃,正丁胺沸点低的原因是
)的沸点为117.6℃,正丁胺沸点低的原因是(4)
 中Ca的配位数为
中Ca的配位数为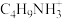 ,A'为
,A'为 ,B为
,B为 ,X为
,X为 ,晶胞参数为a nm和c nm,该晶体的密度为
,晶胞参数为a nm和c nm,该晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】葡萄糖酸锌(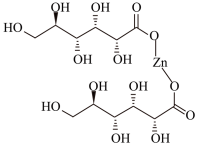 )为有机锌补剂,对胃黏膜刺激小,在体内易被人体吸收,且吸收率高,溶解性好。回答下列问题:
)为有机锌补剂,对胃黏膜刺激小,在体内易被人体吸收,且吸收率高,溶解性好。回答下列问题:
(1)锌元素位于元素周期表_______ 区,锌离子的价电子排布式为_______ 。
(2)葡萄糖酸锌组成元素中电负性最强的元素为_______ ,该元素的单质中属于极性分子的是_______ 。
(3)葡萄糖酸中C原子的杂化方式为_______ ,1 mol葡萄糖分子中含有_______ mol  键。
键。
(4)葡萄糖酸锌溶于氨水能生成 ,离子中配体为
,离子中配体为_______ ,与配体空间构型相同的阳离子为_______ 。
(5)葡萄糖酸易溶于水的原因是_______ ,葡萄糖酸的熔点_______ (填“大于”“小于”或“等于”)葡萄糖酸锌的熔点。
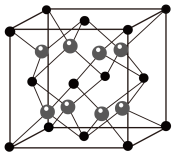
(6)若用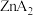 代表葡萄糖酸锌(相对分子质量为456),其晶胞结构如图所示,若晶胞参数为a nm,晶体密度为
代表葡萄糖酸锌(相对分子质量为456),其晶胞结构如图所示,若晶胞参数为a nm,晶体密度为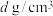 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为_______ (列出计算式即可)。
 )为有机锌补剂,对胃黏膜刺激小,在体内易被人体吸收,且吸收率高,溶解性好。回答下列问题:
)为有机锌补剂,对胃黏膜刺激小,在体内易被人体吸收,且吸收率高,溶解性好。回答下列问题:(1)锌元素位于元素周期表
(2)葡萄糖酸锌组成元素中电负性最强的元素为
(3)葡萄糖酸中C原子的杂化方式为
 键。
键。(4)葡萄糖酸锌溶于氨水能生成
 ,离子中配体为
,离子中配体为(5)葡萄糖酸易溶于水的原因是
(6)若用
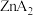 代表葡萄糖酸锌(相对分子质量为456),其晶胞结构如图所示,若晶胞参数为a nm,晶体密度为
代表葡萄糖酸锌(相对分子质量为456),其晶胞结构如图所示,若晶胞参数为a nm,晶体密度为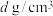 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】纳米磷化钴(CoP)常用于制作特种钻玻璃,制备磷化钴的常用流程如下:

(l)基态P原子的价电子排布式为____ ,P位于元素周期表中____ 区。
(2)尿素中N原子的杂化类型是_____ ;C、N、O三种元素的第一电离能最大的是____ ,电负性由小到大的顺序为____ 。
(3)Co(CO3)0.5(OH)·0.11H2O中CO32-中C的价层电子对数为____ ;该化合物中不含有的化学键有_____ 填标号)。
A 离子键 B 共价键 C 金属键 D 配位键 E 氢键 F 非极性键
(4)一些氧化物的熔点如下表所示:
解释表中氧化物之间熔点差异的原因____ 。
(5)CoP的晶胞结构如图所示,最近且相邻两个钴原子的距离为npm。

设NA为阿伏加 德罗常数的值,则其晶胞密度为_______ -g.cm-3(列出计算式即可)。

(l)基态P原子的价电子排布式为
(2)尿素中N原子的杂化类型是
(3)Co(CO3)0.5(OH)·0.11H2O中CO32-中C的价层电子对数为
A 离子键 B 共价键 C 金属键 D 配位键 E 氢键 F 非极性键
(4)一些氧化物的熔点如下表所示:
| 氧化物 | Fe3O4 | Co3O4 | FeCl3 |
熔点/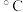 | 1594.5 | 895 | 306 |
(5)CoP的晶胞结构如图所示,最近且相邻两个钴原子的距离为npm。

设NA为阿伏加 德罗常数的值,则其晶胞密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】钾和碘的相关化合物在化工、医药、材料等领域有广泛的应用。回答下列问题:
(1)钾元素的焰色为紫色,其微观原因是___________ 。
(2)碘原子中,占据最高能级的电子的电子云轮廓图形状为___________ 。
(3)请比较KI与KCl晶体的熔点高低___________ ,并说明理由:___________ 。
(4) 常用作食盐添加剂,其晶胞如图所示。
常用作食盐添加剂,其晶胞如图所示。
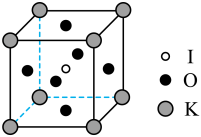
已知 晶胞的边长为apm,晶胞中K、I、O原子分别处于顶角、体心、面心位置。
晶胞的边长为apm,晶胞中K、I、O原子分别处于顶角、体心、面心位置。
则每个K原子周围距离最短的O原子有___________ 个。该晶胞的密度为___________  。
。
(5) 处于
处于 的中心,若将配离子
的中心,若将配离子 中的2个
中的2个 换为
换为 ,则有2种结构,则
,则有2种结构,则 是否为
是否为 杂化?
杂化?___________ (填“是”或“否”), 的空间构型为
的空间构型为___________ 。
(1)钾元素的焰色为紫色,其微观原因是
(2)碘原子中,占据最高能级的电子的电子云轮廓图形状为
(3)请比较KI与KCl晶体的熔点高低
(4)
 常用作食盐添加剂,其晶胞如图所示。
常用作食盐添加剂,其晶胞如图所示。
已知
 晶胞的边长为apm,晶胞中K、I、O原子分别处于顶角、体心、面心位置。
晶胞的边长为apm,晶胞中K、I、O原子分别处于顶角、体心、面心位置。则每个K原子周围距离最短的O原子有
 。
。(5)
 处于
处于 的中心,若将配离子
的中心,若将配离子 中的2个
中的2个 换为
换为 ,则有2种结构,则
,则有2种结构,则 是否为
是否为 杂化?
杂化? 的空间构型为
的空间构型为
您最近一年使用:0次



