处理某铜冶金污水(含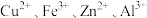 )的部分流程如下:
)的部分流程如下: 如下表所示:
如下表所示:
②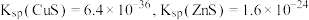 。
。
下列说法错误的是
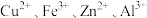 )的部分流程如下:
)的部分流程如下: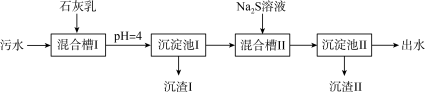
 如下表所示:
如下表所示:| 物质 |  |  |  |  |
开始沉淀 | 1.9 | 4.2 | 6.2 | 3.5 |
完全沉淀 | 3.2 | 6.7 | 8.2 | 4.6 |
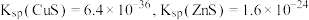 。
。下列说法错误的是
A.“沉渣Ⅰ”中含有 和 和 |
B. 溶液呈碱性,其主要原因是 溶液呈碱性,其主要原因是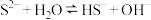 |
C.“沉淀池Ⅱ”中,当 和 和 完全沉淀时,溶液中 完全沉淀时,溶液中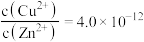 |
| D.“出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水 |
2023·湖南·高考真题 查看更多[18]
2023年高考湖南卷化学真题(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡(已下线)2023年湖南卷高考真题变式题(选择题6-10)(已下线)专题07 无机物的转化 微型工艺流程-2023年高考化学真题题源解密(全国通用)(已下线)选择题11-13安徽省六安第一中学2022-2023学年高二下学期期末考试化学试题(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第32讲难溶电解质的溶解平衡浙江省杭州第十四中学2023-2024学年高二上学期 期中考试化学试卷福建省厦门市 第一中学2023-2024上学期高三上学期12月考化学试题(已下线)难溶电解质的溶解平衡江西省宜春市宜丰中学2023-2024学年高三上学期12月月考化学试题(已下线)专题06 沉淀溶解平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)题型15 沉淀溶解平衡及图像分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)10-2023新东方高二上期中考化学2024届河北省部分示范性高中2023-2024学年高三下学期一模化学试题河北省2024届高三下学期3月大数据应用调研联合测评(六)化学试题
更新时间:2023-06-16 13:57:34
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列离子方程式书写错误的是
A.Na2CO3溶液呈碱性的原因: |
B.HF溶液和NaHCO3溶液混合: |
C.FeCl3溶于水形成胶体: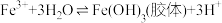 |
D.NaClO溶液中通入足量CO2: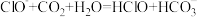 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列化学用语正确的是
A.KHSO4在熔融态的电离方程式为: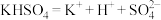 |
B.草酸根的水解方程式为: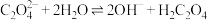 |
C.用电子式表示溴化氢分子的形成过程为: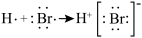 |
D.水的电离方程式为: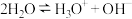 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,用Na2S沉淀Cu2+、Zn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示,下列说法不正确的是( )
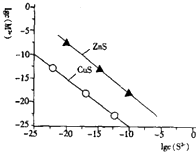

| A.向Cu2+浓度为10-5mol•L-1的工业废水中加入ZnS粉末,会有CuS沉淀析出 |
| B.25℃时K甲(CuS)约为1×10-35 |
| C.向100mLZn2+、Cu2+浓度均为10-5mol•L-1的混合溶液中逐滴加入10-4 mol•L-1的Na2S溶液,Cu2+先沉淀 |
| D.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)═2c(Na+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】还原沉淀法是处理含铬(含 和
和 )工业废水的常用方法,过程如下:
)工业废水的常用方法,过程如下:

已知转化过程中的反应为2 (aq)+2H+(aq)
(aq)+2H+(aq)
 (aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6g/L,
(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6g/L, 有
有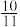 转化为
转化为 ,下列说法不正确的是
,下列说法不正确的是
 和
和 )工业废水的常用方法,过程如下:
)工业废水的常用方法,过程如下:
已知转化过程中的反应为2
 (aq)+2H+(aq)
(aq)+2H+(aq)
 (aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6g/L,
(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6g/L, 有
有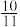 转化为
转化为 ,下列说法不正确的是
,下列说法不正确的是| A.溶液颜色保持不变,说明上述可逆反应达到平衡状态 |
| B.若用绿矾(FeSO4·7H2O)作还原剂,处理1L废水,至少需要917.4g |
| C.常温下转化反应的平衡常数K=l×1014.则转化后所得溶液的pH=6 |
| D.常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】高纯碳酸锰在电子工业中有着重要的应用,湿法浸出软锰矿(主要成分为MnO2,含有少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的流程如下:其中除杂过程包括:①向浸出液中加入一定量的试剂X,调节浸出液的pH为3.5~5.5;②再加入一定量的软锰矿和双氧水,过滤;③…下列说法正确的是(已知室温下:Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3.0×10-34,Ksp[Fe(OH)3]=4.0×10-38。)


| A.浸出时加入植物粉的作用是作为还原剂 |
| B.除杂过程中调节浸出液的pH为3.5~5.5可完全除去Fe、Al、Mg等杂质 |
| C.试剂X可以是MnO、MnO2、MnCO3等物质 |
| D.为提高沉淀MnCO3步骤的速率可以持续升高温度 |
您最近一年使用:0次




 HCO
HCO + OH-
+ OH- 

