喹啉(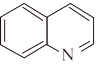 )在医药上主要用于制造烟酸系、8-羟基喹啉系和奎宁系三大类药物。其中8-羟基喹啉系可用于制造医治阿米巴虫病用药和创伤消毒剂以及防霉剂和纺织助剂等。回答下列问题:
)在医药上主要用于制造烟酸系、8-羟基喹啉系和奎宁系三大类药物。其中8-羟基喹啉系可用于制造医治阿米巴虫病用药和创伤消毒剂以及防霉剂和纺织助剂等。回答下列问题:
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为 ,喹啉分子中存在的大π键可表示为
,喹啉分子中存在的大π键可表示为(2)喹啉分子中
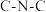 之间的键角
之间的键角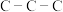 之间的键角(填“>”、“<”或“=”),原因是
之间的键角(填“>”、“<”或“=”),原因是(3)8-羟基喹啉(
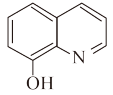 )的熔点明显低于7-羟基喹啉(
)的熔点明显低于7-羟基喹啉( )和6-羟基喹啉(
)和6-羟基喹啉( )的原因是
)的原因是(4)8-羟基喹啉与四氯化锗可制备印迹聚合物。基态
 原子价电子排布式为
原子价电子排布式为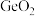 不能形成类似
不能形成类似 分子中的π键,原因是
分子中的π键,原因是
更新时间:2023-07-18 11:52:22
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】我国的天宫空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。
(1)镓的原子结构示意图为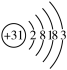 ,其在元素周期表中的位置是
,其在元素周期表中的位置是___________ 。
(2)GaAs熔融状态不能导电,据此判断它可能是___________ (填“共价”或“离子”)化合物。
(3) 基态As原子电子排布式为___________ ;电子占据最高能级的电子云轮廓图为___________ 形。
(4)As与P同族且相邻。磷的最外层电子的轨道表示式为___________ 。
(5)As与Se同周期且相邻,第一电离能As___________ Se;电负性As___________ Se(填“>”或“<”)。
(6) 用
用 还原生成
还原生成 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为___________ , 沸点比
沸点比 的
的___________ (填“高”或“低”),原因是:___________ 。
(1)镓的原子结构示意图为
 ,其在元素周期表中的位置是
,其在元素周期表中的位置是(2)GaAs熔融状态不能导电,据此判断它可能是
(3) 基态As原子电子排布式为
(4)As与P同族且相邻。磷的最外层电子的轨道表示式为
(5)As与Se同周期且相邻,第一电离能As
(6)
 用
用 还原生成
还原生成 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为 沸点比
沸点比 的
的
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】翡翠的主要成分为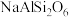 ,还含有其他多种金属阳离子。
,还含有其他多种金属阳离子。
(1)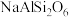 所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物的名称为:
所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物的名称为:___________ 。
(2)Al的电子排布式为___________ 。
(3)配合物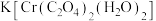 中的配体是:
中的配体是:___________ ,Cr的价层电子的电子排布图:___________ 。
(4)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中 ,
, 采用面心立方最密堆积方式。
采用面心立方最密堆积方式。

①该晶体的化学式为:___________ 。
②已知钙离子、氧离子半径分别为apm、bpm,该晶胞的参数(边长)为___________ pm。
(5)Ga可以形成 等一系列配位数为6的配合物,向上述某物质的溶液中加入足量
等一系列配位数为6的配合物,向上述某物质的溶液中加入足量 溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2.则该溶液中溶质的化学式为
溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2.则该溶液中溶质的化学式为___________ 。
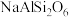 ,还含有其他多种金属阳离子。
,还含有其他多种金属阳离子。(1)
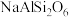 所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物的名称为:
所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物的名称为:(2)Al的电子排布式为
(3)配合物
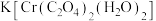 中的配体是:
中的配体是:(4)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中
 ,
, 采用面心立方最密堆积方式。
采用面心立方最密堆积方式。
①该晶体的化学式为:
②已知钙离子、氧离子半径分别为apm、bpm,该晶胞的参数(边长)为
(5)Ga可以形成
 等一系列配位数为6的配合物,向上述某物质的溶液中加入足量
等一系列配位数为6的配合物,向上述某物质的溶液中加入足量 溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2.则该溶液中溶质的化学式为
溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2.则该溶液中溶质的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】有A、B、C、D、E五种元素。其相关信息如下:
回答下列问题:
(1)写出元素符号B:_______ ,C:_______ ,E:_______ 。
(2)F元素可形成F2+和F3+,其中较稳定的是F3+,原因是_______ 。
(3)A和C形成的18电子分子的结构式_______ 。
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有_______ (填序号)。
①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键
[E(CA3)4]2+具有对称的空间构型,若[E(CA3)4]2+中的两个CA3被两个其他基团取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为_______ (填字母)。
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)早在西汉时期的《淮南万毕术》中就记载“曾青得铁则化为铜”,这是有关“湿法炼铜”的最早文献记录。若向盛装有硫酸铜水溶液的试管里加入氨水,首先生成蓝色沉淀,继续滴加氨水,得到深蓝色的透明溶液。请写出蓝色沉淀溶解的离子反应方程式:_______ 。
| 元素 | 相关信息 |
| A | A原子的1s轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道中有三个未成对电子 |
| D | D是主族元素且与E同周期,其最外能层上有两个运动状态不同的电子 |
| E | E能与氧形成砖红色E2O和黑色的EO两种氧化物 |
| F | 基态原子3d能级上有6个电子 |
(1)写出元素符号B:
(2)F元素可形成F2+和F3+,其中较稳定的是F3+,原因是
(3)A和C形成的18电子分子的结构式
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有
①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键
[E(CA3)4]2+具有对称的空间构型,若[E(CA3)4]2+中的两个CA3被两个其他基团取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)早在西汉时期的《淮南万毕术》中就记载“曾青得铁则化为铜”,这是有关“湿法炼铜”的最早文献记录。若向盛装有硫酸铜水溶液的试管里加入氨水,首先生成蓝色沉淀,继续滴加氨水,得到深蓝色的透明溶液。请写出蓝色沉淀溶解的离子反应方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】今有A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子数之和;C元素是第三周期第一电离能最小的元素;D元素在第三周期中电负性最大.
(1)试推断A、B、C、D四种元素的符号:A________ 、B________ 、C________ 、D________ .
(2)写出A元素原子的核外电子排布式:____________ ;写出B元素原子核外电子排布的价电子排布式:__________ ;用电子排布图表示C原子的核外电子排布情况:_______________ .
(1)试推断A、B、C、D四种元素的符号:A
(2)写出A元素原子的核外电子排布式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】已知元素D、E、G、M、Q的原子序数依次增大,D元素是形成化合物种类最多的元素,G元素的族序数是周期数的三倍,M元素为地壳含量排第二位的金属元素,常温下Q单质为红棕色液体。请按要求回答下列几个问题:
(1)元素D的基态原子核外电子排布式为:___________ ;元素Q的基态原子的价电子排布式为:___________ 。
(2)元素M的原子结构示意图为___________ ,其位于周期表第四周期,第___________ 族。
(3)D、E、G的最简单氢化物的稳定性由强到弱的为:___________ (用对应的化学式表示)
(1)元素D的基态原子核外电子排布式为:
(2)元素M的原子结构示意图为
(3)D、E、G的最简单氢化物的稳定性由强到弱的为:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】已知A、B、C、D、E、F是前四周期的核电荷数依次增大主族元素,A的最外层电子数是其电子层数的2倍,C、D同一主族,D元素原子M层有两对成对电子,E在前四周期主族元素中原子半径最大,F的基态原子中有4个未成对电子。
(1)基态Fe2+的电子排布式是_____ 。
(2)B、C、D的第一电离能由大到小的顺序是_____ 。(填字母对应的元素符号)
(3)BC 离子的空间构型为
离子的空间构型为_____ 。
(4)某F的配合物化学式是[F(H2O)5Cl]Cl2·H2O,与中心F3+的形成配位键的原子或离子是_____ 。
(5)F(AC)5常温下是一种浅黄色液体,熔点-20℃,不溶于水、易溶于苯。
每个AC分子与F原子间均有1个配位键。
①1 mol F(AC)5中所含σ键的数目为_____ 。
②F(AC)5分子的结构可能为下图中的_____ (填“甲”或“乙”)
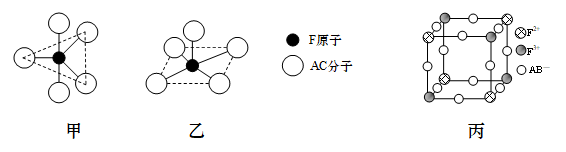
(6)由A、B、E、F元素形成的一种蓝色晶体,其晶体结构示意图如图丙所示(图中E的离子未画出)。该蓝色晶体的化学式为_____ 。
(1)基态Fe2+的电子排布式是
(2)B、C、D的第一电离能由大到小的顺序是
(3)BC
 离子的空间构型为
离子的空间构型为(4)某F的配合物化学式是[F(H2O)5Cl]Cl2·H2O,与中心F3+的形成配位键的原子或离子是
(5)F(AC)5常温下是一种浅黄色液体,熔点-20℃,不溶于水、易溶于苯。
每个AC分子与F原子间均有1个配位键。
①1 mol F(AC)5中所含σ键的数目为
②F(AC)5分子的结构可能为下图中的

(6)由A、B、E、F元素形成的一种蓝色晶体,其晶体结构示意图如图丙所示(图中E的离子未画出)。该蓝色晶体的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】短周期的5种非金属元素,其中A、B、C的特征电子排布可表示为A:asa,B:bsbbpb,C:csccp2c,D与B同主族,E在C的下一周期,且是同周期元素中电负性最大的元素。回答下列问题:
(1)由A、B、C、E四种元素中的两种元素可形成多种分子,下列分子①BC2②BA4③A2C2④BE4,其中属于极性分子的是___ (填序号);分子BC2中含σ键__ 个,含π键__ 个。
(2)C的氢化物比下一周期同族元素的氢化物沸点还要高,其原因是__ 。
(3)B、C两元素都能和A元素组成两种常见的溶剂,其分子式为___ 、__ 。DE4在前者中的溶解度__ (填“大于”或“小于”)在后者中的溶解度。
(4)BA4、BE4和DE4的沸点从高到低的顺序为__ (填化学式)。
(1)由A、B、C、E四种元素中的两种元素可形成多种分子,下列分子①BC2②BA4③A2C2④BE4,其中属于极性分子的是
(2)C的氢化物比下一周期同族元素的氢化物沸点还要高,其原因是
(3)B、C两元素都能和A元素组成两种常见的溶剂,其分子式为
(4)BA4、BE4和DE4的沸点从高到低的顺序为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】短周期元素X、Y、Z、W、Q的原子序数依次增大,Z的原子半径是短周期主族元素中最大的,X、Y、W、Q在元素周期表中的位置如表所示,Y、Q的原子序数之和是X的4倍。回答下列问题:
(1)X元素在周期表中的位置为_______ ,Y的简单氢化物的沸点高于Q的简单氢化物的沸点的原因是_______ 。
(2)Y、Z、Q三种元素所形成的简单离子,半径由大到小的顺序是_______ (填化学式,下同)。
(3)X与Y按原子数之比为1:2形成化合物的电子式为_______ ,Y与Z形成的一种化合物是淡黄色固体,该化合物中所含化学键的类型是_______ 。
(4)以KOH稀溶液作电解质溶液,石墨作电极,X的简单氢化物甲和Y的双原子分子乙可组成燃料电池,其工作原理如图所示。电池工作时,a极的电极反应式为_______ 。

| X | Y | |
| W | Q |
(1)X元素在周期表中的位置为
(2)Y、Z、Q三种元素所形成的简单离子,半径由大到小的顺序是
(3)X与Y按原子数之比为1:2形成化合物的电子式为
(4)以KOH稀溶液作电解质溶液,石墨作电极,X的简单氢化物甲和Y的双原子分子乙可组成燃料电池,其工作原理如图所示。电池工作时,a极的电极反应式为

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为65,中子数为35.请回答下列问题:
(1)AY2是一种常用的溶剂,为_____________ 分子(填“极性”或“非极性”),分子中存在___________ 个σ键。
(2)X形成的单质与NaOH溶液反应的离子方程式为______________________________ ,超高导热绝缘耐高温纳米XB在绝缘材料中应用广泛,其晶体与金刚石类似,属于____ 晶体。
(3)X、氧、B元素的电负性由大到小的顺序为_______________ (用元素符号作答)。
(4)Z的基态原子核外电子排布式为___________________________ 。
(1)AY2是一种常用的溶剂,为
(2)X形成的单质与NaOH溶液反应的离子方程式为
(3)X、氧、B元素的电负性由大到小的顺序为
(4)Z的基态原子核外电子排布式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】(1)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是_______ (用元素符号表示)
(2)A、B、C为同一短周期金属元素。依据下表数据分析,C元素在化合物中的主要化合价为______ ;第二电离能(I2)B小于A的原因是___________________ 。
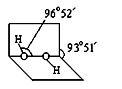
(3)已知过氧化氢分子的空间结构如右图所示,分子中氧原子采取______ 杂化;通常情况下,H2O2与水任意比互溶的主要原因是_____________ 。
(4)R是1~36号元素中未成对电子数最多的原子。R3+在溶液中存在如下转化关系:
R3+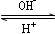 R(OH)3
R(OH)3 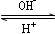 [R(OH)4]-
[R(OH)4]-
①基态R原子的价电子排布式为___________________ 。
②[R(OH)4]-中存在的化学键是___________ 。
A.离子键 B.极性键 C.非极性键 D.配位键
(2)A、B、C为同一短周期金属元素。依据下表数据分析,C元素在化合物中的主要化合价为
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 500 | 4600 | 6900 | 9500 |
| B | 740 | 1500 | 7700 | 10500 |
| C | 580 | 1800 | 2700 | 11600 |
(3)已知过氧化氢分子的空间结构如右图所示,分子中氧原子采取

(4)R是1~36号元素中未成对电子数最多的原子。R3+在溶液中存在如下转化关系:
R3+
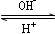 R(OH)3
R(OH)3 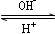 [R(OH)4]-
[R(OH)4]-①基态R原子的价电子排布式为
②[R(OH)4]-中存在的化学键是
A.离子键 B.极性键 C.非极性键 D.配位键
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】过渡金属铬、铅、镍、铁及其化合物在工业上有重要用途,回答下列问题:
(1)基态Cr原子的价层电子的轨道表示式为___________ 。
(2)氮化铬(CrN)在超级电容器领域具有良好的应用前景,可由 与尿素[
与尿素[ ]反应先得到配合物
]反应先得到配合物 ,然后正通有
,然后正通有 和
和 混合气体的反应炉内热分解制得。
混合气体的反应炉内热分解制得。
①尿素中C、N、O三种元素的第一电离能由大到小的顺序为___________ 。
② 中存在的化学键有
中存在的化学键有___________ (填字母)。
A.极性共价键 B.非极性共价键 C.氢键 D.配位键
(3)四卤化硅 的沸点和二卤化铅
的沸点和二卤化铅 的熔点如图所示:
的熔点如图所示: 的沸点依F、Cl、Br、I次序升高的原因是
的沸点依F、Cl、Br、I次序升高的原因是___________ 。
②请解释 随原子序数的递增熔点变化的原因
随原子序数的递增熔点变化的原因___________ 。
(4)丁二酮肟常与 形成图A所示的配合物,图B是图A中硫代氧后的结构简式:
形成图A所示的配合物,图B是图A中硫代氧后的结构简式:___________ 。
(1)基态Cr原子的价层电子的轨道表示式为
(2)氮化铬(CrN)在超级电容器领域具有良好的应用前景,可由
 与尿素[
与尿素[ ]反应先得到配合物
]反应先得到配合物 ,然后正通有
,然后正通有 和
和 混合气体的反应炉内热分解制得。
混合气体的反应炉内热分解制得。①尿素中C、N、O三种元素的第一电离能由大到小的顺序为
②
 中存在的化学键有
中存在的化学键有A.极性共价键 B.非极性共价键 C.氢键 D.配位键
(3)四卤化硅
 的沸点和二卤化铅
的沸点和二卤化铅 的熔点如图所示:
的熔点如图所示:
 的沸点依F、Cl、Br、I次序升高的原因是
的沸点依F、Cl、Br、I次序升高的原因是②请解释
 随原子序数的递增熔点变化的原因
随原子序数的递增熔点变化的原因(4)丁二酮肟常与
 形成图A所示的配合物,图B是图A中硫代氧后的结构简式:
形成图A所示的配合物,图B是图A中硫代氧后的结构简式: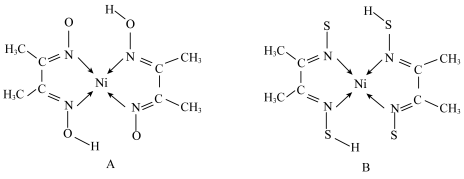
您最近一年使用:0次



