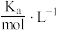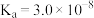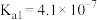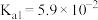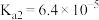表是25℃时某些弱酸的电离平衡常数。
(1)pH相同的NaClO和 溶液,其溶液的物质的量浓度的大小关系是
溶液,其溶液的物质的量浓度的大小关系是
______ NaClO(填“ ”“
”“ ”或“
”或“ ”,下同),两溶液中:
”,下同),两溶液中:
______  。
。
(2)若
 溶液与
溶液与 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的
NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的 ,则
,则
______ 。
(3)取10mL 的
的 溶液,加入少量无水醋酸钠固体(假设加入固体前后溶液体积保持不变),待固体溶解后,溶液中
溶液,加入少量无水醋酸钠固体(假设加入固体前后溶液体积保持不变),待固体溶解后,溶液中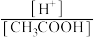 的比值将
的比值将______ (填“增大”“减小”或“无法确定”)。
(4)向碳酸钠溶液中滴加少量氯水的离子方程式______ 。
化学式 |
|
|
|
|
|
|
|
|
|
 溶液,其溶液的物质的量浓度的大小关系是
溶液,其溶液的物质的量浓度的大小关系是
 ”“
”“ ”或“
”或“ ”,下同),两溶液中:
”,下同),两溶液中:
 。
。(2)若

 溶液与
溶液与 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的
NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的 ,则
,则
(3)取10mL
 的
的 溶液,加入少量无水醋酸钠固体(假设加入固体前后溶液体积保持不变),待固体溶解后,溶液中
溶液,加入少量无水醋酸钠固体(假设加入固体前后溶液体积保持不变),待固体溶解后,溶液中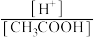 的比值将
的比值将(4)向碳酸钠溶液中滴加少量氯水的离子方程式
更新时间:2023-06-25 21:12:49
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按要求回答下列问题:
(1)向 醋酸溶液中加入少量水,
醋酸溶液中加入少量水,
_____ (填“增大”“减小”或“不变”,下同),
_____ 。
(2)500mL 醋酸溶液a、500mL
醋酸溶液a、500mL 盐酸溶液b分别与足量Zn粉充分反应,初始反应速率a
盐酸溶液b分别与足量Zn粉充分反应,初始反应速率a_____ b(填“<”“>”或“=”,下同),溶液的导电能力a_____ b;最终产生氢气的质量a_____ b.
(3)已知25℃时部分弱电解质的电离平衡常数数据如表所示:
以下说法不正确的是_____(填字母)。
(4)向NaCN溶液中通入过量 气体,发生反应的离子方程式是
气体,发生反应的离子方程式是_____ 。
(1)向
 醋酸溶液中加入少量水,
醋酸溶液中加入少量水,

(2)500mL
 醋酸溶液a、500mL
醋酸溶液a、500mL 盐酸溶液b分别与足量Zn粉充分反应,初始反应速率a
盐酸溶液b分别与足量Zn粉充分反应,初始反应速率a(3)已知25℃时部分弱电解质的电离平衡常数数据如表所示:
| 化学式 |  |  | HClO | HCN |
| 电离平衡常数 |  |   |  | 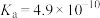 |
| A.向弱酸溶液中加入少量NaOH溶液,电离平衡常数变大 |
| B.多元弱酸的酸性主要由第一步电离决定 |
C.表中四种酸,酸性最强的是 |
D.向NaClO溶液中通入 气体,可以生成HClO 气体,可以生成HClO |
 气体,发生反应的离子方程式是
气体,发生反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】I.按要求回答下列问题:
(1)下列物质中属于强电解质的是___________ (填标号,下同),属于弱电解质的是___________ 。
①HI ②盐酸 ③BaSO4 ④H2O ⑤SO2 ⑥HF
Ⅱ.已知电离平衡常数:
(2)下列离子结合H+能力由强到弱的顺序是___________ (用离子符号表示)。
A.NO B.CN- C.H2PO
B.CN- C.H2PO D.HPO
D.HPO E.PO
E.PO
(3)25℃时,向10mL0.1mol•L-1的HNO2溶液中加入蒸馏水,将其稀释到1L后,下列说法正确的是___________。
(4)取c(H+)相同的盐酸和HNO2溶液各10mL,分别加水稀释到1000mL,稀释过程中c(H+)变化如图所示。表示盐酸c(H+)变化的曲线是___________ ,理由是___________ 。

(5)①HCN能否与NaNO2溶液反应___________ ,原因是___________ 。
②Na3PO4溶液与足量的HNO2溶液反应的离子方程式为___________ 。
(1)下列物质中属于强电解质的是
①HI ②盐酸 ③BaSO4 ④H2O ⑤SO2 ⑥HF
Ⅱ.已知电离平衡常数:
| 弱酸 | HNO2 | HCN | H3PO4 |
| 电离常数(25℃) | 5.6×10-4 | 6.2×10-10 | Ka1=6.9×10-3 Ka2=6.2×10-8 Ka3=4.8×10-13 |
(2)下列离子结合H+能力由强到弱的顺序是
A.NO
 B.CN- C.H2PO
B.CN- C.H2PO D.HPO
D.HPO E.PO
E.PO
(3)25℃时,向10mL0.1mol•L-1的HNO2溶液中加入蒸馏水,将其稀释到1L后,下列说法正确的是___________。
| A.HNO2的电离程度增大 | B.Ka(HNO2)增大 |
| C.H+的数目增多 | D. 减小 减小 |
(4)取c(H+)相同的盐酸和HNO2溶液各10mL,分别加水稀释到1000mL,稀释过程中c(H+)变化如图所示。表示盐酸c(H+)变化的曲线是

(5)①HCN能否与NaNO2溶液反应
②Na3PO4溶液与足量的HNO2溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】醋酸是我们生活中常见的一种酸。请回答下列问题:
(1)在0.1mol·L-1的CH3COOH溶液中,要促进醋酸电离且使H+浓度增大,应采取的措施是___ 。
(2)常温下,有c(H+)相同、体积相同的CH3COOH溶液和HCl溶液,现采取以下措施:
①分别加适量醋酸钠晶体后,CH3COOH溶液中c(H+)___ (填“增大”“减小”或“不变”,下同),HCl溶液中c(H+)____ 。
②分别加水稀释10倍后,CH3COOH溶液中的c(H+)____ (填“>”“=”或“<”)HCl溶液中的c(H+)。
③分别加等浓度的NaOH溶液至恰好反应,所需NaOH溶液的体积:CH3COOH溶液____ (填“>”“=”或“<”)HCl溶液。
④温度都升高20℃,CH3COOH溶液中c(H+)____ (填“>”“<”或“=”)HCl溶液中c(H+)。
(3)将0.1mol·L-1的CH3COOH溶液加水稀释,下列有关稀释后CH3COOH溶液的说法正确的是____ 。
(4)25℃时,醋酸、碳酸和亚硫酸的电离常数如表所示。
①碳酸第一步电离的电离常数表达式为____ 。
②在相同条件下,试比较CH3COO-、 和
和 与H+的结合能力大小:
与H+的结合能力大小:___ 。
③书写亚硫酸与碳酸氢钠溶液反应的离子方程式___ 。
(1)在0.1mol·L-1的CH3COOH溶液中,要促进醋酸电离且使H+浓度增大,应采取的措施是
| A.升温 | B.加水 | C.加入NaOH溶液 | D.加入稀盐酸 |
①分别加适量醋酸钠晶体后,CH3COOH溶液中c(H+)
②分别加水稀释10倍后,CH3COOH溶液中的c(H+)
③分别加等浓度的NaOH溶液至恰好反应,所需NaOH溶液的体积:CH3COOH溶液
④温度都升高20℃,CH3COOH溶液中c(H+)
(3)将0.1mol·L-1的CH3COOH溶液加水稀释,下列有关稀释后CH3COOH溶液的说法正确的是
| A.电离程度增大 | B.溶液中离子总数增多 | C.溶液导电性增强 | D.溶液中醋酸分子增多 |
| 酸 | 电离常数 |
| 醋酸 | K=1.75×10-5 |
| 碳酸 | K1=4.30×10-7,K2=5.61×10-11 |
| 亚硫酸 | K1=1.54×10-2,K2=1.02×10-7 |
①碳酸第一步电离的电离常数表达式为
②在相同条件下,试比较CH3COO-、
 和
和 与H+的结合能力大小:
与H+的结合能力大小:③书写亚硫酸与碳酸氢钠溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】填空。
(1)某温度(t℃)时,水的Kw=10-13,则该温度(填大于、等于或小于)___________ 25℃,将此温度下pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合:
①若所得混合溶液为中性,则a:b=___________ ;
②若所得混合溶液pH=2,则a;b=___________ 。
(2)在一定温度下,有a.氢氧化钡 b.氢氧化钠 c.氨水三种碱:
①同体积、同物质的量浓度的三种碱,中和HCl的能力由大到小的顺序是______ (用a、b、c表示,下同)
②若三者c(OH-)相同时,三种碱的物质的量浓度由大到小的顺序为___________ ;
③将c(OH-)相同的三种碱均加水稀释至原来的100倍后,c(OH-)由大到小的顺序是___________ 。
(1)某温度(t℃)时,水的Kw=10-13,则该温度(填大于、等于或小于)
①若所得混合溶液为中性,则a:b=
②若所得混合溶液pH=2,则a;b=
(2)在一定温度下,有a.氢氧化钡 b.氢氧化钠 c.氨水三种碱:
①同体积、同物质的量浓度的三种碱,中和HCl的能力由大到小的顺序是
②若三者c(OH-)相同时,三种碱的物质的量浓度由大到小的顺序为
③将c(OH-)相同的三种碱均加水稀释至原来的100倍后,c(OH-)由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知:25℃时,H2CO3的电离平衡常数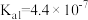 ,
,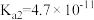 ,由HCOOH的电离平衡常数得到的pKa=3.74(pKa=-lgKa)。请回答下列问题:
,由HCOOH的电离平衡常数得到的pKa=3.74(pKa=-lgKa)。请回答下列问题:
(1)写出在水溶液中H2CO3的第一步电离方程式:_______ 。
(2)将0.1 mol/L的HCOOH溶液逐滴滴入50 mL0.1 mol/L的碳酸钠溶液中,现象为_______ ,写出相应的离子方程式_______ 。
(3)25℃时,将0.1 mol/L的盐酸逐滴滴入0.1 mol/L的碳酸钠溶液中,当溶液中 时,溶液的pH=
时,溶液的pH=_______ 。
(4)25℃时,取50 mL0.1 mol/L的HCOOH溶液,将其稀释1000倍。
①在稀释过程中,随着HCOOH溶液浓度的降低,下列始终保持增大趋势的量是_______ (填标号)。
A.HCOOH分子数 B.c(OH-)
C.c(H+) D.
②稀释到1000倍时溶液的pH的变化量_______ (填“>”、“<”或“=”)3。
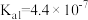 ,
,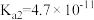 ,由HCOOH的电离平衡常数得到的pKa=3.74(pKa=-lgKa)。请回答下列问题:
,由HCOOH的电离平衡常数得到的pKa=3.74(pKa=-lgKa)。请回答下列问题:(1)写出在水溶液中H2CO3的第一步电离方程式:
(2)将0.1 mol/L的HCOOH溶液逐滴滴入50 mL0.1 mol/L的碳酸钠溶液中,现象为
(3)25℃时,将0.1 mol/L的盐酸逐滴滴入0.1 mol/L的碳酸钠溶液中,当溶液中
 时,溶液的pH=
时,溶液的pH=(4)25℃时,取50 mL0.1 mol/L的HCOOH溶液,将其稀释1000倍。
①在稀释过程中,随着HCOOH溶液浓度的降低,下列始终保持增大趋势的量是
A.HCOOH分子数 B.c(OH-)
C.c(H+) D.

②稀释到1000倍时溶液的pH的变化量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知溶液中的化学反应大多是离子反应。根据要求回答下列问题。
(1)水存在如下平衡:H2O+H2O H3O++OH-,向水中加入NaHSO4固体,水的电离平衡向
H3O++OH-,向水中加入NaHSO4固体,水的电离平衡向________ (填 “左”或“右”)移动, 且所得溶液显____ 性。
(2)向水中加NaHCO3固体,水的电离平衡向____ (填“左”或“右”)移动,且所得溶液显____ 性。
(3)常温下,0.1 mol·L-1 CH3COONa溶液的pH为9,则由水电离出的c(H+)=________ 。
(4)若取pH、体积均相等的NaOH溶液和氨水分别加水稀释m倍、n倍后pH仍相等,则m____ n ( 填“>”“<”或“=”)。
(1)水存在如下平衡:H2O+H2O
 H3O++OH-,向水中加入NaHSO4固体,水的电离平衡向
H3O++OH-,向水中加入NaHSO4固体,水的电离平衡向(2)向水中加NaHCO3固体,水的电离平衡向
(3)常温下,0.1 mol·L-1 CH3COONa溶液的pH为9,则由水电离出的c(H+)=
(4)若取pH、体积均相等的NaOH溶液和氨水分别加水稀释m倍、n倍后pH仍相等,则m
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,将0.01mol NH4Cl和 0.002mol NaOH 溶于水配成1 L 混合溶液。
(1)该溶液中存在的平衡体系有______ 个。
(2)溶液中共有______ 种不同的微粒。
(3)这些微粒中浓度为0.01mol·L -1的是______ ,浓度为0.002mol/L 的是______ 。
(4)两种微粒的物质的量之和______ +______ - n(OH-)=0.008 mol 。
(1)该溶液中存在的平衡体系有
(2)溶液中共有
(3)这些微粒中浓度为0.01mol·L -1的是
(4)两种微粒的物质的量之和
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】写出下列反应的离子方程式或按要求填空:
(1)泡沫灭火器原理:_______ 。
(2)Ba(OH)2溶液与NaHSO4溶液的反应
溶液呈中性:____________ 。
溶液呈碱性:___________ 。
(3)将FeS固体投入到含Hg2+的废水中:_________ 。
(4)写出NaHSO3溶液中各离子浓度的大小:________ 。
(5)在NaH2PO4溶液中:
物料守恒:_________ 。
质子守恒:_________ 。
(1)泡沫灭火器原理:
(2)Ba(OH)2溶液与NaHSO4溶液的反应
溶液呈中性:
溶液呈碱性:
(3)将FeS固体投入到含Hg2+的废水中:
(4)写出NaHSO3溶液中各离子浓度的大小:
(5)在NaH2PO4溶液中:
物料守恒:
质子守恒:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】研究电解质在水溶液中的平衡能了解它的存在形式。已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)物质的量浓度均为 的下列四种溶液:
的下列四种溶液: 由小到大排列的顺序是
由小到大排列的顺序是_______ 。
A. B.
B. C.
C. D.
D.
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是_______ (填序号)。
A.c(H+) B.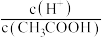 C.c(H+) c(OH—)D.
C.c(H+) c(OH—)D. E.
E.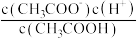
(3)写出向氰化钠溶液中通入少量二氧化碳的离子方程式:_______ 。
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka_______ (用含a、b的代数式表示)。
(5)标准状况下将0.224LCO2,通入100mL0.1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH—)= c(H2CO3)+_______ 。
(6)25℃,氨水的浓度为2.0mol/L,溶液中的c(OH—)=_______ mol/L,将 通入该氨水中,当溶液中c(OH—)降至1×10—7mol/L时,溶液中
通入该氨水中,当溶液中c(OH—)降至1×10—7mol/L时,溶液中
_______  。(填“">”或“<”或“=”)
。(填“">”或“<”或“=”)
(7)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与 类似。
类似。
①写出盐酸肼第一步水解反应的离子方程式_______ 。
②盐酸肼水溶液中离子浓度的排列顺序正确的是_______ (填序号)。
A.c(Cl-)>c(N2H )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.c(Cl-)> c[(N2H5·H2O)]+>c(H+)>c(OH-)
C.2 c(N2H )+ c[(N2H5·H2O)]++c(H+)= c(Cl-)+c(OH-)
)+ c[(N2H5·H2O)]++c(H+)= c(Cl-)+c(OH-)
D.c[(N2H5·H2O)]+>c(Cl-)> c(H+)>c(OH-)
| 化学式 |  |  |  |  |
| 电离平衡常数 | Ka=1.8×10−5 | Kal=4.3×10−7 Ka2=5.6×10−11 | Ka=6.2×10−10 | Kb=1.8×10−5 |
(1)物质的量浓度均为
 的下列四种溶液:
的下列四种溶液: 由小到大排列的顺序是
由小到大排列的顺序是A.
 B.
B. C.
C. D.
D.
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是
A.c(H+) B.
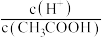 C.c(H+) c(OH—)D.
C.c(H+) c(OH—)D. E.
E.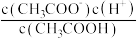
(3)写出向氰化钠溶液中通入少量二氧化碳的离子方程式:
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka
(5)标准状况下将0.224LCO2,通入100mL0.1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH—)= c(H2CO3)+
(6)25℃,氨水的浓度为2.0mol/L,溶液中的c(OH—)=
 通入该氨水中,当溶液中c(OH—)降至1×10—7mol/L时,溶液中
通入该氨水中,当溶液中c(OH—)降至1×10—7mol/L时,溶液中
 。(填“">”或“<”或“=”)
。(填“">”或“<”或“=”)(7)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与
 类似。
类似。①写出盐酸肼第一步水解反应的离子方程式
②盐酸肼水溶液中离子浓度的排列顺序正确的是
A.c(Cl-)>c(N2H
 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)B.c(Cl-)> c[(N2H5·H2O)]+>c(H+)>c(OH-)
C.2 c(N2H
 )+ c[(N2H5·H2O)]++c(H+)= c(Cl-)+c(OH-)
)+ c[(N2H5·H2O)]++c(H+)= c(Cl-)+c(OH-)D.c[(N2H5·H2O)]+>c(Cl-)> c(H+)>c(OH-)
您最近一年使用:0次