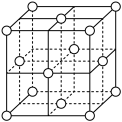
通过下列实验可以从废银催化剂(Ag、 和少量
和少量 )中回收银:
)中回收银:
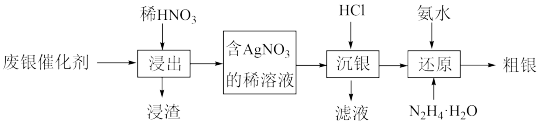
下列说法正确的是
 和少量
和少量 )中回收银:
)中回收银:
下列说法正确的是
A.滤渣的主要成分是 和 和 |
| B.“浸出”时产生的气体可用NaOH溶液吸收 |
C.“还原”过程的离子方程式: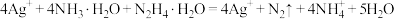 |
D.在元素周期表中,Ag与Cu相邻,则Ag的价电子排布式为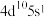 |
更新时间:2023-06-29 07:07:42
|
相似题推荐
【推荐1】对于白磷引起的中毒,硫酸铜溶液是一种解毒剂,有关反应如下:P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平),关于该反应下列说法正确的是
| A.CuSO4既不作氧化剂,也不作还原剂 |
| B.11个P被氧化时,该反应中有30个电子发生转移 |
| C.氧化性:CuSO4>H3PO4 |
| D.该反应的氧化剂和还原剂的个数之比为10:3 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式与所述事实相符且正确的是
| A.用H2O2从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O |
B.向碳酸氢钙溶液中加入过量的NaOH溶液:Ca2++ +OH-=CaCO3↓+H2O +OH-=CaCO3↓+H2O |
C.向明矾溶液中加入Ba(OH)2溶液至生成沉淀的物质的量最多:Al3++2 +2Ba2++4OH-= +2Ba2++4OH-= +2BaSO4↓+2H2O +2BaSO4↓+2H2O |
D.等体积、等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合: +Ba2++OH-=BaCO3↓+H2O +Ba2++OH-=BaCO3↓+H2O |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】用如图所示的装置分别进行如下实验,各离子方程式正确及各组物质反应后,溶液的导电性比反应前增强的是( )


| A.向硝酸银溶液中通入少量氯化氢:Ag++Cl-=AgCl↓ |
| B.向亚硫酸溶液中通入氯气:H2SO3+C12+H2O=SO42-+4H++2Cl- |
| C.向FeBr2溶液中通入少量氯气:2Fe2++Cl2=2Fe3++2Cl- |
| D.向NaOH溶液中通入少量氯气:2OH-+Cl2=Cl-+ClO-+H2O |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯硅制品的主要原料。已知多晶硅第三代工业制取流程如图所示。下列说法错误的是
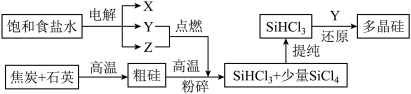

| A.Y、Z分别为H2、Cl2 |
B.制取粗硅过程可能发生反应:SiO2+3C SiC+2CO↑ SiC+2CO↑ |
| C.提纯SiHCl3可采用萃取、分液的方法 |
| D.SiHCl3和SiCl4形成的晶体均为共价晶体 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】一种废料的主要成分是铁镍合金,还含有铜、钙、镁、硅的氧化物。由该废料制备纯度较高的氢氧化镍(已知常温下Ksp[Ni(OH)2]=2.0×10-15),工艺流程如下。下列叙述错误的是


| A.废渣的主要成分为二氧化硅 |
| B.除钙镁过程中,为了提高钙镁的去除率,氟化钠实际用量应该越多越好 |
| C.黄钠铁矾渣中铁元素为+3价 |
| D.“沉镍”过程中为了将镍沉淀完全,需调节溶液pH>8 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、Q、E、M六种元素中,X的原子的基态价电子排布式为2s2,Y的基态原子核外有5种运动状态不同的电子,Z元素的两种同位素原子通常作为示踪原子研究生物化学反应和测定文物的年代,Q是元素周期表中电负性最大的元素,E的阳离子通常存在于硝石、明矾和草木灰中,M的原子序数比E大5.下列说法正确的是
| A.EYQ4 中阴离子中心原子的杂化方式为sp3杂化 |
| B.X、Y元素的第一电离能大小关系:X<Y |
C.Z与氧元素形成的离子ZO 的空间构型为V形 的空间构型为V形 |
| D.M为元素周期表前四周期基态原子未成对电子最多的元素 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】乙二胺(H2NCH2CH2NH2)能与Mg2+、Cu2+等形成稳定环状离子,其中Cu2+与乙二胺形成的化合物稳定性更高。下列说法错误的是
| A.铜的第二电离能小于锌的第二电离能 |
| B.乙二胺中2个N原子均可与Cu2+形成配位键 |
| C.基态铜原子4s电子能量较高,总是在比3s电子离核更远的地方运动 |
| D.基态Mg原子中,电子占据的最高能层具有的原子轨道为9 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法错误的是
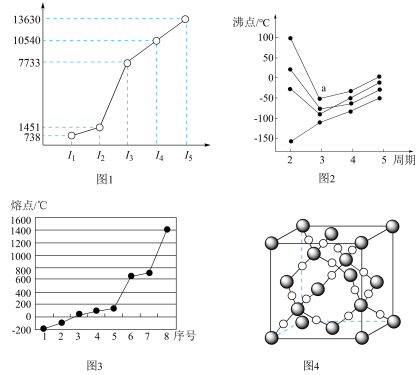

| A.第三周期的某主族元素,其第一至第五电离能数据如图1所示,该元素为Mg |
| B.周期表ⅣA~ⅦA中元素氢化物的沸点变化如图2所示,a点代表HCl |
| C.第三周期8种元素单质熔点高低的顺序如图3所示,序号7对应的元素为Mg |
| D.AB2在高温高压下所形成的晶体其晶胞如图4所示,该晶体属于共价晶体 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性能,是一种新型无机非金属材料,其结构如图所示。下列叙述不正确 的是


| A.氮化铝晶体中距离铝原子最近且距离相等的氮原子数目为4 |
| B.由于 AlN 相对分子质量比立方 BN 大,所以熔沸点 AlN 比 BN 高 |
| C.AlN 中原子 Al 杂化方式为 sp2,N 杂化方式为 sp3 |
| D.氮化铝晶体中含有配位键 |
您最近一年使用:0次

 和
和 的混合物为原料制备AlAs,工艺流程如下:
的混合物为原料制备AlAs,工艺流程如下:

 溶液获得
溶液获得
 的沸点
的沸点