常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
(1)从甲组情况分析,如何判断HA是强酸还是弱酸?__________________________________________________ 。
(2)乙组混合溶液中粒子浓度c(A-)和c(Na+)的大小关系________ 。
A.前者大 B.后者大
C.两者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是__________________
(4)分析丁组实验数据,写出混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=________ mol·L-1。
| 实验 编号 | HA物质的量 浓度/(mol·L-1) | NaOH物质的量 浓度/(mol·L-1) | 混合后溶 液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
(1)从甲组情况分析,如何判断HA是强酸还是弱酸?
(2)乙组混合溶液中粒子浓度c(A-)和c(Na+)的大小关系
A.前者大 B.后者大
C.两者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是
(4)分析丁组实验数据,写出混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=
更新时间:2014-03-25 15:38:27
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】Na2S又称臭碱、硫化碱,是应用广泛的化工原料,也常用于吸收工业废气中的SO2。完成下列填空:
(1)用离子方程式说明Na2S又称臭碱、硫化碱的原因___ 。
(2)向AgCl悬浊液中滴加Na2S溶液,生成黑色沉淀,写出反应的离子方程式___ 。结合你所学习过的其它离子反应分析,离子互换反应进行的方向是___ 。
向Na2S溶液中不断通入SO2,直至不再能吸收。其间看到溶液变浑浊,停止反应后溶液中含硫微粒为:S2O32-、HSO3-、H2SO3、HS-。
(3)反应过程中,溶液的pH逐渐___ (填“变大”、“变小”),生成的沉淀是___ ;
(4)关于反应后得到的溶液,下列离子浓度关系正确的是___ 。
a.c(Na+)=c(S2O32-) +2c(HSO3-)+2c(H2SO3) + 2c(HS-)
b.c(Na+)+c(H+)=2c(S2O32-)+c(HSO3-) +c(HS-) +c(OH-)
c.c(Na+)=2c(HS-)
d.c(Na+)=2c(HS-)+2c(S2O32-)+c(HSO3-)
(1)用离子方程式说明Na2S又称臭碱、硫化碱的原因
(2)向AgCl悬浊液中滴加Na2S溶液,生成黑色沉淀,写出反应的离子方程式
向Na2S溶液中不断通入SO2,直至不再能吸收。其间看到溶液变浑浊,停止反应后溶液中含硫微粒为:S2O32-、HSO3-、H2SO3、HS-。
(3)反应过程中,溶液的pH逐渐
(4)关于反应后得到的溶液,下列离子浓度关系正确的是
a.c(Na+)=c(S2O32-) +2c(HSO3-)+2c(H2SO3) + 2c(HS-)
b.c(Na+)+c(H+)=2c(S2O32-)+c(HSO3-) +c(HS-) +c(OH-)
c.c(Na+)=2c(HS-)
d.c(Na+)=2c(HS-)+2c(S2O32-)+c(HSO3-)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请回答下列问题(25 ℃时):
⑴若向0.1 mol·L-1氨水中加入少量硫酸铵固体,此时溶液中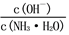
________ (填“增大”、“减小”或“不变”)。
⑵若向0.1 mol·L-1氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式:_______________________________ ;所得溶液的pH______ 7(填“>”、“<”或“=”),用离子方程式表示其原因_____________________________________ 。
⑶若向0.1 mol·L-1氨水中加入稀硫酸至溶液的pH=7,此时c(NH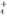 )=a mol·L-1,则c(SO
)=a mol·L-1,则c(SO )为
)为__________________ 。
⑷若向0.1 mol·L-1氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子的物质的量浓度由大到小的顺序是____________________________ 。
⑸将足量的AgCl固体分别放入:①5 mL水,②10 mL 0.2 mol·L-1 MgCl2溶液,③20 mL 0.5 mol·L-1 NaCl溶液,④40 mL 0.1 mol·L-1盐酸中溶解至溶液饱和,各溶液中Ag+的物质的量浓度分别为a、b、c、d,它们由大到小的排列顺序是____________________ 。
⑴若向0.1 mol·L-1氨水中加入少量硫酸铵固体,此时溶液中
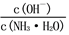
⑵若向0.1 mol·L-1氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式:
⑶若向0.1 mol·L-1氨水中加入稀硫酸至溶液的pH=7,此时c(NH
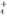 )=a mol·L-1,则c(SO
)=a mol·L-1,则c(SO )为
)为⑷若向0.1 mol·L-1氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子的物质的量浓度由大到小的顺序是
⑸将足量的AgCl固体分别放入:①5 mL水,②10 mL 0.2 mol·L-1 MgCl2溶液,③20 mL 0.5 mol·L-1 NaCl溶液,④40 mL 0.1 mol·L-1盐酸中溶解至溶液饱和,各溶液中Ag+的物质的量浓度分别为a、b、c、d,它们由大到小的排列顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】草酸( )存在于菠菜等蔬菜中,是一种二元弱酸。常温下,向某浓度的草酸溶液中逐滴滴入一定浓度的NaOH溶液,所得溶液中
)存在于菠菜等蔬菜中,是一种二元弱酸。常温下,向某浓度的草酸溶液中逐滴滴入一定浓度的NaOH溶液,所得溶液中 、
、 、
、 三种微粒的物质的量分数(δ)与溶液pH的关系如图1所示。
三种微粒的物质的量分数(δ)与溶液pH的关系如图1所示。

回答下列问题:
(1)用离子方程式说明 溶液显碱性的原因:
溶液显碱性的原因:_______ 。
(2)常温下,若向N点溶液加蒸馏水稀释,在稀释该溶液过程中,下列物理量始终增大的是_______ (填标号)。
a.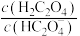 b.
b.
c.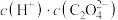 d.
d.
(3)p点,溶液中
_______ 。
(4)下列说法正确的是_______ (填标号)。
a.E、F、Q三点,水的电离程度最大的是Q点
b.E点存在:
c.F点存在:
(5)常温下, 的
的 溶液的物质的量浓度为
溶液的物质的量浓度为 ,水电离出的
,水电离出的 为
为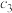 ;
; 的
的 溶液的物质的量浓度为
溶液的物质的量浓度为 ,水电离出的
,水电离出的 为
为 。则
。则
_______  (填“>”“<”或“=”,下同);
(填“>”“<”或“=”,下同);
_______  。
。
(6)已知 。将0.03 mol∙L−1的
。将0.03 mol∙L−1的 溶液与0.01 mol∙L−1的
溶液与0.01 mol∙L−1的 溶液等体积混合,混合溶液中
溶液等体积混合,混合溶液中 的浓度约为
的浓度约为_______ mol∙L−1。(用含a的代数式表示,混合后溶液体积变化忽略不计)。
 )存在于菠菜等蔬菜中,是一种二元弱酸。常温下,向某浓度的草酸溶液中逐滴滴入一定浓度的NaOH溶液,所得溶液中
)存在于菠菜等蔬菜中,是一种二元弱酸。常温下,向某浓度的草酸溶液中逐滴滴入一定浓度的NaOH溶液,所得溶液中 、
、 、
、 三种微粒的物质的量分数(δ)与溶液pH的关系如图1所示。
三种微粒的物质的量分数(δ)与溶液pH的关系如图1所示。
回答下列问题:
(1)用离子方程式说明
 溶液显碱性的原因:
溶液显碱性的原因:(2)常温下,若向N点溶液加蒸馏水稀释,在稀释该溶液过程中,下列物理量始终增大的是
a.
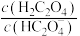 b.
b.
c.
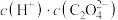 d.
d.
(3)p点,溶液中

(4)下列说法正确的是
a.E、F、Q三点,水的电离程度最大的是Q点
b.E点存在:

c.F点存在:

(5)常温下,
 的
的 溶液的物质的量浓度为
溶液的物质的量浓度为 ,水电离出的
,水电离出的 为
为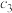 ;
; 的
的 溶液的物质的量浓度为
溶液的物质的量浓度为 ,水电离出的
,水电离出的 为
为 。则
。则
 (填“>”“<”或“=”,下同);
(填“>”“<”或“=”,下同);
 。
。(6)已知
 。将0.03 mol∙L−1的
。将0.03 mol∙L−1的 溶液与0.01 mol∙L−1的
溶液与0.01 mol∙L−1的 溶液等体积混合,混合溶液中
溶液等体积混合,混合溶液中 的浓度约为
的浓度约为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】硫及其化合物在生产、生活中具有广泛的用途,根据所学知识,回答下列问题。
已知:常温下K(NH3·H2O)=1.6×10-5,lg2=0.3。
(1)(NH4)2SO4溶液可用来除铁锈,其原因是_______ (用离子方程式表示)。
(2)常温下,0.1mol·L-1的(NH4)2SO4溶液的pH=_______ ,由水电离出的c(H+)=_______ mol·L-1。
(3)常温下,向100mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol·L-1的NaOH溶液,得到溶液的pH与NaOH溶液的体积的关系如图所示(忽略溶液混合时体积的变化)。
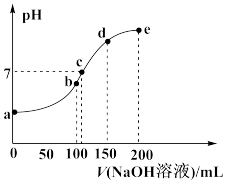
①a点时,溶液中各离子的浓度由大到小的顺序为_______ (用离子符号表示)。
②c点时,c(NH )+c(Na+)
)+c(Na+)_______ (填“>”“<”或“=”)c(SO )。
)。
③d点时, =
=_______ 。
已知:常温下K(NH3·H2O)=1.6×10-5,lg2=0.3。
(1)(NH4)2SO4溶液可用来除铁锈,其原因是
(2)常温下,0.1mol·L-1的(NH4)2SO4溶液的pH=
(3)常温下,向100mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol·L-1的NaOH溶液,得到溶液的pH与NaOH溶液的体积的关系如图所示(忽略溶液混合时体积的变化)。

①a点时,溶液中各离子的浓度由大到小的顺序为
②c点时,c(NH
 )+c(Na+)
)+c(Na+) )。
)。③d点时,
 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据水溶液中的离子平衡回答下列问题。
(1)已知:a.常温下,醋酸和NH3·H2O的电离常数相同。
b.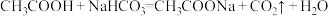
则CH3COONH4溶液呈______ 性(填“酸”“碱”或“中”),NH4HCO3溶液中物质的量浓度最大的离子是______ (填化学式)。
(2)25℃时,浓度均为0.10 mo/L的CH3COOH和CH3COONa的混合溶液pH=4.76。
①CH3COONa水解的离子方程式是___________ 。
②该混合溶液中所有离子浓度由大到小的顺序为___________ 。
(1)已知:a.常温下,醋酸和NH3·H2O的电离常数相同。
b.
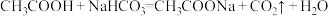
则CH3COONH4溶液呈
(2)25℃时,浓度均为0.10 mo/L的CH3COOH和CH3COONa的混合溶液pH=4.76。
①CH3COONa水解的离子方程式是
②该混合溶液中所有离子浓度由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】常温下向20mL0.1mol·L-1Na2CO3溶液中逐滴加入0.1mol·L-1HCl溶液40mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
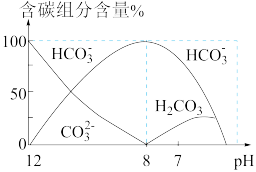
回答下列问题:
(1)在同一溶液中,H2CO3、HCO 、CO
、CO
___ (填“能”或“不能”)大量共存。
(2)当pH=7时,溶液中含碳元素的主要微粒为___ ;溶液中各种离子的物质的量浓度的大小关系为___ 。
(3)已知在25℃时,CO 水解反应的平衡常数即水解常数Kh=2×10-4mol•L-1,当溶液中c(HCO
水解反应的平衡常数即水解常数Kh=2×10-4mol•L-1,当溶液中c(HCO ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=__ 。

回答下列问题:
(1)在同一溶液中,H2CO3、HCO
 、CO
、CO
(2)当pH=7时,溶液中含碳元素的主要微粒为
(3)已知在25℃时,CO
 水解反应的平衡常数即水解常数Kh=2×10-4mol•L-1,当溶液中c(HCO
水解反应的平衡常数即水解常数Kh=2×10-4mol•L-1,当溶液中c(HCO ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=
您最近一年使用:0次



