2022年春晚中舞蹈诗剧《只此青绿》生动还原了北宋名画《千里江山图》。《千里江山图》之所以色彩艳丽,璀璨夺目,与所使用的矿物颜料有关。回答下列问题:
(1)石青,取自蓝铜矿,化学式为Cu3(CO3)2(OH)2. 的空间结构为
的空间结构为_____ ,原子中电子有两种相反的自旋状态,分别用+ 和-
和- 表示,称为电子的自旋磁量子数,则Cu2+中电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则Cu2+中电子自旋磁量子数的代数和为_____ 。
(2)亚铁氰化钾,化学式为K4[Fe(CN)6],呈黄色结晶性粉末。[Fe(CN)6]4-中的C原子的杂化方式为_____ ,[Fe(CN)6]4-中 键和
键和 键的数目之比为
键的数目之比为_____ 。
(3)FeCl3的沸点为319℃,AsCl3的沸点为130.2℃,均属于_____ (填“分子”或“共价”)晶体。列举一种共价晶体:_____ (填化学式)。
(4)某种铜的氧化物的晶胞结构图如图。该铜的氧化物的化学式为_____ ,O2-的配位数为_____ 。若晶胞参数为anm,晶体的密度为dg·cm-3,则阿伏加德罗常数的值为_____ (用含a和d的代数式表示)。

(1)石青,取自蓝铜矿,化学式为Cu3(CO3)2(OH)2.
 的空间结构为
的空间结构为 和-
和- 表示,称为电子的自旋磁量子数,则Cu2+中电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则Cu2+中电子自旋磁量子数的代数和为(2)亚铁氰化钾,化学式为K4[Fe(CN)6],呈黄色结晶性粉末。[Fe(CN)6]4-中的C原子的杂化方式为
 键和
键和 键的数目之比为
键的数目之比为(3)FeCl3的沸点为319℃,AsCl3的沸点为130.2℃,均属于
(4)某种铜的氧化物的晶胞结构图如图。该铜的氧化物的化学式为

更新时间:2023-08-08 11:16:34
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】过渡金属元素在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)原子序数21~30的元素基态原子的价层电子排布中,未成对电子数最多的元素在周期表中的位置是_______ ,其价层电子排布图(轨道表示式)为_______ 。
(2)基态钒原子核外电子的运动状态有_______ 种。
(3)铁的一种配合物的化学式为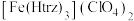 ,其中配体
,其中配体 为1,2,
为1,2, 三氮唑(
三氮唑(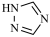 )分子。
)分子。
①该配合物中,阴离子的空间结构为_______ ,其中心原子的杂化轨道类型是_______ 。
②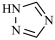 分子中,σ键与π键的个数比为
分子中,σ键与π键的个数比为_______ 。
(4)二茂铁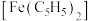 不溶于水,易溶于乙醇等有机溶剂。乙醇的沸点(
不溶于水,易溶于乙醇等有机溶剂。乙醇的沸点(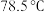 )介于水的沸点(100℃)和乙硫醇(CH3CH2SH)的沸点(36.2℃)之间,其原因是
)介于水的沸点(100℃)和乙硫醇(CH3CH2SH)的沸点(36.2℃)之间,其原因是_______ 。
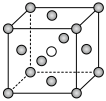
(5)铁单质和氨气在 可发生置换反应,产物之一的晶胞结构如图所示(黑球代表
可发生置换反应,产物之一的晶胞结构如图所示(黑球代表 ,白球代表N),该反应的化学方程式为
,白球代表N),该反应的化学方程式为_______ 。若该晶体的密度是 ,则两个最近的
,则两个最近的 原子间的距离为
原子间的距离为_______  (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)原子序数21~30的元素基态原子的价层电子排布中,未成对电子数最多的元素在周期表中的位置是
(2)基态钒原子核外电子的运动状态有
(3)铁的一种配合物的化学式为
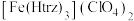 ,其中配体
,其中配体 为1,2,
为1,2, 三氮唑(
三氮唑( )分子。
)分子。①该配合物中,阴离子的空间结构为
②
 分子中,σ键与π键的个数比为
分子中,σ键与π键的个数比为(4)二茂铁
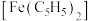 不溶于水,易溶于乙醇等有机溶剂。乙醇的沸点(
不溶于水,易溶于乙醇等有机溶剂。乙醇的沸点(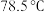 )介于水的沸点(100℃)和乙硫醇(CH3CH2SH)的沸点(36.2℃)之间,其原因是
)介于水的沸点(100℃)和乙硫醇(CH3CH2SH)的沸点(36.2℃)之间,其原因是(5)铁单质和氨气在
 可发生置换反应,产物之一的晶胞结构如图所示(黑球代表
可发生置换反应,产物之一的晶胞结构如图所示(黑球代表 ,白球代表N),该反应的化学方程式为
,白球代表N),该反应的化学方程式为 ,则两个最近的
,则两个最近的 原子间的距离为
原子间的距离为 (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知X、Y、Z都是元素周期表中前四周期的元素,他们的原子序数依次增大,并且不在同一个周期。元素X的原子核外有8个运动状态不同的电子。元素Y基态原子的最外电子层没有空轨道,而且成对电子数是未成对电子数的2倍。元素Z基态原子的内层轨道全部排满电子,且最外层电子数为2。
(1)基态X原子的核外电子排布图(轨道表达式)为_________ ,X的氢化物在乙醇中的溶解度大于Y的氢化物,其原因是________________________ 。
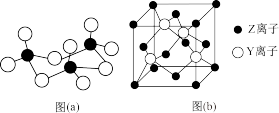
(2)X与Y形成的固体YX3中存在(a)所示的三聚分子,该分子中Y原子的杂化轨道类型为_______ 。基态Y原子中,核外能级最高的原子轨道上,具有的电子数为______ 。
(3)X与Y还可以形成YX42-离子,YX42-的空间构型为_________ ,写出一种与YX42-互为等电子体的分子的化学式________ 。
(4)Z与Y的离子形成化合物晶体的晶胞如图(b)所示。在晶胞中,Z离子的配位数为_________ ,该化合物的化学式为______ 。
(5)Z的氯化物与氨水反应可形成配合物[Z(NH3)4]Cl2,1mol该配合物中含有 键的数目为
键的数目为_______ 。

(1)基态X原子的核外电子排布图(轨道表达式)为
(2)X与Y形成的固体YX3中存在(a)所示的三聚分子,该分子中Y原子的杂化轨道类型为
(3)X与Y还可以形成YX42-离子,YX42-的空间构型为
(4)Z与Y的离子形成化合物晶体的晶胞如图(b)所示。在晶胞中,Z离子的配位数为
(5)Z的氯化物与氨水反应可形成配合物[Z(NH3)4]Cl2,1mol该配合物中含有
 键的数目为
键的数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】硼氢化钠(NaBHa)中氢元素为-1价,具有很强的还原性,被称为“万能还原剂”。回答下列问题:
(1)基态硼原子的电子排布图是____ ,其原子核外共有____ 种运动状态的电子。
(2)硼与铍相比,第一电离能较高的是____ ,原因是____ 。
(3)NaBH4中所含的化学键的类型有____ ,[BH4]-的空间构型是____ ,其中心原子的杂化轨道类型为____ 。
(4)硼氢化钠(NaBH4)的晶胞结构及晶胞参数如图所示:
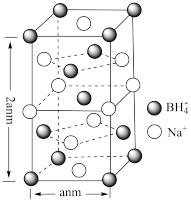
①Na+的配位数是____ 。
②若硼氢化钠晶胞上下底心处的Na+被Li+取代,得到晶体的化学式为____ 。
③NA代表阿伏加德罗常数的值,则NaBH4晶体的密度为____ g•cm-3(用含a、NA的式子表示)。
(1)基态硼原子的电子排布图是
(2)硼与铍相比,第一电离能较高的是
(3)NaBH4中所含的化学键的类型有
(4)硼氢化钠(NaBH4)的晶胞结构及晶胞参数如图所示:

①Na+的配位数是
②若硼氢化钠晶胞上下底心处的Na+被Li+取代,得到晶体的化学式为
③NA代表阿伏加德罗常数的值,则NaBH4晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】Fe、HCN与K2CO3在一定条件下发生如下反应:
Fe+6HCN+2K2CO3=K4Fe(CN)6+H2↑+2CO2↑+2H2O,回答下列问题:
(1)此化学方程式中涉及的第二周期元素的电负性由小到大的顺序为___________________ 。
(2)配合物K4Fe(CN)6的中心离子是____________ ,该离子价电子的基态电子排布图为____________ 。
(3)lmol HCN分子中含有σ键的数目为____________ ,HCN分子中碳原子轨道杂化类型是____________ ,与CN-互为等电子体的阴离子是____________ 。
(4)K2CO3中阴离子的空间构型为____________ ,其中碳原子的价层电子对数为____________ 。
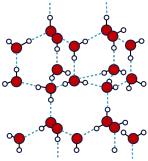
(5)冰的晶体结构模型如图,它的晶胞与金刚石相似,水分子之间以氢键相连接,在一个晶胞有__________ 个氢键,若氢键键长为d nm,则晶体密度(g/cm3)计算式为____________ (用NA表示阿伏加德罗常数的值)。
Fe+6HCN+2K2CO3=K4Fe(CN)6+H2↑+2CO2↑+2H2O,回答下列问题:
(1)此化学方程式中涉及的第二周期元素的电负性由小到大的顺序为
(2)配合物K4Fe(CN)6的中心离子是
(3)lmol HCN分子中含有σ键的数目为
(4)K2CO3中阴离子的空间构型为
(5)冰的晶体结构模型如图,它的晶胞与金刚石相似,水分子之间以氢键相连接,在一个晶胞有

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】钒(V)是一种重要的金属,有金属“维生素”之称,用途涵盖了航空航天、电池、光学、医药等众多领域,主要由五氧化二钒冶炼得到。某种由钒精矿(含 V2O5及少量 MgO、SiO2 等杂质)提取五氧化二钒的工艺流程如下图所示。
(1)钒精矿磨细的目的是____ 。浸出液中含有钒酸钠(Na3VO4)。VO 与PO
与PO 的空间构型相同,VO
的空间构型相同,VO 的空间构型为
的空间构型为____ 。
(2)用硫酸缓慢调节浸出液的pH为7,得到净化液中主要的阴离子是____ 。一定pH下,净化液中含有H4V4O12,已知H4V4O12具有八元环结构,其结构式可表示为____ 。
(3)净化液中加入氯化铵溶液进行氨化沉钒,过滤得到的固体经煅烧后得到V2O5,煅烧过程中发生反应的化学方程式是____ 。
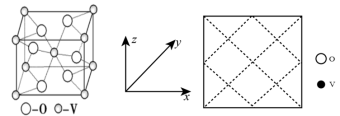
(4)五氧化二钒的结构简式如图所示,该结构中 σ 键与 π 键个数之比是____ 。____ 。请在右图中画出该晶胞沿z轴方向的平面投影图____ 。
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 | VO | VO | V2O | VO |
 与PO
与PO 的空间构型相同,VO
的空间构型相同,VO 的空间构型为
的空间构型为(2)用硫酸缓慢调节浸出液的pH为7,得到净化液中主要的阴离子是
(3)净化液中加入氯化铵溶液进行氨化沉钒,过滤得到的固体经煅烧后得到V2O5,煅烧过程中发生反应的化学方程式是
(4)五氧化二钒的结构简式如图所示,该结构中 σ 键与 π 键个数之比是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】利用太阳能光解水,制备的H2用于还原CO2合成有机物,可实现资源的再利用。回答下列问题:
Ⅰ.半导体光催化剂浸入水或电解质溶液中,光照时可在其表面得到产物
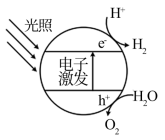
(1)下图为该催化剂在水中发生光催化反应的原理示意图。光解水能量转化形式为___________ 。
(2)若将该催化剂置于Na2SO3溶液中,产物之一为 ,另一产物为
,另一产物为__________ 。若将该催化剂置于AgNO3溶液中,产物之一为O2,写出生成另一产物的离子反应式__________ 。
Ⅱ.用H2还原CO2可以在一定条下合成CH3OH(不考虑副反应):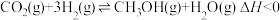
(3)某温度下,恒容密闭容器中,CO2和H2的起始浓度分别为 a mol‧L-1和3 a mol‧L-1,反应平衡时,CH3OH的产率为b,该温度下反应平衡常数的值为___________ 。
(4)恒压下,CO2和H2的起始物质的量比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出H2O。
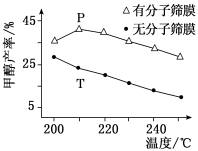
①甲醇平衡产率随温度升高而降低的原因为____________ 。
②P点甲醇产率高于T点的原因为___________ 。
③根据上图,在此条件下采用该分子筛膜时的最佳反应温度为___________ °C。
Ⅲ.调节溶液pH可实现工业废气CO2的捕获和释放
(5) 的空间构型为
的空间构型为__________ 。已知25℃碳酸电离常数为Ka1、Ka2,当溶液pH=12时, =1:
=1:_______ :__________ 。
Ⅰ.半导体光催化剂浸入水或电解质溶液中,光照时可在其表面得到产物
(1)下图为该催化剂在水中发生光催化反应的原理示意图。光解水能量转化形式为

(2)若将该催化剂置于Na2SO3溶液中,产物之一为
 ,另一产物为
,另一产物为Ⅱ.用H2还原CO2可以在一定条下合成CH3OH(不考虑副反应):
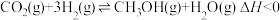
(3)某温度下,恒容密闭容器中,CO2和H2的起始浓度分别为 a mol‧L-1和3 a mol‧L-1,反应平衡时,CH3OH的产率为b,该温度下反应平衡常数的值为
(4)恒压下,CO2和H2的起始物质的量比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出H2O。

①甲醇平衡产率随温度升高而降低的原因为
②P点甲醇产率高于T点的原因为
③根据上图,在此条件下采用该分子筛膜时的最佳反应温度为
Ⅲ.调节溶液pH可实现工业废气CO2的捕获和释放
(5)
 的空间构型为
的空间构型为 =1:
=1:
您最近一年使用:0次
【推荐1】氧化锌、氮化镓及新型多相催化剂组成的纳米材料能利用可见光分解水,生成氢气和氧气。
Zn2+基态核外电子排布式为______________ ,其核外存在______________ 对自旋相反的电子。
写出两个与水分子具有相同空间构型的分子和阴离子:__________ ,____________ 。
水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是______________ (填序号)。
A、氧原子的杂化类型发生了改变 B、微粒的空间构型发生了改变
C、微粒的化学性质发生了改变 D、微粒中的键角发生了改变
在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图甲),已知冰的升华热是+51kJ mol-1,除氢键外,水分子间还存在范德华力(11kJ
mol-1,除氢键外,水分子间还存在范德华力(11kJ mol-1),则冰晶体中氢键的键能是
mol-1),则冰晶体中氢键的键能是___________ kJ mol-1。
mol-1。
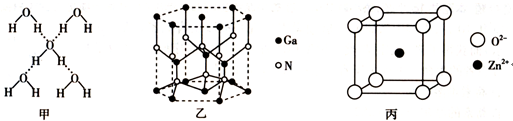
氮化镓的晶体结构如图乙所示,其中氮原子的杂化轨道类型是______________ ;N、Ga原子之间存在配位键,该配位键中提供电子对的原子是______________ ;该晶体的化学式为______________ 。金刚砂(SiC)和氮化镓并称为第三代半导体材料的双雄,它与金刚石具有相似的晶体结构,试比较金刚石和金刚砂的熔点高低,并说明理由:__________________________ 。
某种ZnO晶体的晶胞如图丙所示,Zn2+的配位数为_______________ ,其晶胞中Zn2+和O2-之间的距离为apm,列式表示该晶体的密度:____________ g cm-3(不必计算结果)。
cm-3(不必计算结果)。
Zn2+基态核外电子排布式为
写出两个与水分子具有相同空间构型的分子和阴离子:
水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是
A、氧原子的杂化类型发生了改变 B、微粒的空间构型发生了改变
C、微粒的化学性质发生了改变 D、微粒中的键角发生了改变
在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图甲),已知冰的升华热是+51kJ
 mol-1,除氢键外,水分子间还存在范德华力(11kJ
mol-1,除氢键外,水分子间还存在范德华力(11kJ mol-1),则冰晶体中氢键的键能是
mol-1),则冰晶体中氢键的键能是 mol-1。
mol-1。
氮化镓的晶体结构如图乙所示,其中氮原子的杂化轨道类型是
某种ZnO晶体的晶胞如图丙所示,Zn2+的配位数为
 cm-3(不必计算结果)。
cm-3(不必计算结果)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】镍是一种硬而有延展性并具有铁磁性的金属,它能高度磨光和抗腐蚀,其中一种制备金属镍的方法为NiSO4+H3PO3+H2O= Ni +H3PO4+H2SO4。回答下列问题:
(1)Ni的价电子排布式为___________ , 金属Ni是面心立方堆积,则其配位数为___________ 。
(2)O、P、S三种元素电负性从小到大排列为___________ 。
(3)NiSO4在熔融状态时能导电,上述制备反应所涉及的的六种物质中,所属晶体类型___________ 种。NiSO4水溶液中,Ni2+总是以[ Ni(H2O)6]2+离子存在,Ni2+与H2O之间形成的化学键称为___________ ,提供孤电子对的原子是___________ 。
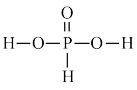
(4)H3PO3称为亚磷酸,结构式可表示如图所示,其中心原子的杂化轨道类型为___________ , 亚磷酸为___________ 元酸。
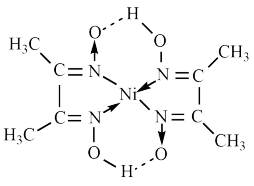
(5)丁二酮肟是检验Ni2+的灵敏试剂,可与Ni2+生成丁二酮肟镍红色沉淀( 结构如图所示)。丁二酮肟镍分子内存在的作用力有___________ (填标号)。
A.金属键 B.氢键 C.离子键 D.配位键 E.范德华力
(1)Ni的价电子排布式为
(2)O、P、S三种元素电负性从小到大排列为
(3)NiSO4在熔融状态时能导电,上述制备反应所涉及的的六种物质中,所属晶体类型
(4)H3PO3称为亚磷酸,结构式可表示如图所示,其中心原子的杂化轨道类型为

(5)丁二酮肟是检验Ni2+的灵敏试剂,可与Ni2+生成丁二酮肟镍红色沉淀( 结构如图所示)。丁二酮肟镍分子内存在的作用力有
A.金属键 B.氢键 C.离子键 D.配位键 E.范德华力

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】元素周期表在化学中有举足轻重的地位。请根据提示回答下列问题:
(1)铁在生活生产中用途广泛,写出 Fe 在元素周期表中的位置_______ 。Fe 分别与硫单质和氯气共热,可以得到两种含铁的二元化合物。请问这两种物质中金属阳离子的未成对电子数之比为_______ 。
(2)古往今来,人类发展的脚步离不开青铜器的冶炼,锻造及使用。如今,铜元素依旧为科研人员所钟爱,请写出铜原子的价电子排布式_______ 。利用铜离子作为中心原子可以形成多种具有良好特性的配合物。我们熟知的是一种深蓝色配合物,向硫酸铜溶液中通入过量氨气,可制备这种深蓝色配合物[Cu(NH3)4]2+。请用适当的化学用语描述该反应过程的实质_______ 。写出[Cu(NH3)4]2+配体的电子式_______ 。
(3)I1表示第一电离,I1(Mg)> I1(Al)> I1(Na),原因是_______ 。
(4)CoO 的晶胞如图所示。
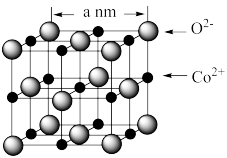
设阿伏加德罗常数的值为 NA,则 CoO 晶体的密度为_______ g﹒cm−3(列出计算式即可)
(5)磷元素在农药的合成中有着重要作用。了解其化合物的结构有助于我们合成新型农药,提高粮食的产量。PO 的 VSEPR 模型为
的 VSEPR 模型为_______ ,其中 P 的杂化轨道类型为_______ 。
(6)配位化学中,硼元素深受研究者的喜爱。其原因在于 B 容易与配体形成配位键,如BF 、B(OH)
、B(OH) 等,从原子结构分析其原因
等,从原子结构分析其原因_______ 。
(7)溶解度、熔沸点、颜色等是每种物质自身特有的性质,但也存在一定的规律。
①水和 H2S 均可以溶于乙醇,但 H2O 在乙醇中的溶解度大于 H2S 的原因_______
a.水和乙醇均为分子晶体 b.水和乙醇分子间可以形成氢键 c.水和乙醇可以发生反应
②比较下列锗卤化物的熔点和沸点,分析其变化规律的原因_______ 。
(1)铁在生活生产中用途广泛,写出 Fe 在元素周期表中的位置
(2)古往今来,人类发展的脚步离不开青铜器的冶炼,锻造及使用。如今,铜元素依旧为科研人员所钟爱,请写出铜原子的价电子排布式
(3)I1表示第一电离,I1(Mg)> I1(Al)> I1(Na),原因是
(4)CoO 的晶胞如图所示。

设阿伏加德罗常数的值为 NA,则 CoO 晶体的密度为
(5)磷元素在农药的合成中有着重要作用。了解其化合物的结构有助于我们合成新型农药,提高粮食的产量。PO
 的 VSEPR 模型为
的 VSEPR 模型为(6)配位化学中,硼元素深受研究者的喜爱。其原因在于 B 容易与配体形成配位键,如BF
 、B(OH)
、B(OH) 等,从原子结构分析其原因
等,从原子结构分析其原因(7)溶解度、熔沸点、颜色等是每种物质自身特有的性质,但也存在一定的规律。
①水和 H2S 均可以溶于乙醇,但 H2O 在乙醇中的溶解度大于 H2S 的原因
a.水和乙醇均为分子晶体 b.水和乙醇分子间可以形成氢键 c.水和乙醇可以发生反应
②比较下列锗卤化物的熔点和沸点,分析其变化规律的原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约 400 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】某铬贫矿主要成分为亚铬酸亚铁 Fe(CrO2)2,还含有 Fe2O3、MgO、 Al2O3,采用次氯酸钠法处理矿石并制备 CrO3的工艺流程如图,已知“氧化浸出”时铁以最高价氧化物存在。

(1)Cr 的价电子排布式为___________ 。
(2)“氧化浸出”过程中 Fe(CrO2)2转化为 Na2CrO4的化学方程式为___________ 。
(3)“电解”过程中生成的化合物I为___________ ,“沉铝”过程中生成的化合物Ⅱ为 ___________ 。
(4) “沉铝”过程中生成 Al(OH)3的离子方程式为___________ 。
(5) “混合”后要进行过滤与洗涤,简述实验室中洗涤沉淀的操作:___________ 。
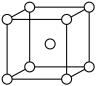
(6)金属铬的晶胞如图所示,晶胞边长为a pm,则该晶胞的密度ρ =___________ g·cm-3(写出计算表达式即可)

(1)Cr 的价电子排布式为
(2)“氧化浸出”过程中 Fe(CrO2)2转化为 Na2CrO4的化学方程式为
(3)“电解”过程中生成的化合物I为
(4) “沉铝”过程中生成 Al(OH)3的离子方程式为
(5) “混合”后要进行过滤与洗涤,简述实验室中洗涤沉淀的操作:
(6)金属铬的晶胞如图所示,晶胞边长为a pm,则该晶胞的密度ρ =

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】请回答下列问题。
(1)基态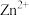 的核外电子排布式为
的核外电子排布式为_______ 。
(2)在醋酸溶液中 可与四苯硼化钠作用生成四苯硼化钾
可与四苯硼化钠作用生成四苯硼化钾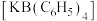 白色沉淀。若将“
白色沉淀。若将“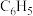 ”(苯基)视为一个整体,则阴离子
”(苯基)视为一个整体,则阴离子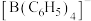 的空间构型是
的空间构型是_______ ,在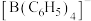 中不存在的化学键是
中不存在的化学键是_______ (填字母)。
A.配位键 B.非极性键 C.π键 D.离子键
(3)已知物质间的转化关系如图所示,其中a、c均大于0。
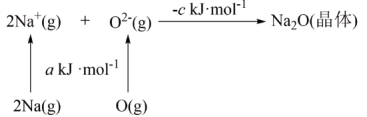
①基态钠原子的第一电离能为_______  。
。
②相同条件下, 的晶格能
的晶格能_______ (填“>”“<”或“=”)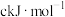 ,原因为
,原因为_______ 。
(4) 的立方晶胞结构如图所示。若紧邻的两个
的立方晶胞结构如图所示。若紧邻的两个 之间的距离为dpm,阿伏加德罗常数的值为
之间的距离为dpm,阿伏加德罗常数的值为 ,晶体的密度为
,晶体的密度为 ,则A原子的分数坐标为
,则A原子的分数坐标为_____ ;Na的摩尔质量可表示为____  (用含有d、ρ、
(用含有d、ρ、 的代数式表示)。
的代数式表示)。

(1)基态
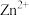 的核外电子排布式为
的核外电子排布式为(2)在醋酸溶液中
 可与四苯硼化钠作用生成四苯硼化钾
可与四苯硼化钠作用生成四苯硼化钾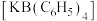 白色沉淀。若将“
白色沉淀。若将“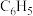 ”(苯基)视为一个整体,则阴离子
”(苯基)视为一个整体,则阴离子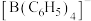 的空间构型是
的空间构型是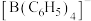 中不存在的化学键是
中不存在的化学键是A.配位键 B.非极性键 C.π键 D.离子键
(3)已知物质间的转化关系如图所示,其中a、c均大于0。

①基态钠原子的第一电离能为
 。
。②相同条件下,
 的晶格能
的晶格能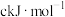 ,原因为
,原因为(4)
 的立方晶胞结构如图所示。若紧邻的两个
的立方晶胞结构如图所示。若紧邻的两个 之间的距离为dpm,阿伏加德罗常数的值为
之间的距离为dpm,阿伏加德罗常数的值为 ,晶体的密度为
,晶体的密度为 ,则A原子的分数坐标为
,则A原子的分数坐标为 (用含有d、ρ、
(用含有d、ρ、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】2021年10月18日《自然•化学》发表我国科学家研究成果,发现AgCrS2(AMX2家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
(1)基态硫原子核外最多有___________ 个电子顺时针旋转。基态铬原子有___________ 种电子运动状态。
(2)氧族元素有氧、硫、硒、碲等元素。这四种元素中,电负性最大的是___________ (填元素符号)。科学家用亚硒酸盐和硫酸盐跟踪固氮酶,研究反应机理。SeO 中硒的杂化轨道类型是
中硒的杂化轨道类型是___________ ,TeO 的空间结构模型为
的空间结构模型为___________ 。H2O、H2S、H2Se、H2Te的键角由大到小的顺序为___________ 。
(3)配合物[Cr(OH)3(H2O)(en)](en为H2NCH2CH2NH2)的中心离子配位数为___________ (Cr与O、N均形成了配位键),1mol该配合物中含___________ molσ键。
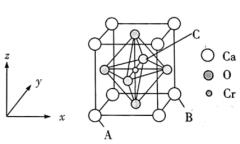
(4)复合材料氧铬酸钙的立方晶胞如图所示。已知A、B的原子坐标分别为(0,0,0)、(1,1,0),则C的原子坐标为___________ ,1个钙原子与___________ 个氧原子等距离且最近,已知钙和氧的最近距离为apm,则该晶体的密度为___________ g/cm3 (列出计算式即可)
(1)基态硫原子核外最多有
(2)氧族元素有氧、硫、硒、碲等元素。这四种元素中,电负性最大的是
 中硒的杂化轨道类型是
中硒的杂化轨道类型是 的空间结构模型为
的空间结构模型为(3)配合物[Cr(OH)3(H2O)(en)](en为H2NCH2CH2NH2)的中心离子配位数为
(4)复合材料氧铬酸钙的立方晶胞如图所示。已知A、B的原子坐标分别为(0,0,0)、(1,1,0),则C的原子坐标为

您最近一年使用:0次



