硫酸亚铁在工农业生产中有许多用途,如可用作农药,防治小麦黑穗病,制造磁性氧化铁、铁催化剂等。回答下列问题:
(1)在 气氛中,
气氛中,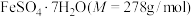 的脱水热分解过程如图所示:
的脱水热分解过程如图所示:
________ 。
(2)已知下列热化学方程式:
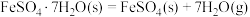

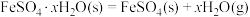

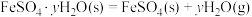

则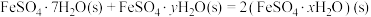 的
的
________  。
。
(3)将 置入抽空的刚性容器中,升高温度发生分解反应:
置入抽空的刚性容器中,升高温度发生分解反应: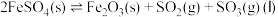 。平衡时
。平衡时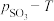 的关系如图所示。660K时,该反应的平衡总压
的关系如图所示。660K时,该反应的平衡总压
________ kPa、平衡常数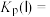
________  。
。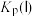 随反应温度升高而
随反应温度升高而________ (填“增大”“减小”或“不变”)。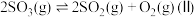 ,平衡时
,平衡时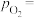
________ (用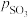 、
、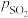 表示)。在929K时,
表示)。在929K时,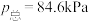 、
、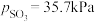 ,则
,则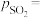
________ kPa,
________ kPa(列出计算式)。
(1)在
 气氛中,
气氛中,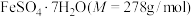 的脱水热分解过程如图所示:
的脱水热分解过程如图所示: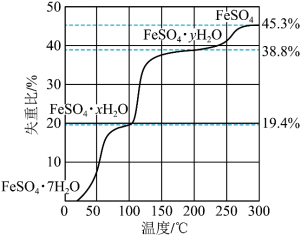

(2)已知下列热化学方程式:
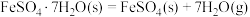

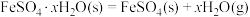

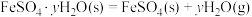

则
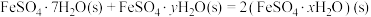 的
的
 。
。(3)将
 置入抽空的刚性容器中,升高温度发生分解反应:
置入抽空的刚性容器中,升高温度发生分解反应: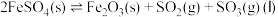 。平衡时
。平衡时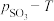 的关系如图所示。660K时,该反应的平衡总压
的关系如图所示。660K时,该反应的平衡总压
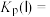
 。
。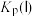 随反应温度升高而
随反应温度升高而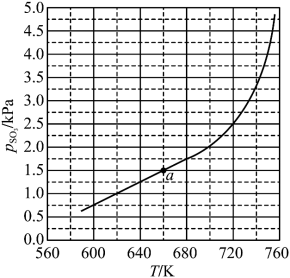
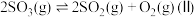 ,平衡时
,平衡时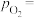
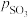 、
、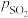 表示)。在929K时,
表示)。在929K时,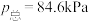 、
、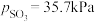 ,则
,则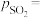

更新时间:2023-07-19 11:03:06
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】节能减排已经成为全社会的共识,有一种思路是将一氧化碳(CO)转化成可燃物质甲醇,甲醇汽油能减少有害气体(CO)排放。现有一种利用煤气化过程中生成的CO和H2来制备甲醇的方案,其反应原理为:CO(g)+2H2(g) CH3OH(g)。请根据下列图示回答问题:
CH3OH(g)。请根据下列图示回答问题:
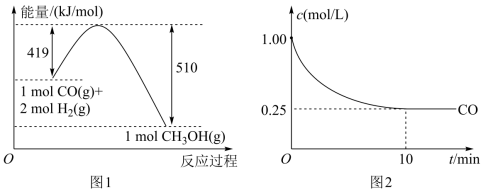
(1)根据(图1),写出此反应的热化学方程式___________ 。下列关于此反应的说法中,正确的是___________ (填字母)
A.任何条件都能自发进行 B.高温条件能够自发进行
C.任何条件都不自发进行 D.低温条件能够自发进行
(2)现进行如下实验,在体积为1L的密闭容器中,充入1
 和3
和3
 ,测得
,测得 的浓度随时间变化如(图2)所示,从反应开始到平衡,
的浓度随时间变化如(图2)所示,从反应开始到平衡, 的平均反应速率
的平均反应速率
___________ 
(3)恒容条件下,上述反应达到平衡后,以下措施中能使 增大的有___________。
增大的有___________。
(4)已知在常温常压下:化学反应①②的平衡常数分别为 ,
,
①2CH3OH(l)+O2(g) CO2(g)+4H2(g) K1
CO2(g)+4H2(g) K1
②2CO(g)+O2(g) CO2(g) K2
CO2(g) K2
则CO(g)+2H2(g) CH3OH(l)的
CH3OH(l)的
___________ (用含有K1,K2的代数式表达)
 CH3OH(g)。请根据下列图示回答问题:
CH3OH(g)。请根据下列图示回答问题:
(1)根据(图1),写出此反应的热化学方程式
A.任何条件都能自发进行 B.高温条件能够自发进行
C.任何条件都不自发进行 D.低温条件能够自发进行
(2)现进行如下实验,在体积为1L的密闭容器中,充入1

 和3
和3
 ,测得
,测得 的浓度随时间变化如(图2)所示,从反应开始到平衡,
的浓度随时间变化如(图2)所示,从反应开始到平衡, 的平均反应速率
的平均反应速率

(3)恒容条件下,上述反应达到平衡后,以下措施中能使
 增大的有___________。
增大的有___________。| A.升高温度 | B.充入 气 气 |
C.再充入1  和3 和3  | D.使用催化剂 |
 ,
,
①2CH3OH(l)+O2(g)
 CO2(g)+4H2(g) K1
CO2(g)+4H2(g) K1②2CO(g)+O2(g)
 CO2(g) K2
CO2(g) K2则CO(g)+2H2(g)
 CH3OH(l)的
CH3OH(l)的
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】按要求回答下列问题:
I.2018年10月15日新华社报道:全国农村应当在“绿色生态·美丽多彩·低碳节能·循环发展”的理念引导下,更快更好地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设。可见“低碳循环”已经引起了国民的重视,试回答下列问题:
(1)煤的气化和液化可以提高燃料的利用率。
已知25℃、101 kPa时: ①C(s)+ O2(g)=CO(g) ΔH=−126.4 kJ∙mol−1
O2(g)=CO(g) ΔH=−126.4 kJ∙mol−1
②2H2(g)+O2(g)=2H2O(l) ΔH=−571.6 kJ∙mol−1 ③H2O(g)=H2O(l) ΔH=−44 kJ∙mol−1,则在25℃、101kPa时: C(s)和H2O(g)反应生成CO(g)和H2(g)的热化学方程式为___________
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g) Fe(s)+CO2(g) ΔH>0
Fe(s)+CO2(g) ΔH>0
已知在1 100℃时,该反应的化学平衡常数K=0.263。1100℃时测得高炉中,c(CO2)=0.025 mol∙L−1,c(CO)=0.1 mol∙L−1,则在这种情况下,该反应向___________ (填“正”或 “逆”) 方向进行
(3)目前工业上可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=−49.0 kJ∙mol−1,现向体积为2 L的容积固定的密闭容器中,充入2mol CO2和6 mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如下图所示
CH3OH(g)+H2O(g) ΔH=−49.0 kJ∙mol−1,现向体积为2 L的容积固定的密闭容器中,充入2mol CO2和6 mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如下图所示

从反应开始到平衡,氢气的平均反应速率υ(H2)=____________
(4)下列措施能使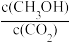 增大的是
增大的是___________ (填字母)
A.升高温度 B.若维持容器内压强不变,充入He(g)
C.再充入CO2 D.将H2O(g)从体系中分离
E.充入He(g),使体系压强增大 F.再充入H2
II.活性炭还原NO2的反应为2NO2(g)+2C(s) N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量活性炭发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量活性炭发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
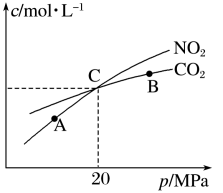
(5)A、B、C三点中NO2的转化率最低的是___________ (填“A”“B”或“C”)点
(6)计算C点时该反应的压强平衡常数Kp=___________ (Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
I.2018年10月15日新华社报道:全国农村应当在“绿色生态·美丽多彩·低碳节能·循环发展”的理念引导下,更快更好地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设。可见“低碳循环”已经引起了国民的重视,试回答下列问题:
(1)煤的气化和液化可以提高燃料的利用率。
已知25℃、101 kPa时: ①C(s)+
 O2(g)=CO(g) ΔH=−126.4 kJ∙mol−1
O2(g)=CO(g) ΔH=−126.4 kJ∙mol−1②2H2(g)+O2(g)=2H2O(l) ΔH=−571.6 kJ∙mol−1 ③H2O(g)=H2O(l) ΔH=−44 kJ∙mol−1,则在25℃、101kPa时: C(s)和H2O(g)反应生成CO(g)和H2(g)的热化学方程式为
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g)
 Fe(s)+CO2(g) ΔH>0
Fe(s)+CO2(g) ΔH>0已知在1 100℃时,该反应的化学平衡常数K=0.263。1100℃时测得高炉中,c(CO2)=0.025 mol∙L−1,c(CO)=0.1 mol∙L−1,则在这种情况下,该反应向
(3)目前工业上可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=−49.0 kJ∙mol−1,现向体积为2 L的容积固定的密闭容器中,充入2mol CO2和6 mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如下图所示
CH3OH(g)+H2O(g) ΔH=−49.0 kJ∙mol−1,现向体积为2 L的容积固定的密闭容器中,充入2mol CO2和6 mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如下图所示
从反应开始到平衡,氢气的平均反应速率υ(H2)=
(4)下列措施能使
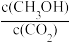 增大的是
增大的是A.升高温度 B.若维持容器内压强不变,充入He(g)
C.再充入CO2 D.将H2O(g)从体系中分离
E.充入He(g),使体系压强增大 F.再充入H2
II.活性炭还原NO2的反应为2NO2(g)+2C(s)
 N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量活性炭发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量活性炭发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
(5)A、B、C三点中NO2的转化率最低的是
(6)计算C点时该反应的压强平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇。
反应Ⅰ:CO2(g)+3H2(g) CH3OH(g)+H2O(g)ΔH1
CH3OH(g)+H2O(g)ΔH1
反应Ⅱ:CO(g)+2H2(g) CH3OH(g)ΔH2
CH3OH(g)ΔH2
下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K2):
(1)写出反应Ⅰ的化学平衡常数表达式:KⅠ=_________ ;保持恒温恒容,将反应Ⅰ的平衡体系中各物质浓度均增大为原来的2倍,则化学平衡____ (填“正向”“逆向”或“不”)移动,平衡常数KⅠ____ (填“变大”“变小”或“不变”)。
(2)在一定条件下将2molCO和6molH2充入2L的密闭容器中发生反应Ⅱ,5min后测得c(CO)=0.4mol·L-1,计算可得此段时间的反应速率(用H2表示)为____ mol·L-1·min-1。
(3)由表中数据判断ΔH2____ (填“>”“<”或“=”)0;反应CO2(g)+H2(g) CO(g)+H2O(g)ΔH3=
CO(g)+H2O(g)ΔH3=____ (用ΔH1和ΔH2表示)。
(4)若容器容积不变,则下列措施可提高反应Ⅱ中CO转化率的是____ (填序号)。
a.使用高效催化剂
b.充入He,使体系总压强增大
c.将CH3OH(g)从体系中分离
d.充入CO,使体系总压强增大
(5)比较这两种合成甲醇的方法,原子利用率较高的是____ (填“Ⅰ”或“Ⅱ”)。
反应Ⅰ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)ΔH1
CH3OH(g)+H2O(g)ΔH1反应Ⅱ:CO(g)+2H2(g)
 CH3OH(g)ΔH2
CH3OH(g)ΔH2下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K2):
| 温度 | 250℃ | 300℃ | 350℃ |
| KⅡ | 2.0 | 0.27 | 0.012 |
(2)在一定条件下将2molCO和6molH2充入2L的密闭容器中发生反应Ⅱ,5min后测得c(CO)=0.4mol·L-1,计算可得此段时间的反应速率(用H2表示)为
(3)由表中数据判断ΔH2
 CO(g)+H2O(g)ΔH3=
CO(g)+H2O(g)ΔH3=(4)若容器容积不变,则下列措施可提高反应Ⅱ中CO转化率的是
a.使用高效催化剂
b.充入He,使体系总压强增大
c.将CH3OH(g)从体系中分离
d.充入CO,使体系总压强增大
(5)比较这两种合成甲醇的方法,原子利用率较高的是
您最近一年使用:0次
【推荐1】研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)ΔH1=+489.0kJ·mol-1
C(s)+CO2(g)=2CO(g)ΔH2=+172.5kJ·mol-1。则CO还原Fe2O3(s)的热化学方程式为_____________ 。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:_____________ 。
(3)①CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如图。
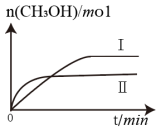
①曲线I、Ⅱ对应的温度大小关系为TⅠ__________ TⅡ(填“>”或“=”或“<”)。
②一定温度下,此反应在恒压 容器中进行,能判断该反应达到化学平衡状态的依据是______________ 。
a.容器中压强不变b.H2的体积分数不变c.c(H2)=3c(CH3OH)
d.容器中密度不变e.2个C=O断裂的同时有3个H-H断裂
(1)CO可用于炼铁,已知:Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)ΔH1=+489.0kJ·mol-1
C(s)+CO2(g)=2CO(g)ΔH2=+172.5kJ·mol-1。则CO还原Fe2O3(s)的热化学方程式为
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:
(3)①CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如图。

①曲线I、Ⅱ对应的温度大小关系为TⅠ
②一定温度下,此反应在
a.容器中压强不变b.H2的体积分数不变c.c(H2)=3c(CH3OH)
d.容器中密度不变e.2个C=O断裂的同时有3个H-H断裂
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题。
(1)治理大气中的 以及废水中的硫化物是环境保护的重要课题。加入固硫剂,是一种有效的治理措施。生石灰是常用的固硫剂,固硫过程中涉及的部分反应如下:
以及废水中的硫化物是环境保护的重要课题。加入固硫剂,是一种有效的治理措施。生石灰是常用的固硫剂,固硫过程中涉及的部分反应如下:
①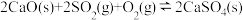
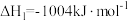
②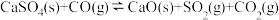
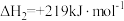
则 的燃烧热为
的燃烧热为___________  。
。
(2)一定条件下铁可以和 发生反应:
发生反应: 。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的
。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中
气体,反应过程中 气体和
气体和 气体的浓度与时间的关系如图所示。
气体的浓度与时间的关系如图所示。 时,正、逆反应速率的大小关系为
时,正、逆反应速率的大小关系为
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。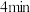 内,
内, 的平均反应速率
的平均反应速率
___________ 。
②下列描述能说明上述反应已达到平衡状态的是___________ (填序号)。
A.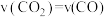
B.单位时间内生成 ,的同时生成
,的同时生成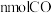
C.容器中气体压强不随时间变化而变化
D.容器中气体的平均相对分子质量不随时间变化而变化
E. 和
和 浓度相等
浓度相等
(3)某温度下在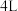 密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图所示:
密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图所示:___________ 。
②平衡时,混合气体中X、Y、Z的体积比为___________ 。
(1)治理大气中的
 以及废水中的硫化物是环境保护的重要课题。加入固硫剂,是一种有效的治理措施。生石灰是常用的固硫剂,固硫过程中涉及的部分反应如下:
以及废水中的硫化物是环境保护的重要课题。加入固硫剂,是一种有效的治理措施。生石灰是常用的固硫剂,固硫过程中涉及的部分反应如下:①
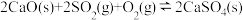
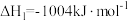
②
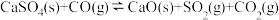
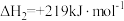
则
 的燃烧热为
的燃烧热为 。
。(2)一定条件下铁可以和
 发生反应:
发生反应: 。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的
。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中
气体,反应过程中 气体和
气体和 气体的浓度与时间的关系如图所示。
气体的浓度与时间的关系如图所示。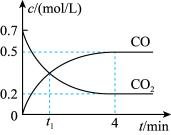
 时,正、逆反应速率的大小关系为
时,正、逆反应速率的大小关系为
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。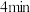 内,
内, 的平均反应速率
的平均反应速率
②下列描述能说明上述反应已达到平衡状态的是
A.
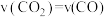
B.单位时间内生成
 ,的同时生成
,的同时生成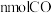
C.容器中气体压强不随时间变化而变化
D.容器中气体的平均相对分子质量不随时间变化而变化
E.
 和
和 浓度相等
浓度相等(3)某温度下在
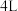 密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图所示:
密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图所示:
②平衡时,混合气体中X、Y、Z的体积比为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】甲醛在医药方面有重要用途。工业上可利用反应Ⅰ: CH3OH(g)  HCHO(g)+H2(g)来合成甲醛。
HCHO(g)+H2(g)来合成甲醛。
(1)已知:
反应Ⅱ : 2CH3OH(g)+O2(g) 2HCHO(g) +2H2O(g) △H2=-313.2kJ·mol-1
2HCHO(g) +2H2O(g) △H2=-313.2kJ·mol-1
反应Ⅲ: 2H2(g)+O2(g) 2H2O(g) △H3=-483. 6kJ ·mol-1
2H2O(g) △H3=-483. 6kJ ·mol-1
则反应Ⅰ : CH3OH(g) HCHO(g)+H2(g) 的△H1=
HCHO(g)+H2(g) 的△H1=_______ kJ·mol-1。
(2)利用反应Ⅰ合成甲醛时,为加快化学反应速率,同时提高CH3OH的平衡转化率,可采取的措施为
_______ 。
(3)T ℃时,向体积恒为2L的密闭容器中充入8mol CH3OH(g)发生反应Ⅰ,5min后反应达到平衡,测得混合体系中的HCHO( g)的体积分数为20%。
①下列事实不能说明该反应已达到化学平衡状态的是_______ (填序号)。
A. v正( HCHO)=v逆(H2)
B. c(CH3OH) : c(HCHO) : c(H2)=1 :1: 1
C.混合气体的平均相对分子质量不变
D.混合气体的密度保持不变
②5min内,v( CH3OH)=_______ mol· L-1· min-1。
③其他条件不变时,向已达平衡的反应体系中充入1mol CH3OH(g)和1mol H2(g),则此时v正_______ v逆(填“大于”“小于”或“等于”)。
(4)在催化剂作用下,甲醇脱氢制甲醛的部分机理如下:
历程i : CH3OH→·H+·CH2OH
历程ii: ·CH2OH-→·H+HCHO
历程iii:·CH2OH+3·H+CO
历程iv:·H+·H→H2
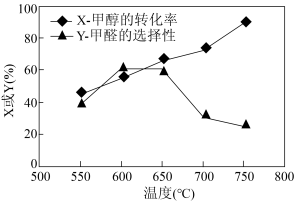
一定条件下测得温度对甲醇的转化率(X)、甲醛的选择性(Y)的影响如图所示[甲醛的选择性(Y)= ]。 则650℃ ~750℃,反应历程ii的速率。
]。 则650℃ ~750℃,反应历程ii的速率。_______ (填“大于”“小于”或“等于”)反应历程iii的速率,判断理由为_______ 。
 HCHO(g)+H2(g)来合成甲醛。
HCHO(g)+H2(g)来合成甲醛。(1)已知:
反应Ⅱ : 2CH3OH(g)+O2(g)
 2HCHO(g) +2H2O(g) △H2=-313.2kJ·mol-1
2HCHO(g) +2H2O(g) △H2=-313.2kJ·mol-1反应Ⅲ: 2H2(g)+O2(g)
 2H2O(g) △H3=-483. 6kJ ·mol-1
2H2O(g) △H3=-483. 6kJ ·mol-1则反应Ⅰ : CH3OH(g)
 HCHO(g)+H2(g) 的△H1=
HCHO(g)+H2(g) 的△H1=(2)利用反应Ⅰ合成甲醛时,为加快化学反应速率,同时提高CH3OH的平衡转化率,可采取的措施为
(3)T ℃时,向体积恒为2L的密闭容器中充入8mol CH3OH(g)发生反应Ⅰ,5min后反应达到平衡,测得混合体系中的HCHO( g)的体积分数为20%。
①下列事实不能说明该反应已达到化学平衡状态的是
A. v正( HCHO)=v逆(H2)
B. c(CH3OH) : c(HCHO) : c(H2)=1 :1: 1
C.混合气体的平均相对分子质量不变
D.混合气体的密度保持不变
②5min内,v( CH3OH)=
③其他条件不变时,向已达平衡的反应体系中充入1mol CH3OH(g)和1mol H2(g),则此时v正
(4)在催化剂作用下,甲醇脱氢制甲醛的部分机理如下:
历程i : CH3OH→·H+·CH2OH
历程ii: ·CH2OH-→·H+HCHO
历程iii:·CH2OH+3·H+CO
历程iv:·H+·H→H2
一定条件下测得温度对甲醇的转化率(X)、甲醛的选择性(Y)的影响如图所示[甲醛的选择性(Y)=
 ]。 则650℃ ~750℃,反应历程ii的速率。
]。 则650℃ ~750℃,反应历程ii的速率。
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】现将一定量NO2和N2O4的混合气体通入一定体积为2L的恒温密闭容器中,反应物浓度随时间变化关系如图。已知:2NO2(g) N2O4(g)+Q。
N2O4(g)+Q。
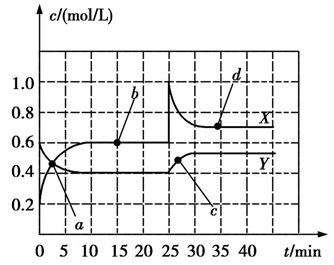
(1)前10min内用NO2表示的化学反应速率v(NO2)=___ ;
(2)a、b、c、d四个点中,表示化学反应处于平衡状态是___ ;
(3)35min时,反应2NO2(g) N2O4(g)在d点的平衡常数K(d)
N2O4(g)在d点的平衡常数K(d)___ K(b)(填“>”、“=”或“<”)。
(4)若要达到使NO2(g)的百分含量与d点相同的化学平衡状态,在25min时还可以采取的措施是___ 。
A.加入催化剂 B.缩小容器体积 C.升高温度 D.加入一定量的N2O4
 N2O4(g)+Q。
N2O4(g)+Q。
(1)前10min内用NO2表示的化学反应速率v(NO2)=
(2)a、b、c、d四个点中,表示化学反应处于平衡状态是
(3)35min时,反应2NO2(g)
 N2O4(g)在d点的平衡常数K(d)
N2O4(g)在d点的平衡常数K(d)(4)若要达到使NO2(g)的百分含量与d点相同的化学平衡状态,在25min时还可以采取的措施是
A.加入催化剂 B.缩小容器体积 C.升高温度 D.加入一定量的N2O4
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】填空。
(1)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为___________ 。
(2)图1是反应CO(g)+2H2(g)⇌CH3OH(g)在不同温度下CO的转化率随时间变化的曲线。
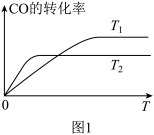
①该反应的焓变ΔH___________ (填“>”“<”或“=”)0。
②T1和T2温度下的平衡常数大小关系是K1___________ (填“>”“<”或“=”)K2。在T1温度下,往体积为1L的密闭容器中,充入1molCO和2molH2,经测得CO和CH3OH(g)的浓度随时间变化如图2所示。则该反应的平衡常数为___________ 。
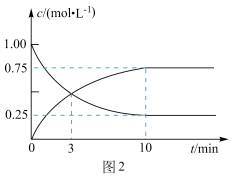
③若容器容积不变,下列措施可增加CO转化率的是___________ (填字母)。
a.升高温度
b.将CH3OH(g)从体系中分离
c.使用合适的催化剂
d.充入He,使体系总压强增大
④在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律。如图3是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系,曲线上a、b、c点对应的化学平衡常数分别为K1、K2、K3,则K1、K2、K3的大小关系为___________ 。
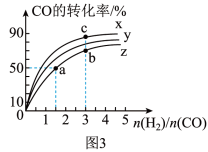
(1)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为
(2)图1是反应CO(g)+2H2(g)⇌CH3OH(g)在不同温度下CO的转化率随时间变化的曲线。

①该反应的焓变ΔH
②T1和T2温度下的平衡常数大小关系是K1

③若容器容积不变,下列措施可增加CO转化率的是
a.升高温度
b.将CH3OH(g)从体系中分离
c.使用合适的催化剂
d.充入He,使体系总压强增大
④在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律。如图3是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系,曲线上a、b、c点对应的化学平衡常数分别为K1、K2、K3,则K1、K2、K3的大小关系为

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】在国家“十二五环保规划”中,氮氧化物成为实行总量控制的污染物,其总量控制消减主要是烟气、燃煤的脱硝,机动车尾气治理等。
Ⅰ.甲烷还原氮的氧化物
(1)已知下列反应:
①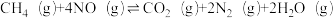 △H1=-1155.5kJ·mol-1
△H1=-1155.5kJ·mol-1
②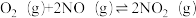 △H2=-112.5kJ·mol-1
△H2=-112.5kJ·mol-1
③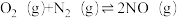 △H3=+178.0kJ·mol-1
△H3=+178.0kJ·mol-1
则反应④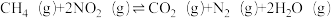 △H4=
△H4=___________ kJ·mol-1。
Ⅱ.三元催化剂直接转化氮的氧化物
(2)机动车尾气在三元催化剂作用下发生反应: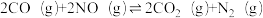 △H,实验测得:
△H,实验测得: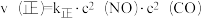 ,
,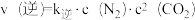 ,其中k正、k逆是只受温度影响的速率常数。在密闭容器中,该反应达到平衡,升温时,测得k逆增大的倍数比k正大,则△H
,其中k正、k逆是只受温度影响的速率常数。在密闭容器中,该反应达到平衡,升温时,测得k逆增大的倍数比k正大,则△H___________ 0(填“>”或“<”)。
Ⅲ.碱液吸收氮的氧化物
(3)用一定浓度的NaOH溶液吸收含氮氧化物的废气(含NO、NO2),生成亚硝酸盐,该反应的离子方程式是___________ 。
Ⅳ.氨气还原氮的氧化物
(4)某科研攻关小组在两个恒容(2.0L)密闭容器中进行如下投料对比实验:
两个容器中的混合气体在相同催化剂表面分别发生如下反应:
⑤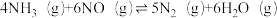 △H3=-1814kJ·mol-1
△H3=-1814kJ·mol-1
⑥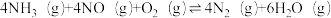 △H6
△H6
反应过程中,测得相同时间时NO的转化率随温度变化的曲线如图所示:
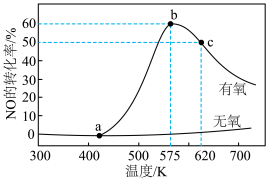
620K时,容器2中反应的平衡常数K=___________ (用分数表示),温度大于575K时,温度升高,容器2中NO转化率逐渐降低的原因是___________ (忽略温度对催化剂的影响);工厂在用氨气处理含氮氧化物的废气时,需通入一定量的空气,从图中曲线变化分析这种操作的优点是___________ 。
Ⅰ.甲烷还原氮的氧化物
(1)已知下列反应:
①
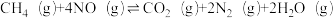 △H1=-1155.5kJ·mol-1
△H1=-1155.5kJ·mol-1②
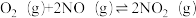 △H2=-112.5kJ·mol-1
△H2=-112.5kJ·mol-1③
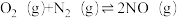 △H3=+178.0kJ·mol-1
△H3=+178.0kJ·mol-1则反应④
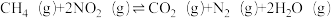 △H4=
△H4=Ⅱ.三元催化剂直接转化氮的氧化物
(2)机动车尾气在三元催化剂作用下发生反应:
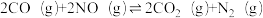 △H,实验测得:
△H,实验测得: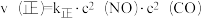 ,
,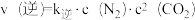 ,其中k正、k逆是只受温度影响的速率常数。在密闭容器中,该反应达到平衡,升温时,测得k逆增大的倍数比k正大,则△H
,其中k正、k逆是只受温度影响的速率常数。在密闭容器中,该反应达到平衡,升温时,测得k逆增大的倍数比k正大,则△HⅢ.碱液吸收氮的氧化物
(3)用一定浓度的NaOH溶液吸收含氮氧化物的废气(含NO、NO2),生成亚硝酸盐,该反应的离子方程式是
Ⅳ.氨气还原氮的氧化物
(4)某科研攻关小组在两个恒容(2.0L)密闭容器中进行如下投料对比实验:
| NH3 | NO | O2 | |
| 容器1 | 4mol | 4mol | 0 |
| 容器2 | 4mol | 4mol | 1mol |
⑤
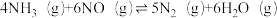 △H3=-1814kJ·mol-1
△H3=-1814kJ·mol-1⑥
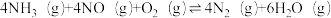 △H6
△H6反应过程中,测得相同时间时NO的转化率随温度变化的曲线如图所示:

620K时,容器2中反应的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下可合成甲醇,发生的主要反应如下:
I.CO(g)+2H2(g) CH3OH(g) △H1=−129.0 kJ∙mol−1
CH3OH(g) △H1=−129.0 kJ∙mol−1
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41 kJ∙mol−1
CO(g)+H2O(g) △H2=+41 kJ∙mol−1
Ⅲ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
回答下列问题:
(1)△H3=______ 。
(2)将2.0molCO2和3.0molH2通入容积为3L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得H2的平衡转化率与温度的关系如图所示。
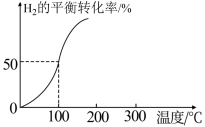
①100℃时反应达到平衡所需的时间为5min,则反应从起始至5min内,用H2表示该反应的平均反应速率为______ 。
②100℃时,反应Ⅱ的平衡常数K=______ 。
③下列可用来判断该反应已达到平衡状态的有______ (填标号)。
A.CO的含量保持不变 B.容器中c(CO2)=c(CO)
C.容器中混合气体的密度保持不变 D.υ正(H2)= υ逆(H2O)
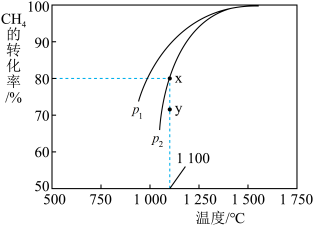
(3)利用天然气制取合成气的原理CO2(g)+CH4(g) 2CO(g)+2H2(g),在密闭容器中通入物质的量浓度均为1 mol∙L−1的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如图所示,则p1
2CO(g)+2H2(g),在密闭容器中通入物质的量浓度均为1 mol∙L−1的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如图所示,则p1______ p2(填“大于”或“小于”);压强为p2时,在Y点:υ正______ υ逆。(填“大于”“小于”“等于”)
I.CO(g)+2H2(g)
 CH3OH(g) △H1=−129.0 kJ∙mol−1
CH3OH(g) △H1=−129.0 kJ∙mol−1Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41 kJ∙mol−1
CO(g)+H2O(g) △H2=+41 kJ∙mol−1Ⅲ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3回答下列问题:
(1)△H3=
(2)将2.0molCO2和3.0molH2通入容积为3L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得H2的平衡转化率与温度的关系如图所示。

①100℃时反应达到平衡所需的时间为5min,则反应从起始至5min内,用H2表示该反应的平均反应速率为
②100℃时,反应Ⅱ的平衡常数K=
③下列可用来判断该反应已达到平衡状态的有
A.CO的含量保持不变 B.容器中c(CO2)=c(CO)
C.容器中混合气体的密度保持不变 D.υ正(H2)= υ逆(H2O)
(3)利用天然气制取合成气的原理CO2(g)+CH4(g)
 2CO(g)+2H2(g),在密闭容器中通入物质的量浓度均为1 mol∙L−1的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如图所示,则p1
2CO(g)+2H2(g),在密闭容器中通入物质的量浓度均为1 mol∙L−1的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如图所示,则p1
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】氮及其化合物与人们的生活生产密切相关。回答下列问题:
(1)微生物作用下,废水中的NH 可转化为NO
可转化为NO ,该反应分两步反应:
,该反应分两步反应:
Ⅰ步:2 NH (aq)+3O2(g)=2NO
(aq)+3O2(g)=2NO (aq)+4H+(aq)+2H2O(l) ΔH=-546 kJ/mol
(aq)+4H+(aq)+2H2O(l) ΔH=-546 kJ/mol
Ⅱ步:2NO (aq)+O2(g)=2NO
(aq)+O2(g)=2NO (aq) ΔH=-146 kJ/mol。
(aq) ΔH=-146 kJ/mol。
则低浓度氨氮废水中的NH (aq)氧化生成NO
(aq)氧化生成NO (aq)的热化学方程式为:NH
(aq)的热化学方程式为:NH (aq)+2O2(g)=2H+(aq)+H2 O(l)+NO
(aq)+2O2(g)=2H+(aq)+H2 O(l)+NO (aq) ΔH=
(aq) ΔH=___________ kJ/mol。
(2)氮与氧能形成多种二元化合物,这些化合物往往不稳定,其中NO2比较稳定。
已知可逆反应N2O4(g) 2NO2(g) ΔH>0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
2NO2(g) ΔH>0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
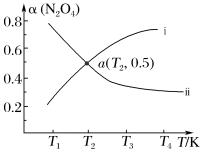
α(N2O4)随温度的变化的正确曲线是___________ (填“i”或“ii”)。若该容器中通入N2O4的起始浓度为2mol/L,则a点温度下的平衡常数K=___________ 。若加入催化剂,图中的曲线会___________ (填“上移”、“下移”或“不移”)。
(3)机动车尾气是造成雾霾的主要因素之一,CO、NO在催化剂作用下可转化为无害气体:2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH<0。已知甲、乙两个恒温恒容容器,容积均为1 L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:
N2(g)+2CO2(g) ΔH<0。已知甲、乙两个恒温恒容容器,容积均为1 L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:
则反应温度高的容器是___________ (填“甲”或“乙”);甲容器中,0~120 min的速率v(N2)=___________ mol/(L·min),达到化学平衡后,乙容器中各物质均加倍,则平衡向___________ (“正反应”或“逆反应”)方向移动。
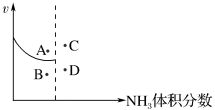
(4)500 ℃时,恒容密闭容器中通入1 mol N2和3 mol H2,模拟合成氨的反应,已知该反应放热,且随着反应的进行合成氨的正反应速率与NH3的体积分数的关系如下图所示,若升高温度再次达到平衡时,可能的点为___________ (从点“A、B、C、D”中选择)。
(1)微生物作用下,废水中的NH
 可转化为NO
可转化为NO ,该反应分两步反应:
,该反应分两步反应:Ⅰ步:2 NH
 (aq)+3O2(g)=2NO
(aq)+3O2(g)=2NO (aq)+4H+(aq)+2H2O(l) ΔH=-546 kJ/mol
(aq)+4H+(aq)+2H2O(l) ΔH=-546 kJ/molⅡ步:2NO
 (aq)+O2(g)=2NO
(aq)+O2(g)=2NO (aq) ΔH=-146 kJ/mol。
(aq) ΔH=-146 kJ/mol。则低浓度氨氮废水中的NH
 (aq)氧化生成NO
(aq)氧化生成NO (aq)的热化学方程式为:NH
(aq)的热化学方程式为:NH (aq)+2O2(g)=2H+(aq)+H2 O(l)+NO
(aq)+2O2(g)=2H+(aq)+H2 O(l)+NO (aq) ΔH=
(aq) ΔH=(2)氮与氧能形成多种二元化合物,这些化合物往往不稳定,其中NO2比较稳定。
已知可逆反应N2O4(g)
 2NO2(g) ΔH>0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
2NO2(g) ΔH>0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
α(N2O4)随温度的变化的正确曲线是
(3)机动车尾气是造成雾霾的主要因素之一,CO、NO在催化剂作用下可转化为无害气体:2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH<0。已知甲、乙两个恒温恒容容器,容积均为1 L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:
N2(g)+2CO2(g) ΔH<0。已知甲、乙两个恒温恒容容器,容积均为1 L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:| t/min | 0 | 40 | 80 | 120 | 160 |
| n甲(CO)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n乙(CO)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
(4)500 ℃时,恒容密闭容器中通入1 mol N2和3 mol H2,模拟合成氨的反应,已知该反应放热,且随着反应的进行合成氨的正反应速率与NH3的体积分数的关系如下图所示,若升高温度再次达到平衡时,可能的点为

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】甲醇是最基本的有机化工原料之一、工业上可用二氧化碳和氢气反应来生产甲醇,反应方程式为:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。
(1)某温度下,在2 L密闭容器中,充入2.4 mol CO2和4.4 mol H2,发生合成甲醇的反应,测得甲醇的物质的量浓度随时间的变化图像如下图中的曲线I,则前4分钟v(CO2)=_______ ;若在1 min时, 改变某一反应条件,曲线I变为曲线II,则改变的条件为_______ ;该温度下反应的化学平衡常数为_______ ;若体系已达到平衡状态,再向该容器中充入0.5 mol CO2,再次达平衡时,H2的平衡转化率_______ (填“增大”、“减小” 或“无变化”)。
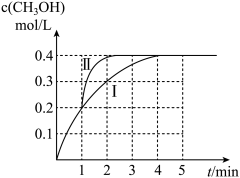
(2)在恒温恒容的条件下,下列选项能说明反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)已达平衡状态的是_______ (填字母) 。
A. v正(H2):v逆(CH3OH)=1:3
B.混合气体的密度不再变化
C.混合气的平均摩尔质量不再变化
D.体系压强不再变化
E. c(CO):c(H2):c(CH3OH):c(H2O)=1:3:1:1
(1)某温度下,在2 L密闭容器中,充入2.4 mol CO2和4.4 mol H2,发生合成甲醇的反应,测得甲醇的物质的量浓度随时间的变化图像如下图中的曲线I,则前4分钟v(CO2)=

(2)在恒温恒容的条件下,下列选项能说明反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)已达平衡状态的是
A. v正(H2):v逆(CH3OH)=1:3
B.混合气体的密度不再变化
C.混合气的平均摩尔质量不再变化
D.体系压强不再变化
E. c(CO):c(H2):c(CH3OH):c(H2O)=1:3:1:1
您最近一年使用:0次



