甲醛在医药方面有重要用途。工业上可利用反应Ⅰ: CH3OH(g)  HCHO(g)+H2(g)来合成甲醛。
HCHO(g)+H2(g)来合成甲醛。
(1)已知:
反应Ⅱ : 2CH3OH(g)+O2(g) 2HCHO(g) +2H2O(g) △H2=-313.2kJ·mol-1
2HCHO(g) +2H2O(g) △H2=-313.2kJ·mol-1
反应Ⅲ: 2H2(g)+O2(g) 2H2O(g) △H3=-483. 6kJ ·mol-1
2H2O(g) △H3=-483. 6kJ ·mol-1
则反应Ⅰ : CH3OH(g) HCHO(g)+H2(g) 的△H1=
HCHO(g)+H2(g) 的△H1=_______ kJ·mol-1。
(2)利用反应Ⅰ合成甲醛时,为加快化学反应速率,同时提高CH3OH的平衡转化率,可采取的措施为
_______ 。
(3)T ℃时,向体积恒为2L的密闭容器中充入8mol CH3OH(g)发生反应Ⅰ,5min后反应达到平衡,测得混合体系中的HCHO( g)的体积分数为20%。
①下列事实不能说明该反应已达到化学平衡状态的是_______ (填序号)。
A. v正( HCHO)=v逆(H2)
B. c(CH3OH) : c(HCHO) : c(H2)=1 :1: 1
C.混合气体的平均相对分子质量不变
D.混合气体的密度保持不变
②5min内,v( CH3OH)=_______ mol· L-1· min-1。
③其他条件不变时,向已达平衡的反应体系中充入1mol CH3OH(g)和1mol H2(g),则此时v正_______ v逆(填“大于”“小于”或“等于”)。
(4)在催化剂作用下,甲醇脱氢制甲醛的部分机理如下:
历程i : CH3OH→·H+·CH2OH
历程ii: ·CH2OH-→·H+HCHO
历程iii:·CH2OH+3·H+CO
历程iv:·H+·H→H2
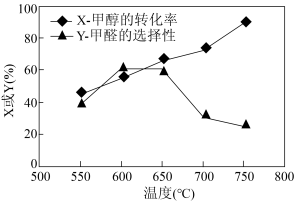
一定条件下测得温度对甲醇的转化率(X)、甲醛的选择性(Y)的影响如图所示[甲醛的选择性(Y)= ]。 则650℃ ~750℃,反应历程ii的速率。
]。 则650℃ ~750℃,反应历程ii的速率。_______ (填“大于”“小于”或“等于”)反应历程iii的速率,判断理由为_______ 。
 HCHO(g)+H2(g)来合成甲醛。
HCHO(g)+H2(g)来合成甲醛。(1)已知:
反应Ⅱ : 2CH3OH(g)+O2(g)
 2HCHO(g) +2H2O(g) △H2=-313.2kJ·mol-1
2HCHO(g) +2H2O(g) △H2=-313.2kJ·mol-1反应Ⅲ: 2H2(g)+O2(g)
 2H2O(g) △H3=-483. 6kJ ·mol-1
2H2O(g) △H3=-483. 6kJ ·mol-1则反应Ⅰ : CH3OH(g)
 HCHO(g)+H2(g) 的△H1=
HCHO(g)+H2(g) 的△H1=(2)利用反应Ⅰ合成甲醛时,为加快化学反应速率,同时提高CH3OH的平衡转化率,可采取的措施为
(3)T ℃时,向体积恒为2L的密闭容器中充入8mol CH3OH(g)发生反应Ⅰ,5min后反应达到平衡,测得混合体系中的HCHO( g)的体积分数为20%。
①下列事实不能说明该反应已达到化学平衡状态的是
A. v正( HCHO)=v逆(H2)
B. c(CH3OH) : c(HCHO) : c(H2)=1 :1: 1
C.混合气体的平均相对分子质量不变
D.混合气体的密度保持不变
②5min内,v( CH3OH)=
③其他条件不变时,向已达平衡的反应体系中充入1mol CH3OH(g)和1mol H2(g),则此时v正
(4)在催化剂作用下,甲醇脱氢制甲醛的部分机理如下:
历程i : CH3OH→·H+·CH2OH
历程ii: ·CH2OH-→·H+HCHO
历程iii:·CH2OH+3·H+CO
历程iv:·H+·H→H2
一定条件下测得温度对甲醇的转化率(X)、甲醛的选择性(Y)的影响如图所示[甲醛的选择性(Y)=
 ]。 则650℃ ~750℃,反应历程ii的速率。
]。 则650℃ ~750℃,反应历程ii的速率。
21-22高三·云南昆明·阶段练习 查看更多[3]
更新时间:2022-07-01 21:40:40
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】甲醇是实现碳中和循环的低碳燃料,是一个取之不尽的能源载体。
(1) 可与
可与 反应生成甲醇和水,其反应过程如下。
反应生成甲醇和水,其反应过程如下。
反应①:

 ;
;
反应②: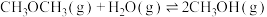

 ;
;
反应③: 的
的
________ ,平衡常数
________ (用 、
、 表示)
表示)
(2)一定条件下向恒容密闭容器中充入 和
和 ,在不同催化剂作用下发生反应Ⅰ、Ⅱ、Ⅲ,相同时间内
,在不同催化剂作用下发生反应Ⅰ、Ⅱ、Ⅲ,相同时间内 的转化率随温度变化如图所示。
的转化率随温度变化如图所示。

①催化剂效果最佳的是反应________ (填“Ⅰ”“Ⅱ”或“Ⅲ”)。
②若反应Ⅲ在 点时已达平衡状态,
点时已达平衡状态, 点
点 的转化率高于
的转化率高于 点和
点和 点的原因是
点的原因是________ 。
(3)在压强为 ,
, 、
、 的起始物质的量比为
的起始物质的量比为 的条件下,发生以下竞争反应。
的条件下,发生以下竞争反应。
反应一:

反应二:
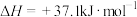
实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度的变化如图所示。
的选择性随温度的变化如图所示。

已知: 的选择性
的选择性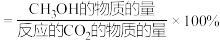 。
。
①有利于提高 的选择性的措施有
的选择性的措施有________ (填字母)。
A.适当降温 B.适当升温 C.选择合适的催化剂
②温度高于350℃时,体系中发生的反应以________ (填“反应一”或“反应二”)为主,并说明理由:________ 。
③其中表示平衡时 的选择性的曲线是
的选择性的曲线是________ (填“ ”或“
”或“ ”)。
”)。
④400℃时,平衡时压强为 ,反应一用气体分压表示的化学平衡常数
,反应一用气体分压表示的化学平衡常数
________ (只代入数据即可,用容器中各气体成分的分压表示,分压=总压×物质的量分数)。
(1)
 可与
可与 反应生成甲醇和水,其反应过程如下。
反应生成甲醇和水,其反应过程如下。反应①:


 ;
;反应②:
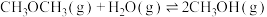

 ;
;反应③:
 的
的

 、
、 表示)
表示)(2)一定条件下向恒容密闭容器中充入
 和
和 ,在不同催化剂作用下发生反应Ⅰ、Ⅱ、Ⅲ,相同时间内
,在不同催化剂作用下发生反应Ⅰ、Ⅱ、Ⅲ,相同时间内 的转化率随温度变化如图所示。
的转化率随温度变化如图所示。
①催化剂效果最佳的是反应
②若反应Ⅲ在
 点时已达平衡状态,
点时已达平衡状态, 点
点 的转化率高于
的转化率高于 点和
点和 点的原因是
点的原因是(3)在压强为
 ,
, 、
、 的起始物质的量比为
的起始物质的量比为 的条件下,发生以下竞争反应。
的条件下,发生以下竞争反应。反应一:


反应二:

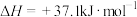
实验测得
 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度的变化如图所示。
的选择性随温度的变化如图所示。
已知:
 的选择性
的选择性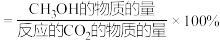 。
。①有利于提高
 的选择性的措施有
的选择性的措施有A.适当降温 B.适当升温 C.选择合适的催化剂
②温度高于350℃时,体系中发生的反应以
③其中表示平衡时
 的选择性的曲线是
的选择性的曲线是 ”或“
”或“ ”)。
”)。④400℃时,平衡时压强为
 ,反应一用气体分压表示的化学平衡常数
,反应一用气体分压表示的化学平衡常数
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】将CO2转化为更有价值的化工原料,正成为科学家们研究的一个重要领域。回答下列问题:
(1)已知:①2H2(g)+O2(g) =2H2O(g) ΔH= − 484 kJ∙mol−1
②2CH3OH(g)+ 3O2(g) =2CO2(g)+4H2O(g) ΔH =−1353 kJ∙mol−1
则CO2(g)+ 3H2(g) = CH3OH(g)+H2O(g) ΔH =_______ kJ∙mol−1。
(2)在恒压密闭容器中通入CO2和H2的混合气体,制备甲醇过程中测得甲醇的时空收率(STY)(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度(T)变化如下表:
①该反应最适宜的温度是_______ 。
②在220°C和170 °C条件下,该反应速率之比: υ(220°C): υ(170°C)=_______ 。
③随温度升高,甲醇的时空收率先增大后减小,可能的原因是_______ 。
(3)CO2催化加氢制甲醇过程中,存在竞争的副反应主要是: CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH =+41 kJ∙mol−1。在恒温密闭容器中,CO2的平衡转化率[α(CO2)%]和甲醇选择性[(CH3OH)%=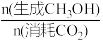 ×100%]随着温度变化关系如下图所示。
×100%]随着温度变化关系如下图所示。_______ 。
②按1 mol CO2(g)、3 mol H2(g)投料反应,计算 244°C时反应生成CH3OH的物质的量为_______ mol。 (保留两位有效数字)
③在压强为p的反应条件下,1 mol CO2(g)和3 mol H2(g)反应并达到平衡状态,CO2平衡转化率为20%,甲醇选择性为50%,该温度下主反应的平衡常数Kp=_______ 。 ( 列出计算式即可)
(1)已知:①2H2(g)+O2(g) =2H2O(g) ΔH= − 484 kJ∙mol−1
②2CH3OH(g)+ 3O2(g) =2CO2(g)+4H2O(g) ΔH =−1353 kJ∙mol−1
则CO2(g)+ 3H2(g) = CH3OH(g)+H2O(g) ΔH =
(2)在恒压密闭容器中通入CO2和H2的混合气体,制备甲醇过程中测得甲醇的时空收率(STY)(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度(T)变化如下表:
| T/°C | 170 | 180 | 1 90 | 200 | 210 | 220 | 230 |
| STY/[mol/(mol·h)] | 0.10 | 0.15 | 0.20 | 0.25 | 0.28 | 0.20 | 0.15 |
②在220°C和170 °C条件下,该反应速率之比: υ(220°C): υ(170°C)=
③随温度升高,甲醇的时空收率先增大后减小,可能的原因是
(3)CO2催化加氢制甲醇过程中,存在竞争的副反应主要是: CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH =+41 kJ∙mol−1。在恒温密闭容器中,CO2的平衡转化率[α(CO2)%]和甲醇选择性[(CH3OH)%=
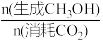 ×100%]随着温度变化关系如下图所示。
×100%]随着温度变化关系如下图所示。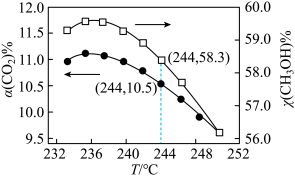
②按1 mol CO2(g)、3 mol H2(g)投料反应,计算 244°C时反应生成CH3OH的物质的量为
③在压强为p的反应条件下,1 mol CO2(g)和3 mol H2(g)反应并达到平衡状态,CO2平衡转化率为20%,甲醇选择性为50%,该温度下主反应的平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】燃煤废气中的氮氧化物(NOx)、CO2、SO2等气体,常要采用不同方法处理,以实现节能减排、废物利用等。
(1)下列为二氧化硫和氮的氧化物转化的部分环节:
①已知:2SO2(g)+O2(g) 2SO3(g) △H=-196.6 kJ・mol-1
2SO3(g) △H=-196.6 kJ・mol-1
2NO(g)+O2(g) 2NO2(g) △H=-113.0 kJ·mol-1
2NO2(g) △H=-113.0 kJ·mol-1
则SO2气体与NO2气体反应生成SO3气体和NO气体的热化学方程式为_________ 。
②一定条件下,工业上可通过下列反应实现燃煤烟气中液态硫的回收,其中Y是单质:SO2(g)+2CO(g)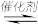 2X(g)+Y(l)。为了测定在某种催化剂作用下的反应速率,某化学兴趣小组在某温度下、固定容器中用超灵敏气体传感器测得不同时间的SO2和CO浓度如下表:
2X(g)+Y(l)。为了测定在某种催化剂作用下的反应速率,某化学兴趣小组在某温度下、固定容器中用超灵敏气体传感器测得不同时间的SO2和CO浓度如下表:
X的化学式为___________ ;当时间为第4 s时,2v(SO2)正____ (填“>”“=”或“<”)v(X)逆。
(2)有科学家经过研究发现,在210~290℃、催化剂条件下用H2可将CO2转化生成甲醇蒸气和水蒸气。一定条件下,往2 L恒容密闭容器中充入1 mol CO2和3. 0 mol H2,在不同催化剂作用下,相同时间内CO2的转化率随温度变化如图所示:

①催化剂效果最佳的是催化剂________ (填“I”“II”或“III”)。
②此反应在a点时已达平衡状态,a点的转化率比c点高的原因是___________ 。已知容器内的起始压强为100 kPa,则图中c点对应温度下反应的平衡常数Kp=______ (保留两位有效数字)(Kp为以分压表示的平衡常数, 分压=总压×物质的量分数)。
(1)下列为二氧化硫和氮的氧化物转化的部分环节:
①已知:2SO2(g)+O2(g)
 2SO3(g) △H=-196.6 kJ・mol-1
2SO3(g) △H=-196.6 kJ・mol-12NO(g)+O2(g)
 2NO2(g) △H=-113.0 kJ·mol-1
2NO2(g) △H=-113.0 kJ·mol-1则SO2气体与NO2气体反应生成SO3气体和NO气体的热化学方程式为
②一定条件下,工业上可通过下列反应实现燃煤烟气中液态硫的回收,其中Y是单质:SO2(g)+2CO(g)
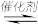 2X(g)+Y(l)。为了测定在某种催化剂作用下的反应速率,某化学兴趣小组在某温度下、固定容器中用超灵敏气体传感器测得不同时间的SO2和CO浓度如下表:
2X(g)+Y(l)。为了测定在某种催化剂作用下的反应速率,某化学兴趣小组在某温度下、固定容器中用超灵敏气体传感器测得不同时间的SO2和CO浓度如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 |
| c(SO2)/mol·L -1 | 1.00 | 0.50 | 0.23 | 3.00×10-37 | 3.00×10-37 |
| c(CO)/mol·L-1 | 4.00 | 3.00 | 2.46 | 2.00 | 2.00 |
(2)有科学家经过研究发现,在210~290℃、催化剂条件下用H2可将CO2转化生成甲醇蒸气和水蒸气。一定条件下,往2 L恒容密闭容器中充入1 mol CO2和3. 0 mol H2,在不同催化剂作用下,相同时间内CO2的转化率随温度变化如图所示:

①催化剂效果最佳的是催化剂
②此反应在a点时已达平衡状态,a点的转化率比c点高的原因是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】乙酸乙酯一般通过乙酸和乙醇酯化合成:

已知纯物质和相关恒沸混合物的常压沸点如表:
请完成:
(1)关于该反应,下列说法不合理的是________ 。
A.反应体系中硫酸有催化作用
B.因为化学方程式前后物质的化学计量数之和相等,所以反应的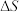 等于零
等于零
C.因为反应的 接近于零,所以温度变化对平衡转化率的影响大
接近于零,所以温度变化对平衡转化率的影响大
D.因为反应前后都是液态物质,所以压强变化对化学平衡的影响可忽略不计
(2)一定温度下该反应的平衡常数 。若按化学方程式中乙酸和乙醇的化学计量数比例投料,则乙酸乙酯的平衡产率y=
。若按化学方程式中乙酸和乙醇的化学计量数比例投料,则乙酸乙酯的平衡产率y=________ ;若乙酸和乙醇的物质的量之比为n:1,相应平衡体系中乙酸乙酯的物质的量分数为x,请在图中绘制x随n变化的示意图________ (计算时不计副反应)。

(3)工业上多采用乙酸过量的方法,将合成塔中乙酸、乙醇和硫酸混合液加热至110℃左右发生酯化反应并回流,直到塔顶温度达到70~71℃,开始从塔顶出料。控制乙酸过量的作用有________ 。
(4)近年,科学家研究了乙醇催化合成乙酸乙酯的新方法: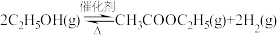 。在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。关于该方法,下列推测合理的是
。在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。关于该方法,下列推测合理的是__________ 。

A.反应温度不宜超过300℃
B.增大体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙醛是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键

已知纯物质和相关恒沸混合物的常压沸点如表:
| 纯物质 | 沸点/℃ | 恒沸混合物(质量分数) | 沸点/℃ |
| 乙醇 | 78.3 | 乙酸乙酯(0.92)+水(0.08) | 70.4 |
| 乙酸 | 117.9 | 乙酸乙酯(0.69)+乙醇(0.31) | 71.8 |
| 乙酸乙酯 | 77.1 | 乙酸乙酯(0.83)+乙醇(0.08)+水(0.09) | 70.2 |
(1)关于该反应,下列说法不合理的是
A.反应体系中硫酸有催化作用
B.因为化学方程式前后物质的化学计量数之和相等,所以反应的
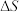 等于零
等于零C.因为反应的
 接近于零,所以温度变化对平衡转化率的影响大
接近于零,所以温度变化对平衡转化率的影响大D.因为反应前后都是液态物质,所以压强变化对化学平衡的影响可忽略不计
(2)一定温度下该反应的平衡常数
 。若按化学方程式中乙酸和乙醇的化学计量数比例投料,则乙酸乙酯的平衡产率y=
。若按化学方程式中乙酸和乙醇的化学计量数比例投料,则乙酸乙酯的平衡产率y=
(3)工业上多采用乙酸过量的方法,将合成塔中乙酸、乙醇和硫酸混合液加热至110℃左右发生酯化反应并回流,直到塔顶温度达到70~71℃,开始从塔顶出料。控制乙酸过量的作用有
(4)近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:
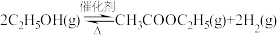 。在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。关于该方法,下列推测合理的是
。在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。关于该方法,下列推测合理的是
A.反应温度不宜超过300℃
B.增大体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙醛是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】2018年是合成氨工业先驱哈伯获得诺贝尔奖100周年。 和
和 生成
生成 的反应为
的反应为
 ,在Fe催化剂作用下的反应历程如下(*表示吸附态)。
,在Fe催化剂作用下的反应历程如下(*表示吸附态)。
化学吸附: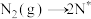 ;
;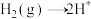 ;
;
表面反应: ;
; ;
; ;
;
脱附: 。
。
其中 的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。请回答:
的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。请回答:
(1)有利于提高平衡混合物中氨含量的条件有__________ (填标号)。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)实际生产中,常用Fe作催化剂,控制温度773K,压强 ,原料气中
,原料气中 和
和 物质的量之比为
物质的量之比为 。分析说明原料气中
。分析说明原料气中 适度过量的两个理由
适度过量的两个理由_______________________________ ;_____________________________________ 。
(3)下列关于合成氨工业的理解正确的是__________ (填标号)。
A.合成氨反应在不同温度下的 和
和 都小于零
都小于零
B.当温度、压强一定时,向合成氨平衡体系中添加少量惰性气体,平衡正向移动
C.基于 有较强的分子间作用力可将其液化,不断将液氨移去,有利于反应正向进行
有较强的分子间作用力可将其液化,不断将液氨移去,有利于反应正向进行
D.分离空气可得 ,通过天然气和水蒸气转化可得
,通过天然气和水蒸气转化可得 ,原料气须经过净化处理,防止催化剂“中毒”
,原料气须经过净化处理,防止催化剂“中毒”
 和
和 生成
生成 的反应为
的反应为
 ,在Fe催化剂作用下的反应历程如下(*表示吸附态)。
,在Fe催化剂作用下的反应历程如下(*表示吸附态)。化学吸附:
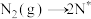 ;
;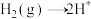 ;
;表面反应:
 ;
; ;
; ;
;脱附:
 。
。其中
 的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。请回答:
的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。请回答:(1)有利于提高平衡混合物中氨含量的条件有
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)实际生产中,常用Fe作催化剂,控制温度773K,压强
 ,原料气中
,原料气中 和
和 物质的量之比为
物质的量之比为 。分析说明原料气中
。分析说明原料气中 适度过量的两个理由
适度过量的两个理由(3)下列关于合成氨工业的理解正确的是
A.合成氨反应在不同温度下的
 和
和 都小于零
都小于零B.当温度、压强一定时,向合成氨平衡体系中添加少量惰性气体,平衡正向移动
C.基于
 有较强的分子间作用力可将其液化,不断将液氨移去,有利于反应正向进行
有较强的分子间作用力可将其液化,不断将液氨移去,有利于反应正向进行D.分离空气可得
 ,通过天然气和水蒸气转化可得
,通过天然气和水蒸气转化可得 ,原料气须经过净化处理,防止催化剂“中毒”
,原料气须经过净化处理,防止催化剂“中毒”
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】甲醇制烯烃(MTO)是煤制烯烃工艺路线的核心技术。煤制烯烃主要包括煤的气化、液化、烯烃化三个阶段。
(1)煤的液化发生的主要反应之一为
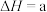 kJ⋅mol
kJ⋅mol ,在不同温度下,K(500°C)
,在不同温度下,K(500°C)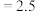 (mol⋅L
(mol⋅L ),K(700°C)
),K(700°C)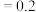 (mol⋅L
(mol⋅L )
)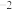 。
。
①
___________ 0(填“>”、“<”、“=”)。
②若反应在容积为2L的密闭容器中进行,500℃测得某一时刻体系内 、CO、
、CO、 物质的量分别为2 mol、1 mol、3 mol,则此时生成
物质的量分别为2 mol、1 mol、3 mol,则此时生成 的速率
的速率___________ 消耗 的速率(填“>”、“<”、“=”)。
的速率(填“>”、“<”、“=”)。
(2)通过研究外界条件对反应的影响,尽可能提高甲醇生成乙烯或丙烯的产率。
甲醇制烯烃的主要反应有:
Ⅰ.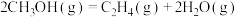
 kJ⋅mol
kJ⋅mol
Ⅱ.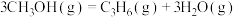
 kJ⋅mol
kJ⋅mol
Ⅲ.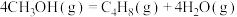
 kJ⋅mol
kJ⋅mol
① 转化为
转化为 的热化学方程式为Ⅳ:
的热化学方程式为Ⅳ: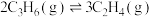
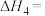
___________ 。
②加入 作为稀释剂,反应Ⅰ中
作为稀释剂,反应Ⅰ中 的产率将
的产率将___________ (填“增大”、“减小”或“不变”)。
(3)为研究不同条件对反应的影响,测得不同温度下平衡时 、
、 和
和 的物质的量分数变化,如图所示:
的物质的量分数变化,如图所示:
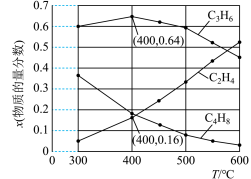
①随着温度的升高, 的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是
的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是___________ 。
②体系总压为0.1 MPa,400℃时反应Ⅳ的平衡常数
___________ 。
(1)煤的液化发生的主要反应之一为

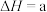 kJ⋅mol
kJ⋅mol ,在不同温度下,K(500°C)
,在不同温度下,K(500°C)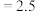 (mol⋅L
(mol⋅L ),K(700°C)
),K(700°C)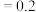 (mol⋅L
(mol⋅L )
)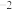 。
。①

②若反应在容积为2L的密闭容器中进行,500℃测得某一时刻体系内
 、CO、
、CO、 物质的量分别为2 mol、1 mol、3 mol,则此时生成
物质的量分别为2 mol、1 mol、3 mol,则此时生成 的速率
的速率 的速率(填“>”、“<”、“=”)。
的速率(填“>”、“<”、“=”)。(2)通过研究外界条件对反应的影响,尽可能提高甲醇生成乙烯或丙烯的产率。
甲醇制烯烃的主要反应有:
Ⅰ.
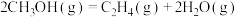
 kJ⋅mol
kJ⋅mol
Ⅱ.
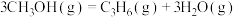
 kJ⋅mol
kJ⋅mol
Ⅲ.
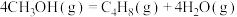
 kJ⋅mol
kJ⋅mol
①
 转化为
转化为 的热化学方程式为Ⅳ:
的热化学方程式为Ⅳ: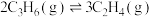
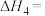
②加入
 作为稀释剂,反应Ⅰ中
作为稀释剂,反应Ⅰ中 的产率将
的产率将(3)为研究不同条件对反应的影响,测得不同温度下平衡时
 、
、 和
和 的物质的量分数变化,如图所示:
的物质的量分数变化,如图所示:
①随着温度的升高,
 的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是
的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是②体系总压为0.1 MPa,400℃时反应Ⅳ的平衡常数

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】按要求完成下列题目
(1)下列反应中,属于吸热反应的是______(填字母)。
(2)利用中和实验装置测量盐酸与NaOH溶液反应的热量变化的过程中,若取50mL 0.50 的盐酸,则还需加入______(填序号)。
的盐酸,则还需加入______(填序号)。
(3)在体积为1L密闭容器中充入3mol 和9mol
和9mol  ,发生反应
,发生反应
 ,测得
,测得 、
、 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
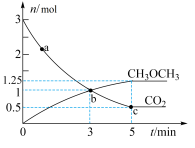
①反应到达3min时,
______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②0~5min内,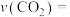
______  。
。
③反应达到平衡状态时, 的体积分数为
的体积分数为______ %(保留1位小数)。
(4)在常温下对反应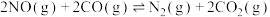 进行研究。若将3mol NO和2mol CO通入10L的恒容密闭容器中,在一定条件下发生上述反应,各组分的物质的量浓度随时间的变化情况如图所示。
进行研究。若将3mol NO和2mol CO通入10L的恒容密闭容器中,在一定条件下发生上述反应,各组分的物质的量浓度随时间的变化情况如图所示。
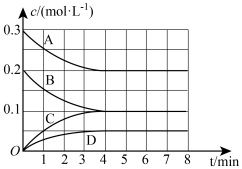
①图中曲线A表示______ (填“NO”“CO”“ ”或“
”或“ ”,下同)的浓度变化,曲线C表示的是
”,下同)的浓度变化,曲线C表示的是______ 浓度变化。
②在0~4min内NO的平均反应速率
______ ,4min末 的浓度为
的浓度为______ 。
③4min末,采用下列措施一定能加快上述反应速率的是______ (填标号)。
A.升高体系的温度 B.充入一定量的 C.将容器体积变为5L D.充入一定量氦气
C.将容器体积变为5L D.充入一定量氦气
④下列叙述能说明反应达到平衡状态的是______ (填字母)。
A.容器内压强保持不变 B. 与
与 的物质的量之比为1∶1
的物质的量之比为1∶1
C.气体的密度保持不变 D.混合气体的平均相对分子质量不变
(1)下列反应中,属于吸热反应的是______(填字母)。
| A.C与水蒸气反应 | B.氧化钙和水反应 |
C. 受热分解 受热分解 | D.锌与盐酸反应 |
(2)利用中和实验装置测量盐酸与NaOH溶液反应的热量变化的过程中,若取50mL 0.50
 的盐酸,则还需加入______(填序号)。
的盐酸,则还需加入______(填序号)。| A.1.0g NaOH固体 | B.50mL 0.55 NaOH溶液 NaOH溶液 | C.50mL 0.50 NaOH溶液 NaOH溶液 |
(3)在体积为1L密闭容器中充入3mol
 和9mol
和9mol  ,发生反应
,发生反应
 ,测得
,测得 、
、 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
①反应到达3min时,

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②0~5min内,
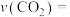
 。
。③反应达到平衡状态时,
 的体积分数为
的体积分数为(4)在常温下对反应
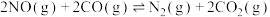 进行研究。若将3mol NO和2mol CO通入10L的恒容密闭容器中,在一定条件下发生上述反应,各组分的物质的量浓度随时间的变化情况如图所示。
进行研究。若将3mol NO和2mol CO通入10L的恒容密闭容器中,在一定条件下发生上述反应,各组分的物质的量浓度随时间的变化情况如图所示。
①图中曲线A表示
 ”或“
”或“ ”,下同)的浓度变化,曲线C表示的是
”,下同)的浓度变化,曲线C表示的是②在0~4min内NO的平均反应速率

 的浓度为
的浓度为③4min末,采用下列措施一定能加快上述反应速率的是
A.升高体系的温度 B.充入一定量的
 C.将容器体积变为5L D.充入一定量氦气
C.将容器体积变为5L D.充入一定量氦气④下列叙述能说明反应达到平衡状态的是
A.容器内压强保持不变 B.
 与
与 的物质的量之比为1∶1
的物质的量之比为1∶1C.气体的密度保持不变 D.混合气体的平均相对分子质量不变
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】用化学用语填空。
(1)图1甲醇( )脱氢法可制备甲醛(HCHO,反应体系中各物质均为气态),结合如图回答。
)脱氢法可制备甲醛(HCHO,反应体系中各物质均为气态),结合如图回答。
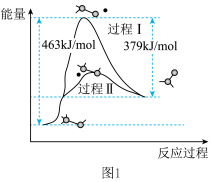
①此反应的热化学方程式是___________ 。
②反应活化能:过程Ⅰ___________ 过程Ⅱ(填“>”“=”或“<”)。
(2)某温度下,在2L密闭容器中X、Y、Z三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图2,据图回答:
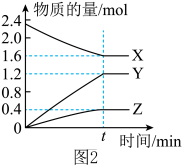
①该反应的化学方程式可表示为___________ 。
②反应起始至t min(设 ),Z的平均反应速率是:
),Z的平均反应速率是:___________ ,Y的体积分数为___________ 。
③下列可判断反应已达到平衡状态的是___________ 。
A.X、Y、Z的反应速率相等 B.体系的压强保持不变
C.混合气体的密度不变 D.生成1 mol Z 的同时生成2 mol X
E.混合气体的平均相对分子质量不变
(1)图1甲醇(
 )脱氢法可制备甲醛(HCHO,反应体系中各物质均为气态),结合如图回答。
)脱氢法可制备甲醛(HCHO,反应体系中各物质均为气态),结合如图回答。
①此反应的热化学方程式是
②反应活化能:过程Ⅰ
(2)某温度下,在2L密闭容器中X、Y、Z三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图2,据图回答:

①该反应的化学方程式可表示为
②反应起始至t min(设
 ),Z的平均反应速率是:
),Z的平均反应速率是:③下列可判断反应已达到平衡状态的是
A.X、Y、Z的反应速率相等 B.体系的压强保持不变
C.混合气体的密度不变 D.生成1 mol Z 的同时生成2 mol X
E.混合气体的平均相对分子质量不变
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】氮的化合物的处理和利用是环境科学研究的热点。
(1)机动车排放的尾气中主要污染物为NOx,可用CH4催化还原NOx以消除其污染。298K时,1.0g CH4(g)与足量的NO气体完全反应生成N2、CO2和H2O(g),放出72.5kJ的热量。该反应的热化学方程式为_______ 。
(2)氮氧化物与悬浮大气中的海盐粒子相互作用会生成NOCl,涉及的相关反应有:
ΔH1、ΔH2、ΔH3之间的关系为ΔH3=_____ ;K1、K2、K3的关系为K3=______ 。
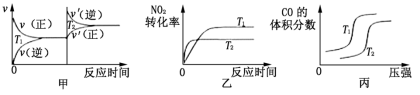
(3)对汽车加装尾气净化装置,可使汽车尾气中含有的CO、NO2等有毒气体转化为无毒气体:4CO(g)+2NO2(g)⇌4CO2(g)+N2(g) ΔH=-1200kJ·mol-1.对于该反应,温度不同(T2﹥T1),其他条件相同时,下列图象正确的是_______ (填序号)。
(4)用活性炭还原法也可以处理氮氧化物。向某密闭容器中加入一定量的活性炭和NO,发生反应:C(s)+2NO(g)⇌N2(g)+CO2(g) ΔH。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
①T1℃时,该反应在0~20min的平均反应速率v(CO2)=____ ;该反应的平衡常数K=_____ ;
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是_______ (填序号);
A.加入一定量的活性炭
B.恒温恒压充入氩气
C.适当缩小容器的体积
D.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则和原平衡相比,NO的转化率_______ (填“升高”或“降低”),反应的平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)机动车排放的尾气中主要污染物为NOx,可用CH4催化还原NOx以消除其污染。298K时,1.0g CH4(g)与足量的NO气体完全反应生成N2、CO2和H2O(g),放出72.5kJ的热量。该反应的热化学方程式为
(2)氮氧化物与悬浮大气中的海盐粒子相互作用会生成NOCl,涉及的相关反应有:
| 热化学方程式 | 平衡常数 | |
| ① | 2NO2(g)+NaCl(s)⇌NaNO3(s)+NOCl(g) ΔH1 | K1 |
| ② | 4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g) ΔH2 | K2 |
| ③ | 2NO(g)+Cl2(g)⇌2NOCl(g) ΔH3 | K3 |
ΔH1、ΔH2、ΔH3之间的关系为ΔH3=
(3)对汽车加装尾气净化装置,可使汽车尾气中含有的CO、NO2等有毒气体转化为无毒气体:4CO(g)+2NO2(g)⇌4CO2(g)+N2(g) ΔH=-1200kJ·mol-1.对于该反应,温度不同(T2﹥T1),其他条件相同时,下列图象正确的是

(4)用活性炭还原法也可以处理氮氧化物。向某密闭容器中加入一定量的活性炭和NO,发生反应:C(s)+2NO(g)⇌N2(g)+CO2(g) ΔH。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
时间/min 浓度/mol·L-1 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①T1℃时,该反应在0~20min的平均反应速率v(CO2)=
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是
A.加入一定量的活性炭
B.恒温恒压充入氩气
C.适当缩小容器的体积
D.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则和原平衡相比,NO的转化率
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】Ⅰ.25℃时,制备亚硝酰氯所涉及的热化学方程式和平衡常数如下表。
(1)则该温度下,
___________  ;K3=
;K3=___________ (用 和
和 表示)。
表示)。
Ⅱ.完成下列问题
(2)25℃时,在体积为2L的恒容密闭容器中通入0.08molNO和0.04mol 发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图Ⅰ实线所示,则
发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图Ⅰ实线所示,则
___________ (填“>”“<”或“=”)0;
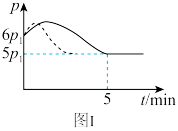
(3)若其他条件相同,仅改变某一条件,测得其压强随时间的变化如图Ⅰ虚线所示,则改变的条件是___________ ;
(4)5min时,再充入0.08molNO和0.04mol ,则达平衡后NO的体积分数将
,则达平衡后NO的体积分数将___________ (填“增大”“减小”或“不变”)。
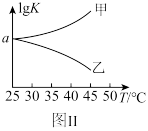
(5)图Ⅱ是甲、乙两同学描绘上述反应③的平衡常数的对数值(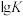 )与温度的变化关系图,其中正确的曲线是
)与温度的变化关系图,其中正确的曲线是___________ (填“甲”或“乙”)。
Ⅲ.在300℃下,将 和
和 按物质的量之比为1:3通入一恒容密闭容器中,容器压强为8MPa,发生反应
按物质的量之比为1:3通入一恒容密闭容器中,容器压强为8MPa,发生反应 ,达到平衡时,测得
,达到平衡时,测得 的平衡转化率为50%,
的平衡转化率为50%,
(6)该反应条件下的平衡常数为
___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
| 热化学方程式 | 平衡常数 | |
| ① | 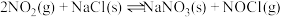 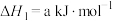 |  |
| ② | 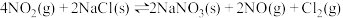 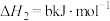 |  |
| ③ |  |  |
(1)则该温度下,

 ;K3=
;K3= 和
和 表示)。
表示)。Ⅱ.完成下列问题
(2)25℃时,在体积为2L的恒容密闭容器中通入0.08molNO和0.04mol
 发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图Ⅰ实线所示,则
发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图Ⅰ实线所示,则

(3)若其他条件相同,仅改变某一条件,测得其压强随时间的变化如图Ⅰ虚线所示,则改变的条件是
(4)5min时,再充入0.08molNO和0.04mol
 ,则达平衡后NO的体积分数将
,则达平衡后NO的体积分数将(5)图Ⅱ是甲、乙两同学描绘上述反应③的平衡常数的对数值(
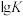 )与温度的变化关系图,其中正确的曲线是
)与温度的变化关系图,其中正确的曲线是
Ⅲ.在300℃下,将
 和
和 按物质的量之比为1:3通入一恒容密闭容器中,容器压强为8MPa,发生反应
按物质的量之比为1:3通入一恒容密闭容器中,容器压强为8MPa,发生反应 ,达到平衡时,测得
,达到平衡时,测得 的平衡转化率为50%,
的平衡转化率为50%,(6)该反应条件下的平衡常数为

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】中国向世界庄严宣布,中国将力争在2030年前实现碳达峰,在2060年前实现碳中和。某科研机构欲利用以下途径减少CO2的排放,并合成清洁燃料CH3OH,相关反应有:
I.CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1<0
CH3OH(g)+H2O(g) ΔH1<0
II.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2>0
CO(g)+H2O(g) ΔH2>0
III.CO(g)+2H2(g) CH3OH(g) ΔH3<0
CH3OH(g) ΔH3<0
(1)ΔH1=____ (用含ΔH2、ΔH3的代数式表示),反应I在相对____ (填“较低”或“较高”)温度下容易自发进行。
(2)反应物中的CO2可用NaOH溶液从工业尾气中捕获。常温下,当捕获液中c(H2CO3)=c(CO )时,溶液的pH=
)时,溶液的pH=____ [已知:常温下,Ka1(H2CO3)=10−6.4、Ka2(H2CO3)=10−10.2]。
(3)向某恒容密闭容器中充入1molCO2和2molH2,只发生上述反应I和II,在催化剂作用下达到平衡状态时,CO2的转化率随温度的变化如图所示:

①温度在210~270℃时,CO2的平衡转化率随温度的升高而下降,其原因可能为___ 。
②平衡时的浓度关系式: (210℃)
(210℃)___  (270℃)(填“大于”“小于”或“等于”)。
(270℃)(填“大于”“小于”或“等于”)。
③一定温度下,反应体系中CO2的平衡转化率为20%,平衡时CH3OH的选择性[甲醇的选择性= ×100%]为70%,则氢气的平衡转化率α(H2)=
×100%]为70%,则氢气的平衡转化率α(H2)=___ ,反应II的化学平衡常数K=____ (计算结果保留2位有效数字)。
I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1<0
CH3OH(g)+H2O(g) ΔH1<0II.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2>0
CO(g)+H2O(g) ΔH2>0III.CO(g)+2H2(g)
 CH3OH(g) ΔH3<0
CH3OH(g) ΔH3<0(1)ΔH1=
(2)反应物中的CO2可用NaOH溶液从工业尾气中捕获。常温下,当捕获液中c(H2CO3)=c(CO
 )时,溶液的pH=
)时,溶液的pH=(3)向某恒容密闭容器中充入1molCO2和2molH2,只发生上述反应I和II,在催化剂作用下达到平衡状态时,CO2的转化率随温度的变化如图所示:

①温度在210~270℃时,CO2的平衡转化率随温度的升高而下降,其原因可能为
②平衡时的浓度关系式:
 (210℃)
(210℃) (270℃)(填“大于”“小于”或“等于”)。
(270℃)(填“大于”“小于”或“等于”)。③一定温度下,反应体系中CO2的平衡转化率为20%,平衡时CH3OH的选择性[甲醇的选择性=
 ×100%]为70%,则氢气的平衡转化率α(H2)=
×100%]为70%,则氢气的平衡转化率α(H2)=
您最近一年使用:0次

 N2O4(g)
N2O4(g)


