钴是重要的战略金属之一,钴粉主要以高温氢还原草酸钴制得。一种利用水钴矿[主要成分为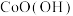 ,还含有少量
,还含有少量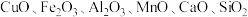 等]制备钻的工艺流程如下。
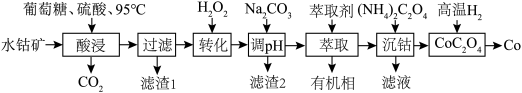
等]制备钻的工艺流程如下。
已知:①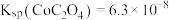 ;
;
②当溶液中离子浓度 时,认为该离子已除尽;
时,认为该离子已除尽;
③部分阳离子以氢氧化物形式沉淀时溶液的 见下表。
见下表。
请根据以上信息,回答下列问题:
(1)为加快“酸浸”的速率和效率,可以采取的措施有___________ (答出1条即可),滤渣1的主要成分为___________ (填化学式)。
(2)在“酸浸”步骤中发生的最主要的氧化还原反应的化学方程式为___________ 。
(3)“转化”步骤中加入 的目的是
的目的是___________ (用离子方程式表示),该步骤反应温度不宜高于 的原因可能是
的原因可能是___________ 。
(4)在“调 ”步骤中加入
”步骤中加入 调节溶液的
调节溶液的 ,其合理范围为
,其合理范围为___________ ;“萃取”步骤中萃取的主要离子是___________ (填离子符号)。
(5)在“沉钴”步骤中为使溶液中的钻沉淀完全,混合溶液中 的最小浓度为
的最小浓度为___________  。
。
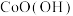 ,还含有少量
,还含有少量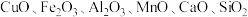 等]制备钻的工艺流程如下。
等]制备钻的工艺流程如下。
已知:①
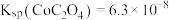 ;
;②当溶液中离子浓度
 时,认为该离子已除尽;
时,认为该离子已除尽;③部分阳离子以氢氧化物形式沉淀时溶液的
 见下表。
见下表。| 金属离子 |  |  |  |  |  |  |
开始沉淀的 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 | 4.7 |
完全沉淀的 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 | 6.7 |
(1)为加快“酸浸”的速率和效率,可以采取的措施有
(2)在“酸浸”步骤中发生的最主要的氧化还原反应的化学方程式为
(3)“转化”步骤中加入
 的目的是
的目的是 的原因可能是
的原因可能是(4)在“调
 ”步骤中加入
”步骤中加入 调节溶液的
调节溶液的 ,其合理范围为
,其合理范围为(5)在“沉钴”步骤中为使溶液中的钻沉淀完全,混合溶液中
 的最小浓度为
的最小浓度为 。
。
更新时间:2023-10-05 09:48:58
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】利用某工业废弃固体(成分为 Cu2S 和 FeS2)制备硫酸铜溶液和硫酸亚铁晶体,流程如图所示。

(已知:①固体 B 含有氧化铜、氧化铁②铁能与硫酸铁反应,生成硫酸亚铁)
(1)操作 I 是____ 。为了提高废弃固体的反应速率,除将固体粉碎、提高温度外,还可以采取的具体措施有____ (写一条)。
(2)写出 FeS2在空气中灼烧的化学方程式_____ 。
(3)溶液 C 中的溶质有_________ (用化学式表示)。
(4)试剂 y 的作用是_____ 。

(已知:①固体 B 含有氧化铜、氧化铁②铁能与硫酸铁反应,生成硫酸亚铁)
(1)操作 I 是
(2)写出 FeS2在空气中灼烧的化学方程式
(3)溶液 C 中的溶质有
(4)试剂 y 的作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某实验小组以含铁污泥(主要成分为 、
、 、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾
、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。

根据所学知识,回答下列问题:
(1)路线Ⅰ中,加入 溶液发生的离子反应方程式是
溶液发生的离子反应方程式是__________ 。
(2)写出“酸浸”时, 与硫酸反应的化学方程式:
与硫酸反应的化学方程式:__________ ;检验含有 的方法是
的方法是__________ 。
(3)“滤液X”中一定含有的阳离子为__________ 。
(4)实验室中配制 溶液时通常需加入少量的试剂a,目的是
溶液时通常需加入少量的试剂a,目的是__________ ,请写出相应的离子方程式:__________ 。
 、
、 、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾
、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。
根据所学知识,回答下列问题:
(1)路线Ⅰ中,加入
 溶液发生的离子反应方程式是
溶液发生的离子反应方程式是(2)写出“酸浸”时,
 与硫酸反应的化学方程式:
与硫酸反应的化学方程式: 的方法是
的方法是(3)“滤液X”中一定含有的阳离子为
(4)实验室中配制
 溶液时通常需加入少量的试剂a,目的是
溶液时通常需加入少量的试剂a,目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】由某镍矿(主要成分为NiO,含少量MgO、SiO2和铁的氧化物等)制取黄钠铁矾[Na2Fe6(SO4)4(OH)12]和NiSO4·6H2O的实验流程如下:

(1)“预处理”时需将Fe2+全部转化为Fe3+,试剂X最好选用_______ (填序号)。
a.稀硝酸 b.双氧水 c.高锰酸钾溶液 d.新制氯水
(2)“沉铁”后溶液的酸性增强,生成黄钠铁矾的离子方程式为_______ 。
(3)“沉镁”前需用MgO调节pH,防止溶液酸性过强,其原因是_______ 。(已知:HF是一元弱酸)
(4)判断“沉镁”完全的操作是_______ 。
(5)硫酸镍的溶解度随温度的变化如图所示。请将由滤液Y制备NiSO4·6H2O晶体的实验方案补充完整:向滤液Y中_______ ,过滤,_______ ,向滤渣中_______ ,蒸发浓缩,_______ ,趁热过滤,将所得固体洗涤、干燥,得到NiSO4·6H2O晶体。
[已知:Ni(OH)2难溶于水和强碱,易溶于强酸
实验中须选用的试剂:BaCl2溶液、稀硫酸、NaOH溶液、蒸馏水]


(1)“预处理”时需将Fe2+全部转化为Fe3+,试剂X最好选用
a.稀硝酸 b.双氧水 c.高锰酸钾溶液 d.新制氯水
(2)“沉铁”后溶液的酸性增强,生成黄钠铁矾的离子方程式为
(3)“沉镁”前需用MgO调节pH,防止溶液酸性过强,其原因是
(4)判断“沉镁”完全的操作是
(5)硫酸镍的溶解度随温度的变化如图所示。请将由滤液Y制备NiSO4·6H2O晶体的实验方案补充完整:向滤液Y中
[已知:Ni(OH)2难溶于水和强碱,易溶于强酸
实验中须选用的试剂:BaCl2溶液、稀硫酸、NaOH溶液、蒸馏水]

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】陆生植物光合作用所需要的碳源主要是空气中的CO2,为了研究NaHCO3溶液可作为植物光合作用的碳源,进行以下实验,实验装置如下图所示:

实验步骤:
①配制0.5000mol·L-1 NaHCO3溶液250mL;
②取100mL 0.5000mol·L-1 NaHCO3溶液,置于B瓶中;
③按上图连接装置,持续通入空气一段时间:通气结束后,取C瓶中混合液进行过滤,沉淀经洗涤、烘干、冷却、称量等操作,得到BaCO3 0.197g。
完成下列填空:
(1)配制250mL 0.5000mol·L-1 NaHCO3溶液需要用到的玻璃仪器有胶头滴管、玻璃棒、_______ 。装置A中氢氧化钠溶液的作用是_______ 。
(2)通气结束后,B瓶溶液的pH比通气前_______ (选填:“增大”、“减小”或“不变”),原因是_______ 。
(3)①根据上述实验结果计算,溶液中NaHCO3的分解率为_______ 。
②会导致实验测定结果偏低的因素是_______ 。
A.B瓶中残留CO2 B. 过滤时间偏长
C. 没有洗涤沉淀 D. 沉淀烘干不完全
(4)用另一种方法也可求NaHCO3的分解率:将反应后C瓶中的沉淀过滤后,用标准盐酸滴定。若采用此法测定NaHCO3的分解率,还需要知道C瓶中Ba(OH)2的_______ 影响溶液中NaHCO3分解的因素有_______ 。

实验步骤:
①配制0.5000mol·L-1 NaHCO3溶液250mL;
②取100mL 0.5000mol·L-1 NaHCO3溶液,置于B瓶中;
③按上图连接装置,持续通入空气一段时间:通气结束后,取C瓶中混合液进行过滤,沉淀经洗涤、烘干、冷却、称量等操作,得到BaCO3 0.197g。
完成下列填空:
(1)配制250mL 0.5000mol·L-1 NaHCO3溶液需要用到的玻璃仪器有胶头滴管、玻璃棒、
(2)通气结束后,B瓶溶液的pH比通气前
(3)①根据上述实验结果计算,溶液中NaHCO3的分解率为
②会导致实验测定结果偏低的因素是
A.B瓶中残留CO2 B. 过滤时间偏长
C. 没有洗涤沉淀 D. 沉淀烘干不完全
(4)用另一种方法也可求NaHCO3的分解率:将反应后C瓶中的沉淀过滤后,用标准盐酸滴定。若采用此法测定NaHCO3的分解率,还需要知道C瓶中Ba(OH)2的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】完成下列问题。
(1)重铬酸钾(K2Cr2O7为橙色,K2CrO4为黄色)溶液存在着如下平衡:Cr2O +H2O⇌2CrO
+H2O⇌2CrO +2H+。
+2H+。
①若平衡体系的pH=2,则溶液显___________ 色。
②能说明该反应达平衡状态的是___________ 。
a.溶液呈酸性 b.溶液的颜色不变
c.2v(Cr2O )=v(CrO
)=v(CrO ) d.Cr2O
) d.Cr2O 和CrO
和CrO 的浓度相同
的浓度相同
(2)25℃时,2NO2(g)⇌N2O4(g)△H=-56.9kJ/mol。
①该反应的化学平衡常数表达式___________________ 。
②其它条件不变,缩小容器体积,达到新平衡,此过程的现象:
_________________________ 。
③其它条件不变,将该体系升温至100oC,此过程的现象:
________________________________ 。
(3)明矾[KAl(SO4)2·12H2O]是一种常用的净水剂。
①用离子方程式表示净水的原因:_________________________ 。
②明矾溶液中滴加Ba(OH)2溶液至SO 刚好沉淀完全时,溶液的pH
刚好沉淀完全时,溶液的pH______ 7(填“>”“=”或“<”,下同)。
③明矾溶液中滴加Ba(OH)2溶液至Al3+刚好沉淀完全时,溶液的pH______ 7。
④明矾溶液中离子浓度由大到小的顺序:______________________________ 。
(1)重铬酸钾(K2Cr2O7为橙色,K2CrO4为黄色)溶液存在着如下平衡:Cr2O
 +H2O⇌2CrO
+H2O⇌2CrO +2H+。
+2H+。①若平衡体系的pH=2,则溶液显
②能说明该反应达平衡状态的是
a.溶液呈酸性 b.溶液的颜色不变
c.2v(Cr2O
 )=v(CrO
)=v(CrO ) d.Cr2O
) d.Cr2O 和CrO
和CrO 的浓度相同
的浓度相同(2)25℃时,2NO2(g)⇌N2O4(g)△H=-56.9kJ/mol。
①该反应的化学平衡常数表达式
②其它条件不变,缩小容器体积,达到新平衡,此过程的现象:
③其它条件不变,将该体系升温至100oC,此过程的现象:
(3)明矾[KAl(SO4)2·12H2O]是一种常用的净水剂。
①用离子方程式表示净水的原因:
②明矾溶液中滴加Ba(OH)2溶液至SO
 刚好沉淀完全时,溶液的pH
刚好沉淀完全时,溶液的pH③明矾溶液中滴加Ba(OH)2溶液至Al3+刚好沉淀完全时,溶液的pH
④明矾溶液中离子浓度由大到小的顺序:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】完成下列填空
(1)已知常温下A-的水解常数Kh=1.61×10-5,常温下,含等物质的量浓度的HA与NaA的混合溶液显___________ (填“酸”、“碱”、“中”)性,c(A-)___________ (填“>”、“<”或“=”)c(HA),该溶液中各离子浓度由大到小的顺序为___________ 。
(2)25℃时,将xmolCH3COONa溶于水,溶液显碱性,向该溶液滴加yL醋酸溶液后溶液呈中性(体积变化忽略不计),则所滴加醋酸溶液的浓度为___________ mol/L(CH3COOH的电离平衡常数取Ka=2×10-5)
(1)已知常温下A-的水解常数Kh=1.61×10-5,常温下,含等物质的量浓度的HA与NaA的混合溶液显
(2)25℃时,将xmolCH3COONa溶于水,溶液显碱性,向该溶液滴加yL醋酸溶液后溶液呈中性(体积变化忽略不计),则所滴加醋酸溶液的浓度为
您最近一年使用:0次
【推荐1】利用硫铁矿(主要成分FeS2)生产硫酸和绿矾(FeSO4·7H2O)的工业流程示意图如下:

(1)沸腾炉中,硫铁矿进行粉碎处理的目的是___________ 。
(2)反应釜中,烧渣经过反应转化为溶液I和固体。
①烧渣中的FeS在反应中作___________ 剂(填“氧化”或“还原”)。
②溶液I中所含溶质的化学式是___________ 。
(3)操作a的主要步骤是:加热浓缩、___________ 、过滤洗涤。
(4)流程中,固体X可以选择硫铁矿(FeS2)或___________ 。
(5)接触室中,发生的主要反应是SO2与O2的反应,其化学方程式是___________ 。若在一体积固定的容器中加入2 mol SO2与1 mol O2模拟该反应,下列各项可作为该反应达到平衡状态的标志的是___________ (填序号)。
A.混合气体的质量不再变化 B.SO2与O2的物质的量比例不变
C.气体密度不再变化 D.气体的平均相对分子质量不再变化
E.SO2的消耗速率与O2的生成速率之比为1:2
若将模拟反应容器中的气体通入到酸性高锰酸钾溶液中,可以恰好使200 mL3 mol/L的高锰酸钾溶液褪色,则模拟反应器中SO2的转化率为___________ 。

(1)沸腾炉中,硫铁矿进行粉碎处理的目的是
(2)反应釜中,烧渣经过反应转化为溶液I和固体。
①烧渣中的FeS在反应中作
②溶液I中所含溶质的化学式是
(3)操作a的主要步骤是:加热浓缩、
(4)流程中,固体X可以选择硫铁矿(FeS2)或
(5)接触室中,发生的主要反应是SO2与O2的反应,其化学方程式是
A.混合气体的质量不再变化 B.SO2与O2的物质的量比例不变
C.气体密度不再变化 D.气体的平均相对分子质量不再变化
E.SO2的消耗速率与O2的生成速率之比为1:2
若将模拟反应容器中的气体通入到酸性高锰酸钾溶液中,可以恰好使200 mL3 mol/L的高锰酸钾溶液褪色,则模拟反应器中SO2的转化率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂质)为主要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。

(1)固体X主要成分是_______ 。
(2)浸取时,高压 的作用
的作用_______ ,写出浸取时CuS溶解的离子方程式_______ 。
(3)中和调pH的范围为_______ 。
(4)还原时,增大溶液酸度_______ (“有利于”或“不利于”)Cu的生成,解释原因_______ 。
(5)最后一步滤液经过一系列操作得到M,用 可以使M离子生成
可以使M离子生成 沉淀,写出该步骤反应的离子方程式
沉淀,写出该步骤反应的离子方程式_______ (M用具体的元素符号表示)。

 |  |  | |
| 开始沉淀pH | 1.9 | 4.2 | 6.2 |
| 沉淀完全pH | 3.2 | 6.7 | 8.2 |
(2)浸取时,高压
 的作用
的作用(3)中和调pH的范围为
(4)还原时,增大溶液酸度
(5)最后一步滤液经过一系列操作得到M,用
 可以使M离子生成
可以使M离子生成 沉淀,写出该步骤反应的离子方程式
沉淀,写出该步骤反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
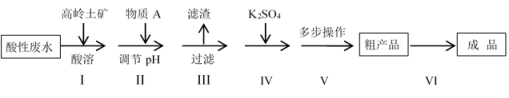
【推荐3】高岭土矿的主要成分是Al2O3、SiO2及少量的Fe2O3,高岭土选矿酸性废水含有大量的H+、SO 、Al3+及少量的Fe3+等离子。工业上利用高岭土矿和酸性废水制备明矾KAl(SO4)2•12H2O(不考虑其它杂质参与反应)。其实验流程如下:
、Al3+及少量的Fe3+等离子。工业上利用高岭土矿和酸性废水制备明矾KAl(SO4)2•12H2O(不考虑其它杂质参与反应)。其实验流程如下:
相关信息:
①Fe3+、Al3+完全沉淀的pH范围
②有关物质的溶解度
请回答:
(1)步骤I中,要加快高岭土酸溶的速率可以采取的措施有___________ 。(至少写两点),
(2)滤渣的主要成分是___________ 。
(3)下列说法中正确的是___________ 。
A.步骤I的主要目的是提高废水中铝离子的浓度
B.步骤II中的A物质可以是KOH或NaOH
C.步骤II中调节pH的范围是3.2<pH<3.4
D.步骤IV中需调控K2SO4的用量,使n(Al3+):n(K+):n(SO )尽可能接近1:1:2
)尽可能接近1:1:2
(4)步骤VI,为了得到较大颗粒且较干燥的晶体,请从下列选项中选出合理的操作(操作不重复)并排序:取粗产品于烧杯中加适量水→___________→___________→___________→抽滤→洗涤→___________。___________
a.70℃蒸发溶剂制成热的饱和溶液 b.30℃~40℃减压蒸发溶剂得到饱和溶液
c.加热烧杯至晶体完全溶解 d.缓慢冷却至室温 e.低温干燥 f.加热干燥
(5)为了测定成品中铝的含量,可采用的方法:将一定体积的成品待测液与过量的EDTA(化学式为Na2H2Y)标准液反应,加入几滴指示剂,再用ZnSO4标准液滴定过量的EDTA,反应原理如下:Al3++H2Y2-(过量)=AlY-+2H+、Zn2++H2Y2-(剩余)=ZnY2-+2H+(终点色为紫红色),过实验测出成品中铝的含量低于理论值,原因可能是___________ 。
A.制备过程中,由于结晶温度控制不当,溶液中硫酸钾晶体同时析出
B.酸式滴定管用蒸馏水洗净后就注入ZnSO4标准液
C.滴定时锥形瓶溶液出现紫红色,立即停止滴定
D.滴定前,滴定管内无气泡,滴定后有气泡
 、Al3+及少量的Fe3+等离子。工业上利用高岭土矿和酸性废水制备明矾KAl(SO4)2•12H2O(不考虑其它杂质参与反应)。其实验流程如下:
、Al3+及少量的Fe3+等离子。工业上利用高岭土矿和酸性废水制备明矾KAl(SO4)2•12H2O(不考虑其它杂质参与反应)。其实验流程如下:
相关信息:
①Fe3+、Al3+完全沉淀的pH范围
| 沉淀 | Fe(OH)3 | Al(OH)3 | ||
| pH范围 | 开始沉淀 | 完全沉淀 | 开始沉淀 | 完全沉淀 |
| 2.0 | 3.2 | 3.4 | 4.7 | |
| 温度/℃ 溶解度/g 物质 | 10 | 20 | 30 | 40 | 50 | 70 |
| K2SO4 | 8.46 | 9.55 | 11.4 | 12.9 | 14.2 | 16.7 |
| Al2(SO4)3 | 25.1 | 26.6 | 28.8 | 31.4 | 34.3 | 42.2 |
| KAl(SO4)2•12H2O | 4.0 | 5.9 | 8.4 | 11.7 | 17 | 40 |
(1)步骤I中,要加快高岭土酸溶的速率可以采取的措施有
(2)滤渣的主要成分是
(3)下列说法中正确的是
A.步骤I的主要目的是提高废水中铝离子的浓度
B.步骤II中的A物质可以是KOH或NaOH
C.步骤II中调节pH的范围是3.2<pH<3.4
D.步骤IV中需调控K2SO4的用量,使n(Al3+):n(K+):n(SO
 )尽可能接近1:1:2
)尽可能接近1:1:2(4)步骤VI,为了得到较大颗粒且较干燥的晶体,请从下列选项中选出合理的操作(操作不重复)并排序:取粗产品于烧杯中加适量水→___________→___________→___________→抽滤→洗涤→___________。
a.70℃蒸发溶剂制成热的饱和溶液 b.30℃~40℃减压蒸发溶剂得到饱和溶液
c.加热烧杯至晶体完全溶解 d.缓慢冷却至室温 e.低温干燥 f.加热干燥
(5)为了测定成品中铝的含量,可采用的方法:将一定体积的成品待测液与过量的EDTA(化学式为Na2H2Y)标准液反应,加入几滴指示剂,再用ZnSO4标准液滴定过量的EDTA,反应原理如下:Al3++H2Y2-(过量)=AlY-+2H+、Zn2++H2Y2-(剩余)=ZnY2-+2H+(终点色为紫红色),过实验测出成品中铝的含量低于理论值,原因可能是
A.制备过程中,由于结晶温度控制不当,溶液中硫酸钾晶体同时析出
B.酸式滴定管用蒸馏水洗净后就注入ZnSO4标准液
C.滴定时锥形瓶溶液出现紫红色,立即停止滴定
D.滴定前,滴定管内无气泡,滴定后有气泡
您最近一年使用:0次



