一定条件下,在体积为10L的固定容器中发生反应:N2(g)+3H2(g) 2NH3(g),反应过程如图。下列说法不正确的是
2NH3(g),反应过程如图。下列说法不正确的是

 2NH3(g),反应过程如图。下列说法不正确的是
2NH3(g),反应过程如图。下列说法不正确的是
| A.t1min时正、逆反应速率相等 |
| B.X曲线表示NH3的物质的量随时间的变化关系 |
| C.0~8min,H2的平均反应速率v(H2)=0.01125mol•L-1•min-1 |
| D.10~12min,N2的平均反应速率v(N2)=0.0025mol•L-1•min-1 |
2023高三·全国·专题练习 查看更多[2]
更新时间:2023-10-21 14:44:32
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】已知 是煤液化的一个反应,在温度
是煤液化的一个反应,在温度 和
和 时将
时将 和
和 充入
充入 密闭容器中测得
密闭容器中测得 随时间(s)的变化如下表
随时间(s)的变化如下表
下列说法正确的是
 是煤液化的一个反应,在温度
是煤液化的一个反应,在温度 和
和 时将
时将 和
和 充入
充入 密闭容器中测得
密闭容器中测得 随时间(s)的变化如下表
随时间(s)的变化如下表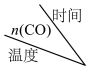 | 0 | 10 | 20 | …… | 40 | 50 |
 | 1.0 | 0.7 | 0.5 | …… | 0.25 | 0.25 |
 | 1.0 | 0.65 | 0.4 | …… | 0.28 | 0.28 |
A. 温度下平衡后恒容再充入 温度下平衡后恒容再充入 ,重新平衡后 ,重新平衡后 总的转化率与 总的转化率与 的相等 的相等 |
B. 温度下 温度下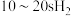 的反应速率为 的反应速率为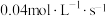 |
C.恒温,恒容条件下,通入等物质的量的反应物,当 的体积分数不变时,该反应达到了平衡状态。 的体积分数不变时,该反应达到了平衡状态。 |
D. 温度下平衡后恒定压强不变充入 温度下平衡后恒定压强不变充入 的体积分数不变 的体积分数不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】T℃下,向0.5L的恒容密闭容器中充入等物质的量的P和Q,发生反应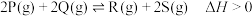 ,反应速率可表示为
,反应速率可表示为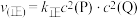 ,
,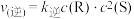 ,其中
,其中 、
、 为速率常数。反应过程中S和P的物质的量浓度变化如图所示:
为速率常数。反应过程中S和P的物质的量浓度变化如图所示:

下列说法错误的是
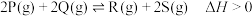 ,反应速率可表示为
,反应速率可表示为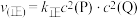 ,
,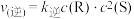 ,其中
,其中 、
、 为速率常数。反应过程中S和P的物质的量浓度变化如图所示:
为速率常数。反应过程中S和P的物质的量浓度变化如图所示:
下列说法错误的是
A.Q与S浓度相等时, |
B.反应开始至平衡,生成R的均速率为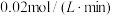 |
| C.容器内压强不再变化时,可逆反应达到平衡状态 |
D.a点时,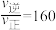 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】某反应A(g)+B(g)→C(g)+D(g)的速率方程为v=k•cm(A)•cn(B),其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为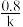 。改变反应物浓度时,反应的瞬时速率如表所示:
。改变反应物浓度时,反应的瞬时速率如表所示:
下列说法不正确 的是
 。改变反应物浓度时,反应的瞬时速率如表所示:
。改变反应物浓度时,反应的瞬时速率如表所示:| c(A)/(mol•L-1) | 0.25 | 0.50 | 1.00 | 0.50 | 1.00 | c1 |
| c(B)/(mol•L-1) | 0.050 | 0.050 | 0.100 | 0.100 | 0.200 | c2 |
| v/(10-3mol•L-1•min-1) | 1.6 | 3.2 | v1 | 3.2 | v2 | 4.8 |
| A.上述表格中的c1=0.75、v2=6.4 |
| B.该反应的速率常数k=6.4×10-3min-1 |
| C.在过量的B存在时,反应掉93.75%的A所需的时间是500min |
| D.升温、加入催化剂、缩小容积(加压),使k增大导致反应的瞬时速率加快 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在2 L密闭容器中将4 mol气体A和2 mol气体B混合,在一定温度下发生反应:3A(g)+2B(g) xC(g)+2D(g)。2 min后达到平衡时生成1.6 mol C,又测得反应速率v(D)=0.2 mol·L-1·min-1,下列说法正确的是( )
xC(g)+2D(g)。2 min后达到平衡时生成1.6 mol C,又测得反应速率v(D)=0.2 mol·L-1·min-1,下列说法正确的是( )
 xC(g)+2D(g)。2 min后达到平衡时生成1.6 mol C,又测得反应速率v(D)=0.2 mol·L-1·min-1,下列说法正确的是( )
xC(g)+2D(g)。2 min后达到平衡时生成1.6 mol C,又测得反应速率v(D)=0.2 mol·L-1·min-1,下列说法正确的是( )| A.x=4 | B.B的转化率为60% |
| C.A的平衡浓度是2.8 mol·L-1 | D.平衡时气体的压强是原来的0.94倍 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图。其中X、Y、Z都为气体,反应在t1min时到达平衡,如图所示,下列说法正确的是
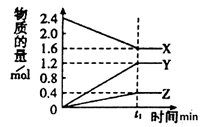

| A.该反应的化学方程式是2X=3Y+Z |
| B.已知1molX完全反应要吸收46kJ的热量,则至t1min时,该反应吸收的热量为36.8kJ·mol-1 |
| C.在此t1min时间内,用Y表示反应的平均速率v(Y)为0.6mol/(L·min) |
| D.在相同状态下,反应前的压强是反应后的0.75倍 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】反应2NO(g)+2H2(g)=N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n待测),其反应包含下列两步:①2NO+H2=N2+H2O2(慢)②H2O2+H2=2H2O(快)
T℃时测得有关实验数据如下:
下列说法错误的是
T℃时测得有关实验数据如下:
| 序号 | c(NO)/(mol·L-1) | c(H2)/(mol·L-1) | 速率/(mol·L-1·min-1) |
| Ⅰ | 0.0060 | 0.0010 | 1.8×10-4 |
| Ⅱ | 0.0060 | 0.0020 | 3.6×10-4 |
| Ⅲ | 0.0010 | 0.0060 | 3.0×10-5 |
| Ⅳ | 0.0020 | 0.0060 | 1.2×10-4 |
| A.整个反应速率由第①步反应决定 |
| B.正反应的活化能一定是①<② |
| C.该反应速率表达式:v=5000c2(NO)·c(H2) |
| D.该反应的热化学方程式为2NO(g)+2H2(g)=N2(g)+2H2O(g)ΔH=-664kJ·mol-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下图所示与对应叙述相符的是
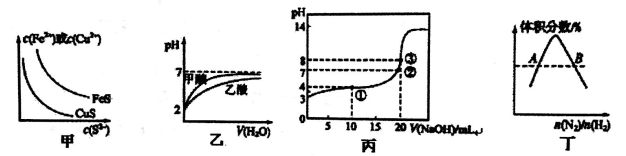

| A.图甲表示一定温度下FeS和CuS的沉淀溶解平衡曲线,则Ksp(FeS)<Ksp(CuS) |
| B.图乙表示pH=2的甲酸与乙酸溶液稀释时的pH变化曲线,则酸性:甲酸<乙酸 |
| C.该温度下向20mL0.1mol/LCH3COOH溶液中逐滴加入0.1mol/LNaOH溶液,pH变化曲线如图丙所示(忽略温度变化),则①点c(CH3COO-)>c(Na+)>c(CH3COOH) |
D.图丁表示反应N2(g)+3H2(g) 2NH3(g)平衡时NH3体积分数随起始 2NH3(g)平衡时NH3体积分数随起始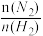 变化的曲线,则转化率:αA(H2)=αB(H2) 变化的曲线,则转化率:αA(H2)=αB(H2) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】在一定条件下,向某 恒容密闭容器中充入
恒容密闭容器中充入 、
、 ,发生反应
,发生反应 ,测得反应
,测得反应 时,不同温度下氢气的转化率如图所示。[已知:该反应的速率方程
时,不同温度下氢气的转化率如图所示。[已知:该反应的速率方程 、
、 ,
, 、
、 只与温度有关]
只与温度有关]
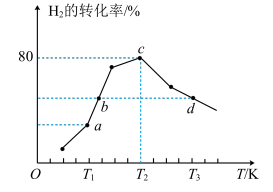
下列说法错误的是
 恒容密闭容器中充入
恒容密闭容器中充入 、
、 ,发生反应
,发生反应 ,测得反应
,测得反应 时,不同温度下氢气的转化率如图所示。[已知:该反应的速率方程
时,不同温度下氢气的转化率如图所示。[已知:该反应的速率方程 、
、 ,
, 、
、 只与温度有关]
只与温度有关]
下列说法错误的是
A.图中a、b、c三点对应的 由大到小的顺序为 由大到小的顺序为 |
| B.该反应在低温下可自发进行 |
C. 温度下,起始时容器内的压强为 温度下,起始时容器内的压强为 , ,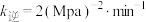 ,则该温度下 ,则该温度下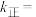 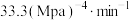 |
| D.升高温度或增大压强,都可以提高反应物的平衡转化率 |
您最近一年使用:0次




