金属钛具有良好的耐高低温、抗酸碱、高强度和低密度等优良特性,广泛应用于航空航天、医疗器械等领域。 的一种制备方法为
的一种制备方法为
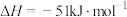 。下列说法中正确的是
。下列说法中正确的是
 的一种制备方法为
的一种制备方法为
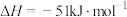 。下列说法中正确的是
。下列说法中正确的是| A.该反应只有在高温下才能自发进行 |
| B.恒温恒容条件下,混合气体的密度保持不变能说明该反应达到平衡状态 |
| C.该反应在工业生产中的适宜条件是低温、低压 |
D.恒温恒容条件下,向平衡体系中再加入少量 , ,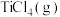 的体积分数将增大 的体积分数将增大 |
更新时间:2023-11-22 20:55:28
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在一定条件下,利用CO2合成CH3OH的反应如下:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1
研究发现,反应过程中会有副反应:
②CO2(g)+H2(g) CO(g)+H2O(g) △H2。
CO(g)+H2O(g) △H2。
温度对CH3OH、CO的产率影响如图所示。下列说法中,不正确 的是

①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1研究发现,反应过程中会有副反应:
②CO2(g)+H2(g)
 CO(g)+H2O(g) △H2。
CO(g)+H2O(g) △H2。温度对CH3OH、CO的产率影响如图所示。下列说法中,

| A.△H1<0,△H2>0 |
| B.增大压强有利于提高CH3OH的产率 |
| C.生产过程中,升温加快①的速率,减慢②的速率 |
D.合成CH3OH反应的平衡常数表达式是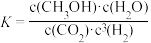 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】以丙烯(C3H6)、 、
、 为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的化学方程式分别为
为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的化学方程式分别为
反应Ⅰ: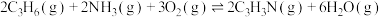
反应Ⅱ:
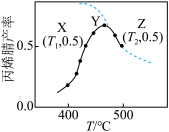
反应时间相同、反应物起始投料相同时,丙烯腈产率与反应温度的关系如图所示(图中虚线表示相同条件下丙烯腈平衡产率随温度的变化)。下列说法正确的是
 、
、 为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的化学方程式分别为
为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的化学方程式分别为反应Ⅰ:
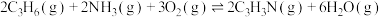
反应Ⅱ:

反应时间相同、反应物起始投料相同时,丙烯腈产率与反应温度的关系如图所示(图中虚线表示相同条件下丙烯腈平衡产率随温度的变化)。下列说法正确的是

| A.其他条件不变,增大压强有利于提高丙烯腈平衡产率 |
| B.图中X点所示条件下,延长反应时间能提高丙烯腈产率 |
| C.图中Y点丙烯腈产率高于X点的原因是温度升高导致反应Ⅰ建立的平衡向正反应方向移动 |
| D.图中X点丙烯腈产率与Z点相等(T1<T2),则Z点的正反应速率一定大于X点的正反应速率 |
您最近一年使用:0次
【推荐3】在温度T1时,向一体积固定为2L的密闭容器中通入1molCO2和3molH2发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0,5min后反应达到平衡,CO2的转化率为20%。下列说法正确的是
CH3OH(g)+H2O(g) △H<0,5min后反应达到平衡,CO2的转化率为20%。下列说法正确的是
 CH3OH(g)+H2O(g) △H<0,5min后反应达到平衡,CO2的转化率为20%。下列说法正确的是
CH3OH(g)+H2O(g) △H<0,5min后反应达到平衡,CO2的转化率为20%。下列说法正确的是| A.前5min,平均反应速率v(H2)=0.06mol·(L·min)-1 |
B.该温度下反应平衡常数的值为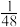 |
| C.当v正(CO2)=3v逆(H2)时,说明反应已达到平衡状态 |
| D.若平衡后升温,正反应速率减小,逆反应速率增大,平衡左移 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】将NO2与SO2以体积比1:2置于恒温恒容密闭容器中发生反应:NO2(g)+SO2(g) SO3(g)+NO(g) ΔH=-41.8kJ·mol-1,下列能说明反应达到平衡状态的是( )
SO3(g)+NO(g) ΔH=-41.8kJ·mol-1,下列能说明反应达到平衡状态的是( )
 SO3(g)+NO(g) ΔH=-41.8kJ·mol-1,下列能说明反应达到平衡状态的是( )
SO3(g)+NO(g) ΔH=-41.8kJ·mol-1,下列能说明反应达到平衡状态的是( )| A.体系压强保持不变 |
| B.混合气体颜色保持不变 |
| C.每消耗1molSO3的同时消耗1molNO |
| D.NO2、SO2、SO3、NO的浓度之比为1:1:1:1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH= −25kJ·mol-1.某温度下的平衡常数为400,此温度下,在1 L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如右表。下列说法中正确的是
CH3OCH3(g)+H2O(g) ΔH= −25kJ·mol-1.某温度下的平衡常数为400,此温度下,在1 L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如右表。下列说法中正确的是
 CH3OCH3(g)+H2O(g) ΔH= −25kJ·mol-1.某温度下的平衡常数为400,此温度下,在1 L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如右表。下列说法中正确的是
CH3OCH3(g)+H2O(g) ΔH= −25kJ·mol-1.某温度下的平衡常数为400,此温度下,在1 L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如右表。下列说法中正确的是物质 | CH3OH | CH3OCH3 | H2O |
c/mol•L-1 | 0.08 | 1.6 | 1.6 |
| A.此时刻反应未达到平衡状态 |
| B.容器内压强不变,不能说明反应达平衡 |
| C.平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH体积分数减小 |
| D.平衡时,反应混合物的总能量降低50 kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】向绝热恒容密闭容器中通入一定量的SO2和NO2,一定条件下发生反应:SO2(g)+NO2(g)⇌SO3(g)+NO(g),正反应是放热反应。测得SO3浓度随时间变化如表所示,下列说法不正确的是
| 反应时间/s | 40 | 50 | 60 | 70 | 80 | 90 | 100 | 110 |
| SO3浓度/mol·L-1 | 0.10 | 0.14 | 0.21 | 0.26 | 0.30 | 0.32 | 0.33 | 0.33 |
| A.50 s时,SO3的生成速率为0.0028 mol·L-1·s-1 |
| B.40 s~90 s时段:v正>v逆 |
| C.v正(SO2)=v逆(SO3)或v正(SO2)=v逆(NO2)均能说明反应达到平衡状态 |
| D.100s开始,容器中的温度不变,反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| B.能自发进行的化学反应,一定是△H<0、△S>0 |
| C.焰色反应是物质燃烧时火焰呈现的颜色变化,属于化学变化 |
| D.钢铁发生电化学腐蚀时,负极的电极反应式为 Fe–3e- =Fe3+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知:ΔG = ΔH-TΔS,ΔH为焓变,T为热力学温度,ΔS为熵变,当ΔG<0时反应能自发进行,ΔG>0时反应不能自发进行。据此判断下列叙述中正确的是 ( )
| A.焓变大于零的反应肯定能自发进行 |
| B.焓变小于零的反应肯定能自发进行 |
| C.焓变大于零的反应肯定不能自发进行 |
| D.焓变小于零且熵变大于零的反应一定能自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 是空气的主要成分之一,
是空气的主要成分之一, 作为原料广泛用于合成氨工业、硝酸工业等。工业上用氨催化氧化生产硝酸,在转化器中发生反应的热化学方程式为
作为原料广泛用于合成氨工业、硝酸工业等。工业上用氨催化氧化生产硝酸,在转化器中发生反应的热化学方程式为
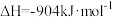 。生产硝酸的尾气中主要含有
。生产硝酸的尾气中主要含有 、
、 等大气污染物,可将其转化成
等大气污染物,可将其转化成 、
、 、
、 等而除去。对于反应
等而除去。对于反应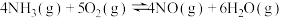 ,下列有关说法正确的是
,下列有关说法正确的是
 是空气的主要成分之一,
是空气的主要成分之一, 作为原料广泛用于合成氨工业、硝酸工业等。工业上用氨催化氧化生产硝酸,在转化器中发生反应的热化学方程式为
作为原料广泛用于合成氨工业、硝酸工业等。工业上用氨催化氧化生产硝酸,在转化器中发生反应的热化学方程式为
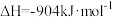 。生产硝酸的尾气中主要含有
。生产硝酸的尾气中主要含有 、
、 等大气污染物,可将其转化成
等大气污染物,可将其转化成 、
、 、
、 等而除去。对于反应
等而除去。对于反应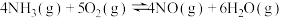 ,下列有关说法正确的是
,下列有关说法正确的是| A.该反应只有在高温条件下能自发进行 |
| B.升高温度,该反应的平衡常数减小 |
C.  和 和  充分反应放出的热量为 充分反应放出的热量为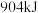 |
D.断裂  键的同时生成 键的同时生成  键,说明反应达到平衡状态 键,说明反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关说法正确的是

| A.某可逆反应若平衡朝正向移动,则平衡常数一定增大 |
B.反应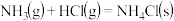 常温下可自发进行,该反应为吸热反应 常温下可自发进行,该反应为吸热反应 |
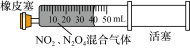
C.保持温度不变,将图中的活塞快速推至 处,新平衡时气体颜色变浅 处,新平衡时气体颜色变浅 |
D.向 溶液中加入少量水,溶液中 溶液中加入少量水,溶液中 与 与 的比值增大 的比值增大 |
您最近一年使用:0次

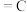 (金刚石,s)
(金刚石,s) 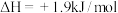 ,则金刚石比石墨稳定
,则金刚石比石墨稳定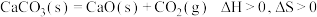 ,不论在何种条件下都不可能自发进行
,不论在何种条件下都不可能自发进行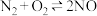 ,若在容器中充入
,若在容器中充入 ,正、逆反应的速率均不变
,正、逆反应的速率均不变