下列实验事实不能证明醋酸是弱电解质的是
| A.相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H2的起始速率相等 |
| B.相同pH、相同体积的盐酸和醋酸溶液中和同浓度NaOH溶液的能力:醋酸>盐酸 |
| C.常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4 |
| D.常温下,醋酸溶液的导电性比同物质的量浓度盐酸的弱 |
更新时间:2023-12-14 12:32:10
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法中不正确的是( )
| A.浓度均为0.1 mol⋅L-1的小苏打溶液与烧碱溶液等体积混合:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-) |
| B.pH相同的盐酸和硫酸,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液pH相等,则m>n |
| C.常温下,0.1 mol⋅L-1某一元酸HA在水中有0.1%发生电离,则该温度下HA的电离常数约为10-7 |
D.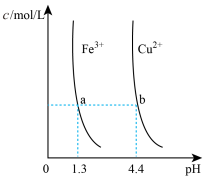 某温度下,Fe(OH)3,Cu(OH)2分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度的变化如图。由图可知:Ksp[Fe(OH)3]<Ksp[Cu(OH)2] 某温度下,Fe(OH)3,Cu(OH)2分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度的变化如图。由图可知:Ksp[Fe(OH)3]<Ksp[Cu(OH)2] |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,关于物质的量浓度均为0.1 mol·L-1的盐酸、硫酸、醋酸的说法不正确的是( )
| A.等体积的三种酸中加入等体积、等物质的量浓度的NaOH,反应后溶液的pH:醋酸>盐酸>硫酸 |
| B.与等物质的量的NaOH溶液反应,消耗三种酸的体积:硫酸>盐酸=醋酸 |
| C.等物质的量浓度的NaHCO3溶液与三种酸反应,产生气体的起始速率:硫酸>盐酸>醋酸 |
| D.三种溶液的pH:醋酸>盐酸>硫酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列验证HClO是弱电解质的实验设计错误的是
| A.25℃时,用pH试纸测0.01mol·L-1HClO的pH大于2 |
| B.25℃时,用pH计测NaClO溶液pH,测得pH=9.12 |
| C.25℃时,若测得HClO溶液pH=a,取该溶液10.0mL,加蒸馏水稀释至100.0mL,测得pH<a+1 |
| D.浓度相同的NaOH溶液分别与等体积,pH相同的次氯酸、盐酸恰好反应,前者消耗的NaOH溶液的体积多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列叙述中正确的是
A.常温下,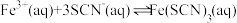 达到平衡后,加水稀释至原溶液体积的2倍,平衡正向移动 达到平衡后,加水稀释至原溶液体积的2倍,平衡正向移动 |
B.硫酸工业生产中, 在高温、高压条件下进行 在高温、高压条件下进行 |
C. 的盐酸和醋酸分别加水稀释至原溶液的100倍, 的盐酸和醋酸分别加水稀释至原溶液的100倍, :盐酸>醋酸 :盐酸>醋酸 |
D.常温下, 的氨水和 的氨水和 的盐酸等体积混合,所得溶液呈酸性 的盐酸等体积混合,所得溶液呈酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,关于溶液的稀释,下列说法正确的是
| A.pH=6的盐酸加水稀释100倍,溶液的pH=8 |
| B.将1L0.1 mol· L-1Ba(OH)2溶液加水稀释为2 L,溶液的pH= 13 |
| C.pH=3的醋酸溶液加水稀释1000倍,所得溶液pH>6 |
| D.pH=10的NaOH溶液加水稀释100倍,溶液的pH=12 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列叙述中,不能用勒夏特列原理解释的是
| A.用饱和食盐水洗气除去氯气中的氯化氢 |
B.将 的乙酸溶液稀释10倍后溶液 的乙酸溶液稀释10倍后溶液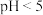 |
| C.合成氨反应常在高压条件下进行 |
D.对 平衡体系压缩容器体积后可使气体颜色变深 平衡体系压缩容器体积后可使气体颜色变深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知某二元酸 在溶液中存在电离:
在溶液中存在电离: ,
, ,
, ,设NA为阿伏加德罗常数的值。关于常温下
,设NA为阿伏加德罗常数的值。关于常温下 的
的 溶液,下列说法正确的是
溶液,下列说法正确的是
 在溶液中存在电离:
在溶液中存在电离: ,
, ,
, ,设NA为阿伏加德罗常数的值。关于常温下
,设NA为阿伏加德罗常数的值。关于常温下 的
的 溶液,下列说法正确的是
溶液,下列说法正确的是| A.该溶液与足量NaOH溶液反应的离子方程式是H2A + 2OH- = A2- + 2H2O |
| B.该溶液的c(H+)< 0.001mol/L |
C.该溶液中存在的粒子有 、 、 、 、 、 、 、 、 |
D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:2CrO42-+2H+⇌Cr2O72-+H2O。25℃时,调节初始浓度为1.0mol⋅L-1的Na2CrO4溶液的pH,测定平衡时溶液中c(Cr2O72-)和c(H+),获得如图所示的曲线。下列说法不正确的是( )
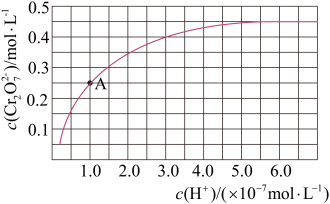

| A.平衡时,pH越小,c(Cr2O72-)越大 |
| B.A点CrO42-的平衡转化率为50% |
| C.A点CrO42-转化为Cr2O72-反应的平衡常数K=1014 |
| D.平衡时,若溶液中c(Cr2O72-)=c(CrO42-),则c(H+)>2.0×10-7mol⋅L-1 |
您最近一年使用:0次

 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大 均为
均为 的4种溶液:①HCl溶液 ②
的4种溶液:①HCl溶液 ② 溶液 ③NaOH溶液 ④氨水。有关上述溶液的比较中不正确的是
溶液 ③NaOH溶液 ④氨水。有关上述溶液的比较中不正确的是 的量①多
的量①多



