下列不能用勒夏特列原理解释的事实是
A.增大压强(减小容器的容积), 与 与 混合气体的颜色先变深后变浅 混合气体的颜色先变深后变浅 |
| B.增大压强(减小容器的容积)氢气、碘蒸气、碘化氢气体组成的平衡体系颜色变深 |
| C.黄绿色的氯水光照后颜色变浅 |
D.向含有 的红色溶液中加铁粉,振荡,溶液红色变浅或褪去 的红色溶液中加铁粉,振荡,溶液红色变浅或褪去 |
更新时间:2023-10-28 20:02:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】铬(VI)在溶液中能以多种形式存在。25℃时,调节初始浓度为0.1mol·L-1的Na2CrO4溶液的pH,平衡时铬(VI)在水溶液中各种存在形式的物质的量分数δ(X)与pH的关系如图所示。已知溶液中存在反应:2CrO +2H+
+2H+ Cr2O
Cr2O +H2O。下列说法不正确的是
+H2O。下列说法不正确的是

 +2H+
+2H+ Cr2O
Cr2O +H2O。下列说法不正确的是
+H2O。下列说法不正确的是
| A.铬酸(H2CrO4)的第一步电离为不完全电离 |
B.a点处,δ(CrO )=δ(Cr2O )=δ(Cr2O )> )> |
| C.Ka2(H2CrO4)的数量级为10-7 |
D.若将Na2CrO4溶液加少量水稀释,则 的值减小 的值减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】反应2SO2+O2 2SO3达到平衡后,再向反应器中充入由18O组成的氧气,经一段时间后,18O可能存在于。
2SO3达到平衡后,再向反应器中充入由18O组成的氧气,经一段时间后,18O可能存在于。
 2SO3达到平衡后,再向反应器中充入由18O组成的氧气,经一段时间后,18O可能存在于。
2SO3达到平衡后,再向反应器中充入由18O组成的氧气,经一段时间后,18O可能存在于。| A.生成的SO3中 | B.O2和SO3中 |
| C.剩余的SO3中 | D.O2、SO2和SO3中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学小组通过测定溶液pH,计算K2Cr2O7溶液中“Cr2O (橙色)+H2O=2CrO
(橙色)+H2O=2CrO (黄色)+2H+”的平衡常数,结果如下:
(黄色)+2H+”的平衡常数,结果如下:
下列说法不合理的是
 (橙色)+H2O=2CrO
(橙色)+H2O=2CrO (黄色)+2H+”的平衡常数,结果如下:
(黄色)+2H+”的平衡常数,结果如下:| 实验序号 | 温度(°C) | K2Cr2O7溶液浓度(mol/L) | pH | 平衡常数 |
| ① | 26.3 | 0.1000 | a | 2.5×10-15 |
| ② | 26.3 | 0.3000 | 3.78 | b |
| ③ | 50.0 | 0.1000 | 3.75 | 1.01×10-14 |
| A.a大于3.78 |
| B.b等于2.5×10-15 |
| C.由实验①③结果可说明该反应为吸热反应 |
| D.向实验①2mL溶液中加入6滴6mol/LNaOH溶液,溶液橙色加深;恢复原温度,平衡常数不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列事实中,不能用勒夏特列原理解释的是
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低
③实验室常用排饱和食盐水的方法收集氯气
④棕红色NO2加压后颜色先变深后变浅
⑤500℃时比室温更有利于合成氨的反应
⑥由H2(g)、I2(g)和HI(g)组成的平衡体系加压后颜色变深
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低
③实验室常用排饱和食盐水的方法收集氯气
④棕红色NO2加压后颜色先变深后变浅
⑤500℃时比室温更有利于合成氨的反应
⑥由H2(g)、I2(g)和HI(g)组成的平衡体系加压后颜色变深
| A.①②⑥ | B.①③⑤ | C.②⑤⑥ | D.②③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.铜的金属活泼性比铁的弱,可在海轮外壳上镶入若干铜块以减缓其腐蚀 |
| B.向0.1 mol·L-1 CH3COONa溶液中加入少量水,溶液中c(H+)/c(CH3COO-)减小 |
| C.反应TiO2(s)+2Cl2(g)===TiCl4(g)+O2(g);ΔH>0能自发进行,其原因是ΔS>0 |
D.一定温度下,增大反应2BaO2(s) 2BaO(s) +O2(g)容器的体积,平衡不移动 2BaO(s) +O2(g)容器的体积,平衡不移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实不能用勒夏特列原理解释的是
①工业合成氨
 ,反应条件选择高温
,反应条件选择高温
②实验室可以用排饱和食盐水的方法收集氯气
③硫酸工业中 ,增大
,增大 的浓度有利于提高
的浓度有利于提高 的转化率
的转化率
④对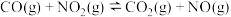
 ,平衡体系增大压强可使颜色变深
,平衡体系增大压强可使颜色变深
①工业合成氨

 ,反应条件选择高温
,反应条件选择高温②实验室可以用排饱和食盐水的方法收集氯气
③硫酸工业中
 ,增大
,增大 的浓度有利于提高
的浓度有利于提高 的转化率
的转化率④对
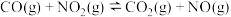
 ,平衡体系增大压强可使颜色变深
,平衡体系增大压强可使颜色变深| A.②③ | B.②④ | C.①③ | D.①④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已达到平衡的下列可逆反应中,增大压强(缩小体积),体系的颜色不变深的是( )
A.2NO2(g)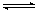 N2O4(g) N2O4(g) |
B.FeCl3(ag)+3KSCN(ag) 3KCl(ag)+Fe(SCN)3(ag) 3KCl(ag)+Fe(SCN)3(ag) |
C.2NO2(g)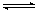 2NO(g)+O2(g) 2NO(g)+O2(g) |
D.2HBr(g)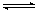 H2(g)+Br2(g) H2(g)+Br2(g) |
您最近一年使用:0次

 符合图中(Ⅰ)(Ⅱ)所示关系,
符合图中(Ⅰ)(Ⅱ)所示关系, 表示A气体在混合气体中的体积分数,Y为未知物理量。由此判断,下列说法正确的是
表示A气体在混合气体中的体积分数,Y为未知物理量。由此判断,下列说法正确的是


 H2(g)+I2(g),减小容器体积,气体颜色变深
H2(g)+I2(g),减小容器体积,气体颜色变深

