已知下列热化学方程式:回答下列问题:
H2(g)+ O2(g)=H2O(l) △H=-285.8kJ•mol-1
O2(g)=H2O(l) △H=-285.8kJ•mol-1
C(s)+ O2(g)=CO(g) △H=-110.5kJ•mol-1
O2(g)=CO(g) △H=-110.5kJ•mol-1
H2(g)+ O2(g)=H2O(g) △H=-241.8kJ•mol-1
O2(g)=H2O(g) △H=-241.8kJ•mol-1
C(s)+O2(g)=CO2(g) △H=-393.5kJ•mol-1
(1)H2的燃烧热△H=________ ;C的燃烧热为________ 。
(2)用CO2制备CH3OH可实现CO2的能源化利用,反应如下:CO2+3H2 CH3OH+H2O。温度为250℃时,测得上述反应中生成8.0gCH3OH(g)放出的热量为12.3kJ,反应的热化学方程式为
CH3OH+H2O。温度为250℃时,测得上述反应中生成8.0gCH3OH(g)放出的热量为12.3kJ,反应的热化学方程式为_______ 。
(3)某温度下,在一个1L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:
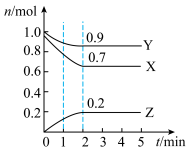
①从开始至2min,X的平均反应速率为_______ 。
②该反应的化学方程式为________ 。
③1min时,正逆反应速率的大小关系为:v(正)________ v(逆)(填“>”或“<”或“=”)。
④若X、Y、Z均为气体,在2min时,向容器中通入氩气,增大体系压强,X的化学反应速率将________ (填“变大”或、“不变”或“变小”)。
⑤10s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示。则下列说法符合该图像的是_______ 。
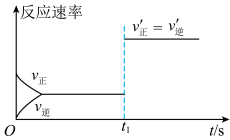
A.t1时刻,增大了X的浓度 B.t1时刻,缩小了容器体积
C.t1时刻,升高了体系温度 D.t1时刻,使用了催化剂
H2(g)+
 O2(g)=H2O(l) △H=-285.8kJ•mol-1
O2(g)=H2O(l) △H=-285.8kJ•mol-1C(s)+
 O2(g)=CO(g) △H=-110.5kJ•mol-1
O2(g)=CO(g) △H=-110.5kJ•mol-1H2(g)+
 O2(g)=H2O(g) △H=-241.8kJ•mol-1
O2(g)=H2O(g) △H=-241.8kJ•mol-1C(s)+O2(g)=CO2(g) △H=-393.5kJ•mol-1
(1)H2的燃烧热△H=
(2)用CO2制备CH3OH可实现CO2的能源化利用,反应如下:CO2+3H2
 CH3OH+H2O。温度为250℃时,测得上述反应中生成8.0gCH3OH(g)放出的热量为12.3kJ,反应的热化学方程式为
CH3OH+H2O。温度为250℃时,测得上述反应中生成8.0gCH3OH(g)放出的热量为12.3kJ,反应的热化学方程式为(3)某温度下,在一个1L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:

①从开始至2min,X的平均反应速率为
②该反应的化学方程式为
③1min时,正逆反应速率的大小关系为:v(正)
④若X、Y、Z均为气体,在2min时,向容器中通入氩气,增大体系压强,X的化学反应速率将
⑤10s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示。则下列说法符合该图像的是

A.t1时刻,增大了X的浓度 B.t1时刻,缩小了容器体积
C.t1时刻,升高了体系温度 D.t1时刻,使用了催化剂
更新时间:2023-10-31 15:06:47
|
相似题推荐
【推荐1】科研及生产中常涉及氮及其化合物。
(1)硝酸工业的重要反应之一是2NO(g)+O2(g)═2NO2(g)。800℃时在2L密闭容器中加入0.020molNO和0.010molO2,n(NO)随时间的变化如表:
①0~2s内该反应的平均速率v(O2)=_______ 。
②下列能说明该反应已经达到平衡状态的是_______ 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内的密度保持不变
③800℃时该反应的平衡常数K=_______
(2)肼(N2H4)可用做发射卫星的火箭燃料。已知:
①N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ•mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=﹣543kJ•mol-1
写出气态肼和NO2生成氮气和水蒸气的热化学方程式_______ 。肼-空气燃料电池的电解质溶液是20%~30%的KOH溶液,反应方程式是:N2H4+O2=N2+2H2O,该燃料电池的负极电极反应式是_______ 。
(3)用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一、Fe还原水体中
)已成为环境修复研究的热点之一、Fe还原水体中 的反应原理如图所示。
的反应原理如图所示。

①作负极的物质是_______ 。
②正极的电极反应式是_______ 。
(1)硝酸工业的重要反应之一是2NO(g)+O2(g)═2NO2(g)。800℃时在2L密闭容器中加入0.020molNO和0.010molO2,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.006 | 0.004 | 0.004 | 0.004 |
①0~2s内该反应的平均速率v(O2)=
②下列能说明该反应已经达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内的密度保持不变
③800℃时该反应的平衡常数K=
(2)肼(N2H4)可用做发射卫星的火箭燃料。已知:
①N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ•mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=﹣543kJ•mol-1
写出气态肼和NO2生成氮气和水蒸气的热化学方程式
(3)用零价铁(Fe)去除水体中的硝酸盐(
 )已成为环境修复研究的热点之一、Fe还原水体中
)已成为环境修复研究的热点之一、Fe还原水体中 的反应原理如图所示。
的反应原理如图所示。
①作负极的物质是
②正极的电极反应式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】抗氧剂亚硫酸钠可利用硫酸工业的炉气和尾气与纯碱反应来制取,生产流程如下图:
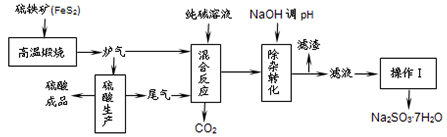
已知:①炉气、尾气中含有SO2;②混合反应中还溶解有少量Fe2O3、MgO等矿尘。
(1)煅烧1molFeS2放出热量为853kJ,则FeS2燃烧的热化学方程式为_____________ 。
(2)“混合反应”中纯碱(Na2CO3)参与反应的化学方程式为_____________ (任写一个)。
(3)用NaOH“除杂”时,主要的离子方程式为_____________ (任写一个)。
(4)通过“操作Ⅰ”可以得到亚硫酸钠晶体,写出主要操作步骤的名称:__________ 。
(3)硫酸生产中炉气转化反应为:2SO2(g)+ O2(g)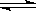 2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是
2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是________

A.该反应的正反应为放热反应
B.曲线Ⅰ上A、C两点反应速率的关系是:vA>vC
C.反应达到B点时,2v正(O2)=v逆(SO3)
D.已知V2O5的催化效果比Fe2O3好,若Ⅰ表示用V2O5催化剂的曲线,则Ⅱ是Fe2O3作催化剂的曲线

已知:①炉气、尾气中含有SO2;②混合反应中还溶解有少量Fe2O3、MgO等矿尘。
(1)煅烧1molFeS2放出热量为853kJ,则FeS2燃烧的热化学方程式为
(2)“混合反应”中纯碱(Na2CO3)参与反应的化学方程式为
(3)用NaOH“除杂”时,主要的离子方程式为
(4)通过“操作Ⅰ”可以得到亚硫酸钠晶体,写出主要操作步骤的名称:
(3)硫酸生产中炉气转化反应为:2SO2(g)+ O2(g)
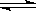 2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是
2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是
A.该反应的正反应为放热反应
B.曲线Ⅰ上A、C两点反应速率的关系是:vA>vC
C.反应达到B点时,2v正(O2)=v逆(SO3)
D.已知V2O5的催化效果比Fe2O3好,若Ⅰ表示用V2O5催化剂的曲线,则Ⅱ是Fe2O3作催化剂的曲线
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】积极发展清洁能源,推动经济社会绿色低碳转型,已经成为国际社会应对全球气候变化的普遍共识。已知:
①某些常见化学键的键能(指常温常压下,气态分子中 化学键解离成气态原子所吸收的能量)数据如下:
化学键解离成气态原子所吸收的能量)数据如下:
②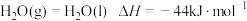 ;
;
③在 和
和 下,
下, 的燃烧热
的燃烧热 。
。
(1)氢能是理想的绿色能源。已知 。
。
①断开1molH—〇需要吸收___________  能量。
能量。
②与天然气相比,氢能的优点是___________ (任写1点)。
(2)CH3OH是一种重要的清洁燃料, 在
在 和
和 下完全燃烧生成
下完全燃烧生成 和
和 时,放出
时,放出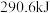 热量。
热量。
①表示 (1)燃烧热的热化学方程式为
(1)燃烧热的热化学方程式为___________ ,该反应中反应物的总键能___________ (填“大于”“小于”或“等于”)生成物的总键能。
②由 催化加氢可制备
催化加氢可制备 ,则
,则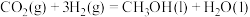

___________  ,若生成气态水,则
,若生成气态水,则
___________ (填“大于”“小于”或“等于”)该计算值。
(3)在 和
和 下,
下, 和
和 的混合气体
的混合气体 完全燃烧生成
完全燃烧生成 和
和 时,放出
时,放出 热量,则该混合气体中
热量,则该混合气体中 的物质的量分数为
的物质的量分数为___________  。
。
①某些常见化学键的键能(指常温常压下,气态分子中
 化学键解离成气态原子所吸收的能量)数据如下:
化学键解离成气态原子所吸收的能量)数据如下:| 化学键 |  |  |
键能 | 436 | 496 |
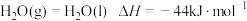 ;
;③在
 和
和 下,
下, 的燃烧热
的燃烧热 。
。(1)氢能是理想的绿色能源。已知
 。
。①断开1molH—〇需要吸收
 能量。
能量。②与天然气相比,氢能的优点是
(2)CH3OH是一种重要的清洁燃料,
 在
在 和
和 下完全燃烧生成
下完全燃烧生成 和
和 时,放出
时,放出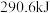 热量。
热量。①表示
 (1)燃烧热的热化学方程式为
(1)燃烧热的热化学方程式为②由
 催化加氢可制备
催化加氢可制备 ,则
,则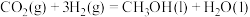

 ,若生成气态水,则
,若生成气态水,则
(3)在
 和
和 下,
下, 和
和 的混合气体
的混合气体 完全燃烧生成
完全燃烧生成 和
和 时,放出
时,放出 热量,则该混合气体中
热量,则该混合气体中 的物质的量分数为
的物质的量分数为 。
。
您最近一年使用:0次
【推荐1】Ⅰ.次磷酸 具有较强的还原性,可用于制药工业。
具有较强的还原性,可用于制药工业。
(1) 是一元酸,25℃时,
是一元酸,25℃时, 。写出其电离方程式:
。写出其电离方程式:___________ 。
(2)用电渗析法制备 的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
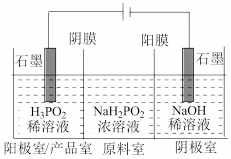
①写出阴极的电极反应:___________ 。
② 的移动方向是:
的移动方向是: 移向
移向___________ (填“阴极室”或“原料室”)。
③阳极室得到 ,
, 的浓度逐渐增大。
的浓度逐渐增大。
a.结合电极反应说明其原因是___________ 。
b.该方法得到的产品 溶液中会混有
溶液中会混有 。产生
。产生 的原因是
的原因是___________ 。
Ⅱ.氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(3)298K时, 燃烧生成
燃烧生成 放热121kJ,
放热121kJ,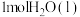 蒸发吸热44kJ,表示
蒸发吸热44kJ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ 。
(4)氢氧燃料电池中氢气在___________ (填“正”或“负”)极发生反应。
(5)在允许 自由迁移的固体电解质燃料电池中,
自由迁移的固体电解质燃料电池中,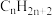 放电的电极反应式为
放电的电极反应式为___________ 。
(6)甲醇燃料电池中,吸附在催化剂表面的甲醇分子逐步脱氢得到CO,四步可能脱氢产物及其相对能量如图,则最可行途径为a→___________ (用b~j等代号表示)。

 具有较强的还原性,可用于制药工业。
具有较强的还原性,可用于制药工业。(1)
 是一元酸,25℃时,
是一元酸,25℃时, 。写出其电离方程式:
。写出其电离方程式:(2)用电渗析法制备
 的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
①写出阴极的电极反应:
②
 的移动方向是:
的移动方向是: 移向
移向③阳极室得到
 ,
, 的浓度逐渐增大。
的浓度逐渐增大。a.结合电极反应说明其原因是
b.该方法得到的产品
 溶液中会混有
溶液中会混有 。产生
。产生 的原因是
的原因是Ⅱ.氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(3)298K时,
 燃烧生成
燃烧生成 放热121kJ,
放热121kJ,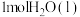 蒸发吸热44kJ,表示
蒸发吸热44kJ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为(4)氢氧燃料电池中氢气在
(5)在允许
 自由迁移的固体电解质燃料电池中,
自由迁移的固体电解质燃料电池中,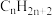 放电的电极反应式为
放电的电极反应式为(6)甲醇燃料电池中,吸附在催化剂表面的甲醇分子逐步脱氢得到CO,四步可能脱氢产物及其相对能量如图,则最可行途径为a→

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】I.反应热的研究对于化学学科发展具有重要意义。
(1)已知反应:①101kPa,2C(s)+O2(g)=2CO(g) △H=-221kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1
下列结论中正确的是____ 。
A.碳的燃烧热等于110.5kJ·mol-1
B.稀硫酸与稀NaOH溶液反应的中和热为114.6kJ·mol-1
C.含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.65kJ的热量
II.利用如图所示装置测定中和热的实验步骤如图:

①用量筒量取100mL0.50mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取100mL0.55mol·L-1溶液,并用同一温度计测出其温度;
③将NaOH和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测混合液最高温度。
(2)仪器a的名称是____ ;烧杯间填满碎泡沫塑料的作用是____ 。
(3)配制100mL0.55mol·L-1的氢氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒以及____ 。
(4)实验中改用80mL0.50mol·L-1盐酸跟80mL0.55mol·L-1溶液进行反应,与上述实验相比,所放出的热量____ (填“相等”“不相等”)。用Ba(OH)2溶液和硫酸代替上述试剂,所测中和热的数值____ 。(填“偏大”、“偏小”或“不变”)
(5)倒入NaOH和盐酸溶液的正确操作是____ (填字母)。
A.沿玻璃棒缓慢倒入 B.分多次倒入 C.一次迅速倒入
(6)现将一定量稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别与1L1.0mol·L-1的稀盐酸恰好完全反应,其反应热分别为△H1、△H2、ΔH3,则△H1、△H2、△H3的大小关系为____ 。
(1)已知反应:①101kPa,2C(s)+O2(g)=2CO(g) △H=-221kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1
下列结论中正确的是
A.碳的燃烧热等于110.5kJ·mol-1
B.稀硫酸与稀NaOH溶液反应的中和热为114.6kJ·mol-1
C.含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.65kJ的热量
II.利用如图所示装置测定中和热的实验步骤如图:

①用量筒量取100mL0.50mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取100mL0.55mol·L-1溶液,并用同一温度计测出其温度;
③将NaOH和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测混合液最高温度。
(2)仪器a的名称是
(3)配制100mL0.55mol·L-1的氢氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒以及
(4)实验中改用80mL0.50mol·L-1盐酸跟80mL0.55mol·L-1溶液进行反应,与上述实验相比,所放出的热量
(5)倒入NaOH和盐酸溶液的正确操作是
A.沿玻璃棒缓慢倒入 B.分多次倒入 C.一次迅速倒入
(6)现将一定量稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别与1L1.0mol·L-1的稀盐酸恰好完全反应,其反应热分别为△H1、△H2、ΔH3,则△H1、△H2、△H3的大小关系为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】(1)CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH= +120 kJ/mol。
2CO(g)+2H2(g) ΔH= +120 kJ/mol。
①分别在V L恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是___________ (填“A”或“B”)。
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图所示。此反应优选温度为900 ℃的原因是___________ 。


(2)氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行。
已知:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) ΔH1= +175.4 kJ/mol
2C(s)+O2(g)=2CO(g) ΔH2= -220.9 kJ/mol
①TiO2加碳氯化生成TiCl4(g)和CO(g)的热化学方程式:___________ 。
②氯化过程中CO和CO2可以相互转化,根据上图判断:CO2生成CO反应的ΔH___________ 0(填“>”“<”或“=”),判断依据:___________ 。
(3)已知C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5 kJ/mol、285.8 kJ/mol、870.3 kJ/mol,则2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=___________ kJ/mol。
 2CO(g)+2H2(g) ΔH= +120 kJ/mol。
2CO(g)+2H2(g) ΔH= +120 kJ/mol。 ①分别在V L恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图所示。此反应优选温度为900 ℃的原因是


(2)氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行。
已知:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) ΔH1= +175.4 kJ/mol
2C(s)+O2(g)=2CO(g) ΔH2= -220.9 kJ/mol
①TiO2加碳氯化生成TiCl4(g)和CO(g)的热化学方程式:
②氯化过程中CO和CO2可以相互转化,根据上图判断:CO2生成CO反应的ΔH
(3)已知C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5 kJ/mol、285.8 kJ/mol、870.3 kJ/mol,则2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=
您最近一年使用:0次
【推荐1】减弱温室效应的方法之一是将CO2回收利用,科学家研究利用回收的CO2制取甲醛,反应的热化学方程式为CO2(g)+2H2(g)⇌CH2O(g)+H2O(g) ∆H。请回答下列问题:
(1)已知:
①CH2O(g)+O2(g)=CO2(g)+H2O(g) ∆H1=-480kJ/mol
②相关化学键的键能数据如表所示:
则CO2(g)+2H2(g)⇌CH2O(g)+H2O(g) ∆H=____________
(2)一定条件下,将n(CO2):n(H2)=1:2的混合气体充入恒温恒容的密闭容器中,发生反应CO2(g)+2H2(g)⇌CH2O(g)+H2O(g)。
①下列说明反应已经达到平衡状态的是____ (填选项字母)。
a.容器内气体密度保持不变b.H2O的体积分数保持不变
c.该反应的平衡常数保持不变d.混合气体的平均相对分子质量不变
②下列措施既能提高H2的转化率又能加快反应速率的是_____ 填选项字母)
a.升高温度b.使用高效催化剂c.缩小容器体积d.扩大容器体积
(3)实验室在2L密闭容器中进行模拟上述合成CH2O的实验。T1℃时,将体积比为1:4的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:
①已知:vp(B)= 则反应开始10 min内,用H2的压强变化表示该反应的平均反应速率为
则反应开始10 min内,用H2的压强变化表示该反应的平均反应速率为___ kPa∙min-1。
②T1℃时,反应的平衡常数Kp的代数式为Kp=_______ kPa-1(Kp为用各气体分压表示的平衡常数,分压=总压×物质的量分数)。
(4)T2℃时,向体积为2L的恒容密闭容器中充入一定量的H2和CO2的混合气体,容器内气体压强为1.2 kPa,反应达到平衡时,CH2O的分压与起始的 关系如图所示:
关系如图所示:

①当 =2时,反应达到平衡后,若再向容器中加入CO2(g)和H2O(g),使二者分压均增大0.05 kPa,则达到新平衡时,H2的转化率将
=2时,反应达到平衡后,若再向容器中加入CO2(g)和H2O(g),使二者分压均增大0.05 kPa,则达到新平衡时,H2的转化率将_______ (填“增大”“减小”或“不变”)。
②当 =2.5时,达到平衡状态后,CH2O的分压可能是图像中的点
=2.5时,达到平衡状态后,CH2O的分压可能是图像中的点____ (填“D”“E”或“F”),原因为_______
(1)已知:
①CH2O(g)+O2(g)=CO2(g)+H2O(g) ∆H1=-480kJ/mol
②相关化学键的键能数据如表所示:
| 化学键 | O=O | H-H | O-H |
| 键能/kJ∙mol-1 | 498 | 436 | 464 |
则CO2(g)+2H2(g)⇌CH2O(g)+H2O(g) ∆H=
(2)一定条件下,将n(CO2):n(H2)=1:2的混合气体充入恒温恒容的密闭容器中,发生反应CO2(g)+2H2(g)⇌CH2O(g)+H2O(g)。
①下列说明反应已经达到平衡状态的是
a.容器内气体密度保持不变b.H2O的体积分数保持不变
c.该反应的平衡常数保持不变d.混合气体的平均相对分子质量不变
②下列措施既能提高H2的转化率又能加快反应速率的是
a.升高温度b.使用高效催化剂c.缩小容器体积d.扩大容器体积
(3)实验室在2L密闭容器中进行模拟上述合成CH2O的实验。T1℃时,将体积比为1:4的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:
| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 压强/kPa | 1.08 | 0.96 | 0.88 | 0.82 | 0.80 | 0.80 | 0.80 |
①已知:vp(B)=
 则反应开始10 min内,用H2的压强变化表示该反应的平均反应速率为
则反应开始10 min内,用H2的压强变化表示该反应的平均反应速率为②T1℃时,反应的平衡常数Kp的代数式为Kp=
(4)T2℃时,向体积为2L的恒容密闭容器中充入一定量的H2和CO2的混合气体,容器内气体压强为1.2 kPa,反应达到平衡时,CH2O的分压与起始的
 关系如图所示:
关系如图所示:
①当
 =2时,反应达到平衡后,若再向容器中加入CO2(g)和H2O(g),使二者分压均增大0.05 kPa,则达到新平衡时,H2的转化率将
=2时,反应达到平衡后,若再向容器中加入CO2(g)和H2O(g),使二者分压均增大0.05 kPa,则达到新平衡时,H2的转化率将②当
 =2.5时,达到平衡状态后,CH2O的分压可能是图像中的点
=2.5时,达到平衡状态后,CH2O的分压可能是图像中的点
您最近一年使用:0次
【推荐2】我国提出2060年前实现碳中和,降低大气中CO2含量是当今世界重要科研课题之一,以CO2为原料制备甲烷、戊烷、甲醇等能源物质具有较好的发展前景。回答下列问题:
(1)CO2在固体催化剂表面加氢合成甲烷过程中发生以下两个反应:
主反应:CO2(g)+4H2(g) CH4(g)+2H2O(g) ∆H1=-156.9 kJ·mol-l
CH4(g)+2H2O(g) ∆H1=-156.9 kJ·mol-l
副反应:CO2(g)+H2(g) CO(g)+H2O(g) ∆H2=+41.1 kJ·mol-1
CO(g)+H2O(g) ∆H2=+41.1 kJ·mol-1
①已知:2H2(g)+O2(g)=2H2O(g) △H3=-395.6 kJ·mol-1,则CH4燃烧的热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=
___________ 。
②加氢合成甲烷时,为使反应有较高的反应速率,通常控制温度为500℃左右,其主要原因为___________ 。
③500℃时,向1 L恒容密闭容器中充入4 mol CO2和12 mol H2,初始压强为p,20 min时主、副反应都达到平衡状态,测得c(H2O)=5 mol·L-1,体系压强为 ,则0~ 20 min内v(CH4)=
,则0~ 20 min内v(CH4)=___________ ,平衡时CH4选择性=___________ (CH4选择性 × 100%, 计算保留三位有效数字)。
× 100%, 计算保留三位有效数字)。
(2)我国科研人员将CO2和H2在Na-Fe3O4 / HZSM-5催化下转变为汽油(C5~C11的烃),反应过程如下图所示。

①若CO2在该条件下转化为戊烷(C5H12),则该反应的化学方程式为___________ 。
②催化剂中的Fe3O4可用电解法制备。电解时以Fe作电极,电解质溶液为稀硫酸,铁电极的反应式为___________ (需标注电极名称)。
(3)甲醇催化制取乙烯的过程中发生如下反应:
反应1:3CH3OH(g) C3H6(g)+3H2O(g);
C3H6(g)+3H2O(g);
反应2:2CH3OH(g) C2H4(g)+2H2O(g)
C2H4(g)+2H2O(g)
反应1的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arhenius经验公式RInk=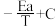 (Ea为活化能,k为速率常数,R和C为常数)。则该反应的活化能Ea=
(Ea为活化能,k为速率常数,R和C为常数)。则该反应的活化能Ea=___________ kJ·mol-l。当改变外界条件时,实验数据如图中的曲线b所示,则实验可能改变的外界条件是___________ 。
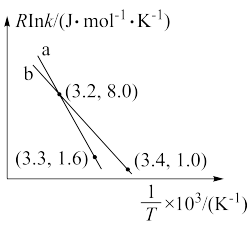
(1)CO2在固体催化剂表面加氢合成甲烷过程中发生以下两个反应:
主反应:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ∆H1=-156.9 kJ·mol-l
CH4(g)+2H2O(g) ∆H1=-156.9 kJ·mol-l副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2=+41.1 kJ·mol-1
CO(g)+H2O(g) ∆H2=+41.1 kJ·mol-1①已知:2H2(g)+O2(g)=2H2O(g) △H3=-395.6 kJ·mol-1,则CH4燃烧的热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=
②加氢合成甲烷时,为使反应有较高的反应速率,通常控制温度为500℃左右,其主要原因为
③500℃时,向1 L恒容密闭容器中充入4 mol CO2和12 mol H2,初始压强为p,20 min时主、副反应都达到平衡状态,测得c(H2O)=5 mol·L-1,体系压强为
 ,则0~ 20 min内v(CH4)=
,则0~ 20 min内v(CH4)= × 100%, 计算保留三位有效数字)。
× 100%, 计算保留三位有效数字)。(2)我国科研人员将CO2和H2在Na-Fe3O4 / HZSM-5催化下转变为汽油(C5~C11的烃),反应过程如下图所示。

①若CO2在该条件下转化为戊烷(C5H12),则该反应的化学方程式为
②催化剂中的Fe3O4可用电解法制备。电解时以Fe作电极,电解质溶液为稀硫酸,铁电极的反应式为
(3)甲醇催化制取乙烯的过程中发生如下反应:
反应1:3CH3OH(g)
 C3H6(g)+3H2O(g);
C3H6(g)+3H2O(g); 反应2:2CH3OH(g)
 C2H4(g)+2H2O(g)
C2H4(g)+2H2O(g)反应1的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arhenius经验公式RInk=
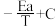 (Ea为活化能,k为速率常数,R和C为常数)。则该反应的活化能Ea=
(Ea为活化能,k为速率常数,R和C为常数)。则该反应的活化能Ea=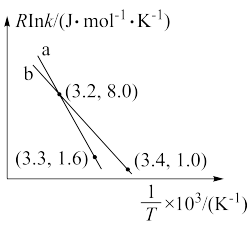
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】一定温度下,在体积为0.5L的恒容密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色) N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:

(1)曲线___ (填“X”或“Y”)表示N2O4的物质的量随时间的变化曲线。
(2)在0~3min内,用NO2表示的反应速率为___ 。
(3)若在一保温容器中加入一定量NO2,反应一段时间后,混合气体温度升高,说明2molNO2(g)的能量比1mol N2O4(g)的能量___ (填“高”或“低”)。
(4)反应达到平衡后,若降低温度,混合气体的颜色变浅,相对于降温前v(正)___ (填“增大”“减小”或“不变”,下同),v(逆)___ 。
(5)氮氧化物是重要的大气污染物,如图是监测NO含量的传感器工作原理示意图。NiO电极发生___ (填“氧化”或“还原”)反应,Pt电极是电池___ (填“正极”或“负极”)。

 N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
(1)曲线
(2)在0~3min内,用NO2表示的反应速率为
(3)若在一保温容器中加入一定量NO2,反应一段时间后,混合气体温度升高,说明2molNO2(g)的能量比1mol N2O4(g)的能量
(4)反应达到平衡后,若降低温度,混合气体的颜色变浅,相对于降温前v(正)
(5)氮氧化物是重要的大气污染物,如图是监测NO含量的传感器工作原理示意图。NiO电极发生

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】过氧乙酸(CH3COOOH)不仅在卫生医疗、食品消毒及漂白剂领域有广泛应用,也应用于环境工程、精细化工等领域。实验室利用醋酸(CH3COOH)与双氧水(H2O2)共热,在固体酸的催化下制备过氧乙酸(CH3COOOH),其装置如下图所示。请回答下列问题:
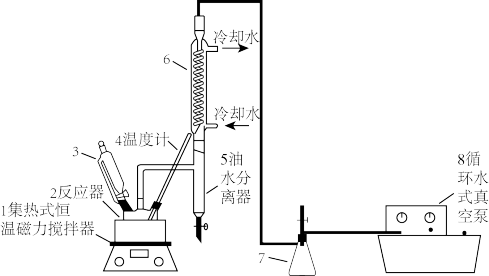
实验步骤:
Ⅰ.先在反应瓶中加入冰醋酸、乙酸丁酯和固体酸催化剂,开通仪器1和8,温度维持为55℃;
Ⅱ.待真空度达到反应要求时,打开仪器3的活塞,逐滴滴入浓度为35%的双氧水,再通入冷却水;
Ⅲ.从仪器5定期放出乙酸丁酯和水的混合物,待反应结束后分离反应器2中的混合物,得到粗产品。
(1)反应器 2中制备过氧乙酸(CH3COOOH)的化学反应方程式为_______ 。
(2)反应中维持冰醋酸过量,目的是提高_______ ;分离反应器 中的混合物得到粗产品,分离的方法是
中的混合物得到粗产品,分离的方法是_______ 。
(3)实验中加入乙酸丁酯的主要作用是_______(选填字母序号)。
(4)待观察到_______ (填现象)时,反应结束。
(5)粗产品中过氧乙酸(CH3COOOH)含量的测定:取一定体积的样品V mL,分成6等份,用过量KI溶液与过氧化物作用,以0.1 mol·L-1的硫代硫酸钠溶液滴定碘(I2+2S2O =2I-+S4O
=2I-+S4O );重复3次,平均消耗量为V1 mL。再以0.02 mol·L-1的酸性高锰酸钾溶液滴定样品,重复3次,平均消耗量为V2 mL。则样品中的过氧乙酸的浓度为
);重复3次,平均消耗量为V1 mL。再以0.02 mol·L-1的酸性高锰酸钾溶液滴定样品,重复3次,平均消耗量为V2 mL。则样品中的过氧乙酸的浓度为_______ mol·L-1。
(6)通过研究发现Fe3+、Cu2+可催化过氧乙酸分解为氧气和乙酸,现需设计实验比较Fe3+、Cu2+对过氧乙酸的催化效率。可供选择的试剂和主要器材有:a. 过氧乙酸溶液、b. 1mol·L-1的FeCl3溶液、c. 0.5 mol·L-1的Fe2(SO4)3溶液、d. 0.5 mol·L-1的CuCl2溶液、e.1 mol·L-1的CuSO4溶液、f.计时器、g.测量气体体积的针筒、i. 带导气管的试管。
你设计的实验方案为_______ 。

实验步骤:
Ⅰ.先在反应瓶中加入冰醋酸、乙酸丁酯和固体酸催化剂,开通仪器1和8,温度维持为55℃;
Ⅱ.待真空度达到反应要求时,打开仪器3的活塞,逐滴滴入浓度为35%的双氧水,再通入冷却水;
Ⅲ.从仪器5定期放出乙酸丁酯和水的混合物,待反应结束后分离反应器2中的混合物,得到粗产品。
(1)反应器 2中制备过氧乙酸(CH3COOOH)的化学反应方程式为
(2)反应中维持冰醋酸过量,目的是提高
 中的混合物得到粗产品,分离的方法是
中的混合物得到粗产品,分离的方法是(3)实验中加入乙酸丁酯的主要作用是_______(选填字母序号)。
| A.作为反应溶剂,提高反应速率 |
| B.与固体酸一同作为催化剂使用,提高反应速率 |
| C.与水形成沸点更低的混合物,利于水的蒸发,提高产率 |
| D.增大油水分离器5的液体量,便于实验观察 |
(5)粗产品中过氧乙酸(CH3COOOH)含量的测定:取一定体积的样品V mL,分成6等份,用过量KI溶液与过氧化物作用,以0.1 mol·L-1的硫代硫酸钠溶液滴定碘(I2+2S2O
 =2I-+S4O
=2I-+S4O );重复3次,平均消耗量为V1 mL。再以0.02 mol·L-1的酸性高锰酸钾溶液滴定样品,重复3次,平均消耗量为V2 mL。则样品中的过氧乙酸的浓度为
);重复3次,平均消耗量为V1 mL。再以0.02 mol·L-1的酸性高锰酸钾溶液滴定样品,重复3次,平均消耗量为V2 mL。则样品中的过氧乙酸的浓度为(6)通过研究发现Fe3+、Cu2+可催化过氧乙酸分解为氧气和乙酸,现需设计实验比较Fe3+、Cu2+对过氧乙酸的催化效率。可供选择的试剂和主要器材有:a. 过氧乙酸溶液、b. 1mol·L-1的FeCl3溶液、c. 0.5 mol·L-1的Fe2(SO4)3溶液、d. 0.5 mol·L-1的CuCl2溶液、e.1 mol·L-1的CuSO4溶液、f.计时器、g.测量气体体积的针筒、i. 带导气管的试管。
你设计的实验方案为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】氮的氧化物是大气污染物之一,用活性炭或CO还原氮氧化物,可防止空气污染。回答下列问题
已知:2C(s)+O2(g)=2CO(g) ΔH1=-221 kJ∙mol−1
C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ∙mol−1
N2(g)+O2(g)=2NO(g) ΔH3=+181 kJ∙mol−1
(1)若某反应的平衡常数表达式为 ,请写出此反应的热方程式
,请写出此反应的热方程式 __________ 。
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应:C(s)+2NO(g) N2(g)+CO2(g),NO和N2的物质的量变化如下表所示
N2(g)+CO2(g),NO和N2的物质的量变化如下表所示
①0~5min内,以CO2表示的该反应速率υ(CO2)=_____________ 。
②第15min后,温度调整到T2℃,数据变化如上表所示,则 T1_________ T2(填“>”“<”“=” )
)
(3)工业上可以用氨水除去反应C(s)+2NO(g) N2(g)+CO2(g)中产生的CO2,得到NH4HCO3溶液,反应NH
N2(g)+CO2(g)中产生的CO2,得到NH4HCO3溶液,反应NH +
+ +H2O
+H2O  NH3·H2O+H2CO3的平衡常数K=
NH3·H2O+H2CO3的平衡常数K= __________ 。(已知常温下NH3·H2O的电离平衡常数Kb=2×10−5,H2CO3的电离平衡常数Ka1=4×10−7,Ka2=4×10−11)
已知:2C(s)+O2(g)=2CO(g) ΔH1=-221 kJ∙mol−1
C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ∙mol−1
N2(g)+O2(g)=2NO(g) ΔH3=+181 kJ∙mol−1
(1)若某反应的平衡常数表达式为
 ,请写出此反应的热方程式
,请写出此反应的热方程式 (2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应:C(s)+2NO(g)
 N2(g)+CO2(g),NO和N2的物质的量变化如下表所示
N2(g)+CO2(g),NO和N2的物质的量变化如下表所示| 物质的 量/mol | T1℃ | T2℃ | |||||
| 0 | 5min | 10min | 15min | 20min | 25min | 30min | |
| NO | 2.00 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
| N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
②第15min后,温度调整到T2℃,数据变化如上表所示,则 T1
 )
)(3)工业上可以用氨水除去反应C(s)+2NO(g)
 N2(g)+CO2(g)中产生的CO2,得到NH4HCO3溶液,反应NH
N2(g)+CO2(g)中产生的CO2,得到NH4HCO3溶液,反应NH +
+ +H2O
+H2O  NH3·H2O+H2CO3的平衡常数K=
NH3·H2O+H2CO3的平衡常数K=
您最近一年使用:0次
【推荐3】利用天然气制氢称为“蓝氢”。化学原理如下:
Ⅰ.
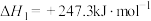
Ⅱ.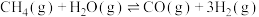
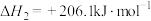
Ⅲ.

(1)
___________  。
。
(2)一定温度下,向某恒容密闭容器中充入1mol (g)和2mol
(g)和2mol (g),若仅发生反应Ⅱ和Ⅲ,下列说法正确的是
(g),若仅发生反应Ⅱ和Ⅲ,下列说法正确的是___________ (填字母)。
A.充入惰性气体,反应Ⅱ平衡向右移动
B.平衡后升高温度,反应速率增大
C.平衡时 的体积分数可能大于80%
的体积分数可能大于80%
(3)为了探究浓度对平衡的影响,某研究小组设计选择性膜反应器(如图所示)。已知:仅发生反应Ⅰ且在反应区内进行,膜可以对产物进行选择性释放。反应区内通过控制使压强恒定为100kPa.反应开始时,投料均为1mol (g)和1mol
(g)和1mol (g)。膜反应器1中0~80s内
(g)。膜反应器1中0~80s内 的平均渗透速率为
的平均渗透速率为 。膜反应器2中
。膜反应器2中 的平均渗透速率不小于膜反应器1。反应区内的部分实验数据如下表(温度相同且保持不变)。请填写下表中空格:
的平均渗透速率不小于膜反应器1。反应区内的部分实验数据如下表(温度相同且保持不变)。请填写下表中空格:
(4)一定条件下,向VL恒容密闭容器中通入2mol (g)、1mol
(g)、1mol (g)、1mol
(g)、1mol (g)发生上述反应Ⅰ、Ⅱ和Ⅲ,达到平衡时,容器中
(g)发生上述反应Ⅰ、Ⅱ和Ⅲ,达到平衡时,容器中 (g)为amol,
(g)为amol, (g)为bmol,
(g)为bmol, (g)为cmol。此温度下,反应Ⅲ的平衡常数
(g)为cmol。此温度下,反应Ⅲ的平衡常数
___________ (用含a、b的代数式表示, 为用平衡分压代替平衡浓度计算的平衡常数,分压=总压×物质的量分数)。
为用平衡分压代替平衡浓度计算的平衡常数,分压=总压×物质的量分数)。
Ⅰ.

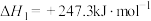
Ⅱ.
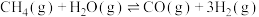
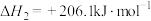
Ⅲ.


(1)

 。
。(2)一定温度下,向某恒容密闭容器中充入1mol
 (g)和2mol
(g)和2mol (g),若仅发生反应Ⅱ和Ⅲ,下列说法正确的是
(g),若仅发生反应Ⅱ和Ⅲ,下列说法正确的是A.充入惰性气体,反应Ⅱ平衡向右移动
B.平衡后升高温度,反应速率增大
C.平衡时
 的体积分数可能大于80%
的体积分数可能大于80%(3)为了探究浓度对平衡的影响,某研究小组设计选择性膜反应器(如图所示)。已知:仅发生反应Ⅰ且在反应区内进行,膜可以对产物进行选择性释放。反应区内通过控制使压强恒定为100kPa.反应开始时,投料均为1mol
 (g)和1mol
(g)和1mol (g)。膜反应器1中0~80s内
(g)。膜反应器1中0~80s内 的平均渗透速率为
的平均渗透速率为 。膜反应器2中
。膜反应器2中 的平均渗透速率不小于膜反应器1。反应区内的部分实验数据如下表(温度相同且保持不变)。请填写下表中空格:
的平均渗透速率不小于膜反应器1。反应区内的部分实验数据如下表(温度相同且保持不变)。请填写下表中空格:| 反应器示意图 | 无膜反应器 | 膜反应器1 | 膜反应器2 |
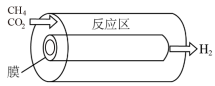 | 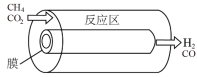 | ||
| 物质 |  |  | |
| 80s达平衡后的物质的量/mol | 0.6 | ② | |
 平衡转化率/% 平衡转化率/% | ①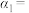 | 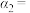 50% 50% | ③  (填“>”“<”或“=”) (填“>”“<”或“=”) |
(4)一定条件下,向VL恒容密闭容器中通入2mol
 (g)、1mol
(g)、1mol (g)、1mol
(g)、1mol (g)发生上述反应Ⅰ、Ⅱ和Ⅲ,达到平衡时,容器中
(g)发生上述反应Ⅰ、Ⅱ和Ⅲ,达到平衡时,容器中 (g)为amol,
(g)为amol, (g)为bmol,
(g)为bmol, (g)为cmol。此温度下,反应Ⅲ的平衡常数
(g)为cmol。此温度下,反应Ⅲ的平衡常数
 为用平衡分压代替平衡浓度计算的平衡常数,分压=总压×物质的量分数)。
为用平衡分压代替平衡浓度计算的平衡常数,分压=总压×物质的量分数)。
您最近一年使用:0次



