甲醇是一种可再生能源,具有开发和应用的广阔前景,CO用于合成甲醇反应方程式(于固定容器中进行):
 。反应达平衡后,下列操作既能快反应速率,又能使平衡正向移动的是
。反应达平衡后,下列操作既能快反应速率,又能使平衡正向移动的是

 。反应达平衡后,下列操作既能快反应速率,又能使平衡正向移动的是
。反应达平衡后,下列操作既能快反应速率,又能使平衡正向移动的是| A.升温 | B.恒容条件下充入He | C.加入合适的催化剂 | D.压缩体积 |
更新时间:2023-11-01 21:52:05
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】用 溶液氧化废水中的还原性污染物M,为研究降解效果,设计如下对比实验探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间的关系如图所示:
溶液氧化废水中的还原性污染物M,为研究降解效果,设计如下对比实验探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间的关系如图所示:
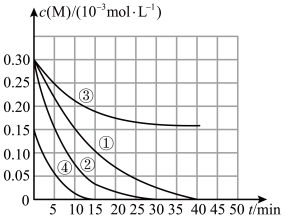
下列说法正确的是
 溶液氧化废水中的还原性污染物M,为研究降解效果,设计如下对比实验探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间的关系如图所示:
溶液氧化废水中的还原性污染物M,为研究降解效果,设计如下对比实验探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间的关系如图所示:实验编号 | 温度/ºC | pH |
① | 25 | 1 |
② | 45 | 1 |
③ | 25 | 7 |
④ | 25 | 1 |

下列说法正确的是
A.实验①中0~15min内M的降解速率为 |
| B.若其他条件相同,则实验①②说明升高温度,M的降解速率增大 |
| C.若其他条件相同,则实验①③说明pH越大,越有利于M的降解 |
| D.若其他条件相同,则实验①④说明M的浓度越小,降解的速率越快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用 CO2与丙烷反应生成丙烯和水蒸气的反应机理如图所示。下列说法错误的是


| A.C3H8是还原剂 | B.CrO3作催化剂 |
| C.Cr2O3是反应的中间体 | D.增大压强有利于提高 CO2的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定温度下,将a mol PCl5通入一个容积不变的密闭容器中,发生反应: PCl5(g)  PCl3(g)+Cl2(g),平衡时测得混合气体的压强为P1,此时向容器中再通入a mol PCl5,在相同温度下再次达到平衡时,测得压强为P2,下列判断正确的是
PCl3(g)+Cl2(g),平衡时测得混合气体的压强为P1,此时向容器中再通入a mol PCl5,在相同温度下再次达到平衡时,测得压强为P2,下列判断正确的是
 PCl3(g)+Cl2(g),平衡时测得混合气体的压强为P1,此时向容器中再通入a mol PCl5,在相同温度下再次达到平衡时,测得压强为P2,下列判断正确的是
PCl3(g)+Cl2(g),平衡时测得混合气体的压强为P1,此时向容器中再通入a mol PCl5,在相同温度下再次达到平衡时,测得压强为P2,下列判断正确的是| A.2P1>P2 | B.P1>P2 |
| C.PCl5的转化率增大 | D.Cl2的体积分数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】合成氨反应:N2(g)+3H2(g) 2NH3(g) ΔH<0。图1表示在2L恒容密闭容器中NH3的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时NH3的体积分数随起始时H2的物质的量的变化曲线。下列说法正确的是
2NH3(g) ΔH<0。图1表示在2L恒容密闭容器中NH3的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时NH3的体积分数随起始时H2的物质的量的变化曲线。下列说法正确的是
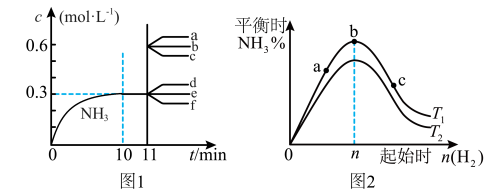
 2NH3(g) ΔH<0。图1表示在2L恒容密闭容器中NH3的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时NH3的体积分数随起始时H2的物质的量的变化曲线。下列说法正确的是
2NH3(g) ΔH<0。图1表示在2L恒容密闭容器中NH3的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时NH3的体积分数随起始时H2的物质的量的变化曲线。下列说法正确的是
| A.图1中,其他条件不变,第11min改用更为高效的催化剂,则c(NH3)-t的变化趋势为曲线b所示 |
| B.图1中,其他条件不变,第11min迅速压缩容器体积为1L,则c(NH3)-t的变化趋势为曲线a所示 |
| C.图2中,反应物N2的平衡转化率:b>a>c |
| D.图2中,T1、T2表示温度,则T1>T2 |
您最近一年使用:0次

 2CO ΔH>0的速率为v,若升高温度逆反应速率减小
2CO ΔH>0的速率为v,若升高温度逆反应速率减小

