下列有关叙述正确的是
①工业上通常采用铁触媒、400~500℃和10MPa~30Mpa的条件下合成氨
②等体积、等pH的盐酸和醋酸,分别与等浓度的NaOH反应,醋酸消耗的NaOH体积大
③化学平衡常数变化,化学平衡不一定发生移动
④通过压缩体积增大压强,可以提高单位体积内活化分子百分数,从而提高反应速率
⑤在中和反应反应热的测定实验中,每组实验至少三次使用温度计
⑥反应CaSO4(s)=CaO(s)+SO3(g) ∆H>0在高温下能自发进行
①工业上通常采用铁触媒、400~500℃和10MPa~30Mpa的条件下合成氨
②等体积、等pH的盐酸和醋酸,分别与等浓度的NaOH反应,醋酸消耗的NaOH体积大
③化学平衡常数变化,化学平衡不一定发生移动
④通过压缩体积增大压强,可以提高单位体积内活化分子百分数,从而提高反应速率
⑤在中和反应反应热的测定实验中,每组实验至少三次使用温度计
⑥反应CaSO4(s)=CaO(s)+SO3(g) ∆H>0在高温下能自发进行
| A.①②③⑥ | B.①②⑤⑥ | C.②④⑤⑥ | D.①③④⑤ |
更新时间:2023-12-06 08:45:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
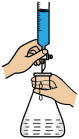
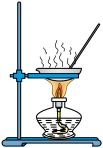
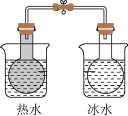
【推荐1】下列实验装置及其应用的描述均正确的是


| A.用①装置验证铁钉的析氢腐蚀 |
| B.用②装置进行强酸强碱稀溶液的中和热测定 |
| C.用③装置测定未知稀盐酸的物质的量浓度 |
| D.用④装置探究反应物浓度对反应速率的影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验装置(部分夹持装置已略去)能达到对应实验目的是
|
|
|
|
| A.测定中和热 | B.用 溶液滴定盐酸溶液 溶液滴定盐酸溶液 | C.将 溶液蒸干制备 溶液蒸干制备 | D.烧瓶中盛有 和 和 ,验证温度对化学平衡的影响 ,验证温度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知某化学反应的平衡常数表达式为K= ,在不同的温度下该反应的平衡常数如下表:
,在不同的温度下该反应的平衡常数如下表:

下列有关叙述不正确的是
 ,在不同的温度下该反应的平衡常数如下表:
,在不同的温度下该反应的平衡常数如下表:
下列有关叙述不正确的是
A.该反应的化学方程式是CO(g)+H2O(g) CO2(g)+H2(g) CO2(g)+H2(g) |
| B.上述反应的正反应是放热反应 |
| C.若在一定体积的密闭容器中通入CO2和H2各1mol,5 min后温度升高到830℃,此时测得CO2为0.4 mol时,该反应达到平衡状态 |
D.若平衡浓度符合下列关系式: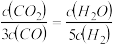 ,则此时的温度为1000℃ ,则此时的温度为1000℃ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知恒容密闭容器中发生反应:
 ,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示,下列叙述正确的是
,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示,下列叙述正确的是
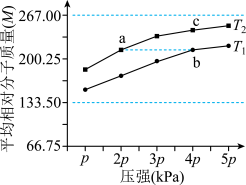

 ,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示,下列叙述正确的是
,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示,下列叙述正确的是
A.温度: | B.平衡常数: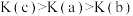 |
C.反应速率: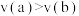 | D.当M为200.25时转化率约为33% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】一定温度下,在三个体积均为1.0L的恒容密闭容器中,充入一定量的H2和SO2发生下列反应:3H2(g)+SO2(g) ⇌2H2O(g)+H2S(g)
下列说法正确的是
| 容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
| H2 | SO2 | H2 | SO2 | ||
| 容器Ⅰ | 300 | 0.3 | 0.1 | / | 0.02 |
| 容器Ⅱ | 300 | 0.6 | 0.2 | / | / |
| 容器Ⅲ | 240 | 0.3 | 0.1 | / | 0.01 |
| A.该反应正反应为吸热反应 |
| B.容器II达到平衡时KII>KI |
| C.容器III达到平衡的时间比容器I短 |
| D.240℃时,起始时向容器III中充入0.02molH2、0.02molSO2、0.04molH2O(g)、0.04molH2S,此时反应将向正反应方向进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法不 正确的是
A.已知反应2NO2(g) N2O4(g)在低温下可自发进行,则△H>0 N2O4(g)在低温下可自发进行,则△H>0 |
| B.夏天冰箱保鲜食品的原理是降低温度,减小化学反应速率 |
| C.当锌粒和稀硫酸反应制氢气时,往溶液中加少量醋酸钠固体会减缓反应 |
| D.当锌粒和盐酸反应制氢气时,往溶液中滴加少量CuSO4溶液可加快反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于化学反应方向的确定,下列说法正确的是
| A.在温度、压强一定的条件下,焓变和熵变共同决定一个化学反应的方向 |
| B.温度、压强一定时,放热的熵增加反应一定不能自发进行 |
| C.焓变是决定反应能否自发进行的唯一因素 |
| D.固体的溶解过程熵不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】电解质溶液的电导率越大,导电能力越强。用0.100 mol·L-1的NaOH溶液滴定10.00 mL浓度均为0.100 mol·L-1的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液 的电导率如图所示。下列说法不正确的是


| A.A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.0500 mol·L-1 |
| B.曲线②代表滴定CH3COOH溶液的曲线 |
| C.在相同温度下,A、B、C三点溶液中水的电离程度:A>C>B |
| D.B点溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断正确的是
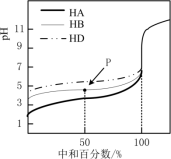

| A.三种酸的酸性强弱关系:HD>HB>HA |
| B.滴定至P点时,溶液中:c(HB)>c(B-)>c(Na+)>c(H+)>c(OH-) |
| C.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) |
| D.当中和百分数达100%时,将三种溶液混合后:c(OH-)-c(H+)=c(HA)+c(HB)+c(HD) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验操作及现象、推论不相符 的是
| 选项 | 操作及现象 | 推论 |
| A | 用pH试纸测得0.1mol/LCH3COOH溶液pH约为3 | CH3COOH是弱电解质 |
| B | 用pH计测定相同浓度的CH3COONa溶液和NaClO溶液的pH,前者的pH小于后者的pH | HClO的酸性弱于CH3COOH |
| C | 向2mL1mol/LNaOH溶液中加入1mL0.1mol/LMgCl2溶液,产生白色沉淀;再加入1mL0.1mol/LFeCl3溶液,沉淀变为红褐色 | Mg(OH)2沉淀转化为Fe(OH)3沉淀 |
| D | 将纯水加热到95℃,pH<7 | 加热可促进水的电离 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



 偏大
偏大

