工业合成氨反应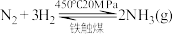
 ,下列说法正确的是
,下列说法正确的是
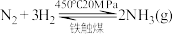
 ,下列说法正确的是
,下列说法正确的是| A.合成氨反应为放热反应,高温可提高该反应的限度 |
| B.高压条件有利于平衡正向移动,加快正向反应速率,降低逆向反应速率 |
| C.使用高效催化剂可以提高原料的平衡转化率 |
| D.及时将体系中的NH3液化分离有利于平衡正向移动 |
更新时间:2023-12-12 18:37:07
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】反应C(s)+H2O(g) CO(g)+H2(g)在一个体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
①增加固体碳的量
②保持压强不变,充入Ar使体系体积增大
③加入适当的催化剂
④保持体积不变,充入Ar使体系压强增大
 CO(g)+H2(g)在一个体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是①增加固体碳的量
②保持压强不变,充入Ar使体系体积增大
③加入适当的催化剂
④保持体积不变,充入Ar使体系压强增大
| A.①③ | B.①④ | C.①② | D.③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】十氢萘(C10H18)是具有高储氢密度的氢能载体,经历“C10H18 C10H12
C10H12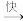 C10H8”的脱氢过程释放氢气。反应Ⅰ:C10H18(l)
C10H8”的脱氢过程释放氢气。反应Ⅰ:C10H18(l) C10H12(l)+3H2(g) ΔH1;反应Ⅱ:C10H12(l)
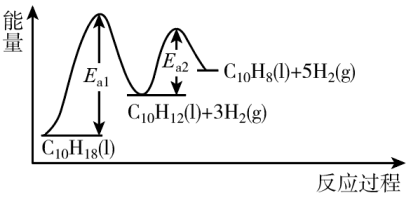
C10H12(l)+3H2(g) ΔH1;反应Ⅱ:C10H12(l) C10H8(l)+2H2(g) ΔH2;在一定温度下,其反应过程对应的能量变化如图。下列说法正确的是
C10H8(l)+2H2(g) ΔH2;在一定温度下,其反应过程对应的能量变化如图。下列说法正确的是
 C10H12
C10H12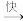 C10H8”的脱氢过程释放氢气。反应Ⅰ:C10H18(l)
C10H8”的脱氢过程释放氢气。反应Ⅰ:C10H18(l) C10H12(l)+3H2(g) ΔH1;反应Ⅱ:C10H12(l)
C10H12(l)+3H2(g) ΔH1;反应Ⅱ:C10H12(l) C10H8(l)+2H2(g) ΔH2;在一定温度下,其反应过程对应的能量变化如图。下列说法正确的是
C10H8(l)+2H2(g) ΔH2;在一定温度下,其反应过程对应的能量变化如图。下列说法正确的是 
| A.总反应的ΔH1=Ea1-Ea2 |
| B.C10H18(1)的脱氢过程中,不会有大量中间产物C10H12(1)积聚 |
| C.十氢萘脱氢的总反应速率由反应Ⅱ决定 |
| D.选择合适的催化剂不能改变Ea1、Ea2的大小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】各可逆反应达平衡后,改变反应条件,其变化趋势正确的是
A.CH3COOH CH3COO-+H+(忽略溶液体积变化) CH3COO-+H+(忽略溶液体积变化)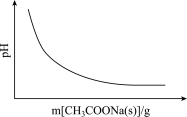 |
B.FeCl3+3KSCN Fe(SCN)3+3KCl(忽略溶液体积变化) Fe(SCN)3+3KCl(忽略溶液体积变化)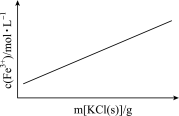 |
C.N2(g)+3H2(g)  2NH3(g)(恒温恒压) 2NH3(g)(恒温恒压) 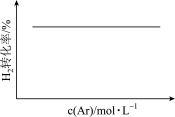 |
D.CH3OCH3(g)+3H2O(g)  6H2(g)+2CO2(g) △H>0(密闭容器,恒压) 6H2(g)+2CO2(g) △H>0(密闭容器,恒压)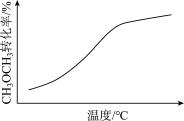 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
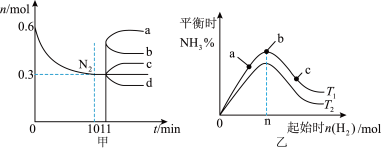
【推荐2】一定条件下,关于工业合成氨的反应, ,图甲表示1L密闭容器中
,图甲表示1L密闭容器中 随时间的变化曲线,图乙表示在恒温恒容下,初始投料0.6mol
随时间的变化曲线,图乙表示在恒温恒容下,初始投料0.6mol ,改变起始时
,改变起始时 对该平衡的影响。下列说法正确的是
对该平衡的影响。下列说法正确的是
 ,图甲表示1L密闭容器中
,图甲表示1L密闭容器中 随时间的变化曲线,图乙表示在恒温恒容下,初始投料0.6mol
随时间的变化曲线,图乙表示在恒温恒容下,初始投料0.6mol ,改变起始时
,改变起始时 对该平衡的影响。下列说法正确的是
对该平衡的影响。下列说法正确的是
A.甲:10min内该反应的平均速率 |
B.甲:从11min起其他条件不变,压缩容器体积,则 的变化曲线为b 的变化曲线为b |
C.乙:a、b、c三点所处的平衡状态中,b点 的转化率最高 的转化率最高 |
D.乙: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】随着科学技术的发展,对氨的需要量日益增长。关于合成氨工艺,下列理解不正确的是
A.合成氨反应在不同温度下的 和 和 都小于零 都小于零 |
B.温度、压强一定时,在原料气( 和 和 的比例不变)中添加少量惰性气体,可提高反应气平衡转化率 的比例不变)中添加少量惰性气体,可提高反应气平衡转化率 |
| C.原料气须经过净化处理,以防止催化剂中毒和安全事故发生 |
D.由于 易液化,不断将反应体系中的液氨移去,有利于反应正向进行 易液化,不断将反应体系中的液氨移去,有利于反应正向进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】化学是一门以实验为基础的学科。下列实验操作能达到目的的是
| 选项 | 目的 | 实验操作 |
| A | 探究温度对化学平衡的影响 | 加热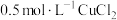 溶液 溶液 |
| B | 探究浓硫酸具有吸水性 | 向蔗糖中滴入浓硫酸 |
| C | 除去Cu粉中混有的CuO | 加入稀硝酸溶解,过滤、洗涤、干燥 |
| D | 获得纯净干燥的氯气 | 将混有氯化氢和水蒸气的氯气依次通过浓硫酸和饱和食盐水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 探究温度对化学平衡的影响 | 加热0.5 mol·L  溶液 溶液 |
| B | 证明干燥的氯气不具有漂白性 | 将干燥的氯气通入盛有红色鲜花的集气瓶中 |
| C | 证明溴与苯发生了取代反应 | 向溴水中加入苯,振荡后静置,水层颜色变浅 |
| D | 验证还原性: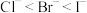 | 向NaCl、KI的混合溶液中加入少量溴水和 ,振荡,四氯化碳层为紫色 ,振荡,四氯化碳层为紫色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】用双氧水与环己酮制备6-羟基已酸( )的反应历程如图所示。该反应的副产物为
)的反应历程如图所示。该反应的副产物为 ,下列说法错误的是
,下列说法错误的是

 )的反应历程如图所示。该反应的副产物为
)的反应历程如图所示。该反应的副产物为 ,下列说法错误的是
,下列说法错误的是
| A.温度升高,生成6-羟基己酸的正反应速率增大的程度大于其逆反应速率增大的程度 |
| B.温度升高,产品纯度降低 |
C.主反应的决速步为步骤 +H2O2→ +H2O2→ |
D.达平衡前,若加入催化剂能降低 +H2O2→ +H2O2→ 的活化能,则可能使产品纯度更高 的活化能,则可能使产品纯度更高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】对于可逆反应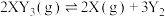 (?)
(?)  ,有关图像
,有关图像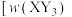 表示平衡时
表示平衡时 所占的体积分数]如图所示,下列说法正确的是
所占的体积分数]如图所示,下列说法正确的是

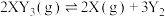 (?)
(?)  ,有关图像
,有关图像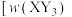 表示平衡时
表示平衡时 所占的体积分数]如图所示,下列说法正确的是
所占的体积分数]如图所示,下列说法正确的是
A.依据图1可知 , , 为液体 为液体 |
B.图2中 时改变的条件不可能为压缩容器体积 时改变的条件不可能为压缩容器体积 |
| C.图3中曲线b表示的是该反应的正反应速率 |
D.已知100℃时,平衡常数 。若在此温度下,测得某密闭容器中某时刻 。若在此温度下,测得某密闭容器中某时刻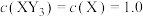 mol⋅L mol⋅L , ,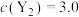 mol⋅L mol⋅L ,则此时 ,则此时 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】将BaO2放入密闭的真空容器中,发生反应:2BaO2(s) 2BaO(s)+O2(g)并达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
2BaO(s)+O2(g)并达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
 2BaO(s)+O2(g)并达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
2BaO(s)+O2(g)并达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是| A.平衡常数减小 | B.BaO物质的量不变 |
| C.总压强增大 | D.BaO2 物质的量增加 |
您最近一年使用:0次

 溶液中加入少量
溶液中加入少量 固体,促进
固体,促进 和
和 的混合气体,压缩后颜色加深
的混合气体,压缩后颜色加深

