工业上利用镁精矿石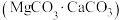 可以制备单质Mg,其反应原理为
可以制备单质Mg,其反应原理为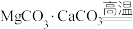
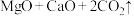 、
、 。请回答下列问题:
。请回答下列问题:
(1)基态硅原子核外电子云轮廓图呈球形、哑铃形的能级上电子数之比为______ ;上述反应原理中所涉及的非金属元素的电负性从大到小的顺序为______ (用元素符号表示)。
(2)钙或钙盐的焰色为砖红色,该光谱属于______ 光谱(填“吸收”或“发射”)。
(3)单质镁、单质硅的晶体类型依次为______ 、______ 。
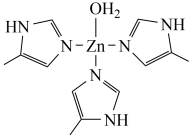
(4)排放出的二氧化碳可用碳酸酐酶固定,碳酸酐酶的部分结构如图所示:
已知: 为平面形分子。
为平面形分子。
①上述碳酸酐酶的部分结构中氮原子、氧原子的杂化类型依次为______ 、______ 。
②1mol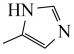 分子中含有
分子中含有______  键。
键。
(5)MgO具有NaCl型结构,X射线衍射实验测得MgO晶胞边长为anm。

设 为阿伏加德罗常数的值,则MgO晶体的密度为
为阿伏加德罗常数的值,则MgO晶体的密度为______  ((用含a、
((用含a、 的代数式表示)。
的代数式表示)。
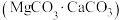 可以制备单质Mg,其反应原理为
可以制备单质Mg,其反应原理为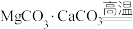
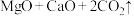 、
、 。请回答下列问题:
。请回答下列问题:(1)基态硅原子核外电子云轮廓图呈球形、哑铃形的能级上电子数之比为
(2)钙或钙盐的焰色为砖红色,该光谱属于
(3)单质镁、单质硅的晶体类型依次为
(4)排放出的二氧化碳可用碳酸酐酶固定,碳酸酐酶的部分结构如图所示:

已知:
 为平面形分子。
为平面形分子。①上述碳酸酐酶的部分结构中氮原子、氧原子的杂化类型依次为
②1mol
 分子中含有
分子中含有 键。
键。(5)MgO具有NaCl型结构,X射线衍射实验测得MgO晶胞边长为anm。

设
 为阿伏加德罗常数的值,则MgO晶体的密度为
为阿伏加德罗常数的值,则MgO晶体的密度为 ((用含a、
((用含a、 的代数式表示)。
的代数式表示)。
更新时间:2023-12-13 08:44:39
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】近日,济南大学原长洲教授制备了一种高性能的钾离子电池负极材料(Bi—MOF),反应可简单表示为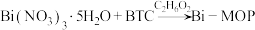 。回答下列问题:
。回答下列问题:
(1)铋(Bi)位于元素周期表中第6周期ⅤA族,基态Bi原子的价层电子排布式为_______ ,Bi(NO3)3中阴离子的中心原子的杂化方式为_______ 。基态O原子核外成对电子数与未成对电子数之比为_______ 。
(2)BTC分子中组成元素C、N、O的电负性由大到小排序为_______ 。
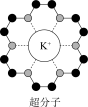
(3)冠醚是皇冠状的分子,可用不同大小的空穴适配不同大小的碱金属离子。18—冠—6(18指C、O原子总数为18,6指氧原子数)与钾离子形成的超分子结构如图所示。
①冠醚分子中C原子的杂化类型为_______ 。
②下列叙述正确的是_______ (填字母)。
A.含该超分子的物质属于分子晶体 B.冠醚可用于分离不同的碱金属离子
C.中心碱金属离子的配位数固定不变 D.冠醚与碱金属离子之间形成离子键
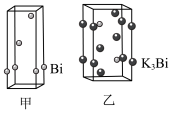
(4)铋的相关晶胞如图所示。_______ 。
②已知乙晶胞底边长为acm,高为bcm, 为阿伏加德罗常数的值。该晶体密度
为阿伏加德罗常数的值。该晶体密度_______ g·cm-3(只列计算式)。
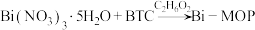 。回答下列问题:
。回答下列问题:(1)铋(Bi)位于元素周期表中第6周期ⅤA族,基态Bi原子的价层电子排布式为
(2)BTC分子中组成元素C、N、O的电负性由大到小排序为
(3)冠醚是皇冠状的分子,可用不同大小的空穴适配不同大小的碱金属离子。18—冠—6(18指C、O原子总数为18,6指氧原子数)与钾离子形成的超分子结构如图所示。
①冠醚分子中C原子的杂化类型为
②下列叙述正确的是
A.含该超分子的物质属于分子晶体 B.冠醚可用于分离不同的碱金属离子
C.中心碱金属离子的配位数固定不变 D.冠醚与碱金属离子之间形成离子键
(4)铋的相关晶胞如图所示。
②已知乙晶胞底边长为acm,高为bcm,
 为阿伏加德罗常数的值。该晶体密度
为阿伏加德罗常数的值。该晶体密度
您最近一年使用:0次
【推荐2】过渡金属元素在工业生产中发挥着重要作用。技术人员晒制蓝图时,用K3[Fe(C2O4)3]●3H2O(三草酸合铁酸钾晶体)作感光剂,再以K3[Fe(CN)6](六氰合铁酸钾)溶液作显影剂。
请回答以下问题:
(1)铁元素位于元素周期表的___________ 区,Fe3+的基态价电子排布图为___________ ;在上述两种钾盐中第一电离能最大的元素为___________ 。
(2)C与Si为同主族元素,高纯硅制备过程中会生成SiHCl3、SiCl4等中间产物。 已知电负性:H>Si,则SiHCl3中H的化合价为___________ ;SiCl4中硅原子的杂化类型是___________ ; 沸点:SiHCl3<SiC14原因是___________ 。
(3)复兴号亚运智能动车组列车材质用到Mn、Co等元素。Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],CH3CN中σ 键与π 键数目之比为___________ ;CH3CN与Mn形成___________ 键。
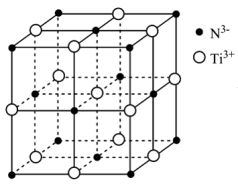
(4)时速600千米的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图),晶胞参数(晶胞棱长)为a D(1D= 10-10m),其中阴离子(N3-)采用面心立方最密堆积方式,则1个晶胞中含有___________ 个TiN;该氮化钛的密度为___________ g/cm3(列出计算式,阿伏加德罗常数的值为NA)。
请回答以下问题:
(1)铁元素位于元素周期表的
(2)C与Si为同主族元素,高纯硅制备过程中会生成SiHCl3、SiCl4等中间产物。 已知电负性:H>Si,则SiHCl3中H的化合价为
(3)复兴号亚运智能动车组列车材质用到Mn、Co等元素。Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],CH3CN中σ 键与π 键数目之比为
(4)时速600千米的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图),晶胞参数(晶胞棱长)为a D(1D= 10-10m),其中阴离子(N3-)采用面心立方最密堆积方式,则1个晶胞中含有

您最近一年使用:0次
【推荐3】Co2+能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下:

(1)Co2+的基态核外电子排布式为_________ 。
(2)H、N、O电负性大小关系是_________ 。
(3)1mol水杨醛中的σ键的数目为_________ mol。水杨醛缩对氯苯胺中的C原子的杂化方式_________ 。
(4)与H2O互为等电子体的阴离子是_________ 。
(5)Co、Mn、Al形成的合金薄膜的晶胞如图所示,该合金薄膜的化学式为_________ 。
 。
。

(1)Co2+的基态核外电子排布式为
(2)H、N、O电负性大小关系是
(3)1mol水杨醛中的σ键的数目为
(4)与H2O互为等电子体的阴离子是
(5)Co、Mn、Al形成的合金薄膜的晶胞如图所示,该合金薄膜的化学式为
 。
。
您最近一年使用:0次
【推荐1】我国某科研工作者制备了一种高性能的钾离子电池负极材料(Bi-MOF),如图所示。回答下列问题:
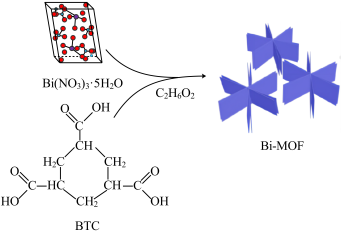
(1)铋的原子序数为83,则铋在元素周期表中的位置为___________ ,能量最高的电子所占据的原子轨道的电子云轮廓图为___________ 形。
(2)BTC中C原子的杂化类型有___________ 。
(3)该电池负极材料充电时,会形成钾铋合金(化学式为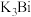 ),其晶胞结构如图。晶胞参数为
),其晶胞结构如图。晶胞参数为 、
、 、
、 ,以晶胞参数为单位长度建立原子分数坐标,表示晶胞中的原子位置,若1号原子的坐标为
,以晶胞参数为单位长度建立原子分数坐标,表示晶胞中的原子位置,若1号原子的坐标为 ,3号原子的坐标为
,3号原子的坐标为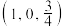 。
。

①2号原子的坐标为___________ 。
②设 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为___________  (列式即可)。
(列式即可)。

(1)铋的原子序数为83,则铋在元素周期表中的位置为
(2)BTC中C原子的杂化类型有
(3)该电池负极材料充电时,会形成钾铋合金(化学式为
 ),其晶胞结构如图。晶胞参数为
),其晶胞结构如图。晶胞参数为 、
、 、
、 ,以晶胞参数为单位长度建立原子分数坐标,表示晶胞中的原子位置,若1号原子的坐标为
,以晶胞参数为单位长度建立原子分数坐标,表示晶胞中的原子位置,若1号原子的坐标为 ,3号原子的坐标为
,3号原子的坐标为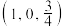 。
。
①2号原子的坐标为
②设
 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 (列式即可)。
(列式即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】传统中药的砷剂俗称“砒霜”,请回答下列问题:
(1)砷剂的分子结构如图甲所示.该化合物中As原子的杂化方式为__ .
(2)基态砷原子的价层电子排布式为__ ,砷与硒的第一电离能较大的是__ .
(3)已知:
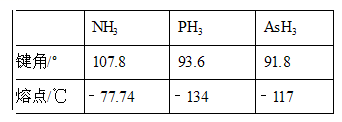
依据表中数据解释NH3熔点最高的原因__ .
(4)砷酸(H3AsO4)是一种三元中强酸,根据价层电子对互斥理论推测AsO43﹣的空间构型为__ .
(5)砷镍合金的晶胞如图乙所示,该晶体中与每个Ni原子距离最近的As原子有__ 个.
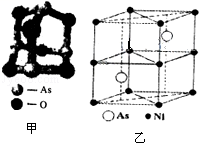
(1)砷剂的分子结构如图甲所示.该化合物中As原子的杂化方式为
(2)基态砷原子的价层电子排布式为
(3)已知:

依据表中数据解释NH3熔点最高的原因
(4)砷酸(H3AsO4)是一种三元中强酸,根据价层电子对互斥理论推测AsO43﹣的空间构型为
(5)砷镍合金的晶胞如图乙所示,该晶体中与每个Ni原子距离最近的As原子有

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】尿素[CO(NH2)2]合成方法的发展体现了化学科学与技术的不断进步。
(1)德国化学家韦勒(F. Wohler)首次在实验室里用无机物合成了尿素[CO(NH2)2],打破了无机物和有机物之间的界限。尿素分子中σ键和π键个数之比为___________ ,尿素中碳原子的杂化轨道类型为___________ 。
(2)二十世纪初,工业上以CO2和NH3为原料在一定温度和压强下合成尿素。反应分为两步:ⅰ.CO2和NH3生成H2NCOONH4;ⅱ。H2NCOONH4分解生成尿素。
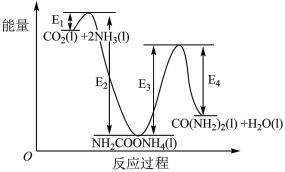
结合反应过程中能量变化示意图,下列说法正确的是___________ (填字母)。
a.活化能:反应ⅰ<反应ⅱ
b.CO2(l) +2NH3(l)= H2NCOONH4(l) △H=+(E2-E1)kJ/mol
c. H2NCOONH4(l)=CO(NH2)2(l)+ H2O(1) △H=+(E3- E4)kJ/mol
d.对反应体系加热,可加快反应速率和提高尿素的产率
(3)近年研究发现,电催化CO2和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通入CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示(阴、阳极区溶液均为KNO3溶液)。
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通入CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示(阴、阳极区溶液均为KNO3溶液)。

①电解池中电极X应接直流电源的___________ 极。
②电解过程中生成尿素的电极反应式是___________ 。
(4)尿素样品含氮量的测定方法如下。
已知:溶液中c( )不能直接用NaOH溶液准确滴定。
)不能直接用NaOH溶液准确滴定。
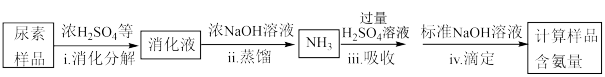
①消化液中的含氮粒子是___________ 。
②下列装置,可以完成蒸馏操作的是___________ (填字母)。
A.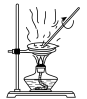 B.
B. 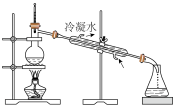 C.
C.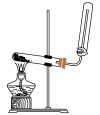 D.
D. 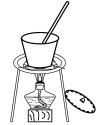
③步骤iv中标准NaOH溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有___________ 。
(1)德国化学家韦勒(F. Wohler)首次在实验室里用无机物合成了尿素[CO(NH2)2],打破了无机物和有机物之间的界限。尿素分子中σ键和π键个数之比为
(2)二十世纪初,工业上以CO2和NH3为原料在一定温度和压强下合成尿素。反应分为两步:ⅰ.CO2和NH3生成H2NCOONH4;ⅱ。H2NCOONH4分解生成尿素。

结合反应过程中能量变化示意图,下列说法正确的是
a.活化能:反应ⅰ<反应ⅱ
b.CO2(l) +2NH3(l)= H2NCOONH4(l) △H=+(E2-E1)kJ/mol
c. H2NCOONH4(l)=CO(NH2)2(l)+ H2O(1) △H=+(E3- E4)kJ/mol
d.对反应体系加热,可加快反应速率和提高尿素的产率
(3)近年研究发现,电催化CO2和含氮物质(
 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通入CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示(阴、阳极区溶液均为KNO3溶液)。
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通入CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示(阴、阳极区溶液均为KNO3溶液)。
①电解池中电极X应接直流电源的
②电解过程中生成尿素的电极反应式是
(4)尿素样品含氮量的测定方法如下。
已知:溶液中c(
 )不能直接用NaOH溶液准确滴定。
)不能直接用NaOH溶液准确滴定。
①消化液中的含氮粒子是
②下列装置,可以完成蒸馏操作的是
A.
 B.
B.  C.
C. D.
D. 
③步骤iv中标准NaOH溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】过渡金属及其化合物在生产生活中有着广泛应用。回答下列问题:
(1)铂可溶于王水(浓盐酸和浓硝酸按体积比为3∶1组成的混合物),王水中含有亚硝酰氯(NOCl)。NOCl分子中各原子满足8电子稳定结构。基态氮原子的外围电子排布图为___________ ,NOCl分子中 键和
键和 键的个数比为
键的个数比为___________ 。
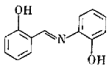
(2)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与 形成黄色的配合物。锰试剂的结构如图所示,锰试剂分子中原子采取的杂化方式有
形成黄色的配合物。锰试剂的结构如图所示,锰试剂分子中原子采取的杂化方式有___________ (填“sp”、“ ”或“
”或“ ”)杂化,锰试剂
”)杂化,锰试剂___________ (填“能”或“不能”)形成分子内氢键。
(3)EAN规则指的是配合物中心原子价电子数和配体提供的电子数之和为18,符合EAN规则的配合物分
子结构和化学性质都较稳定。已知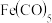 和
和 ,均符合EAN规则,性质稳定,而
,均符合EAN规则,性质稳定,而 在化学反应中表现氧化性。
在化学反应中表现氧化性。
①
___________ 。
②结合上述信息解释 在化学反应中表现氧化性的原因:
在化学反应中表现氧化性的原因:___________ 。
(4)氙的一种配合物六氟合铂酸氙,其化学式为 ,不溶于
,不溶于 等非极性溶剂,且加热熔化可产生
等非极性溶剂,且加热熔化可产生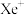 和
和 两种离子。据此可确定
两种离子。据此可确定 中化学键的类型为
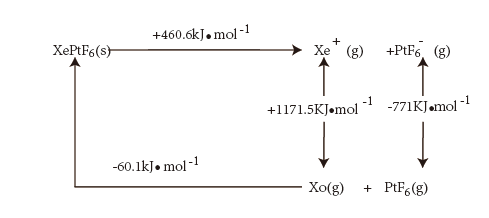
中化学键的类型为___________ 。利用如图born-Habe循环计算得到Xe(g)和 (g)合成
(g)合成 (s)的反应热。Xe原子的第一电离能为
(s)的反应热。Xe原子的第一电离能为___________  ,
, (s)的晶格能为
(s)的晶格能为___________  。
。
(5)在金属铜表面覆盖WBN型氮化硼(熔点为2967 )也可以达到金属铜的防腐目的,已知WBN型氮化硼晶体为六方晶系,其结构单元如图所示。
)也可以达到金属铜的防腐目的,已知WBN型氮化硼晶体为六方晶系,其结构单元如图所示。

①WBN型氮化硼晶体中N原子的配位数为___________ 。
②已知阿伏加德罗常数的值为 ,则WBN型氮化硼的密度为
,则WBN型氮化硼的密度为___________ 。
(1)铂可溶于王水(浓盐酸和浓硝酸按体积比为3∶1组成的混合物),王水中含有亚硝酰氯(NOCl)。NOCl分子中各原子满足8电子稳定结构。基态氮原子的外围电子排布图为
 键和
键和 键的个数比为
键的个数比为(2)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与
 形成黄色的配合物。锰试剂的结构如图所示,锰试剂分子中原子采取的杂化方式有
形成黄色的配合物。锰试剂的结构如图所示,锰试剂分子中原子采取的杂化方式有 ”或“
”或“ ”)杂化,锰试剂
”)杂化,锰试剂
(3)EAN规则指的是配合物中心原子价电子数和配体提供的电子数之和为18,符合EAN规则的配合物分
子结构和化学性质都较稳定。已知
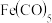 和
和 ,均符合EAN规则,性质稳定,而
,均符合EAN规则,性质稳定,而 在化学反应中表现氧化性。
在化学反应中表现氧化性。①

②结合上述信息解释
 在化学反应中表现氧化性的原因:
在化学反应中表现氧化性的原因:(4)氙的一种配合物六氟合铂酸氙,其化学式为
 ,不溶于
,不溶于 等非极性溶剂,且加热熔化可产生
等非极性溶剂,且加热熔化可产生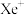 和
和 两种离子。据此可确定
两种离子。据此可确定 中化学键的类型为
中化学键的类型为 (g)合成
(g)合成 (s)的反应热。Xe原子的第一电离能为
(s)的反应热。Xe原子的第一电离能为 ,
, (s)的晶格能为
(s)的晶格能为 。
。
(5)在金属铜表面覆盖WBN型氮化硼(熔点为2967
 )也可以达到金属铜的防腐目的,已知WBN型氮化硼晶体为六方晶系,其结构单元如图所示。
)也可以达到金属铜的防腐目的,已知WBN型氮化硼晶体为六方晶系,其结构单元如图所示。
①WBN型氮化硼晶体中N原子的配位数为
②已知阿伏加德罗常数的值为
 ,则WBN型氮化硼的密度为
,则WBN型氮化硼的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】铝的单质、合金及其化合物在生产、生活中具有广泛的应用。
(1)Al属于周期表中_______ 区元素,其基态原子核外具有_______ 种空间运动状态不同的电子。
(2)与Al位于同一周期,且第一电离能比Al小的元素有_______ (填元素符号)。
(3)一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键;如果两个成键元素间的电负性差值小于1.7,它们之间通常形成共价键。部分主族元素的电负性如下表所示:
下列含铝化合物属于离子化合物的是_______(填标号)。
(4)Al的熔点为660℃,Ga的熔点为29.76℃,Al的熔点更高的原因为_______ 。
(5)三甲基铝(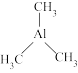 )是一种金属有机化合物,可作烯烃聚合催化剂、引火燃料。
)是一种金属有机化合物,可作烯烃聚合催化剂、引火燃料。
①三甲基铝分子中C原子的VSEPR模型为_______ ,Al原子的杂化轨道类型为_______ 。
②该物质可与胺类(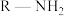 ,R表示烃基)结合,原因是
,R表示烃基)结合,原因是_______ 。
(6)X-射线衍射实验表明,合金Cr-Al晶体(有序)属四方晶系,其晶胞参数如图所示,晶胞棱边夹角均为90°。
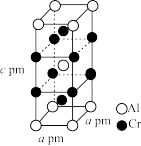
①该合鑫Cr-Al晶体的化学式为_______ 。
②用NA表示阿伏加德罗常数的值,则合金Cr-Al晶体的密度为_______  (写出计算式即可,不要求化简)。
(写出计算式即可,不要求化简)。
(1)Al属于周期表中
(2)与Al位于同一周期,且第一电离能比Al小的元素有
(3)一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键;如果两个成键元素间的电负性差值小于1.7,它们之间通常形成共价键。部分主族元素的电负性如下表所示:
| 5 B 2.0 | 6 C 2.5 | 7 N 3.0 | 8 O 3.5 | 9 F 4.0 |
| 13 Al 1.5 | 14 Si 1.8 | 15 P 2.1 | 16 S 2.5 | 17 Cl 3.0 |
| 31 Ga 1.6 | 32 Ge 1.8 | 33 As 2.0 | 34 Se 2.4 | 35 Br 2.8 |
A. | B. | C. | D.AlP |
(5)三甲基铝(
 )是一种金属有机化合物,可作烯烃聚合催化剂、引火燃料。
)是一种金属有机化合物,可作烯烃聚合催化剂、引火燃料。①三甲基铝分子中C原子的VSEPR模型为
②该物质可与胺类(
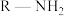 ,R表示烃基)结合,原因是
,R表示烃基)结合,原因是(6)X-射线衍射实验表明,合金Cr-Al晶体(有序)属四方晶系,其晶胞参数如图所示,晶胞棱边夹角均为90°。

①该合鑫Cr-Al晶体的化学式为
②用NA表示阿伏加德罗常数的值,则合金Cr-Al晶体的密度为
 (写出计算式即可,不要求化简)。
(写出计算式即可,不要求化简)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】2019年10月9日消息,诺贝尔化学奖颁给约翰●B.古迪纳夫、M●斯坦利●威廷汉和吉野彰,以表彰他们“开发锂离子电池”的贡献。磷酸亚铁锂(化学式:LiFePO4)是锂离子电池电极材料,主要用于动力锂离子电池,作为正极活性物质使用,人们习惯也称其为磷酸铁锂。
(1)基态锂原子核外能量最高的电子电子云轮廓图形状为__ ;基态磷原子第一电离能比基态硫的__ (填“大”或“小”),原因是__ 。
(2)实验室中可用KSCN或K4[Fe(CN)6]来检验Fe3+。FeCl3与KSCN溶液混合,可得到配位数为5的配合物的化学式是__ ,其中硫、碳的杂化类型分别是__ 、__ 。
(3)磷酸和亚磷酸(H3PO3)是磷元素的两种含氧酸。PO43-的空间构型为__ ;亚磷酸与NaOH反应只生成Na2HPO3和NaH2PO3两种盐,则H3PO3的结构式为__ 。
(4)磷酸分子间脱水可生成多磷酸,其某一钙盐的结构如图所示:
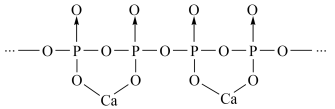
由图推知该多磷酸钙盐的通式为__ 。
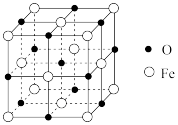
(5)氧化亚铁晶体的晶胞如图所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加 德罗常数的值。在该晶胞中,与O2-紧邻且等距离的Fe2+数目为__ ,Fe2+与O2-最短核间距为___ pm。
(1)基态锂原子核外能量最高的电子电子云轮廓图形状为
(2)实验室中可用KSCN或K4[Fe(CN)6]来检验Fe3+。FeCl3与KSCN溶液混合,可得到配位数为5的配合物的化学式是
(3)磷酸和亚磷酸(H3PO3)是磷元素的两种含氧酸。PO43-的空间构型为
(4)磷酸分子间脱水可生成多磷酸,其某一钙盐的结构如图所示:

由图推知该多磷酸钙盐的通式为
(5)氧化亚铁晶体的晶胞如图所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加 德罗常数的值。在该晶胞中,与O2-紧邻且等距离的Fe2+数目为

您最近一年使用:0次



