关于反应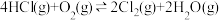
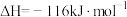 ,下列说法正确的是
,下列说法正确的是
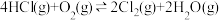
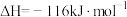 ,下列说法正确的是
,下列说法正确的是| A.断裂4 mol H−Cl键的同时,有4 mol H−O键生成,说明该反应达到平衡状态 |
| B.反应活化能:Ea(正)>Ea(逆) |
| C.每生成22.4 LCl2,放出58 kJ的热量 |
D.温度降低,平衡时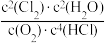 的值会增大 的值会增大 |
更新时间:2024-01-11 09:28:53
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】可逆反应H2(g)+I2(g) 2HI(g)达到平衡的标志是( )
2HI(g)达到平衡的标志是( )
 2HI(g)达到平衡的标志是( )
2HI(g)达到平衡的标志是( )| A.v(H2):v(HI)=1:2 |
| B.H2、I2、HI分子个数比为1:1:2 |
| C.混合气体中I2和H2的体积分数相等 |
| D.混合气体的颜色不再改变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】恒容容器中发生反应4HCl(g) + O2(g)  2H2O(g) + 2Cl2(g) ΔH<0,下列说法正确的是
2H2O(g) + 2Cl2(g) ΔH<0,下列说法正确的是
 2H2O(g) + 2Cl2(g) ΔH<0,下列说法正确的是
2H2O(g) + 2Cl2(g) ΔH<0,下列说法正确的是| A.各物质浓度不再发生变化,表明该反应达到平衡状态 |
| B.催化剂可以改变反应的焓变 |
C.该反应的平衡常数K=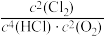 |
D.其他条件不变,增大 ,HCl的平衡转化率增大 ,HCl的平衡转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】可逆反应2NO2 (g) ⇌N2O4 (g) ΔH= −56.9 kJ·mol−1在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。某同学的部分实验报告如下。
下列说法不正确的是
| 1.向左侧烧杯中加入NH4NO3晶体,甲瓶的红棕色变浅。 2.向右侧烧杯中加入CaO固体,乙瓶的红棕色变深。 |
下列说法不正确的是
| A.甲瓶的红棕色变浅,说明平衡2NO2 (g)⇌N2O4 (g)向正反应方向移动 |
| B.可根据现象判断NH4NO3晶体溶于水吸热,CaO固体溶于水放热 |
| C.甲瓶中反应的化学平衡常数(K)增大 |
| D.乙瓶中由于反应的化学平衡常数(K)改变,使Qc<K,平衡发生移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在高温下,反应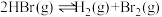
 ;要使混合气体颜色加深,下列不可采取的方法是
;要使混合气体颜色加深,下列不可采取的方法是
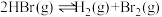
 ;要使混合气体颜色加深,下列不可采取的方法是
;要使混合气体颜色加深,下列不可采取的方法是| A.保持容积不变,加入HBr(g) | B.降低温度 |
| C.升高温度 | D.将容器的体积压缩到一半 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】法国化学家PaulSabatier较早提出可以利用工业废弃物CO2转化为CH4,其反应原理为CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) △H=-165kJ・mol-1。若在密闭容器中充入1molCO2、1mol H2引发该反应进行,下列说法正确的是
| A | B | C | D |
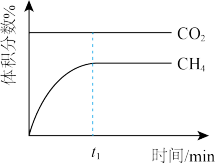 | 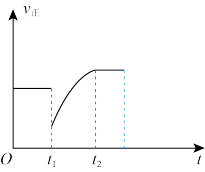 |  | 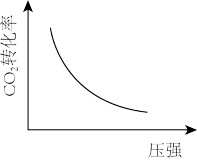 |
| 恒温恒容下,混合气体中CH4与CO2的体积分数变化 | 恒温恒压条件平衡后,t1时改变条件可能是充入少量N2 | 升高温度,平衡常数Kc的变化趋势 | CO2平衡转化率随压强的变化趋势 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知反应 达平衡时,
达平衡时,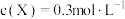 ,其他条件不变,若容器扩大到原来的2倍,再次达平衡时
,其他条件不变,若容器扩大到原来的2倍,再次达平衡时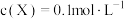 ,下列说法正确的是
,下列说法正确的是
 达平衡时,
达平衡时,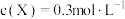 ,其他条件不变,若容器扩大到原来的2倍,再次达平衡时
,其他条件不变,若容器扩大到原来的2倍,再次达平衡时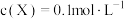 ,下列说法正确的是
,下列说法正确的是| A.反应向逆方向移动 | B. 可能是固体或液体 可能是固体或液体 |
C.系数 一定大于 一定大于 | D.再次平衡时,平衡常数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,在恒容密闭容器加入一定量水蒸气和足量的碳,发生反应:C(s)+H2O(g)  CO(g)+H2(g)。一段时间后,反应达到平衡状态。下列叙述正确的是
CO(g)+H2(g)。一段时间后,反应达到平衡状态。下列叙述正确的是
 CO(g)+H2(g)。一段时间后,反应达到平衡状态。下列叙述正确的是
CO(g)+H2(g)。一段时间后,反应达到平衡状态。下列叙述正确的是| A.移去部分C(s),水蒸气浓度不变 |
| B.再充入一定量H2O(g),水蒸气的转化率不变 |
| C.再充入一定量的N2(g),水蒸气的体积分数不变 |
D.升高温度, 值不变 值不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】某温度下,在恒容(2 L)密闭容器中发生反应:N2(g)+3H2(g)⇌2NH3(g)。甲、乙、丙三种情况下,起始充入N2和H2的物质的量如表所示,其中甲经2 min达平衡时,N2的转化率为50%。下列判断正确的是
| 起始物质的量mol | 甲 | 乙 | 丙 |
| n(N2) | 1 | 2 | 2 |
| n(H2) | 3 | 3 | 6 |
| A.容器中气体的密度可作为判断反应是否达到平衡状态的标志 |
| B.平衡时,乙中H2转化率大于50% |
| C.反应达平衡时,丙中H2的物质的量浓度c(H2)等于甲中的2倍 |
| D.甲、乙、丙三种条件下的化学平衡常数之间的关系为K甲<K乙<K丙 |
您最近一年使用:0次

 C(s)+2H2(g)
C(s)+2H2(g) 。下列有关判断正确的是
。下列有关判断正确的是


