按要求填空:
(1)若要在铁制品表面镀镍,电镀液用硫酸镍溶液,则镍应与电源的___________ 极相连,铁制应与电源的___________ 极相连。
(2)影响化学平衡移动的因素有___________ 、___________ 、___________ 。
(1)若要在铁制品表面镀镍,电镀液用硫酸镍溶液,则镍应与电源的
(2)影响化学平衡移动的因素有
更新时间:2024-01-24 16:45:11
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)相同温度时,向两个开始体积相同的容器中分别充入2molSO2和1molO2,甲容器保持恒压,乙容器保持恒容,达到平衡时:(填“大于“小于”“等于”)
反应速率v甲_____ v乙,SO2的转化率ω甲_____ ω乙,所需时间t甲____ t乙。
(2)在容积相同的两个密闭容器A和B中,保持温度为423K,若同时分别向A和B中加入amol和2amol的HI气体,待反应:2HI(g) H2(g)+I2(g)均达到平衡时:(填“大于“小于”“等于”)
H2(g)+I2(g)均达到平衡时:(填“大于“小于”“等于”)
I2的浓度c(I2)A____ c(I2)B;I2蒸气在混合气体中的体积分数A容器______ B容器。
反应速率v甲
(2)在容积相同的两个密闭容器A和B中,保持温度为423K,若同时分别向A和B中加入amol和2amol的HI气体,待反应:2HI(g)
 H2(g)+I2(g)均达到平衡时:(填“大于“小于”“等于”)
H2(g)+I2(g)均达到平衡时:(填“大于“小于”“等于”)I2的浓度c(I2)A
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率增大;当减小压强时,混合体系中C的质量分数也减小。
pC(g),达到平衡后,当升高温度时,B的转化率增大;当减小压强时,混合体系中C的质量分数也减小。
(1)该反应的逆反应为___________ 反应(填“吸热”或“放热”)。
(2)恒温压缩体积时,A的质量将___________ (填“增大”“减小”或“不变”,下同)。
(3)若恒容条件下加入B,则A的转化率___________ ,B的转化率___________ 。
(4)若升高温度,则平衡时B、C的浓度之比 将
将___________ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量___________ 。
 pC(g),达到平衡后,当升高温度时,B的转化率增大;当减小压强时,混合体系中C的质量分数也减小。
pC(g),达到平衡后,当升高温度时,B的转化率增大;当减小压强时,混合体系中C的质量分数也减小。(1)该反应的逆反应为
(2)恒温压缩体积时,A的质量将
(3)若恒容条件下加入B,则A的转化率
(4)若升高温度,则平衡时B、C的浓度之比
 将
将(5)若加入催化剂,平衡时气体混合物的总物质的量
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/[c(CH3OH)]2,该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44.
请回答下列问题:
(1)写出上述反应的化学方程式_____________________ .
(2)该反应的正反应是_________ 反应(填“放热”或者“吸热”)
(3)已知在密闭容器中,测得某时刻各组分的浓度如下:

①此时系统温度400℃,比较正、逆反应速率的大小:v正____ v逆(填“>”、“<”或“=”).
②若以甲醇百分含量为纵坐标,以温度为横坐标,此时反应点在图象的位置是图中____ 点.比较图中B、D两点所对应的正反应速率B___ D(填“>”、“<”或“=”).理由是__________________ .

(4)一定条件下要提高反应物的转化率,可以采用的措施是________
a.升高温度b.加入催化剂
c.压缩容器的体积d.增加水蒸气的浓度
e.及时分离出产物.
请回答下列问题:
(1)写出上述反应的化学方程式
(2)该反应的正反应是
(3)已知在密闭容器中,测得某时刻各组分的浓度如下:

①此时系统温度400℃,比较正、逆反应速率的大小:v正
②若以甲醇百分含量为纵坐标,以温度为横坐标,此时反应点在图象的位置是图中

(4)一定条件下要提高反应物的转化率,可以采用的措施是
a.升高温度b.加入催化剂
c.压缩容器的体积d.增加水蒸气的浓度
e.及时分离出产物.
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】下列四种装置中,①盛200 mL硫酸铜溶液 ②盛200 mL 0.01 mol·L-1硫酸溶液 ③盛200 mL氯化锌溶液 ④盛200 mL氯化钾溶液

(1)上述装置中①为___________ 池,反应一段时间溶液浓度基本不变的是___________ 。装置①中两电极的电极反应式分别是___________ 、___________ (注明电极名称)。
(2)用离子方程式回答:通电时装置④中的总反应是___________ 溶液中可能发生的副反应是___________ 。
(3)若将装置④中的外加电源拆去,用导线将两个电极连接,则Fe极上发生的反应是___________ 。

(1)上述装置中①为
(2)用离子方程式回答:通电时装置④中的总反应是
(3)若将装置④中的外加电源拆去,用导线将两个电极连接,则Fe极上发生的反应是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】用下图所示的装置进行电解。通电一会儿,发现湿润的淀粉KI试纸的C端变为蓝色。

(1)A中发生反应的化学方程式为_________________________________ 。
(2)在B中观察到的现象是______________________________________ 。
(3)室温下,若从电解开始到时间ts,A、B装置中共收集到气体0.168 L(标准状况),若电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为1000 mL,则A溶液的pH为______________________________________ 。

(1)A中发生反应的化学方程式为
(2)在B中观察到的现象是
(3)室温下,若从电解开始到时间ts,A、B装置中共收集到气体0.168 L(标准状况),若电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为1000 mL,则A溶液的pH为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为___________ 。
②Y电极上的电极反应式为___________
③该反应的总反应离子方程式是:___________ 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是___________ ,
②Y电极的材料是___________
(3)如要用电镀方法铁上镀铜,电解液a选用CuSO4溶液,则:
①X电极的材料是___________ ,电极反应式是___________ 。
②Y电极的材料是___________ ,电极反应式是___________ 。

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为
②Y电极上的电极反应式为
③该反应的总反应离子方程式是:
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是
②Y电极的材料是
(3)如要用电镀方法铁上镀铜,电解液a选用CuSO4溶液,则:
①X电极的材料是
②Y电极的材料是
您最近一年使用:0次
【推荐2】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一
(1)如图装置中,U形管内为红墨水,a、b试管内分别盛有氯化铵溶液(显酸性)和食盐水,各加入生铁块,放置一段时间均被腐蚀。
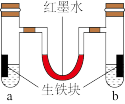
①红墨水柱两边的液面变为左低右高,则_______ (填“a”或“b”)试管内盛有食盐水。
②a试管中铁发生的是_______ (填“析氢”或“吸氧”)腐蚀,生铁中碳上发生的电极反应式为_______ 。
(2)钢铁表面常电镀一层铬(Cr)达到防腐蚀的目的,这是由于铬具有优良的抗腐蚀性能。电镀时,把待镀的金属制品与直流电源的_______ 极(填“正”或“负”)相连,把镀层金属铬作_______ 极(填“阳”或“阴”)。电镀铬时,不能用含有CrO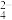 或Cr2O
或Cr2O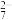 的溶液作电镀液,原因是
的溶液作电镀液,原因是_______ (用电极反应式表明原因)。
(3)利用如图装置,可以模拟铁的电化学保护。
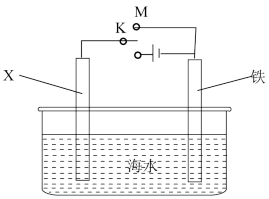
若X为碳棒,为减缓铁的腐蚀,开关K应置于N处,该电化学保护法称为_______ 若X为锌,开关K置于M处,铁棒上发生的电极反应式_______
(1)如图装置中,U形管内为红墨水,a、b试管内分别盛有氯化铵溶液(显酸性)和食盐水,各加入生铁块,放置一段时间均被腐蚀。

①红墨水柱两边的液面变为左低右高,则
②a试管中铁发生的是
(2)钢铁表面常电镀一层铬(Cr)达到防腐蚀的目的,这是由于铬具有优良的抗腐蚀性能。电镀时,把待镀的金属制品与直流电源的
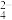 或Cr2O
或Cr2O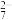 的溶液作电镀液,原因是
的溶液作电镀液,原因是(3)利用如图装置,可以模拟铁的电化学保护。

若X为碳棒,为减缓铁的腐蚀,开关K应置于N处,该电化学保护法称为
您最近一年使用:0次

 氯气参与反应时,转移电子数为
氯气参与反应时,转移电子数为

