油气开采、煤化工等行业的硫化氢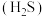 废气转化为
废气转化为 (熔点
(熔点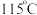 )是资源利用和环境保护的重要研究课题。
)是资源利用和环境保护的重要研究课题。

Ⅰ.高温热分解法: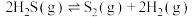
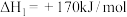
(1) 分解所得
分解所得 ,在低温高压时和氢气反应得到一种新型超导材料(晶胞如图-1所示)。该物质化学式为
,在低温高压时和氢气反应得到一种新型超导材料(晶胞如图-1所示)。该物质化学式为_______ 。
Ⅱ.克劳斯法: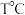 时,
时,
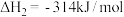
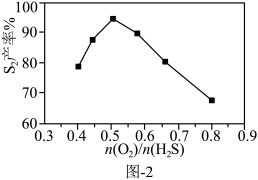
(2)其他条件不变时,相同时间内 的产率随
的产率随 值的变化如图-2所示。当
值的变化如图-2所示。当 时,
时, 产率随
产率随 值增大而减小的可能原因是
值增大而减小的可能原因是_______ 。
Ⅲ.用 脱除法。
脱除法。
(3)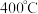 时,将
时,将 和
和 混合气体以一定流速通过装有
混合气体以一定流速通过装有 脱硫剂的反应器,得到
脱硫剂的反应器,得到 和
和 。
。
①该反应的化学方程式为_______ 。
②取反应后的固体,在 的混合气体中加热再生,
的混合气体中加热再生, 随温度变化的曲线如图-3所示。在
随温度变化的曲线如图-3所示。在 范围内,固体质量减小的主要原因:(ⅰ)
范围内,固体质量减小的主要原因:(ⅰ) 和
和 被氧化成
被氧化成 ;(ⅱ)
;(ⅱ)_______ 。

Ⅳ.电化学脱除法
(4)我国科学家设计了 协同转化装置(右侧电解质溶液中含有
协同转化装置(右侧电解质溶液中含有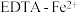 ),实现对天然气中
),实现对天然气中 和
和 的高效去除,工作原理如图-4所示。
的高效去除,工作原理如图-4所示。

①电极 上发生的电极式为
上发生的电极式为_______ 。
②在图-4中,图右侧的反应可描述为_______ 。
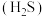 废气转化为
废气转化为 (熔点
(熔点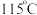 )是资源利用和环境保护的重要研究课题。
)是资源利用和环境保护的重要研究课题。
Ⅰ.高温热分解法:
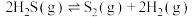
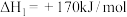
(1)
 分解所得
分解所得 ,在低温高压时和氢气反应得到一种新型超导材料(晶胞如图-1所示)。该物质化学式为
,在低温高压时和氢气反应得到一种新型超导材料(晶胞如图-1所示)。该物质化学式为Ⅱ.克劳斯法:
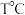 时,
时,
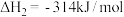
(2)其他条件不变时,相同时间内
 的产率随
的产率随 值的变化如图-2所示。当
值的变化如图-2所示。当 时,
时, 产率随
产率随 值增大而减小的可能原因是
值增大而减小的可能原因是
Ⅲ.用
 脱除法。
脱除法。(3)
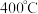 时,将
时,将 和
和 混合气体以一定流速通过装有
混合气体以一定流速通过装有 脱硫剂的反应器,得到
脱硫剂的反应器,得到 和
和 。
。①该反应的化学方程式为
②取反应后的固体,在
 的混合气体中加热再生,
的混合气体中加热再生, 随温度变化的曲线如图-3所示。在
随温度变化的曲线如图-3所示。在 范围内,固体质量减小的主要原因:(ⅰ)
范围内,固体质量减小的主要原因:(ⅰ) 和
和 被氧化成
被氧化成 ;(ⅱ)
;(ⅱ)
Ⅳ.电化学脱除法
(4)我国科学家设计了
 协同转化装置(右侧电解质溶液中含有
协同转化装置(右侧电解质溶液中含有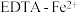 ),实现对天然气中
),实现对天然气中 和
和 的高效去除,工作原理如图-4所示。
的高效去除,工作原理如图-4所示。
①电极
 上发生的电极式为
上发生的电极式为②在图-4中,图右侧的反应可描述为
更新时间:2024-01-31 19:29:03
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】以方潜矿(PbS)为原料制备铅蓄电池的电极材料的工艺流程如图所示:
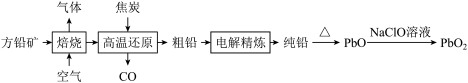
部分化合物的Ksp如下表所示:
请回答下列问题:
(1)“焙烧”生成的气体可用于工业制备____________ 。
(2)写出“高温还原”的主要化学方程式:____________ 。
(3)“粗铅”的杂质主要有锌,铁,铜,银等,电解精炼时阴极反应式为____________ 。阳极泥的主要成分为____________ 。
(4)铅与稀盐酸反应产生少量气泡后反应终止,原因是____________ 。写出制备PbO2的离子方程式:____________ 。
(5)Pb(NO3)2是强酸弱碱盐,氢硫酸(H2S)是弱酸,向Pb(NO3)2溶液中通入H2S气体是否能产生黑色PbS沉淀____________ ?(列式计算说明,Ka1(H2S)=1.3×10-7,Ka2(H2S)=7.1×10-15)。
(6)将PbCrO4加入足量硝酸中,部分振荡,观察到主要现象是____________ ,反应的离子方程式为____________ 。

部分化合物的Ksp如下表所示:
| 物质 | PbCl2 | PbS | PbCrO4 |
| Ksp | 1.2×10-5 | 9.0×10-29 | 1.8×10-14 |
请回答下列问题:
(1)“焙烧”生成的气体可用于工业制备
(2)写出“高温还原”的主要化学方程式:
(3)“粗铅”的杂质主要有锌,铁,铜,银等,电解精炼时阴极反应式为
(4)铅与稀盐酸反应产生少量气泡后反应终止,原因是
(5)Pb(NO3)2是强酸弱碱盐,氢硫酸(H2S)是弱酸,向Pb(NO3)2溶液中通入H2S气体是否能产生黑色PbS沉淀
(6)将PbCrO4加入足量硝酸中,部分振荡,观察到主要现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】锡及其化合物在生产、生活中有着重要的用途。工业上SnSO4是一种重要的可溶性硫酸盐,广泛应用于镀锡工业,其制备路线如下:
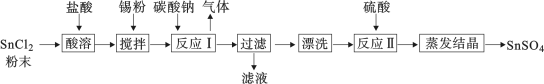
已知:酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化,SnCl2易水解生成碱式氯化亚锡[Sn(OH)Cl],SnCl4极易水解、熔点为−33 ℃、沸点为114 ℃。请按要求回答下列相关问题:
(1)写出SnCl4的电子式_______ 。
(2)SnCl2粉末需加浓盐酸进行溶解,请结合相关反应方程式解释原因_______ 。
(3)加入Sn粉的作用有两个:a.调节溶液pH;b_______
(4)反应I生成的沉淀为SnO,写出该反应的化学方程式_______
(5)检验沉淀已经“漂洗”干净的方法_______
(6)酸性条件下,SnSO4还可以用作双氧水去除剂,请写出发生反应的离子方程式_______

已知:酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化,SnCl2易水解生成碱式氯化亚锡[Sn(OH)Cl],SnCl4极易水解、熔点为−33 ℃、沸点为114 ℃。请按要求回答下列相关问题:
(1)写出SnCl4的电子式
(2)SnCl2粉末需加浓盐酸进行溶解,请结合相关反应方程式解释原因
(3)加入Sn粉的作用有两个:a.调节溶液pH;b
(4)反应I生成的沉淀为SnO,写出该反应的化学方程式
(5)检验沉淀已经“漂洗”干净的方法
(6)酸性条件下,SnSO4还可以用作双氧水去除剂,请写出发生反应的离子方程式
您最近一年使用:0次
【推荐3】李克强总理在十二届全国人大五次会议上作政府工作报告时强调,坚决打好蓝天保卫战。今年二氧化硫、氮氧化物排放量要分别下降3%,重点地区细颗粒物(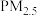 )浓度明显下降。其中二氧化硫、氮氧化物等的排放与工业燃烧煤、石油等化石燃料有很大的关系,所以对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
)浓度明显下降。其中二氧化硫、氮氧化物等的排放与工业燃烧煤、石油等化石燃料有很大的关系,所以对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
I.脱硝:
(1)催化剂存在下, 还原
还原 生成水蒸气和另一种无毒气体的化学方程式为
生成水蒸气和另一种无毒气体的化学方程式为_______
II.脱碳:一定条件下 会和
会和 反应合成
反应合成 。方程式为:
。方程式为: 。现向
。现向 恒容密闭容器中加入
恒容密闭容器中加入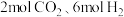 ,在恒温下发生反应。后反应达到平衡,此时容器内
,在恒温下发生反应。后反应达到平衡,此时容器内 的浓度为
的浓度为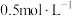 ,请回答以下问题:
,请回答以下问题:
(2)前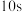 内的平均反应速率
内的平均反应速率
_______ 。
(3)下列叙述能说明原反应达到平衡状态的是_______ 。
a.单位时间内消耗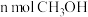 的同时生成
的同时生成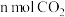
b.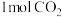 生成的同时有
生成的同时有 键断裂
键断裂
c. 和
和 的浓度保持不变
的浓度保持不变
d.容器内压强保持不变
e. 和
和 的物质的量之比保持不变
的物质的量之比保持不变
III.脱硫:燃煤的烟气脱硫技术是当前应用最广、效率最高的脱硫技术。其更多的是利用碱溶液与烟道气相遇,烟道气中 溶解在水中,形成一种稀酸溶液,然后与
溶解在水中,形成一种稀酸溶液,然后与 浊液等发生中和反应。
浊液等发生中和反应。
(4)已知中和反应为常见的放热反应,下列有关反应放热、吸热的说法正确的是_______
a.可燃物燃烧一般都需要加热,所以都是吸热反应
b.化学键的断裂要吸收能量
c.当反应物的总能量低于生成物的总能量时,据能量守恒定律可知反应会放热
d.已知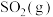 与
与 反应生成
反应生成 为放热反应,则
为放热反应,则 分解生成
分解生成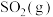 与
与 的反应为吸热反应
的反应为吸热反应
(5)请写出脱硫过程发生的主要化学方程式:_______
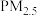 )浓度明显下降。其中二氧化硫、氮氧化物等的排放与工业燃烧煤、石油等化石燃料有很大的关系,所以对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
)浓度明显下降。其中二氧化硫、氮氧化物等的排放与工业燃烧煤、石油等化石燃料有很大的关系,所以对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。I.脱硝:
(1)催化剂存在下,
 还原
还原 生成水蒸气和另一种无毒气体的化学方程式为
生成水蒸气和另一种无毒气体的化学方程式为II.脱碳:一定条件下
 会和
会和 反应合成
反应合成 。方程式为:
。方程式为: 。现向
。现向 恒容密闭容器中加入
恒容密闭容器中加入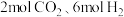 ,在恒温下发生反应。后反应达到平衡,此时容器内
,在恒温下发生反应。后反应达到平衡,此时容器内 的浓度为
的浓度为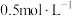 ,请回答以下问题:
,请回答以下问题:(2)前
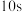 内的平均反应速率
内的平均反应速率
(3)下列叙述能说明原反应达到平衡状态的是
a.单位时间内消耗
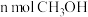 的同时生成
的同时生成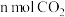
b.
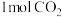 生成的同时有
生成的同时有 键断裂
键断裂c.
 和
和 的浓度保持不变
的浓度保持不变d.容器内压强保持不变
e.
 和
和 的物质的量之比保持不变
的物质的量之比保持不变III.脱硫:燃煤的烟气脱硫技术是当前应用最广、效率最高的脱硫技术。其更多的是利用碱溶液与烟道气相遇,烟道气中
 溶解在水中,形成一种稀酸溶液,然后与
溶解在水中,形成一种稀酸溶液,然后与 浊液等发生中和反应。
浊液等发生中和反应。(4)已知中和反应为常见的放热反应,下列有关反应放热、吸热的说法正确的是
a.可燃物燃烧一般都需要加热,所以都是吸热反应
b.化学键的断裂要吸收能量
c.当反应物的总能量低于生成物的总能量时,据能量守恒定律可知反应会放热
d.已知
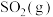 与
与 反应生成
反应生成 为放热反应,则
为放热反应,则 分解生成
分解生成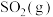 与
与 的反应为吸热反应
的反应为吸热反应(5)请写出脱硫过程发生的主要化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】氮及其化合物在生产、生活中具有广泛的应用。
(1)已知一定条件下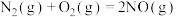
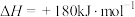 。1mol
。1mol 分子中的化学键断裂时需吸收498kJ的能量,1molNO分子中的化学键断裂时需吸收632kJ的能量。则
分子中的化学键断裂时需吸收498kJ的能量,1molNO分子中的化学键断裂时需吸收632kJ的能量。则 的键能为
的键能为___________ 。
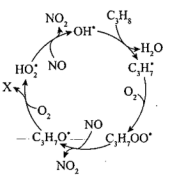
(2)某些过氧由基可以将NO氧化为 ,其反应机理如图所示(标*的为自由基)。X的分子式为
,其反应机理如图所示(标*的为自由基)。X的分子式为___________ ,总反应的化学方程式为___________ 。
(3)反应 的速率方程可表示为
的速率方程可表示为 ,其中k是与温度有关的常数,实验测得反应在650K时的数据如表:
,其中k是与温度有关的常数,实验测得反应在650K时的数据如表:
根据表中数据计算,
___________ ,
___________ 。温度为650K时该反应的速率常数
___________ 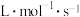 。
。
(4) 储存还原技术法(NSR)利用催化剂消除汽车尾气中的
储存还原技术法(NSR)利用催化剂消除汽车尾气中的 ,反应的化学方程式:
,反应的化学方程式: 。在一定温度下,向2L恒容密闭容器中充入等物质的S的NO和CO模拟NSR反应,在有催化剂和无催化剂条件下测得c(NO)随时间变化的曲线如图所示:
。在一定温度下,向2L恒容密闭容器中充入等物质的S的NO和CO模拟NSR反应,在有催化剂和无催化剂条件下测得c(NO)随时间变化的曲线如图所示:
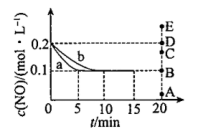
①曲线a和b中,表示在该温度下使用NSR催化技术的是曲线___________ 。
②曲线b表示的反应前10min内CO的平均反应速率
___________  。
。
③若保持其他条件不变,15min时将容器的体积压缩至1L,20min时反应重新达到平衡,NO的物质的量浓度对应的点可能是___________ 点。
(1)已知一定条件下
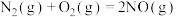
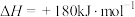 。1mol
。1mol 分子中的化学键断裂时需吸收498kJ的能量,1molNO分子中的化学键断裂时需吸收632kJ的能量。则
分子中的化学键断裂时需吸收498kJ的能量,1molNO分子中的化学键断裂时需吸收632kJ的能量。则 的键能为
的键能为(2)某些过氧由基可以将NO氧化为
 ,其反应机理如图所示(标*的为自由基)。X的分子式为
,其反应机理如图所示(标*的为自由基)。X的分子式为
(3)反应
 的速率方程可表示为
的速率方程可表示为 ,其中k是与温度有关的常数,实验测得反应在650K时的数据如表:
,其中k是与温度有关的常数,实验测得反应在650K时的数据如表:| 实验编号 | 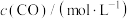 | 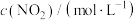 | 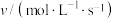 |
| ① | 0.025 | 0.040 | 2.2×10-4 |
| ② | 0.050 | 0.040 | 4.4×10-4 |
| ③ | 0.025 | 0.120 | 6.6×10-4 |



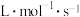 。
。(4)
 储存还原技术法(NSR)利用催化剂消除汽车尾气中的
储存还原技术法(NSR)利用催化剂消除汽车尾气中的 ,反应的化学方程式:
,反应的化学方程式: 。在一定温度下,向2L恒容密闭容器中充入等物质的S的NO和CO模拟NSR反应,在有催化剂和无催化剂条件下测得c(NO)随时间变化的曲线如图所示:
。在一定温度下,向2L恒容密闭容器中充入等物质的S的NO和CO模拟NSR反应,在有催化剂和无催化剂条件下测得c(NO)随时间变化的曲线如图所示:
①曲线a和b中,表示在该温度下使用NSR催化技术的是曲线
②曲线b表示的反应前10min内CO的平均反应速率

 。
。③若保持其他条件不变,15min时将容器的体积压缩至1L,20min时反应重新达到平衡,NO的物质的量浓度对应的点可能是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】I.某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白。

(1)该反应的化学方程式为_______ 。
(2)反应开始至2 min,气体Z的平均反应速率
_______ 。
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的_______ 倍。
②若容器内温度升高,X的转化率减小,则该反应的正反应为_______ (填“放热”或“吸热”)反应。
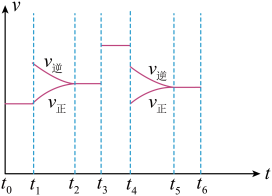
(4)上述反应在 内反应速率与时间图像如图所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是_______(填字母)。
内反应速率与时间图像如图所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是_______(填字母)。
Ⅱ.电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。

(5)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择_______ (填字母序号)。
A.碳棒 B.锌板 C.铜板
(6)图2中,钢闸门C做_______ 极。用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极反应式为_______ ,检测该电极反应产物的方法是_______ 。

(1)该反应的化学方程式为
(2)反应开始至2 min,气体Z的平均反应速率

(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的
②若容器内温度升高,X的转化率减小,则该反应的正反应为
(4)上述反应在
 内反应速率与时间图像如图所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是_______(填字母)。
内反应速率与时间图像如图所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是_______(填字母)。
A.在 时增大了压强 时增大了压强 | B.在 时加入催化剂 时加入催化剂 |
C.在 时降低了温度 时降低了温度 | D. 时X的转化率最高 时X的转化率最高 |
Ⅱ.电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。

(5)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择
A.碳棒 B.锌板 C.铜板
(6)图2中,钢闸门C做
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】完成下列问题。
I.
(1)丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
①C4H10(g)=C4H8(g)+H2(g) ΔH1
②已知:②C4H10(g)+ O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
③H2(g)+ O2(g)=H2O(g) ΔH3=-242 kJ·mol-1
O2(g)=H2O(g) ΔH3=-242 kJ·mol-1
反应①的ΔH1为___________ 。
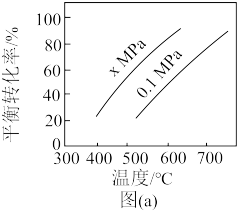
图(a)是反应①平衡转化率与反应温度及压强的关系图,x___________ (填“大于”或“小于”)0.1;欲使丁烯的平衡产率提高,应采取的措施是___________ (填标号)。
a.升高温度 B.降低温度 C.增大压强 D.降低压强
II.亚硝酰氯(NOCl)可由NO与Cl2反应得到,化学方程式为2NO(g)+Cl2(g)⇌2NOCl(g)。
(2)在一定温度下,该反应于一恒容密闭容器中达到平衡,继续通入Cl2,逆反应速率_______ (填“增大”“减小”或“不变”)。
(3)在10 L的恒容密闭容器中充入2 mol NO(g)和1 molCl2(g),在不同温度下测得c(NOCl)与时间的关系如下图:
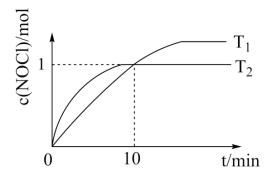
该反应的ΔH___________ (填“>”“<”或“=”)0,从反应开始到10 min时NO的平均反应速率v(NO)=______ 。T2时该反应的平衡常数K=_______ 。
I.
(1)丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
①C4H10(g)=C4H8(g)+H2(g) ΔH1
②已知:②C4H10(g)+
 O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1③H2(g)+
 O2(g)=H2O(g) ΔH3=-242 kJ·mol-1
O2(g)=H2O(g) ΔH3=-242 kJ·mol-1反应①的ΔH1为
图(a)是反应①平衡转化率与反应温度及压强的关系图,x
a.升高温度 B.降低温度 C.增大压强 D.降低压强

II.亚硝酰氯(NOCl)可由NO与Cl2反应得到,化学方程式为2NO(g)+Cl2(g)⇌2NOCl(g)。
(2)在一定温度下,该反应于一恒容密闭容器中达到平衡,继续通入Cl2,逆反应速率
(3)在10 L的恒容密闭容器中充入2 mol NO(g)和1 molCl2(g),在不同温度下测得c(NOCl)与时间的关系如下图:

该反应的ΔH
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】天然气的主要成分为CH4,还含有C2H6等烃类,是重要的燃料和化工原料。
(1)乙烷在一定条件可发生如下反应:C2H6(g) C2H4(g)+H2(g)ΔH,相关物质的燃烧热数据如下表所示:
C2H4(g)+H2(g)ΔH,相关物质的燃烧热数据如下表所示:
①ΔH=___________ kJ•mol-1。
②提高该反应平衡转化率的方法有___________ 、___________ 。
(2)密闭容器中通入等物质的量的乙烷和氢气,在等温等压下(p)发生上述反应C2H6(g) C2H4(g)+H2(g)。
C2H4(g)+H2(g)。
①可判断该反应达平衡的标志为___________ (填选项字母)。
A.容器内混合气体的密度恒定
B.容器内混合气体的压强恒定
C.容器内乙烷和氢气的物质的量之比恒定
D.生成乙烯的速率和乙烷消耗的速率相等
②如果乙烷的平衡转化率为α,反应的平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)高温下,甲烷生成乙烷的反应如下:2CH4 C2H6+H2,反应在初期阶段的速率方程为:r=kc(CH4),其中k为反应速率常数,设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=
C2H6+H2,反应在初期阶段的速率方程为:r=kc(CH4),其中k为反应速率常数,设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=___________ r1。
(4)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:___________ 。
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH4和CO2体积比为___________ 。
(1)乙烷在一定条件可发生如下反应:C2H6(g)
 C2H4(g)+H2(g)ΔH,相关物质的燃烧热数据如下表所示:
C2H4(g)+H2(g)ΔH,相关物质的燃烧热数据如下表所示:| 物质 | C2H6(g) | C2H4(g) | H2(g) |
| 燃烧热ΔH/(kJ•mol-1) | —1560 | —1411 | —286 |
②提高该反应平衡转化率的方法有
(2)密闭容器中通入等物质的量的乙烷和氢气,在等温等压下(p)发生上述反应C2H6(g)
 C2H4(g)+H2(g)。
C2H4(g)+H2(g)。①可判断该反应达平衡的标志为
A.容器内混合气体的密度恒定
B.容器内混合气体的压强恒定
C.容器内乙烷和氢气的物质的量之比恒定
D.生成乙烯的速率和乙烷消耗的速率相等
②如果乙烷的平衡转化率为α,反应的平衡常数Kp=
(3)高温下,甲烷生成乙烷的反应如下:2CH4
 C2H6+H2,反应在初期阶段的速率方程为:r=kc(CH4),其中k为反应速率常数,设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=
C2H6+H2,反应在初期阶段的速率方程为:r=kc(CH4),其中k为反应速率常数,设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=(4)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
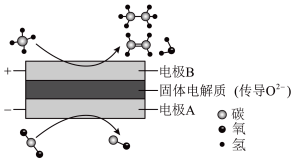
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH4和CO2体积比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表为长式周期表的一部分,其中的序号代表对应的元素。
(1)写出上表中元素⑨的三价离子的结构示意图_______ 。
(2)元素⑩的晶体中原子堆积方式是_______ ,晶体中原子的空间利用率是_______
(3)元素②的第二电离能_______ Na(填写“>”“=”或“<”)的第二电离能;元素⑨的氧化物MXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,若晶体中的M分别为M2﹢、M3﹢,此晶体中M2﹢与M3﹢的最简整数比为_______
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是_______ 。
(5)用惰性电极电解足量的由元素⑦与元素⑧形成的化合物的水溶液,写出电解反应的离子方程式为_______ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ |
(2)元素⑩的晶体中原子堆积方式是
(3)元素②的第二电离能
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是
(5)用惰性电极电解足量的由元素⑦与元素⑧形成的化合物的水溶液,写出电解反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】按要求完成下列方程式的书写:
(1)在实验室配制 溶液时,常滴加几滴
溶液时,常滴加几滴 溶液,试用离子方程式说明原因:
溶液,试用离子方程式说明原因:____ 。
(2)汽车发动机工作时会引发 和
和 反应,其能量变化示意图如下(常温常压下测定):
反应,其能量变化示意图如下(常温常压下测定):
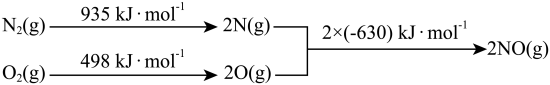
写出该反应的热化学方程式:_______________________ 。
(3)已知:常温下, 的电离常数
的电离常数 ;
; 的电离常数
的电离常数 ,
,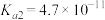 。向
。向 溶液中通入少量
溶液中通入少量 气体,则发生反应的离子方程式为
气体,则发生反应的离子方程式为_____________ 。
(4)用电解法处理含铬废水(主要成分 )时,以铁板作阴、阳极,处理过程中在电解质溶液中发生反应:
)时,以铁板作阴、阳极,处理过程中在电解质溶液中发生反应: ,最后
,最后 以
以 形式除去,则阳极的电极反应式为
形式除去,则阳极的电极反应式为_______________________ 。
(5)我国学者结合实验与计算机模拟结果,研究了丙烷在六方氮化硼催化剂表面氧化脱氢制丙烯的反应历程,部分历程如图所示,其中吸附在催化剂表面的物种用 标注。
标注。
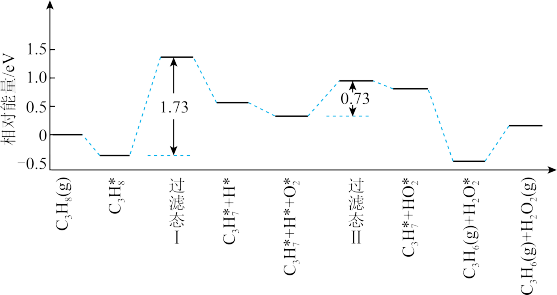
该历程中决速步骤对应的化学方程式为_______________________ 。
(1)在实验室配制
 溶液时,常滴加几滴
溶液时,常滴加几滴 溶液,试用离子方程式说明原因:
溶液,试用离子方程式说明原因:(2)汽车发动机工作时会引发
 和
和 反应,其能量变化示意图如下(常温常压下测定):
反应,其能量变化示意图如下(常温常压下测定):
写出该反应的热化学方程式:
(3)已知:常温下,
 的电离常数
的电离常数 ;
; 的电离常数
的电离常数 ,
,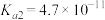 。向
。向 溶液中通入少量
溶液中通入少量 气体,则发生反应的离子方程式为
气体,则发生反应的离子方程式为(4)用电解法处理含铬废水(主要成分
 )时,以铁板作阴、阳极,处理过程中在电解质溶液中发生反应:
)时,以铁板作阴、阳极,处理过程中在电解质溶液中发生反应: ,最后
,最后 以
以 形式除去,则阳极的电极反应式为
形式除去,则阳极的电极反应式为(5)我国学者结合实验与计算机模拟结果,研究了丙烷在六方氮化硼催化剂表面氧化脱氢制丙烯的反应历程,部分历程如图所示,其中吸附在催化剂表面的物种用
 标注。
标注。
该历程中决速步骤对应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】不锈钢是由铁、铬、镍、碳及众多不同元素所组成的合金,铁是主要成分元素,铬是第一主要的合金元素。其中铬的含量不能低于11%,不然就不能生成致密氧化膜CrO3以防止腐蚀。
(1)基态碳原子的电子排布图为_______ 。
(2)铬和镍元素都易形成配位化合物:
①[Cr(H2O)4Cl2]Cl•2H2O中Cr3+的配位数为_______ 。
②硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是_______ ,在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为_______ 。
③氨是_______ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______ ,氨的沸点高于PH3,原因是_______ 。
(3)镍元素基态原子的价电子排布式为_______ ,3d能级上的未成对电子数为_______ 。
(4)单质铜及镍都是由金属键形成的晶体,元素铜与镍的第二电离能分别为:ICu=1958kJ/mol、INi=1753kJ/mol,ICu>INi的原因是_______ 。
(5)某镍白铜合金的立方晶胞结构如图所示。若合金的密度为dg/cm3,晶胞参数a=_______ cm。

(1)基态碳原子的电子排布图为
(2)铬和镍元素都易形成配位化合物:
①[Cr(H2O)4Cl2]Cl•2H2O中Cr3+的配位数为
②硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是
③氨是
(3)镍元素基态原子的价电子排布式为
(4)单质铜及镍都是由金属键形成的晶体,元素铜与镍的第二电离能分别为:ICu=1958kJ/mol、INi=1753kJ/mol,ICu>INi的原因是
(5)某镍白铜合金的立方晶胞结构如图所示。若合金的密度为dg/cm3,晶胞参数a=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】已知A、B、C、D、E都是周期表中前四周期的元素,它们的原子序数依次增大。其中A元素原子的核外p电子数比s电子数少1。C是电负性最大的元素。D原子次外层电子数是最外层电子数2倍,E是第Ⅷ族中原子序数最小的元素。
(1)写出基态C原子的电子排布式_________________ 。
(2)A、B两种元素的第一电离能由大到小的顺序为______________ (用元素符号表示),原因是___________________ 。
(3)已知DC4常温下为气体,则该物质的晶体类型是_________ ,组成微粒的中心原子的轨道杂化类型为____________ ,空间构型是___________ 。
(4)Cu2+容易与AH3形成配离子[Cu(AH3)4]2+,但AC3不易与Cu2+形成配离子,其原因是______________________ 。
(5)A、B两元素分别与D形成的共价键中,极性较强的是__________ 。A、B两元素间能形成多种二元化合物,其中与A3—互为等电子体的物质的化学式为__________ 。
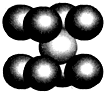
(6)已知E单质的晶胞如图所示,则晶体中E原子的配位数为__________ ,一个E的晶胞质量为___________ 。
(1)写出基态C原子的电子排布式
(2)A、B两种元素的第一电离能由大到小的顺序为
(3)已知DC4常温下为气体,则该物质的晶体类型是
(4)Cu2+容易与AH3形成配离子[Cu(AH3)4]2+,但AC3不易与Cu2+形成配离子,其原因是
(5)A、B两元素分别与D形成的共价键中,极性较强的是
(6)已知E单质的晶胞如图所示,则晶体中E原子的配位数为

您最近一年使用:0次
【推荐3】铍及其化合物的应用正日益被重视。
(1)最重要的含铍矿物是绿柱石,含2%铬(Cr)的绿柱石即为祖母绿。基态Cr原子价电子的轨道表示式为__________ 。
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有______ (填字母)。
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液pH均小于7
(3)氯化铍在气态时存在BeCl2分子(a)和二聚分子(BeCl2)2(b),固态时则具有如下图所示的链状结构(c)。
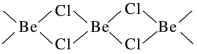
①a属于________ (填“极性”或“非极性”)分子。
②二聚分子(BeCl2)2中Be原子的杂化方式相同,且所有原子都在同一平面上。b 的结构式为__________ (标出配位键)。
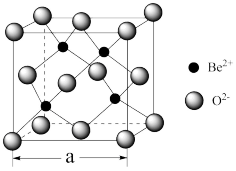
(4)BeO立方晶胞如下图所示,若BeO晶体的密度为d g·cm-3,则晶胞参数a=______ nm。
(1)最重要的含铍矿物是绿柱石,含2%铬(Cr)的绿柱石即为祖母绿。基态Cr原子价电子的轨道表示式为
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液pH均小于7
(3)氯化铍在气态时存在BeCl2分子(a)和二聚分子(BeCl2)2(b),固态时则具有如下图所示的链状结构(c)。

①a属于
②二聚分子(BeCl2)2中Be原子的杂化方式相同,且所有原子都在同一平面上。b 的结构式为
(4)BeO立方晶胞如下图所示,若BeO晶体的密度为d g·cm-3,则晶胞参数a=

您最近一年使用:0次



