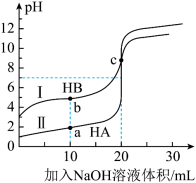
25℃时,用0.1000 mol/L NaOH溶液分别滴定20.00mL浓度均为0.1000mol/L的HA、HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如图。下列说法正确的是

| A.用NaOH溶液滴定HB溶液时适宜用酚酞作指示剂 |
| B.中和等体积、等浓度的HB和HA,所需NaOH:HA>HB |
| C.曲线Ⅰ上的c点溶液中:c(B-) > c(Na+) >c(OH-)>c(H+) |
| D.水的电离程度:b > c |
更新时间:2024-02-23 21:58:32
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】室温下,下列实验探究方案能够达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向盛有NaOH溶液(滴有2滴酚酞)的试管中通入 ,观察溶液颜色变化 ,观察溶液颜色变化 | 证明 具有漂白性 具有漂白性 |
| B | 常温下,向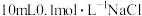 溶液中滴加5滴 溶液中滴加5滴 溶液,充分反应后,再滴加5滴 溶液,充分反应后,再滴加5滴 溶液,观察沉淀颜色变化 溶液,观察沉淀颜色变化 | 证明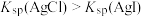 |
| C | 向久置氯水中滴加少量 溶液,观察有无气体生成 溶液,观察有无气体生成 | 证明HClO是否分解完全 |
| D | 测定等体积的盐酸和醋酸溶液的pH,并比较pH大小 | 证明HCl是强电解质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】有pH=2的X、Y、Z三种酸的溶液各1mL,分别向其中加水稀释到1000mL,其pH与溶液体积(V)的变化关系如图所示,下列说法正确的是


| A.Y的酸性强于X | B.X、Y、Z均为弱酸 |
C.稀释前的浓度大小为 | D.稀释后的浓度关系: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,用0.1mol·L-1NaOH溶液滴定40mL0.1mol·L-1H2SO3溶液,所得滴定曲线如图所示(忽略混合时溶液体积的变化)。下列叙述错误的是


| A.可求出Ka1(H2SO3)、Ka2(H2SO3)的值 |
| B.滴定中两次反应终点可依次用甲基橙、酚酞作指示剂 |
C.图中Y点对应的溶液中3c(SO )=c(Na+)+c(H+)-c(OH-) )=c(Na+)+c(H+)-c(OH-) |
D.图中Z点对应的溶液中:c(Na+)>c(SO )>c(HSO )>c(HSO )>c(OH-) )>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
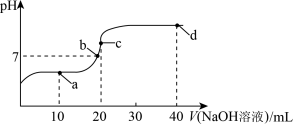
【推荐2】常温下,向20mL 0.1mol/L的醋酸溶液中不断滴入0.1mol/L NaOH溶液,溶液的pH变化如图所示。下列说法正确的是

| A.滴定过程中溶液中可能出现:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| B.a点溶液中:c(H+)-c(OH-)=c(CH3COO-)-c(CH3COOH) |
| C.水的电离程度大小关系:b点>c点 |
| D.b点溶液中:c(H+)+c(Na+)>c(OH-)+c(CH3COOH) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】室温下,下列溶液中粒子浓度关系正确的是( )
| A.Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O4-)+c(H2C2O4) |
| B.20 mL 0.1 mol•L-1 CH3COONa溶液与10 mL 0.1 mol•L-1 HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
| C.CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) |
| D.pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-) |
您最近一年使用:0次



