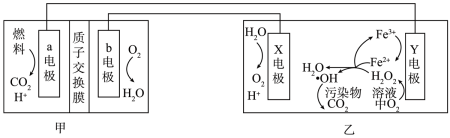
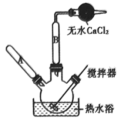
下列实验及现象可解释或得出结论正确的是
| 选项 | 实验及现象 | 解释或结论 |
| A | 25℃时,向 溶液中滴加甲基橙溶液,溶液变黄 溶液中滴加甲基橙溶液,溶液变黄 | 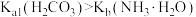 |
| B | 用铁电极电解硫酸铜溶液,开始时阴极析出铜 | 无法证明金属活动性: |
| C | 向 溶液中加入少量 溶液中加入少量 固体,颜色变深 固体,颜色变深 |  的水解程度变大 的水解程度变大 |
| D | 向 溶液中加入过量的 溶液中加入过量的 溶液,产生 溶液,产生 沉淀 沉淀 | 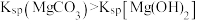 |
| A.A | B.B | C.C | D.D |
更新时间:2024-02-17 10:20:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式能用来解释相应实验现象的是
| 实验现象 | 离子方程式 | |
| A | 用氨水吸收烟气中少量的 | 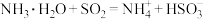 |
| B |  溶液和稍过量的 溶液和稍过量的 制备 制备 | 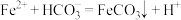 |
| C | 向 悬浊液中滴加 悬浊液中滴加 溶液,沉淀溶解 溶液,沉淀溶解 |  |
| D | FeO溶于稀硝酸 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知常温下测得浓度均为0.1 mol·L-1的下列6种溶液的pH:
请根据上述信息判断下列反应不能发生的是
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | NaAlO2 |
| pH | 8.8 | 9.1 | 11.6 | 10.3 | 11.1 | 12.3 |
| A.CO2 + H2O + 2NaClO === Na2CO3 + 2HClO |
| B.CH3COOH + NaHCO3 === CH3COONa + CO2 ↑+ H2O |
| C.CO2 + 3H2O + 2NaAlO2 === 2Al(OH)3↓ + Na2CO3 |
| D.CH3COOH + NaCN === CH3COONa + HCN |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】25℃时,下列说法正确的是
| A.某溶液中,由水电离的H+浓度为10-9mol·L-1,则此溶液呈酸性 |
| B.已知 NH3∙H2O与CH3COOH的电离平衡常数相等,某浓度的NH4Cl溶液的pH=4.3,则相同浓度的CH3COONa溶液的pH=9.7 |
C.N2H4的水溶液呈弱碱性,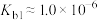 ,则0.01 mol·L-1N2H4水溶液的pH≈11 ,则0.01 mol·L-1N2H4水溶液的pH≈11 |
| D.pH=7的某溶液,溶质对水的电离平衡肯定无影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上利用锰矿(主要成分为 ,含
,含 、
、 、
、 、
、 、
、 、
、 等杂质)制备金属锰的工艺流程如图所示。下列说法错误的是
等杂质)制备金属锰的工艺流程如图所示。下列说法错误的是
已知:“脱硫”环节是在催化剂作用下将金属硫化物转化为氢氧化物。
 ,含
,含 、
、 、
、 、
、 、
、 、
、 等杂质)制备金属锰的工艺流程如图所示。下列说法错误的是
等杂质)制备金属锰的工艺流程如图所示。下列说法错误的是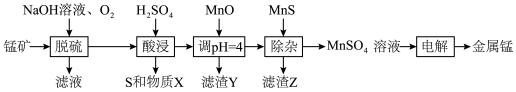
 |  |  | |
| 开始沉淀pH | 1.9 | 4.2 | 6.5 |
| 沉淀完全pH | 3.2 | 6.7 | 8.5 |
A.“脱硫”过程中 的反应为: 的反应为: |
B.X为 ,滤渣Y的主要成分为 ,滤渣Y的主要成分为 |
C.“除杂”工序是利用物质溶度积差异除去溶液中的 和 和 |
| D.“电解”所得阳极产物有两种,均可在流程中循环利用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化工生产中含Cu2+的废水常用MnS(s)作沉淀剂,其反应原理为Cu2+(aq)+MnS(s) CuS(s)+Mn2+(aq)。下列有关该反应的推理错误的是
CuS(s)+Mn2+(aq)。下列有关该反应的推理错误的是
 CuS(s)+Mn2+(aq)。下列有关该反应的推理错误的是
CuS(s)+Mn2+(aq)。下列有关该反应的推理错误的是| A.该反应达到平衡时:c(Cu2+)=c(Mn2+) |
| B.相同温度下,CuS的溶解度比MnS的溶解度小 |
| C.向含有等物质的量的CuSO4和MnSO4混合溶液中逐滴加入Na2S溶液,最先出现CuS沉淀 |
| D.往平衡体系中加入少量CuSO4(s)后,c(Mn2+)变大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】25℃,向AgCl的白色悬浊液中依次加入等浓度的KI溶液和Na2S溶液,先出现黄色沉淀,最终生成黑色沉淀。已知有关物质的颜色和溶度积如表:
下列叙述不正确的是
| 物质 | AgCl | AgI | Ag2S |
| 颜色 | 白 | 黄 | 黑 |
| Ksp(25℃) | 1.8×10-10 | 8.5×10-17 | 6.3×10-50 |
| A.溶度积小的沉淀可以转化为溶度积更小的沉淀 |
| B.若先加入Na2S溶液,再加入等浓度的KI溶液,则无黄色沉淀产生 |
| C.25℃时,饱和AgCl、AgI、Ag2S溶液中所含Ag+的浓度相同 |
| D.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某些无公害免农药果园利用如图所示电解装置,进行果品的安全生产,解决了农药残留所造成的生态及健康危害问题。下列说法正确的是


| A.a为直流电源的负极,与之相连的电极为阴极 |
| B.离子交换膜为阴离子交换膜 |
| C.“酸性水”具有强氧化性,能够杀菌 |
| D.阴极反应式为H2O+2e-===H2↑+O2- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】电化学脱硫在金属冶炼和废水处理中均有应用。一种电化学脱硫工作原理示意图如图所示。该装置工作时,下列说法不正确的是


| A.a为直流电源负极 |
| B.导线中通过4.5 mol e-时阳极区溶液质量增加44 g |
C.阳极反应式:Mn2+-e-=Mn3+,FeS+9Mn3++4H2O=9Mn2++8H++Fe3++SO |
| D.阴极区溶液pH无明显变化 |
您最近一年使用:0次
【推荐1】下列实验中,不能达到预期目的的是
①苯、浓溴水、溴化铁混合制溴苯
②用2mL 1 硫酸铜溶液和4mL 0.4
硫酸铜溶液和4mL 0.4 氢氧化钠溶液,混合后加入0.5mL 40%的乙醛溶液,加热至沸腾,检验醛的还原性
氢氧化钠溶液,混合后加入0.5mL 40%的乙醛溶液,加热至沸腾,检验醛的还原性
③用溴水除去混在苯中的乙烯,分液得到纯净的苯
④敞口久置的电石与饱和食盐水混合制乙炔
⑤将电石与水反应产生的乙炔通入溴水中,溴水褪色,证明乙炔和溴水发生了加成反应
①苯、浓溴水、溴化铁混合制溴苯
②用2mL 1
 硫酸铜溶液和4mL 0.4
硫酸铜溶液和4mL 0.4 氢氧化钠溶液,混合后加入0.5mL 40%的乙醛溶液,加热至沸腾,检验醛的还原性
氢氧化钠溶液,混合后加入0.5mL 40%的乙醛溶液,加热至沸腾,检验醛的还原性③用溴水除去混在苯中的乙烯,分液得到纯净的苯
④敞口久置的电石与饱和食盐水混合制乙炔
⑤将电石与水反应产生的乙炔通入溴水中,溴水褪色,证明乙炔和溴水发生了加成反应
| A.只有②④ | B.①②③④⑤ | C.只有①②④ | D.只有①③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。下列判断不正确 的是( )
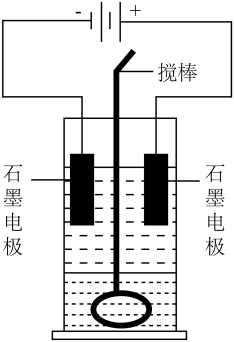

| A.原上层液体可能是KI的水溶液,原下层液体可能是CCl4 |
| B.搅拌后两层液体颜色发生变化的原因是I2在CCl4中的溶解度大于在水中溶解度,所以绝大部分I2都转移到CCl4中 |
| C.阴极区域pH增大的原因是水分子得电子生成了OH— |
| D.阳极上的电极反应式2H++2e - =H2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】乙酰乙酸乙酯是一种重要的有机中间体,实验室制备乙酰乙酸乙酯的反应、装置示意图和有关数据如下:
 (乙酰乙酸乙酯)
(乙酰乙酸乙酯)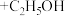
实验步骤:
ⅰ.向三颈烧瓶中加入4.0g钠、5.0g细砂和18mL二甲苯。加热使钠熔化,回流下搅拌5~6min,使其分散成小钠珠。静置冷却后,用倾析法除去上层液体。
ⅱ.迅速向三颈烧瓶中加入10mL环己烷、22.0g乙酸乙酯和极少量的乙醇,搅拌并加热,发生反应。
ⅲ.向反应后的体系中加入3mL乙醇,过滤。向滤液中加入50%乙酸至其呈弱酸性,再向其中加入饱和食盐水,分液。向有机层加入无水 ,过滤,蒸馏,收集到目标馏分10.4g。根据上述实验,下列说法不正确的是
,过滤,蒸馏,收集到目标馏分10.4g。根据上述实验,下列说法不正确的是
 (乙酰乙酸乙酯)
(乙酰乙酸乙酯)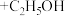
| 相对分子质量 | 沸点/℃ |
| |
| 乙醇 | 46 | 78 | |
| 乙酸乙酯 | 88 | 77 | |
| 乙酰乙酸乙酯 | 130 | 180.4 |
ⅰ.向三颈烧瓶中加入4.0g钠、5.0g细砂和18mL二甲苯。加热使钠熔化,回流下搅拌5~6min,使其分散成小钠珠。静置冷却后,用倾析法除去上层液体。
ⅱ.迅速向三颈烧瓶中加入10mL环己烷、22.0g乙酸乙酯和极少量的乙醇,搅拌并加热,发生反应。
ⅲ.向反应后的体系中加入3mL乙醇,过滤。向滤液中加入50%乙酸至其呈弱酸性,再向其中加入饱和食盐水,分液。向有机层加入无水
 ,过滤,蒸馏,收集到目标馏分10.4g。根据上述实验,下列说法不正确的是
,过滤,蒸馏,收集到目标馏分10.4g。根据上述实验,下列说法不正确的是| A.可以用四氯化碳代替二甲苯 |
| B.球形管应连接气体收集装置 |
| C.步骤ⅲ中,加入饱和食盐水目的是增大水层密度,便于分层 |
D.从结构角度分析知,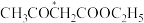 中标*号碳原子上的氢的活性强于 中标*号碳原子上的氢的活性强于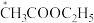 中标*号碳原子上的氢的活性 中标*号碳原子上的氢的活性 |
您最近一年使用:0次