 是9种中学化学中常见的元素。
是9种中学化学中常见的元素。(1)原子结构与元素性质
①基态氢原子中,核外电子的电子云轮廓图形状为
②3种元素
 中,离子半径最小的是
中,离子半径最小的是③基态
 的价层电子轨道表示式为
的价层电子轨道表示式为(2)微粒间相互作用与物质性质
①胆矾(
 )的结构示意图如下所示。
)的结构示意图如下所示。
 与
与 与
与 的作用力分别为
的作用力分别为②
 的VSEPR模型为
的VSEPR模型为 的分子空间构型为
的分子空间构型为 是
是③写出
 电子式:
电子式: 形成过程的电子式:
形成过程的电子式:④比较
 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:⑤相同条件下,
 在水中的溶解度大于
在水中的溶解度大于 的,理由是
的,理由是
更新时间:2024-02-19 16:39:52
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、J、R、Q六种短周期主族元素,原子序数依次增大。元素Z在地壳中含量最高,Y的简单氢化物水溶液呈碱性,J元素的焰色试验呈黄色,X能与J形成离子化合物,且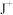 的半径大于
的半径大于 的半径,R的周期序数等于主族序数,Q的最外层电子数与其电子总数之比为
的半径,R的周期序数等于主族序数,Q的最外层电子数与其电子总数之比为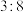 。请回答:
。请回答:
(1)Q元素在周期表中的位置为_______ 。
(2)六种元素原子半径最大的是_______ ,简单离子半径最大的是_______ 。(填元素符号)。
(3)元素的非金属性Z_______ (填“>”或“<”)Q。下列各项中,不能说明这一结论的事实有_______ (填字母)。
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4)R的最高价氧化物与J的最高价氧化物的水化物反应的化学方程式_______ 。
(5)X与Z简单化合物的空间构型为_______ ,用电子式表示X与J化合物的形成过程_______ ;X与Q在一定条件下可以形成极不稳定的原子个数比为 的化合物,该化合物分子中既有极性键又有非极性键,写出该分子的结构式:
的化合物,该化合物分子中既有极性键又有非极性键,写出该分子的结构式:_______ 。
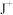 的半径大于
的半径大于 的半径,R的周期序数等于主族序数,Q的最外层电子数与其电子总数之比为
的半径,R的周期序数等于主族序数,Q的最外层电子数与其电子总数之比为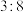 。请回答:
。请回答:(1)Q元素在周期表中的位置为
(2)六种元素原子半径最大的是
(3)元素的非金属性Z
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4)R的最高价氧化物与J的最高价氧化物的水化物反应的化学方程式
(5)X与Z简单化合物的空间构型为
 的化合物,该化合物分子中既有极性键又有非极性键,写出该分子的结构式:
的化合物,该化合物分子中既有极性键又有非极性键,写出该分子的结构式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】为纪念元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。下图是扇形元素周期表的一部分,针对元素①~⑩按要求作答。

(1)⑩的原子结构示意图为___________ ;
(2)①和②组成的相对氢气密度为14的化合物的电子式为___________ 。
(3)④和⑤的简单离子半径较大的是___________ (填离子符号);
(4)某元素的简单氢化物含10电子,该氢化物与其最高价氧化物对应水化物反应可得到盐。该元素为___________ (填序号);
(5)将过量②的氧化物投入⑥的一种盐溶液中可产生白色沉淀。发生反应的离子方程式为___________ ;
(6)写出一个能证明⑧和⑨非金属性强弱的离子方程式___________ ;
(7)⑦的氧化物用途广泛,写出其中一种___________ 。写出一种能与该氧化物反应的酸的化学式___________ 。

(1)⑩的原子结构示意图为
(2)①和②组成的相对氢气密度为14的化合物的电子式为
(3)④和⑤的简单离子半径较大的是
(4)某元素的简单氢化物含10电子,该氢化物与其最高价氧化物对应水化物反应可得到盐。该元素为
(5)将过量②的氧化物投入⑥的一种盐溶液中可产生白色沉淀。发生反应的离子方程式为
(6)写出一个能证明⑧和⑨非金属性强弱的离子方程式
(7)⑦的氧化物用途广泛,写出其中一种
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氯仿(CHCl3)不溶于水,但在一定条件下水解生成两种酸,其中一种是甲酸(HCOOH)。在19世纪氯仿广泛用于麻醉,可由“乙醛漂白粉法”制得。在光照条件下,氯仿易被空气氧化生成剧毒光气(COCl2)和一种化合物。因此氯仿需要小口钢罐贮存运输,使用前要检验其是否变质。
(1)CHCl3的电子式为__________ ,HCOOH中C的杂化方式为__________ ;
(2)漂白粉中三种元素的简单离子的半径的大小顺序为__________ (用离子符号表示);
(3)氯仿不溶于水而甲酸易溶于水的原因是__________ ;
(4)Fe2+的外围电子排布图为__________ ;
(5)纯铁的一种同素异形体的晶胞为面心立方晶胞,该晶体中原子的配位数为__________ ,若铁原子的半径为a cm,则该晶体的密度为__________ 。
(1)CHCl3的电子式为
(2)漂白粉中三种元素的简单离子的半径的大小顺序为
(3)氯仿不溶于水而甲酸易溶于水的原因是
(4)Fe2+的外围电子排布图为
(5)纯铁的一种同素异形体的晶胞为面心立方晶胞,该晶体中原子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铜、镍等金属材料在现代社会中有着重要应用。请回答下列问题:
(1)铜在元素周期表中的位置为____ ,基态镍原子的电子排布式为_____ 。
(2)氢氧化镍可生成单质镍的配合物: 。CH3NC的结构简式为
。CH3NC的结构简式为 ,1个CH3NC分子中
,1个CH3NC分子中 键的数目为
键的数目为___ , 键的数目为
键的数目为___ 。C、N、O三种元素的第一电离能由大到小的顺序为____ 。
(3)据报道,只含镁、镍、碳三种元素的晶体具有超导性。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方最密堆积,如图所示,晶体中每个镁原子周围距离最近的镍原子有______ 个。晶体中镁、镍、碳的原子个数比为_____ 。

(1)铜在元素周期表中的位置为
(2)氢氧化镍可生成单质镍的配合物:
 。CH3NC的结构简式为
。CH3NC的结构简式为 ,1个CH3NC分子中
,1个CH3NC分子中 键的数目为
键的数目为 键的数目为
键的数目为(3)据报道,只含镁、镍、碳三种元素的晶体具有超导性。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方最密堆积,如图所示,晶体中每个镁原子周围距离最近的镍原子有

您最近一年使用:0次
【推荐2】现有A、B、C、D、E、F、G、H8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1) 的电子式为
的电子式为________ 。(A、C为字母代号,请将字母代号用元素符号表示,下同)。
(2)B元素基态原子中能量最高的电子所占据的原子轨道呈________ 形。
(3)E元素基态原子的核外价电子轨道表示式为________ ,该元素的 远远大于
远远大于 ,其原因是
,其原因是________ 。
(4)D、E、F三种元素的简单离子半径由大到小的顺序是________________ 。
(5)G的最高价氧化物对应的水化物与E的氧化物反应的离子方程式________________________ 。
(6)H位于元素周期表中________ 区(按电子排布分区)。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素是形成化合物种类最多的元素 |
| C元素基态原子的核外p能级电子数比s能级电子数少1 |
| D元素基态原子的核外p轨道中有两个未成对电子 |
E元素的气态基态原子的第一至第四电离能分别是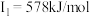 , ,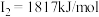 , ,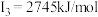 , ,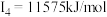 |
| F元素的主族序数与周期数的差为4 |
| G元素是前四周期中电负性最小的元素 |
| H元素位于元素周期表中的第8列 |
 的电子式为
的电子式为(2)B元素基态原子中能量最高的电子所占据的原子轨道呈
(3)E元素基态原子的核外价电子轨道表示式为
 远远大于
远远大于 ,其原因是
,其原因是(4)D、E、F三种元素的简单离子半径由大到小的顺序是
(5)G的最高价氧化物对应的水化物与E的氧化物反应的离子方程式
(6)H位于元素周期表中
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】高锰酸钾生产过程中产生的废锰矿(主要成分为MnO2、MgO和Fe2O3)可用于制备MnSO4固体,工艺流程如下:

该工艺条件下金属离子开始沉淀和完全沉淀的pH如下表所示:
回答以下问题:
(1)Mn2+基态核外电子排布式为_______ 。
(2)“滤渣2”为淡黄色单质固体,“反应2”的离子方程式为_______ 。
(3)“调pH”步骤中,应调节pH范围为_______ 。
(4)MnSO4在不同温度下的溶解度和该温度范围内析出晶体的组成如图所示。从过滤3所得滤液中获得较高纯度MnSO4·H2O的操作为:控制温度在80℃以上蒸发结晶,_______ ,使晶体MnSO4·H2O与溶液分离,_______ ,真空干燥。

(5)取3.02gMnSO4固体样品溶于适量水中,加硫酸酸化,用过量PbO2(难溶于水)将其完全氧化为MnO ,过滤,洗涤。洗涤液并入滤液后,加入10.72gNa2C2O4固体,充分反应后,用0.640mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液20.00mL。发生的反应为:C2O
,过滤,洗涤。洗涤液并入滤液后,加入10.72gNa2C2O4固体,充分反应后,用0.640mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液20.00mL。发生的反应为:C2O +MnO
+MnO +H+=CO2↑+Mn2++H2O(未配平)。计算样品中MnSO4的质量分数
+H+=CO2↑+Mn2++H2O(未配平)。计算样品中MnSO4的质量分数_______ (写出计算过程)。

该工艺条件下金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀pH | 2.10 | 7.45 | 9.27 | 9.60 |
| 完全沉淀pH | 3.20 | 8.95 | 10.87 | 11.13 |
回答以下问题:
(1)Mn2+基态核外电子排布式为
(2)“滤渣2”为淡黄色单质固体,“反应2”的离子方程式为
(3)“调pH”步骤中,应调节pH范围为
(4)MnSO4在不同温度下的溶解度和该温度范围内析出晶体的组成如图所示。从过滤3所得滤液中获得较高纯度MnSO4·H2O的操作为:控制温度在80℃以上蒸发结晶,

(5)取3.02gMnSO4固体样品溶于适量水中,加硫酸酸化,用过量PbO2(难溶于水)将其完全氧化为MnO
 ,过滤,洗涤。洗涤液并入滤液后,加入10.72gNa2C2O4固体,充分反应后,用0.640mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液20.00mL。发生的反应为:C2O
,过滤,洗涤。洗涤液并入滤液后,加入10.72gNa2C2O4固体,充分反应后,用0.640mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液20.00mL。发生的反应为:C2O +MnO
+MnO +H+=CO2↑+Mn2++H2O(未配平)。计算样品中MnSO4的质量分数
+H+=CO2↑+Mn2++H2O(未配平)。计算样品中MnSO4的质量分数
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】我国“嫦娥”五号首次实现地外天体采样返回,这是我国航天事业的又一突破。带回的月壤中含有H、N、O、Al、S、Cd、Zn、Ti、Cu、Au、Cr等多种元素。请完成下列问题:
(1)N、O、Al、S四种元素第一电离能从大到小的顺序为_______ 。
(2)Cu、Au是同一副族的元素,Au的原子序数更大,它们属于_______ 区元素,基态Au原子的价电子排布式为_______ 。
(3)SO2分子的空间构型为_______ ,请写出一种与SO2互为等电子体的单质_______ (填化学式)。
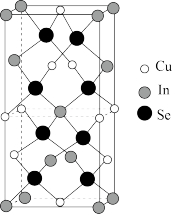
(4)某晶体的晶胞结构如图所示,该晶体的化学式为_______ 。如果将Se原子看做密堆积,则其堆积模型为_______ 。
(1)N、O、Al、S四种元素第一电离能从大到小的顺序为
(2)Cu、Au是同一副族的元素,Au的原子序数更大,它们属于
(3)SO2分子的空间构型为
(4)某晶体的晶胞结构如图所示,该晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】某硫与锌元素组成的化合物M不溶于水、易溶于酸,见阳光色变暗。若在该化合物中加入微量的Cu、Mn、Ag做活化剂,经光照后,能发出不同颜色的荧光。回答下列问题:
(1)基态铜原子的价电子排布图为_____ 。第一电离能介于Si、P之间的第三周期元素为_____ (填元素符号)。
(2)SO2中S的杂化类型为_____ ,该分子的空间构型为_____ 。
(3)1mol[Ag(NH3)2]OH中含有σ键的数目为_____ NA,NH3分子在独立存在时H-N-H键角为107°,[Ag(NH3)2]+中H-N-H键角变大的原因:________________ 。
(4)M的晶胞结构如图。
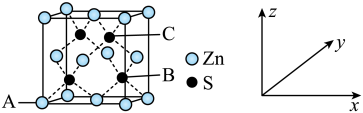
①观察图形推测,该晶体中每个Zn2+周围距离相等且最近的Zn2+数目为___ 个,M的化学式__ 。
②Zn的第三电离能大于Cu的第三电离能的原因是_____ 。
(1)基态铜原子的价电子排布图为
(2)SO2中S的杂化类型为
(3)1mol[Ag(NH3)2]OH中含有σ键的数目为
(4)M的晶胞结构如图。

①观察图形推测,该晶体中每个Zn2+周围距离相等且最近的Zn2+数目为
②Zn的第三电离能大于Cu的第三电离能的原因是
您最近一年使用:0次
【推荐3】周期表前四周期的元素X、Y、Z、T、W,原子序数依次增大。X的核外电子总数与其周期数相同,Y基态原子的p电子数比s电子数少1个,Z基态原子的价电子层中有2个未成对电子,T与Z同主族,W基态原子的M层全充满,N层只有一个电子。回答下列问题:
(1)Y、Z、T中单质熔点最高是______ (填元素符号)
(2)比W原子序数少5的基态原子中单电子数为_________________ 。
(3)T与Z形成的化合物中,中心原子杂化类型是_______
(4)X和上述其他元素中的一种形成的化合物中:分子呈三角锥形的是________ (填化学式);分子中既含有极性共价键,又含有非极性共价键的化合物是_______ (填化学式,写一种)。
(5)这5种元素形成的一种阴阳离子个数比为1:1型的配合物中,阴离子呈四面体结构,阳离子的结构如图所示。该配合物的化学式为__________ ,阳离子中存在的化学键类型有_______ 。

(1)Y、Z、T中单质熔点最高是
(2)比W原子序数少5的基态原子中单电子数为
(3)T与Z形成的化合物中,中心原子杂化类型是
(4)X和上述其他元素中的一种形成的化合物中:分子呈三角锥形的是
(5)这5种元素形成的一种阴阳离子个数比为1:1型的配合物中,阴离子呈四面体结构,阳离子的结构如图所示。该配合物的化学式为

您最近一年使用:0次
【推荐1】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子核外有_______ 个未成对电子。
(2)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。CO2和CH4都属于_______ 分子(填极性或非极性)。
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的作用力是_______ 。
(4)已知Ge单晶的晶胞如图所示,则一个晶胞所含Ge原子数是_______ 。

(1)基态Ge原子核外有
(2)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。CO2和CH4都属于
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(4)已知Ge单晶的晶胞如图所示,则一个晶胞所含Ge原子数是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】有以下物质:①HF、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦ 、⑧
、⑧ 、⑨HCN、⑩
、⑨HCN、⑩ 。
。
(1)既含有σ键又含有π键的是___________ 。
(2)分子中既含有极性键又含有非极性键的是___________ 。仅由极性键构成的非极性分子有___________
(3) 是一种常见的配体。钴的一种配位聚合物的化学式为
是一种常见的配体。钴的一种配位聚合物的化学式为 。bte的分子式为
。bte的分子式为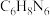 ,其结构简式如图所示。
,其结构简式如图所示。

①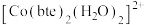 中,与
中,与 形成配位键的原子是
形成配位键的原子是___________ (填元素符号)。
②bte分子中碳原子轨道杂化类型为___________ 。
③1molbte分子中含键为___________ mol。
 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦ 、⑧
、⑧ 、⑨HCN、⑩
、⑨HCN、⑩ 。
。(1)既含有σ键又含有π键的是
(2)分子中既含有极性键又含有非极性键的是
(3)
 是一种常见的配体。钴的一种配位聚合物的化学式为
是一种常见的配体。钴的一种配位聚合物的化学式为 。bte的分子式为
。bte的分子式为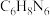 ,其结构简式如图所示。
,其结构简式如图所示。
①
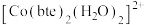 中,与
中,与 形成配位键的原子是
形成配位键的原子是②bte分子中碳原子轨道杂化类型为
③1molbte分子中含键为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】前四周期元素A、B、C、D、E的原子序数依次增大,基态A原子核外电子占据3个轨道,基态B原子核外电子占据3个能级且每个能级上电子数相等,C的双原子单质分子中σ键和π键数目之比为1∶2,D的最高化合价和最低化合价代数和等于4;基态E原子核外有6个未成对电子。
(1)基态E原子的核外电子排布式为____ ,该元素位于周期表的____ 区,基态D原子核外电子所占据____ 个轨道。
(2)A元素的各级电离能数据如表:
分析表中数据可知,相邻两级的电离能中,I3和I4之间差异最大,其主要原因是____ 。
(3)A、B、C元素的最高价氧化物对应的水化物酸性依次增强,其原因是____ 。
(4)氯元素与元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp3杂化、空间结构为三角锥形的是____ (填分子式)。
(5)(DC)4为热色性固体,且有色温效应。其颜色在低于-30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色。在淡黄色→橙黄色→深红色的转化中,破坏的作用力是___ ;在常压下,(DC)4高于130℃分解为相应的单质,这一变化中破坏的作用力是____ 。在B、C、D的简单气态氢化物中,属于非极性分子的是____ (填分子式)。
(1)基态E原子的核外电子排布式为
(2)A元素的各级电离能数据如表:
| 符号 | I1 | I2 | I3 | I4 | I5 |
| 电离能/(kJ·mol-1) | 800.6 | 2427 | 3660 | 25026 | 32827 |
(3)A、B、C元素的最高价氧化物对应的水化物酸性依次增强,其原因是
(4)氯元素与元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp3杂化、空间结构为三角锥形的是
(5)(DC)4为热色性固体,且有色温效应。其颜色在低于-30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色。在淡黄色→橙黄色→深红色的转化中,破坏的作用力是
您最近一年使用:0次



