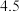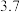锌焙砂是锌精矿经焙烧后所得的产物,是褐色微颗粒状固体,其主要成分为 ,还含有
,还含有 、
、 和少量
和少量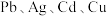 ,以锌焙砂为原料制备
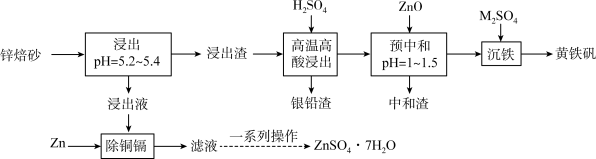
,以锌焙砂为原料制备 和黄铁矾的工艺流程如下:
和黄铁矾的工艺流程如下:
已知:① 可以看成
可以看成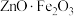 ,在高温高酸环境下才会溶解;
,在高温高酸环境下才会溶解;
② 下,
下, 和
和 开始沉淀和沉淀完全(
开始沉淀和沉淀完全(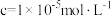 )时的
)时的 如下表:
如下表:
回答下列问题:
(1)基态 原子的简化电子排布式为
原子的简化电子排布式为_______ ,基态 原子价层电子轨道表示式为
原子价层电子轨道表示式为_______ ,基态 原子未成对电子数目为
原子未成对电子数目为_______ ,铜元素的焰色为绿色,该光谱属于_______ (填“发射”或“吸收”)光谱。
(2)欲提高 在5.2~5.4时的“浸出”速率,可采用的方法是
在5.2~5.4时的“浸出”速率,可采用的方法是_______ (写两种)。
(3)在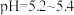 “浸出”时,锌焙砂中的铜转化为
“浸出”时,锌焙砂中的铜转化为 反应的离子方程式为
反应的离子方程式为_______ 。
(4) 时,浸出液中
时,浸出液中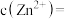
_______  。
。
(5)当有 、
、 或
或 存在时,调节含
存在时,调节含 溶液的
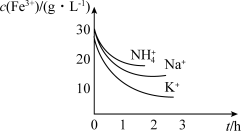
溶液的 ,即可生成黄铁矾。不同种类的阳离子“沉铁”效果如图,则工艺流程中,
,即可生成黄铁矾。不同种类的阳离子“沉铁”效果如图,则工艺流程中, 最好选用
最好选用_______ (填化学式)。
(6)获得 的一系列操作是
的一系列操作是_______ 、_______ 过滤、洗涤、干燥。
 ,还含有
,还含有 、
、 和少量
和少量 ,以锌焙砂为原料制备
,以锌焙砂为原料制备 和黄铁矾的工艺流程如下:
和黄铁矾的工艺流程如下:
已知:①
 可以看成
可以看成 ,在高温高酸环境下才会溶解;
,在高温高酸环境下才会溶解;②
 下,
下, 和
和 开始沉淀和沉淀完全(
开始沉淀和沉淀完全(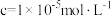 )时的
)时的 如下表:
如下表:| 金属离子 |  | |
| 开始沉淀 | 沉淀完全 | |
 | 6.2 | 8.2 |
 | 1.5 | 3.2 |
(1)基态
 原子的简化电子排布式为
原子的简化电子排布式为 原子价层电子轨道表示式为
原子价层电子轨道表示式为 原子未成对电子数目为
原子未成对电子数目为(2)欲提高
 在5.2~5.4时的“浸出”速率,可采用的方法是
在5.2~5.4时的“浸出”速率,可采用的方法是(3)在
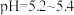 “浸出”时,锌焙砂中的铜转化为
“浸出”时,锌焙砂中的铜转化为 反应的离子方程式为
反应的离子方程式为(4)
 时,浸出液中
时,浸出液中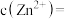
 。
。(5)当有
 、
、 或
或 存在时,调节含
存在时,调节含 溶液的
溶液的 ,即可生成黄铁矾。不同种类的阳离子“沉铁”效果如图,则工艺流程中,
,即可生成黄铁矾。不同种类的阳离子“沉铁”效果如图,则工艺流程中,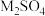 最好选用
最好选用
(6)获得
 的一系列操作是
的一系列操作是
更新时间:2024-02-14 19:22:54
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】由于金属锌本身的价值不高,在我国工业锌废料的回收利用率比较低。某课题组研究利用含少量铜、铁的粗锌制备硫酸锌及相关物质的资源综合利用,其工艺流程图(图中加入的物质均为足量)及有关数据如下:

请回答下列问题:
(1)固体A的主要成分是_______________ ;加入固体B的主要作用是____________ 。
(2)粗锌中的铜与稀混酸溶液反应的离子方程式为_____________________________ 。
(3)若溶液II中c(Cu2+)为0.05mol·L—1,则溶液II的pH≤_________ 。
(4)若B是Zn,取8.320gC完全溶解于500mL 1mol·L—1稀硝酸中,共收集到2240mL气体,再向所得溶液中加入NaOH溶液至刚好生成沉淀最多,此时所得沉淀质量(m)的取值范围是___________ ;若B是另一种物质,取部分C于试管中,加入盐酸后产生了有臭鸡蛋味气体,则该反应的离子方程式为________________________ 。
(5)溶液III还可以与(NH4)2S溶液反应制备ZnS,实际生产中选用(NH4)2S溶液而不是Na2S溶液作为反应物,是因为后者制得的ZnS中会含有较多的___________ 杂质。

| 物质 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS |
| Ksp | 4.0×10—38 | 5.0×10—20 | 2.0×10—16 | 8.5×10—45 | 1.2×10—23 |
请回答下列问题:
(1)固体A的主要成分是
(2)粗锌中的铜与稀混酸溶液反应的离子方程式为
(3)若溶液II中c(Cu2+)为0.05mol·L—1,则溶液II的pH≤
(4)若B是Zn,取8.320gC完全溶解于500mL 1mol·L—1稀硝酸中,共收集到2240mL气体,再向所得溶液中加入NaOH溶液至刚好生成沉淀最多,此时所得沉淀质量(m)的取值范围是
(5)溶液III还可以与(NH4)2S溶液反应制备ZnS,实际生产中选用(NH4)2S溶液而不是Na2S溶液作为反应物,是因为后者制得的ZnS中会含有较多的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某实验小组以含铁污泥(主要成分为 、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾(
、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾( )和柠檬酸铁铵。
)和柠檬酸铁铵。
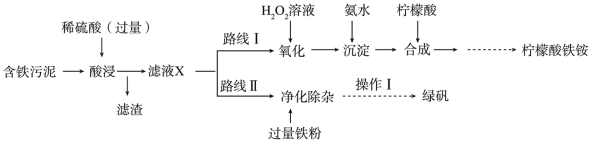
根据所学知识,回答下列问题:
(1)写出“酸浸”时, 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:_______ 。
(2)“滤液X”中一定含有的阳离子为_______ 。
(3)路线Ⅰ中,加入 溶液的目的是
溶液的目的是_______ 。
(4)写出加入过量铁粉时发生反应的离子方程式:_______ 。
(5)“操作Ⅰ”为过滤、_______ 、_______ 、过滤、洗涤、低温烘干。
(6)“酸浸”时加入400mL1.5 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为_______ g。
 、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾(
、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾( )和柠檬酸铁铵。
)和柠檬酸铁铵。
根据所学知识,回答下列问题:
(1)写出“酸浸”时,
 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:(2)“滤液X”中一定含有的阳离子为
(3)路线Ⅰ中,加入
 溶液的目的是
溶液的目的是(4)写出加入过量铁粉时发生反应的离子方程式:
(5)“操作Ⅰ”为过滤、
(6)“酸浸”时加入400mL1.5
 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:
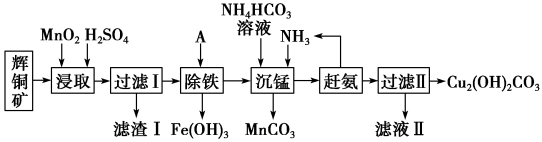
已知:①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
②Ksp[Fe(OH)3]=4.0×10-38
(1)加快“浸取”速率,除适当增加硫酸浓度外,还可采取的措施有____ (任写一种)。
(2)滤渣I中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的化学方程式:_____ 。
(3)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为____ ,若加A后溶液的pH调为4.0,则溶液中Fe3+的浓度为____ mol/L。
(4)写出“沉锰”(除Mn2+)过程中反应的离子方程式:____ 。
(5)过滤II得到的沉淀经过洗涤、干燥可以得到碱式碳酸铜,判断沉淀是否洗净的操作是___ 。

已知:①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
| 开始沉淀 | 7.5 | 2.7 | 5.6 | 8.3 |
| 完全沉淀 | 9.0 | 3.7 | 6.7 | 9.8 |
②Ksp[Fe(OH)3]=4.0×10-38
(1)加快“浸取”速率,除适当增加硫酸浓度外,还可采取的措施有
(2)滤渣I中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的化学方程式:
(3)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为
(4)写出“沉锰”(除Mn2+)过程中反应的离子方程式:
(5)过滤II得到的沉淀经过洗涤、干燥可以得到碱式碳酸铜,判断沉淀是否洗净的操作是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】钴及其化合物广泛应用于航天、电池、磁性合金等高科技领域,我国钴资源贫乏,再生钴资源的回收利用是解决钴资源供给的重要途径.一种利用含钴废料(主要成分为 ,含少量
,含少量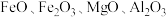 、有机物)制取
、有机物)制取 的工艺流程如下:
的工艺流程如下: ,回答下列问题:
,回答下列问题:
(1)“焙烧”的主要目的是____________ 。
(2)“浸取”过程中 发生反应的离子方程式为
发生反应的离子方程式为________ 。
(3)“沉淀"时先加入 溶液,
溶液, 的作用主要是
的作用主要是_____________ 。再加入 溶液调节
溶液调节 为6.0,此时滤液中的
为6.0,此时滤液中的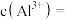
________  ,滤渣的主要成分为:
,滤渣的主要成分为:________ 。
(4)“萃取”用到的玻璃仪器主要有________ 烧杯。为得到纯净的 ,“沉钴”后要进行洗涤,如何判断沉淀是否洗涤干净?
,“沉钴”后要进行洗涤,如何判断沉淀是否洗涤干净?____________ 。
(5)萃取原理可表述为: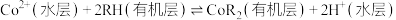 ,“反萃取”需加入A的水溶液,试剂A为
,“反萃取”需加入A的水溶液,试剂A为________ 。
 ,含少量
,含少量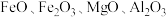 、有机物)制取
、有机物)制取 的工艺流程如下:
的工艺流程如下:
 ,回答下列问题:
,回答下列问题:金属离子 |
|
|
|
|
|
开始沉淀 | 7.5 | 1.8 | 3.4 | 9.1 | 6.5 |
沉淀完全 | 9.5 | 3.2 | 4.7 | 11.1 | 8.5 |
(1)“焙烧”的主要目的是
(2)“浸取”过程中
 发生反应的离子方程式为
发生反应的离子方程式为(3)“沉淀"时先加入
 溶液,
溶液, 的作用主要是
的作用主要是 溶液调节
溶液调节 为6.0,此时滤液中的
为6.0,此时滤液中的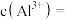
 ,滤渣的主要成分为:
,滤渣的主要成分为:(4)“萃取”用到的玻璃仪器主要有
 ,“沉钴”后要进行洗涤,如何判断沉淀是否洗涤干净?
,“沉钴”后要进行洗涤,如何判断沉淀是否洗涤干净?(5)萃取原理可表述为:
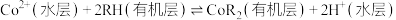 ,“反萃取”需加入A的水溶液,试剂A为
,“反萃取”需加入A的水溶液,试剂A为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】从铜电解液中分离得到的粗硫酸镍晶体中含有大量的杂质元素(Cu、Fe、As、Ca、Zn等),我国科学家对粗硫酸镍进行精制提纯,其工艺流程如下。
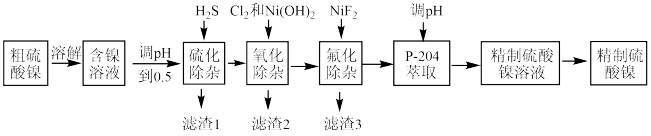
已知:i.含镍溶液中的主要离子有:Ni2+、 、Cu2+、Fe2+、
、Cu2+、Fe2+、 、Ca2+和Zn2+;
、Ca2+和Zn2+;
ii.饱和H2S溶液中,c(H2S)≈0.1mol/L;
iii.部分物质的电离常数和溶度积常数如下表。
(1)在“溶解”时,为加快溶解速率,可采取的措施有___________ 。(任写一条即可)。
(2)滤渣1中含有As2S3和S等沉淀,写出生成As2S3和S的离子方程式___________ 。
(3)“氧化除杂”中通入Cl2的主要目的是___________ 。
(4)滤渣3的主要成分为___________ 。
(5)“P-204萃取”水溶液的pH约为3,结合下图解释原因___________ 。

(6)理论上“硫化除杂”之后,溶液中c(Cu2+)=___________ mol/L[计算时c(H2S)取0.1mol/L,结果保留两位有效数字]。

已知:i.含镍溶液中的主要离子有:Ni2+、
 、Cu2+、Fe2+、
、Cu2+、Fe2+、 、Ca2+和Zn2+;
、Ca2+和Zn2+;ii.饱和H2S溶液中,c(H2S)≈0.1mol/L;
iii.部分物质的电离常数和溶度积常数如下表。
| 物质 | 电离常数 | 物质 | 溶度积常数 | 物质 | 溶度积常数 |
| H2S | Ka1=1.1×10-7 Ka2=l.3×10-13 | CuS | 6.3×10-36 | FeS | 6.3×10-18 |
| NiS | 3.2×10-19 | Ni(OH)2 | 5.5×10-16 | ||
| CaF2 | 4×10-11 | Fe(OH)3 | 2.8×10-39 |
(2)滤渣1中含有As2S3和S等沉淀,写出生成As2S3和S的离子方程式
(3)“氧化除杂”中通入Cl2的主要目的是
(4)滤渣3的主要成分为
(5)“P-204萃取”水溶液的pH约为3,结合下图解释原因

(6)理论上“硫化除杂”之后,溶液中c(Cu2+)=
您最近一年使用:0次
【推荐1】含硫、氮物质的使用在为人类带来益处的同时,也给人们带来了一些困扰。利用化学原理处理含硫、氮的废气、废液等具有重要意义。二氧化氯(ClO2)可用于烟气中SO2和NO的脱除。研究发现ClO2氧化SO2和NO时涉及以下基元反应。
脱硝:
ⅰ
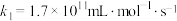
ⅱ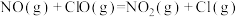
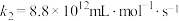
脱硫:
ⅲ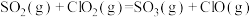

ⅳ
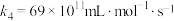
其中k为速率常数。对于基元反应: ,其速率方程表达式为
,其速率方程表达式为
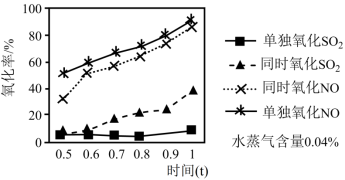
实验测得:ClO2分别单独氧化纯SO2、纯NO以及同时氧化二者混合物的氧化率随时间(t)的变化情况如图所示。_______ 。
2.脱硝反应和脱硫反应哪个活化能更大?说明理由_______ 。
3.请结合ⅰ、ⅲ、ⅳ的速率常数,判断NO的存在是否会影响ClO2氧化SO2的速率并说明理由_______ 。
CO也可以与NO反应生成无污染物: 。
。
已知:
ⅰ 在浓度平衡常数表达式中,用相对分压代替浓度,可得到相对压力平衡常数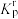 。
。
ⅱ 气体的相对分压等于其分压(单位为kPa)除以 (
(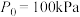 )。
)。
4.在某温度下,原料组成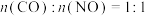 ,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
_______ 。
5.该反应中,如果在恒压密闭容器中,仍保持原料组成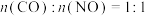 ,以下哪些条件可以判断反应达到平衡_______。
,以下哪些条件可以判断反应达到平衡_______。
脱硝:
ⅰ

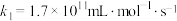
ⅱ
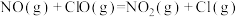
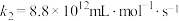
脱硫:
ⅲ
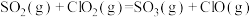

ⅳ

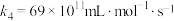
其中k为速率常数。对于基元反应:
 ,其速率方程表达式为
,其速率方程表达式为
实验测得:ClO2分别单独氧化纯SO2、纯NO以及同时氧化二者混合物的氧化率随时间(t)的变化情况如图所示。
2.脱硝反应和脱硫反应哪个活化能更大?说明理由
3.请结合ⅰ、ⅲ、ⅳ的速率常数,判断NO的存在是否会影响ClO2氧化SO2的速率并说明理由
CO也可以与NO反应生成无污染物:
 。
。已知:
ⅰ 在浓度平衡常数表达式中,用相对分压代替浓度,可得到相对压力平衡常数
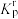 。
。ⅱ 气体的相对分压等于其分压(单位为kPa)除以
 (
(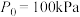 )。
)。4.在某温度下,原料组成
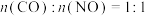 ,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
5.该反应中,如果在恒压密闭容器中,仍保持原料组成
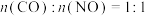 ,以下哪些条件可以判断反应达到平衡_______。
,以下哪些条件可以判断反应达到平衡_______。| A.CO的消耗速率等于NO的消耗速率 | B.容器内气体密度保持不变 |
| C.容器内平均相对分子质量保持不变 | D.CO的转化率保持不变 |
您最近一年使用:0次
【推荐2】2023年8月1日起,中国对镓、锗相关物项进行出口管制。金属镓有“电子工业脊梁”的美誉,与铝的化学性质类似,广泛应用于电子、航空航天、光学等领域。从刚玉渣(含钛、镓的低硅铁合金,还含有少量氧化铝)回收镓的流程如图所示:
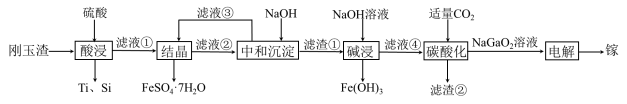
室温时,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 |
|
|
|
|
开始沉淀时( )的pH )的pH |
|
|
|
|
沉淀完全时( )的pH )的pH |
|
|
|
|
回答下列问题:
(1)基态镓原子的价电子排布式为
(2)从溶液中得到
 的具体操作为
的具体操作为(3)“中和沉淀”过程中分离出的滤渣①有
 和
和 ,“中和沉淀”过程中pH应调节的范围为
,“中和沉淀”过程中pH应调节的范围为(4)“碱浸”时镓元素发生的离子方程式为
(5)“碳酸化”过程中为防止镓损耗,不能通入过量
 的原因为
的原因为(6)以纯镓为原料可制得GaN,GaN晶体的一种立方晶胞如图所示,Ga的配位数为
 ,则GaN的晶体密度为
,则GaN的晶体密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.2021年诺贝尔化学奖授予德国科学家Benjamin List和美国科学家David W.C.MacMillan,以表彰他们在不对称有机催化的发展方面的贡献。金属钴络合物R在有机不对称合成中起催化诱导效应,其结构简式如图1所示。

(1)络合物R中,碳原子的杂化类型为_______ 杂化;第一电离能: ,原因是
,原因是_______ 。
(2)基态 的核外电子排布式为
的核外电子排布式为_______ ;已知:CoO的熔点是1935℃,CoS的熔点是1182℃,CoO的熔点较高的原因是_______ 。
Ⅱ.铀对于核能的发展具有重要作用,沥青铀矿的晶胞结构如图2所示。

(3)该物质的化学式为_______ ,U的配位数为_______ 。
(4)以晶胞中A点U为原点建立空间直角坐标系,晶胞内B点U的坐标为 ,则晶胞内C和D氧原子的坐标分别为
,则晶胞内C和D氧原子的坐标分别为_______ 、_______ 。
(5)已知:铀原子半径为anm,氧原子半径为bnm,晶胞参数为0.5nm,阿伏加德罗常数的值为 。该晶胞中原子的空间占有率为
。该晶胞中原子的空间占有率为_______ (列出计算式即可,下同),该晶体的密度为_______  。
。

(1)络合物R中,碳原子的杂化类型为
 ,原因是
,原因是(2)基态
 的核外电子排布式为
的核外电子排布式为Ⅱ.铀对于核能的发展具有重要作用,沥青铀矿的晶胞结构如图2所示。

(3)该物质的化学式为
(4)以晶胞中A点U为原点建立空间直角坐标系,晶胞内B点U的坐标为
 ,则晶胞内C和D氧原子的坐标分别为
,则晶胞内C和D氧原子的坐标分别为(5)已知:铀原子半径为anm,氧原子半径为bnm,晶胞参数为0.5nm,阿伏加德罗常数的值为
 。该晶胞中原子的空间占有率为
。该晶胞中原子的空间占有率为 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】锌的化学性质与铝相似,工业上有较高的利用价值。某含锌废催化剂中锌以氧化物的形式存在,还含有镍、铁、铅等元素杂质,采用“氨浸除杂蒸发煅烧”新工艺生产高纯碱式碳酸锌,达到了废物综合利用的目的,工艺流程如图,请回答下列问题。
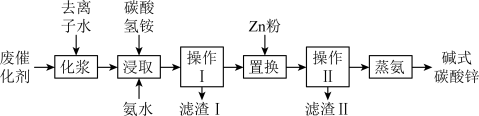
已知:“浸取”步骤后生成了锌氨配合物和镍氨配合物进行后续生产。
(1)Zn2+的价电子排布图____ ;金属配合物的结构和稳定性常用18e-经验规则预测,即中心体的价电子数加配体提供的电子数等于18,请试写出“浸取”后锌元素的存在微粒形式____ 。(填化学式)
(2)“浸取”步骤中,废催化剂中含锌物质的反应方程式为____ 。
(3)“浸取”中锌的浸出率对本工艺至关重要,图一、图二是锌浸出率分别受温度、氨水与碳酸氢铵比(氮元素浓度固定)的影响。请分析:

①图一中适宜选择的温度为42℃左右。温度不宜过高的原因是____ 。
②图二中随着氨水与碳酸氢铵比的增大,锌的浸出率先增大后减小,然后再增大。当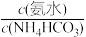 <0.75时,溶液pH值较低,试判断锌的存在形式为
<0.75时,溶液pH值较低,试判断锌的存在形式为____ ;当0.75<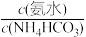 <1时,溶液pH值升高,锌的存在形式为
<1时,溶液pH值升高,锌的存在形式为____ ;当1<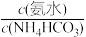 后,溶液pH值继续升高,锌的存在形式为
后,溶液pH值继续升高,锌的存在形式为___ 。
(4)滤渣II的成分为过量的Zn外,还有____ 。(填化学式)
(5)“蒸氨”操作中锌氨溶液最终以ZnCO3•2Zn(OH)2形式从溶液中析出,经过滤洗涤、干燥后得到碱式碳酸锌,其化学反应方程式为:____ 。
(6)整个过程中可以循环利用的物质为____ 。

已知:“浸取”步骤后生成了锌氨配合物和镍氨配合物进行后续生产。
(1)Zn2+的价电子排布图
(2)“浸取”步骤中,废催化剂中含锌物质的反应方程式为
(3)“浸取”中锌的浸出率对本工艺至关重要,图一、图二是锌浸出率分别受温度、氨水与碳酸氢铵比(氮元素浓度固定)的影响。请分析:

①图一中适宜选择的温度为42℃左右。温度不宜过高的原因是
②图二中随着氨水与碳酸氢铵比的增大,锌的浸出率先增大后减小,然后再增大。当
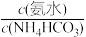 <0.75时,溶液pH值较低,试判断锌的存在形式为
<0.75时,溶液pH值较低,试判断锌的存在形式为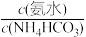 <1时,溶液pH值升高,锌的存在形式为
<1时,溶液pH值升高,锌的存在形式为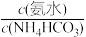 后,溶液pH值继续升高,锌的存在形式为
后,溶液pH值继续升高,锌的存在形式为(4)滤渣II的成分为过量的Zn外,还有
(5)“蒸氨”操作中锌氨溶液最终以ZnCO3•2Zn(OH)2形式从溶液中析出,经过滤洗涤、干燥后得到碱式碳酸锌,其化学反应方程式为:
(6)整个过程中可以循环利用的物质为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某厂排出的废液主要含有硝酸锌和硝酸银,为了从中回收金属银和硝酸锌,某中学化学课外活动小组设计了以下的实验步骤:
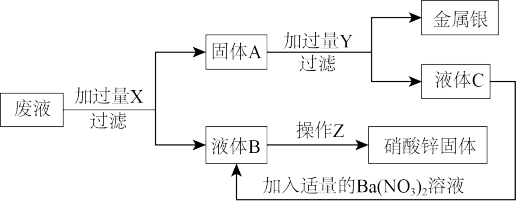
(1)X是____ ,Y是____ (写化学式,下同)。
(2)固体A、滤液C的主要成分:A____ ,C____ 。
(3)Z处进行的操作是____ 。
(4)写出C生成B的化学方程式____ 。

(1)X是
(2)固体A、滤液C的主要成分:A
(3)Z处进行的操作是
(4)写出C生成B的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】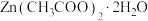 常用作媒染剂、木材防腐剂等。实验室以含锌废液(主要成分为
常用作媒染剂、木材防腐剂等。实验室以含锌废液(主要成分为 ,含少量的
,含少量的 、
、 )为原料制备
)为原料制备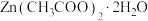 的实验流程如下:
的实验流程如下:

已知:①金属离子开始沉淀和完全沉淀时的pH如表所示。
② 属于两性化合物。
属于两性化合物。
回答下列问题:
(1)已知 中存在一个过氧键(-O-O-),则
中存在一个过氧键(-O-O-),则 中S元素的化合价为
中S元素的化合价为___________ 。
(2)写出“除锰”时生成 的离子方程式:
的离子方程式:___________ 。
(3)“除铁”时调节溶液的pH范围为___________ ,该过程不用Zn代替ZnO调节pH,原因是___________ 。
(4)“沉锌”时溶液的pH不能大于10.5,目的是___________ 。
(5)向 中加入足量醋酸后可得醋酸锌溶液,经
中加入足量醋酸后可得醋酸锌溶液,经___________ 、过滤、洗涤、干燥等一系列操作可得到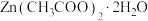 晶体。
晶体。
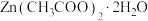 常用作媒染剂、木材防腐剂等。实验室以含锌废液(主要成分为
常用作媒染剂、木材防腐剂等。实验室以含锌废液(主要成分为 ,含少量的
,含少量的 、
、 )为原料制备
)为原料制备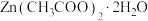 的实验流程如下:
的实验流程如下:
已知:①金属离子开始沉淀和完全沉淀时的pH如表所示。
| 物质 |  |  |  |
| 开始沉淀的pH | 1.9 | 6.8 | 6.2 |
| 完全沉淀的pH | 3.3 | 8.3 | 8.2 |
 属于两性化合物。
属于两性化合物。回答下列问题:
(1)已知
 中存在一个过氧键(-O-O-),则
中存在一个过氧键(-O-O-),则 中S元素的化合价为
中S元素的化合价为(2)写出“除锰”时生成
 的离子方程式:
的离子方程式:(3)“除铁”时调节溶液的pH范围为
(4)“沉锌”时溶液的pH不能大于10.5,目的是
(5)向
 中加入足量醋酸后可得醋酸锌溶液,经
中加入足量醋酸后可得醋酸锌溶液,经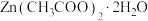 晶体。
晶体。
您最近一年使用:0次






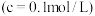 的
的 的
的