甲醇水蒸气重整制氢(SRM)系统可作为电动汽车燃料电池的理想氢源。系统中的两个反应如下:
主反应:CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g) ΔH1>0
副反应:H2(g)+CO2(g)⇌CO(g)+H2O(g) ΔH2>0
单位时间内,CH3OH转化率与CO生成率随温度的变化如图所示:
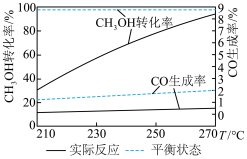
升温过程中CH3OH实际反应转化率不断接近平衡状态转化率的原因是_______ ;温度升高,CO实际反应生成率并没有不断接近平衡状态的生成率,其原因可能是_______
A.副反应逆向进行 B.部分CO转化为CH3OH
C.催化剂对副反应的选择性低 D.升温提高了副反应的焓变
主反应:CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g) ΔH1>0
副反应:H2(g)+CO2(g)⇌CO(g)+H2O(g) ΔH2>0
单位时间内,CH3OH转化率与CO生成率随温度的变化如图所示:

升温过程中CH3OH实际反应转化率不断接近平衡状态转化率的原因是
A.副反应逆向进行 B.部分CO转化为CH3OH
C.催化剂对副反应的选择性低 D.升温提高了副反应的焓变
2024高三下·全国·专题练习 查看更多[1]
(已下线)题型四 平衡图像原因解释-备战2024年高考化学答题技巧与模板构建
更新时间:2024-02-29 22:28:58
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】实验I:定性探究影响化学反应速率的外界因素
实验原理:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O、2H2O2 2H2O+O2↑
2H2O+O2↑
实验原理:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O、2H2O2
 2H2O+O2↑
2H2O+O2↑| 影响因素 | 实验步骤 | 实验现象 | 实验结论 |
| 浓度 | 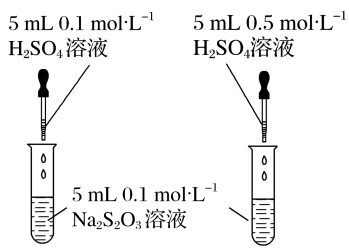 | 均出现 | 增大浓度,化学反应速率 |
| 温度 | 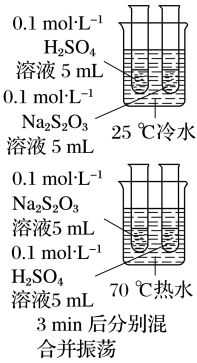 | 混合后均出现 | 升高温度,化学反应速率 |
| 催化剂 | 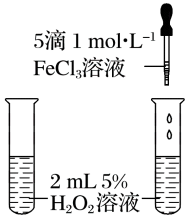 | 前者 | 催化剂能 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】图Ⅰ、Ⅱ依次表示在酶浓度一定时,反应速率与反应物浓度、温度的关系。请据图回答下列问题:

(1)图Ⅰ中,反应物达到某一浓度时,反应速率不再上升,其原因是___________ 。
(2)图Ⅱ中,催化效率最高的温度为___________ (填“ ”或“
”或“ ”)点所对应的温度。
”)点所对应的温度。
(3)图Ⅱ中, 点到
点到 点曲线急剧下降,其原因是
点曲线急剧下降,其原因是___________ 。
(4)将装有酶、足量反应物的甲、乙两试管分别放入12℃和75℃的水浴锅内, 后取出,转入25℃的水浴锅中保温,试管中反应速率加快的为
后取出,转入25℃的水浴锅中保温,试管中反应速率加快的为___________ (填“甲”或“乙”)。

(1)图Ⅰ中,反应物达到某一浓度时,反应速率不再上升,其原因是
(2)图Ⅱ中,催化效率最高的温度为
 ”或“
”或“ ”)点所对应的温度。
”)点所对应的温度。(3)图Ⅱ中,
 点到
点到 点曲线急剧下降,其原因是
点曲线急剧下降,其原因是(4)将装有酶、足量反应物的甲、乙两试管分别放入12℃和75℃的水浴锅内,
 后取出,转入25℃的水浴锅中保温,试管中反应速率加快的为
后取出,转入25℃的水浴锅中保温,试管中反应速率加快的为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】CO2催化加氢合成二甲醚(CH3OCH3)是一种CO2转化方法,反应原理为:
2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)
(1)加快该反应速率的措施有___________________ (填两条)。
(2)能证明上述反应达到平衡状态是____ (填标号)。
A.v正(CO2)=3v逆(H2) B.CH3OCH3的浓度不再改变
C.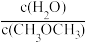 不再变化 D.混合气体的平均相对分子质量不再改变
不再变化 D.混合气体的平均相对分子质量不再改变
(3)某温度下,在体积为2 L的密闭容器中加入2 mol CO2与5 mol H2发生催化反应,经过10 min后CO2的浓度不再变化,测得其体积分数为20%。试计算:
①在0~10 min时段,用CH3OCH3表示的平均反应速率____ 。
②起始状态与平衡状态容器内的压强之比____ 。(无计算过程不给分)
2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)
(1)加快该反应速率的措施有
(2)能证明上述反应达到平衡状态是
A.v正(CO2)=3v逆(H2) B.CH3OCH3的浓度不再改变
C.
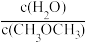 不再变化 D.混合气体的平均相对分子质量不再改变
不再变化 D.混合气体的平均相对分子质量不再改变(3)某温度下,在体积为2 L的密闭容器中加入2 mol CO2与5 mol H2发生催化反应,经过10 min后CO2的浓度不再变化,测得其体积分数为20%。试计算:
①在0~10 min时段,用CH3OCH3表示的平均反应速率
②起始状态与平衡状态容器内的压强之比
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】工业上,常采用氧化还原方法处理尾气中的CO。沥青混凝土可作为反应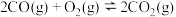 的催化剂。图中表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土(
的催化剂。图中表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土( 型、
型、 型)催化时,
型)催化时, 的转化率与温度的关系。
的转化率与温度的关系。

在a、b、c、d四点中,未达到平衡状态的是___________ (填序号)。
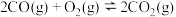 的催化剂。图中表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土(
的催化剂。图中表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土( 型、
型、 型)催化时,
型)催化时, 的转化率与温度的关系。
的转化率与温度的关系。
在a、b、c、d四点中,未达到平衡状态的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】回答下列问题:
(1)在一定条件下,反应H2(g)+Br2(g) 2HBr(g)的△H<0,达到化学平衡状态且其他条件不变时:
2HBr(g)的△H<0,达到化学平衡状态且其他条件不变时:
①如果升高温度,平衡混合物的颜色___________ ;
②体积固定,容器中加入一定量的氢气,化学平衡___________ 移动,α[Br2(g)]___________ (变大、变小)
(2)铬酸钾(K2CrO4)与重铬酸钾(K2Cr2O7)有如下转化:已知重铬酸钾的稀溶液呈橙红色。2CrO (黄色)+2H+
(黄色)+2H+ Cr2O
Cr2O (橙红色)+H2O
(橙红色)+H2O
①向重铬酸钾的稀溶液中加入NaOH,溶液呈___________ 色;
②向(1)的溶液中再加入过量的H2SO4,溶液呈___________ 色;
③向重铬酸钾的稀溶液中加入Ba(NO3)2溶液(BaCrO4为黄色沉淀),平衡向___________ 移动(左,右)
(1)在一定条件下,反应H2(g)+Br2(g)
 2HBr(g)的△H<0,达到化学平衡状态且其他条件不变时:
2HBr(g)的△H<0,达到化学平衡状态且其他条件不变时:①如果升高温度,平衡混合物的颜色
②体积固定,容器中加入一定量的氢气,化学平衡
(2)铬酸钾(K2CrO4)与重铬酸钾(K2Cr2O7)有如下转化:已知重铬酸钾的稀溶液呈橙红色。2CrO
 (黄色)+2H+
(黄色)+2H+ Cr2O
Cr2O (橙红色)+H2O
(橙红色)+H2O①向重铬酸钾的稀溶液中加入NaOH,溶液呈
②向(1)的溶液中再加入过量的H2SO4,溶液呈
③向重铬酸钾的稀溶液中加入Ba(NO3)2溶液(BaCrO4为黄色沉淀),平衡向
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】影响化学平衡的外界因素
若其他条件不变,改变下列条件对化学平衡的影响如下:
若其他条件不变,改变下列条件对化学平衡的影响如下:
改变的条件(其他条件不变) | 化学平衡移动的方向 | ||
| 浓度 | 增大反应物浓度或减小生成物浓度 | 向 | |
| 减小反应物浓度或增大生成物浓度 | 向 | ||
| 压强(对于有气体参加的可逆反应) | 反应前后气体体积改变 | 增大压强 | 向气体分子总数 |
| 减小压强 | 向气体分子总数 | ||
| 反应前后气体体积不变 | 改变压强 | 平衡 | |
| 温度 | 升高温度 | 向 | |
降低温度 | 向 | ||
| 催化剂 | 同等程度地改变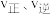 ,平衡不移动 ,平衡不移动 | ||
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】1.已知H2S高温热分解制H2的反应如下:2H2S(g)⇌2H2(g)+S2(g)。在恒容密闭容器中,控制不同温度进行H2S的分解实验。以H2S的起始浓度均为cmol·L-1测定H2S的转化率,结果如图所示。图中曲线a为H2S的平衡转化率与温度关系曲线,曲线b表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。请说明随温度的升高,曲线b向曲线a逼近的原因:___________ 。


您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】甲醇是一种重要的化工原料又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
由图可判断△H____ 0,A、B两点对应的平衡常数关系是KA____ KB(填“>、<、=”)。
(2)某温度下,充分反应后,达到平衡时测得c(CO)=0.02mol/L,则此温度下的平衡常数K=____ 。
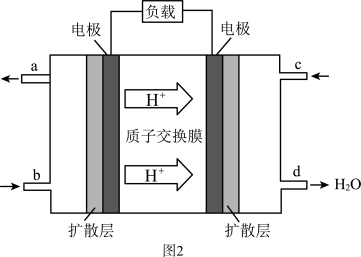
(3)我国在甲醇燃料电池技术方面获得新突破,组装出自呼吸电池及主动式电池。其工作原理如图2所示。该电池工作时,c口通入的物质为___  (填化学式)
(填化学式) ;电池负极的电极反应式为
;电池负极的电极反应式为____ 。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g)
 CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
由图可判断△H
(2)某温度下,充分反应后,达到平衡时测得c(CO)=0.02mol/L,则此温度下的平衡常数K=
(3)我国在甲醇燃料电池技术方面获得新突破,组装出自呼吸电池及主动式电池。其工作原理如图2所示。该电池工作时,c口通入的物质为
 (填化学式)
(填化学式) ;电池负极的电极反应式为
;电池负极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】(1).用合成气生成甲醇的反应:CO(g)+2H2(g)  CH3OH(g) ΔH,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200 ℃时n(H2)随时间的变化如下表所示:
CH3OH(g) ΔH,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200 ℃时n(H2)随时间的变化如下表所示:
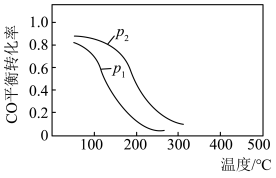
①ΔH________ (填“>”“<”或“= ”)0。
②写出一条可同时提高反应速率和CO转化率的措施:________________________ 。
③下列说法正确的是________ (填字母)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
④0~3 min内用CH3OH表示的反应速率v(CH3OH)=__________________ 。
⑤ 200 ℃时,该反应的平衡常数K=________ 。向上述200 ℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡________ (填“正向”“逆向”或“不”)移动。
 CH3OH(g) ΔH,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200 ℃时n(H2)随时间的变化如下表所示:
CH3OH(g) ΔH,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200 ℃时n(H2)随时间的变化如下表所示:
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①ΔH
②写出一条可同时提高反应速率和CO转化率的措施:
③下列说法正确的是
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
④0~3 min内用CH3OH表示的反应速率v(CH3OH)=
⑤ 200 ℃时,该反应的平衡常数K=
您最近一年使用:0次



