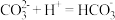下列说法正确的是
A.70℃时,纯水的 ,显酸性 ,显酸性 |
B.常温下,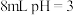 的醋酸溶液中加入 的醋酸溶液中加入 的 的 溶液,混合液 溶液,混合液 |
C.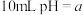 的HA溶液加蒸馏水稀释至 的HA溶液加蒸馏水稀释至 ,若 ,若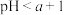 ,则 ,则 为弱酸 为弱酸 |
D.等体积等 的稀硫酸和醋酸分别与等浓度的 的稀硫酸和醋酸分别与等浓度的 溶液反应至中性,消耗 溶液反应至中性,消耗 溶液的体积前者小于后者 溶液的体积前者小于后者 |
更新时间:2024-03-11 15:58:27
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】在某温度时,水的离子积为1×10-12 mol2·L-2,若该温度下某溶液中H+浓度为1×10-7 mol·L-1,则该溶液( )
①呈碱性 ②呈酸性 ③c(H+)=100c(OH-) ④c(OH-)=100c(H+) ⑤呈中性
①呈碱性 ②呈酸性 ③c(H+)=100c(OH-) ④c(OH-)=100c(H+) ⑤呈中性
| A.①④ | B.② |
| C.②③ | D.⑤ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,一定浓度的某溶液由水电离出的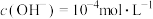 ,则该溶液中的溶质可能是
,则该溶液中的溶质可能是
① ②
② ③NaOH ④
③NaOH ④
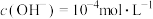 ,则该溶液中的溶质可能是
,则该溶液中的溶质可能是①
 ②
② ③NaOH ④
③NaOH ④
| A.①②③④ | B.②③ | C.①②④ | D.①④ |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关电解质溶液的叙述正确的是

A.将稀氨水逐滴加入稀硫酸中,当溶液 , , |
B.两种醋酸溶液的物质的量浓度分别为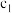 和 和 ,pH分别为a和 ,pH分别为a和 ,则 ,则 |
C. 的NaOH溶液与 的NaOH溶液与 的醋酸溶液等体积混合,滴入石蕊溶液呈蓝色 的醋酸溶液等体积混合,滴入石蕊溶液呈蓝色 |
D.向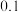  的氨水中加入少量硫酸铵固体,则溶液中 的氨水中加入少量硫酸铵固体,则溶液中 增大 增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】在相同温度下,有两种较稀的醋酸溶液A和B。A溶液中c(CH3COOH)=a mol·L-1,电离度为α1,B溶液中c(CH3COO-)=a mol·L-1,电离度为α2。下列叙述中正确的是( )
A.B溶液中c(CH3COOH)=  mol·L-1 mol·L-1 |
| B.A溶液的pH值小于B溶液的pH值 |
| C.α2>α1 |
| D.A溶液的c(H+)是B溶液c(H+)的0.5α1倍 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
| A.NaHCO3溶液中:c(H+)=c(OH-)+c(H2CO3) |
| B.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| C.0.1mol/L Na2CO3与0.1mol/L NaHCO3溶液等体积混合: 2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3) |
| D.0.1mol/L Na2C2O4与0.1mol/L 的盐酸等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结 论 |
| A | 向一定浓度的Na2SiO3 溶液中通入适量CO2 气体, 出现白色沉淀。 | H2SiO3 的酸性比H2CO3的酸性强 |
| B | 将少量Fe(NO3)2加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液,溶液变成血红色 | Fe(NO3)2已变质 |
| C | 室温下,测得:0.1mol·L-1 Na2SO3溶液的pH约为10;0.1mol·L-1 NaHSO3溶液的pH约为5。 | HSO3- 结合H+ 的能力比SO32-的强 |
| D | 分别向25mL冷水和25mL沸水中滴入6滴FeCl3 饱和溶液,前者为黄色,后者为红褐色。 | 温度升高,Fe3+的水解程度增大 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】HA是一元酸,下列说法不正确的是
| A.25℃时,若测得0.01 mol∙L−1NaA溶液pH>7,则HA是弱酸 |
| B.体积相同、浓度相同的HA溶液与NaOH溶液恰好完全反应,则HA是弱酸 |
| C.25℃时,若测得0.01 mol∙L−1HA溶液pH>2且pH<7,则HA是弱酸 |
| D.0.1 mol∙L−1HA溶液与0.1 mol∙L−1NaOH溶液混合呈中性,则c(Na+)=c(A﹣) |
您最近半年使用:0次


 的
的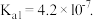 室温下,
室温下,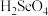 存在以下电离过程:
存在以下电离过程: ;
; ,
, 下列相关叙述正确的是
下列相关叙述正确的是 溶液和
溶液和 溶液均显碱性
溶液均显碱性
 溶液中加入少量
溶液中加入少量