《化学世界》刊载了我国科学家的研究成果:在钴锰氧化物 的催化作用下,偶氮桥联二呋咱高能炸药也可作固体火箭推进剂,M是合成该推进剂的中间体,M的结构简式如图所示。回答下列问题:
的催化作用下,偶氮桥联二呋咱高能炸药也可作固体火箭推进剂,M是合成该推进剂的中间体,M的结构简式如图所示。回答下列问题:

(1)中间体M分子中,碳原子的杂化类型是___________ 。
(2)Co和Ni都属于第Ⅷ族元素,均能与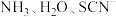 等配体组成配合物。
等配体组成配合物。
①一种Ni2+配离子的结构如图所示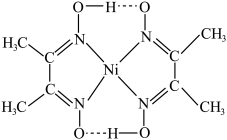 ,该配离子中存在的化学键类型有
,该配离子中存在的化学键类型有___________ (填标号)。
A.离子键B.σ键C.π键D.氢键E.配位键
②SCN-与金属离子形成的配合物中配位原子一般是S而不是N,其原因是___________ 。
(3)比较熔点大小:CoO___________ MnO(填“<”,“=”或“>”)
(4)KMnF3晶体有钻钛矿型的立方结构,晶胞结构如图1所示。
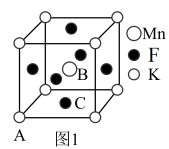
①若原子坐标参数A为(0,0,0);B为(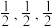 ),则C原子的坐标参数为
),则C原子的坐标参数为___________ 。
②若阿伏加德罗常数的值为NA,晶胞参数为anm,则晶体密度为___________ g∙cm-3。
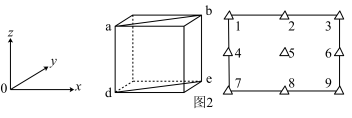
③在KMnF3晶胞结构的另一种表示中,Mn处于各顶角位置。该晶胞结构中,沿立方格子对角面取得的截图如图2所示。F在晶胞中的位置为___________ (填阿拉伯数字序号)。
 的催化作用下,偶氮桥联二呋咱高能炸药也可作固体火箭推进剂,M是合成该推进剂的中间体,M的结构简式如图所示。回答下列问题:
的催化作用下,偶氮桥联二呋咱高能炸药也可作固体火箭推进剂,M是合成该推进剂的中间体,M的结构简式如图所示。回答下列问题:
(1)中间体M分子中,碳原子的杂化类型是
(2)Co和Ni都属于第Ⅷ族元素,均能与
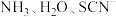 等配体组成配合物。
等配体组成配合物。①一种Ni2+配离子的结构如图所示
 ,该配离子中存在的化学键类型有
,该配离子中存在的化学键类型有A.离子键B.σ键C.π键D.氢键E.配位键
②SCN-与金属离子形成的配合物中配位原子一般是S而不是N,其原因是
(3)比较熔点大小:CoO
(4)KMnF3晶体有钻钛矿型的立方结构,晶胞结构如图1所示。

①若原子坐标参数A为(0,0,0);B为(
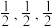 ),则C原子的坐标参数为
),则C原子的坐标参数为②若阿伏加德罗常数的值为NA,晶胞参数为anm,则晶体密度为
③在KMnF3晶胞结构的另一种表示中,Mn处于各顶角位置。该晶胞结构中,沿立方格子对角面取得的截图如图2所示。F在晶胞中的位置为

更新时间:2024-03-22 20:46:07
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】砷化镓是继硅之后研究最深入、应用最广泛的半导体材料。回答下列问题:
(1) As基态原子核外有_______ 个未成对电子。
(2)Ga、As、Se的第一电离能由大到小的顺序是_______ 。
(3)比较表中镓的卤化物的熔点和沸点,分析其变化规律及原因:_______ 。
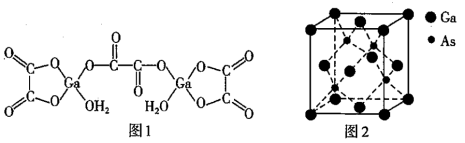
(4)二水合草酸镓的结构如图1所示,其中镓原子的配位数为_______ ,草酸根离子中碳原子的杂化轨道类型为_______ 。
(5)砷化镓的立方晶胞结构如图2(其中灰球应为Ga)所示,晶胞参数为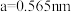 ,砷化镓晶体的密度为
,砷化镓晶体的密度为_______  (设NA为阿伏加德罗常数的值,列出计算式即可)。
(设NA为阿伏加德罗常数的值,列出计算式即可)。
(1) As基态原子核外有
(2)Ga、As、Se的第一电离能由大到小的顺序是
(3)比较表中镓的卤化物的熔点和沸点,分析其变化规律及原因:
| 镓的卤化物 | GaCl3 | GaBr3 | GaI3 |
| 熔点/℃ | 77.75 | 122.3 | 211.5 |
| 沸点/℃ | 201.5 | 279 | 346 |
(5)砷化镓的立方晶胞结构如图2(其中灰球应为Ga)所示,晶胞参数为
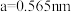 ,砷化镓晶体的密度为
,砷化镓晶体的密度为 (设NA为阿伏加德罗常数的值,列出计算式即可)。
(设NA为阿伏加德罗常数的值,列出计算式即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】用黄铜矿(主要成分是CuFeS2)生产粗铜的反应原理如下:
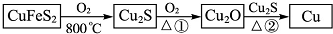
(1)已知在反应①、②中均生成相同的气体分子,该气体具有漂白性。请分别写出反应①、②的化学方程式________________ 、__________________ 。
(2)基态铜原子的核外电子排布式为____________ ,硫、氧元素相比,第一电离能较大的是______ 。
(3)反应①和②生成的气体分子的中心原子的杂化类型是______ ,分子的空间构型是______ 。
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键________________ 。
(5)Cu2O的晶胞结构如图所示,该晶胞的边长为a cm,则Cu2O的密度为__________ g·cm-3(用NA表示阿伏伽德罗常数的数值)。

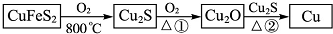
(1)已知在反应①、②中均生成相同的气体分子,该气体具有漂白性。请分别写出反应①、②的化学方程式
(2)基态铜原子的核外电子排布式为
(3)反应①和②生成的气体分子的中心原子的杂化类型是
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键
(5)Cu2O的晶胞结构如图所示,该晶胞的边长为a cm,则Cu2O的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】氟化镁钾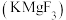 是一种具有优良光学性能的材料,其晶胞结构如图。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。
是一种具有优良光学性能的材料,其晶胞结构如图。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。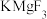 晶体中,每个
晶体中,每个 周围有
周围有__________ 个距离最近的 。
。
②已知晶胞棱长为a nm,则该晶胞的密度为__________  (用含a的代数式表示计算结果,
(用含a的代数式表示计算结果, ,
,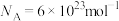 ,下同)。
,下同)。
③已知 与
与 离子半径相近,从原子结构角度解释原因
离子半径相近,从原子结构角度解释原因__________ 。
(2) 半径与
半径与 接近,将
接近,将 部分由
部分由 取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
①基态 中未成对的电子数为
中未成对的电子数为__________ 。
②某实验室合成新型催化剂材料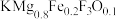 (
( 是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。若要合成厚度为
是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。若要合成厚度为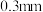 、面积为
、面积为 的催化剂材料,理论上需要掺杂的
的催化剂材料,理论上需要掺杂的 约为
约为__________ mol。
(3)我国科研工作者以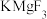 晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的
晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的 晶体。其框架中的
晶体。其框架中的 由
由 取代,
取代, 位置嵌入有机阳离子
位置嵌入有机阳离子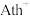 ,
, 位置沿棱方向嵌入直线型
位置沿棱方向嵌入直线型 。
。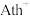 与
与 的结构简式分别为
的结构简式分别为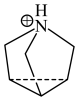 和
和 。
。
① 中心N原子的杂化方式为
中心N原子的杂化方式为__________ 。
② 的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在其他相互作用,如邻近的
的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在其他相互作用,如邻近的 与
与 间还存在
间还存在__________ ,上述相互作用不会随 的转动改变。
的转动改变。
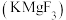 是一种具有优良光学性能的材料,其晶胞结构如图。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。
是一种具有优良光学性能的材料,其晶胞结构如图。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。 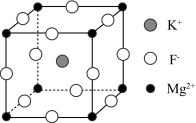
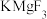 晶体中,每个
晶体中,每个 周围有
周围有 。
。②已知晶胞棱长为a nm,则该晶胞的密度为
 (用含a的代数式表示计算结果,
(用含a的代数式表示计算结果, ,
,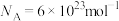 ,下同)。
,下同)。③已知
 与
与 离子半径相近,从原子结构角度解释原因
离子半径相近,从原子结构角度解释原因(2)
 半径与
半径与 接近,将
接近,将 部分由
部分由 取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。①基态
 中未成对的电子数为
中未成对的电子数为②某实验室合成新型催化剂材料
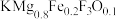 (
( 是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。若要合成厚度为
是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。若要合成厚度为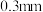 、面积为
、面积为 的催化剂材料,理论上需要掺杂的
的催化剂材料,理论上需要掺杂的 约为
约为(3)我国科研工作者以
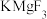 晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的
晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的 晶体。其框架中的
晶体。其框架中的 由
由 取代,
取代, 位置嵌入有机阳离子
位置嵌入有机阳离子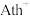 ,
, 位置沿棱方向嵌入直线型
位置沿棱方向嵌入直线型 。
。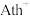 与
与 的结构简式分别为
的结构简式分别为 和
和 。
。①
 中心N原子的杂化方式为
中心N原子的杂化方式为②
 的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在其他相互作用,如邻近的
的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在其他相互作用,如邻近的 与
与 间还存在
间还存在 的转动改变。
的转动改变。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】三氯化六氨合钴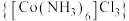 是一种橙黄色晶体,可溶于水和稀酸溶液、不溶于乙醇,与热的强碱溶液反应产生
是一种橙黄色晶体,可溶于水和稀酸溶液、不溶于乙醇,与热的强碱溶液反应产生 、
、 .某实验小组利用下列方法制备
.某实验小组利用下列方法制备 并测定其组成.
并测定其组成.
I.制备晶体:
向锥形瓶中加入适量研细的 、
、 和蒸馏水.加热溶解后加入活性炭催化剂.冷却,加入浓氨水,继续冷却至10℃以下,缓慢加入双氧水,水浴加热至60℃左右并恒温20min,然后用冰水冷却,生成产品沉淀.抽滤,将沉淀溶解于50mL沸热的稀盐酸中,趁热过滤.在滤液中缓慢加入浓盐酸,立即有大量橙黄色晶体析出,冷却、过滤、洗涤、干燥.
和蒸馏水.加热溶解后加入活性炭催化剂.冷却,加入浓氨水,继续冷却至10℃以下,缓慢加入双氧水,水浴加热至60℃左右并恒温20min,然后用冰水冷却,生成产品沉淀.抽滤,将沉淀溶解于50mL沸热的稀盐酸中,趁热过滤.在滤液中缓慢加入浓盐酸,立即有大量橙黄色晶体析出,冷却、过滤、洗涤、干燥.
Ⅱ.测定晶体组成:
(ⅰ)氨含量的测定(装置如图所示):
称取 样品于锥形瓶中,加水溶解.在另一锥形瓶中加入
样品于锥形瓶中,加水溶解.在另一锥形瓶中加入 标准HCl溶液并置于冰水浴中.从漏斗中加入足量20%的NaOH溶液,加热,保持微沸状态并持续1小时左右.然后取出插入标准HCl溶液中的导管,用纯水冲洗导管内外,洗涤液并入装有标准HCl溶液的锥形瓶中.取出锥形瓶,加入指示剂,用
标准HCl溶液并置于冰水浴中.从漏斗中加入足量20%的NaOH溶液,加热,保持微沸状态并持续1小时左右.然后取出插入标准HCl溶液中的导管,用纯水冲洗导管内外,洗涤液并入装有标准HCl溶液的锥形瓶中.取出锥形瓶,加入指示剂,用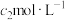 NaOH标准溶液滴定剩余的HCl,达到滴定终点时消耗NaOH标准溶液
NaOH标准溶液滴定剩余的HCl,达到滴定终点时消耗NaOH标准溶液 .
.

(ⅱ)钴含量的测定:
将上述左侧锥形瓶内样品残渣转移到碘量瓶中,冷却后加入足量KI溶液,立即盖上瓶塞并充分振荡后,加入浓盐酸,在暗处放置15min(还原产物为 )。然后加入蒸馏水和淀粉溶液,用
)。然后加入蒸馏水和淀粉溶液,用 标准溶液滴定至终点,记录消耗
标准溶液滴定至终点,记录消耗 标准溶液的体积(已知:
标准溶液的体积(已知: )。
)。
回答下列问题:
(1)制备实验中,生成 的化学方程式为
的化学方程式为______ 。
(2)“水浴加热至60℃”的原因为______ ;“洗涤”时适宜选择的洗涤剂为______ 。
(3)由氨含量的测定实验,可得样品中氨的质量分数为______ (用含 、
、 、
、 、
、 、m的代数式表示);若省略“纯水冲洗导管内外”,会使测定结果
、m的代数式表示);若省略“纯水冲洗导管内外”,会使测定结果______ (填“偏高”、“偏低”或“无影响”)。
(4)钴含量的测定实验中,含钴粒子发生反应的离子方程式为______ ;滴定终点时溶液颜色的变化为______ 。
(5)小组成员查阅资料得知,若不加活性炭催化剂,制备产物主要是 。现有10mL浓度为
。现有10mL浓度为 的
的 或
或 溶液,请设计实验区分:
溶液,请设计实验区分:______ 。
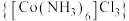 是一种橙黄色晶体,可溶于水和稀酸溶液、不溶于乙醇,与热的强碱溶液反应产生
是一种橙黄色晶体,可溶于水和稀酸溶液、不溶于乙醇,与热的强碱溶液反应产生 、
、 .某实验小组利用下列方法制备
.某实验小组利用下列方法制备 并测定其组成.
并测定其组成.I.制备晶体:
向锥形瓶中加入适量研细的
 、
、 和蒸馏水.加热溶解后加入活性炭催化剂.冷却,加入浓氨水,继续冷却至10℃以下,缓慢加入双氧水,水浴加热至60℃左右并恒温20min,然后用冰水冷却,生成产品沉淀.抽滤,将沉淀溶解于50mL沸热的稀盐酸中,趁热过滤.在滤液中缓慢加入浓盐酸,立即有大量橙黄色晶体析出,冷却、过滤、洗涤、干燥.
和蒸馏水.加热溶解后加入活性炭催化剂.冷却,加入浓氨水,继续冷却至10℃以下,缓慢加入双氧水,水浴加热至60℃左右并恒温20min,然后用冰水冷却,生成产品沉淀.抽滤,将沉淀溶解于50mL沸热的稀盐酸中,趁热过滤.在滤液中缓慢加入浓盐酸,立即有大量橙黄色晶体析出,冷却、过滤、洗涤、干燥.Ⅱ.测定晶体组成:
(ⅰ)氨含量的测定(装置如图所示):
称取
 样品于锥形瓶中,加水溶解.在另一锥形瓶中加入
样品于锥形瓶中,加水溶解.在另一锥形瓶中加入 标准HCl溶液并置于冰水浴中.从漏斗中加入足量20%的NaOH溶液,加热,保持微沸状态并持续1小时左右.然后取出插入标准HCl溶液中的导管,用纯水冲洗导管内外,洗涤液并入装有标准HCl溶液的锥形瓶中.取出锥形瓶,加入指示剂,用
标准HCl溶液并置于冰水浴中.从漏斗中加入足量20%的NaOH溶液,加热,保持微沸状态并持续1小时左右.然后取出插入标准HCl溶液中的导管,用纯水冲洗导管内外,洗涤液并入装有标准HCl溶液的锥形瓶中.取出锥形瓶,加入指示剂,用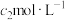 NaOH标准溶液滴定剩余的HCl,达到滴定终点时消耗NaOH标准溶液
NaOH标准溶液滴定剩余的HCl,达到滴定终点时消耗NaOH标准溶液 .
.
(ⅱ)钴含量的测定:
将上述左侧锥形瓶内样品残渣转移到碘量瓶中,冷却后加入足量KI溶液,立即盖上瓶塞并充分振荡后,加入浓盐酸,在暗处放置15min(还原产物为
 )。然后加入蒸馏水和淀粉溶液,用
)。然后加入蒸馏水和淀粉溶液,用 标准溶液滴定至终点,记录消耗
标准溶液滴定至终点,记录消耗 标准溶液的体积(已知:
标准溶液的体积(已知: )。
)。回答下列问题:
(1)制备实验中,生成
 的化学方程式为
的化学方程式为(2)“水浴加热至60℃”的原因为
(3)由氨含量的测定实验,可得样品中氨的质量分数为
 、
、 、
、 、
、 、m的代数式表示);若省略“纯水冲洗导管内外”,会使测定结果
、m的代数式表示);若省略“纯水冲洗导管内外”,会使测定结果(4)钴含量的测定实验中,含钴粒子发生反应的离子方程式为
(5)小组成员查阅资料得知,若不加活性炭催化剂,制备产物主要是
 。现有10mL浓度为
。现有10mL浓度为 的
的 或
或 溶液,请设计实验区分:
溶液,请设计实验区分:
您最近一年使用:0次
【推荐2】硼、氮、镁、铝、铜等在工业生产中都有广泛的用途。
(1)Cu+基态核外电子排布式为___________ 。
(2)金属Mg、Al 中第一电离能较大的是_________ 。
(3)化合物CH3COO[Cu(NH3)3·CO] 中与Cu+形成配离子的配体为______ (填化学式)。
(4)NH4NO3中N 原子杂化轨道类型为_______ 。C、N、O三种元素的电负性由大到小的顺序为________ ,根据等电子原理,CO分子的结构式为________ 。
(5) 1mol CO(NH2)2·H2O2 (过氧化尿素) 中含有的σ键的数目为_________ 。
(6)氮化硼可用于制造飞机轴承,其晶胞如图所示,则处于晶胞顶点上的原子的配位数为_____ ,若立方氮化硼的密度为ρg/cm3,阿伏伽德罗常数的值为NA,则距离最近的两个N 原子之间的距离为_______ cm。

(1)Cu+基态核外电子排布式为
(2)金属Mg、Al 中第一电离能较大的是
(3)化合物CH3COO[Cu(NH3)3·CO] 中与Cu+形成配离子的配体为
(4)NH4NO3中N 原子杂化轨道类型为
(5) 1mol CO(NH2)2·H2O2 (过氧化尿素) 中含有的σ键的数目为
(6)氮化硼可用于制造飞机轴承,其晶胞如图所示,则处于晶胞顶点上的原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】硼元素对植物生长及人体健康有着十分重要的作用,硼的化合物被广泛应用于新材料制备、生活生产等诸多领域。
(1)下列硼原子电子排布图表示的状态中,能量最低和最高的分别为________ 、________ (填标号)
A.
B.
C.
D.
(2)晶体硼单质能自发呈现出正二十面体的多面体外形,这种性质称为晶体的________ 。
(3)硼元素的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
①B2H6分子结构如图,则B原子的杂化方式为________ 。

②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是________ ,写出一种与氨硼烷互为等电子体的分子________ (填化学式)。
(4)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。
①H3BO3晶体中单元结构如图Ⅰ所示。各单元中的氧原子通过________ 氢键(用“A—B…C”表示,A、B、C表示原子)连结成层状结构,其片层结构如图Ⅱ所示,层与层之间以________ (填作用力名称)相结合构成整个硼酸晶体。

②硼氢化钠中 的键角大小是
的键角大小是________ ,立体构型为________ 。
③根据上述结构判断下列说法正确的是________
a.H3BO3分子的稳定性与氢键有关
b.硼酸晶体有滑腻感,可作润滑剂
c.H3BO3分子中硼原子最外层为8e-稳定结构
d.含1mol H3BO3的晶体中有3 mol氢键
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是________ ;已知晶胞边长为a pm,则磷化硼晶体的密度是________ g·cm-3(列出含a、NA的计算式即可)。

(1)下列硼原子电子排布图表示的状态中,能量最低和最高的分别为
A.

B.

C.

D.

(2)晶体硼单质能自发呈现出正二十面体的多面体外形,这种性质称为晶体的
(3)硼元素的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
①B2H6分子结构如图,则B原子的杂化方式为

②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是
(4)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。
①H3BO3晶体中单元结构如图Ⅰ所示。各单元中的氧原子通过

②硼氢化钠中
 的键角大小是
的键角大小是③根据上述结构判断下列说法正确的是
a.H3BO3分子的稳定性与氢键有关
b.硼酸晶体有滑腻感,可作润滑剂
c.H3BO3分子中硼原子最外层为8e-稳定结构
d.含1mol H3BO3的晶体中有3 mol氢键
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】材料是人类文明进步的阶梯,第ⅢA、ⅣA、VA及过渡元素是组成特殊材料的重要元素。 回答下列问题:
(1) 铬是最硬的金属单质,被称为“不锈钢的添加剂”。写出Cr在周期表中的位置___________ ;其原子核外电子排布的最高能层符号___________ 。
(2)第一电离能介于Al、P之间的第三周期元素有____ 种。GaCl3中心原子的杂化方式为_________ ,写出与GaCl3结构相同的一种等电子体(写离子)______________ 。
(3)一定压强下,将AsH3、NH3和PH3的混合气体降温时,液化先后顺序是____________ ,理由是___________________________________________________ 。
(4)砷的一种氧化物俗称“砒霜”,我国科研人员研究发现砒霜对白血病有明显的治疗作用,其结构如下图所示,“砒霜”的化学式为_________ ,“砒霜”在一定条件下能转化成Na3AsO4,Na3AsO4中阴离子的空间构型为__________________ 。

(5)Fe的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的A~D图中正确的是_______ (填字母标号)。


铁原子的配位数是____________ ,假设铁原子的半径是r cm,该晶体的密度是ρ g/cm3 ,则铁的相对原子质量为___________ (设阿伏加 德罗常数的值为NA)。
(1) 铬是最硬的金属单质,被称为“不锈钢的添加剂”。写出Cr在周期表中的位置
(2)第一电离能介于Al、P之间的第三周期元素有
(3)一定压强下,将AsH3、NH3和PH3的混合气体降温时,液化先后顺序是
(4)砷的一种氧化物俗称“砒霜”,我国科研人员研究发现砒霜对白血病有明显的治疗作用,其结构如下图所示,“砒霜”的化学式为

(5)Fe的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的A~D图中正确的是


铁原子的配位数是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】近年来,有机-无机杂化金属卤素钙钛矿作为优良的光电材料受到广泛研究和关注,回答下列问题。
(1) Ca、Ti元素基态原子核外电子占据能级数之比为___________ ,与 Ti 处于同周期单电子数与Ti相同的元素还有___________ 种,Ca的前三级电离能数据分别为589.8 kJ/mol、1145.4 kJ/mol、4912.4 kJ/mol,第三电离能增大较多的原因是___________ 。
(2)卤族元素可与N和P元素形成多种稳定卤化物,其中NCl3分子构型为___________ , P元素可形成稳定的PCl3和PCl5,而氮元素只存在稳定的NCl3,理由是___________ 。
(3)Ti的配合物有多种。Ti(CO)6、Ti(H2O) 、TiF
、TiF 中的配体所含原子中电负性最小的是
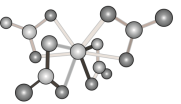
中的配体所含原子中电负性最小的是___________ ;Ti(NO3)4的球棍结构如图,Ti4+的配位数是___________ 。
(4)研究表明,TiO2通过氮掺杂反应生成TiO2-aNb,能使TiO2对可见光具有活性,反应如图所示。
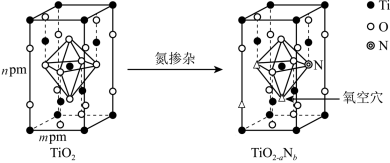
已知TiO2晶胞为长方体,设阿伏加德罗常数的值为NA,TiO2的密度为___________ g/cm3(列出计算式)。TiO2-aNb晶体中a=___________ ,b=___________ 。
(1) Ca、Ti元素基态原子核外电子占据能级数之比为
(2)卤族元素可与N和P元素形成多种稳定卤化物,其中NCl3分子构型为
(3)Ti的配合物有多种。Ti(CO)6、Ti(H2O)
 、TiF
、TiF 中的配体所含原子中电负性最小的是
中的配体所含原子中电负性最小的是
(4)研究表明,TiO2通过氮掺杂反应生成TiO2-aNb,能使TiO2对可见光具有活性,反应如图所示。

已知TiO2晶胞为长方体,设阿伏加德罗常数的值为NA,TiO2的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】第四周期有18种元素,其相关化合物在化工、医药、材料等领域均有着广泛的应用。请回答下列问题:
(1)基态钙原子核外电子云形状为____________ ,电子占据的最高能层符号是____________ 。
(2)五氧化二钒(V2O5)是硫酸工业中重要的催化剂,基态钒原子的价电子排布式为____________ 。
(3)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,其中“亚铁”是关键成分,K3[Fe(CN)6]溶液是检验Fe2+的试剂,1molCN-中含π键的数目为____________ ,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是____________ 。
(4)镓、锗、砷、硒的第一电离能由大到小的顺序为____________ (用元素符号表示);其中锗的化合物四氯化锗可用作光导纤维渗杂剂,其熔点为-49.5℃,沸点为83.1℃,则其晶体类型为____________ ,中心原子的杂化类型为____________ ;砷酸酸性弱于硒酸,从分子结构的角度解释原因____________ ;砷化硼是一种新型材料,或成为最好的热导体,其结构与金刚石相似,已知砷化硼晶胞参数为bpm,则该晶体的密度为____________ g ·cm-3。(NA表示阿伏伽德罗常数的值)。
(1)基态钙原子核外电子云形状为
(2)五氧化二钒(V2O5)是硫酸工业中重要的催化剂,基态钒原子的价电子排布式为
(3)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,其中“亚铁”是关键成分,K3[Fe(CN)6]溶液是检验Fe2+的试剂,1molCN-中含π键的数目为
(4)镓、锗、砷、硒的第一电离能由大到小的顺序为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】硅和卤素单质反应可以得到SiX4。
SX4的熔沸点
①0℃时,SiF4、SiCl4、SiBr4、SiI4呈液态的是___________ (填化学式),沸点依次升高的原因是___________ ,气态SiX4分子的空间构型是___________ ;
②SiCl4与N﹣甲基咪唑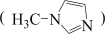 反应可以得到M2+,其结构如图所示:
反应可以得到M2+,其结构如图所示:
N-甲基咪唑分子中碳原子的杂化轨道类型为___________ ,H、C、N的电负性由大到小的顺序为___________ ,1个M2+中含有___________ 个σ键;
SX4的熔沸点
| SiF4 | SiCl4 | SiBr4 | SiI4 | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
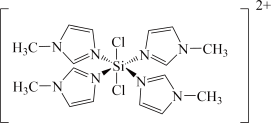
②SiCl4与N﹣甲基咪唑
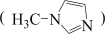 反应可以得到M2+,其结构如图所示:
反应可以得到M2+,其结构如图所示:
N-甲基咪唑分子中碳原子的杂化轨道类型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】钙钛矿( )型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
(2)下表列出了 的四卤化物的熔点,分析发现
的四卤化物的熔点,分析发现 熔点明显高于其他三种卤化物,而
熔点明显高于其他三种卤化物,而 、
、 、
、 的熔点依次升高,请解释原因
的熔点依次升高,请解释原因_______ 。
(3)① 的立方晶胞如图所示,与
的立方晶胞如图所示,与 最邻近等距离的氧离子构成的几何图为
最邻近等距离的氧离子构成的几何图为_______ 。

②若设晶胞边长为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,
, 的摩尔质量为
的摩尔质量为 ,则
,则 与最近的
与最近的 间的距离为
间的距离为_______  ,该晶体密度为
,该晶体密度为_______  (填含a的表达式)。
(填含a的表达式)。
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为 、
、 和有机碱离子
和有机碱离子 ,其晶胞如图所示。
,其晶胞如图所示。

①其中 为
为 ,另两种离子为
,另两种离子为 和
和 ,则
,则 离子为
离子为_______ 。
② 中,存在的化学键有
中,存在的化学键有_______ (填标号)。
A.共价键 B. 离子键 C. 金属键 D. 配位键 E. 氢键
③如图b所示,晶胞中 离子的分数坐标为
离子的分数坐标为 ,则
,则 的分数坐标为
的分数坐标为_______ , 的分数坐标为
的分数坐标为_______ ( 的任写一个即可)。
的任写一个即可)。
 )型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为(2)下表列出了
 的四卤化物的熔点,分析发现
的四卤化物的熔点,分析发现 熔点明显高于其他三种卤化物,而
熔点明显高于其他三种卤化物,而 、
、 、
、 的熔点依次升高,请解释原因
的熔点依次升高,请解释原因| 化合物 |  |  |  |  |
熔点/ | 377 | -24.12 | 38.3 | 155 |
 的立方晶胞如图所示,与
的立方晶胞如图所示,与 最邻近等距离的氧离子构成的几何图为
最邻近等距离的氧离子构成的几何图为
②若设晶胞边长为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,
, 的摩尔质量为
的摩尔质量为 ,则
,则 与最近的
与最近的 间的距离为
间的距离为 ,该晶体密度为
,该晶体密度为 (填含a的表达式)。
(填含a的表达式)。(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为
 、
、 和有机碱离子
和有机碱离子 ,其晶胞如图所示。
,其晶胞如图所示。
①其中
 为
为 ,另两种离子为
,另两种离子为 和
和 ,则
,则 离子为
离子为②
 中,存在的化学键有
中,存在的化学键有A.共价键 B. 离子键 C. 金属键 D. 配位键 E. 氢键
③如图b所示,晶胞中
 离子的分数坐标为
离子的分数坐标为 ,则
,则 的分数坐标为
的分数坐标为 的分数坐标为
的分数坐标为 的任写一个即可)。
的任写一个即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E、F、G是原子序数依次增大的前四周期元素,A元素原子核外电子只有一种自旋取向,A、B元素原子的最外层电子数相等;C元素原子核外s能级上的电子总数与p能级上的电子总数相等;D元素原子半径是短周期主族元素中最大的;E元素的价层电子在s和p能级的原子轨道中运动的电子数相等; 与F元素的基态原子均有5个未成对电子。请回答下列问题:
与F元素的基态原子均有5个未成对电子。请回答下列问题:
(1)若A离子与B离子的电子层结构相同,半径较大的是___________ (填离子符号),A与B形成的二元化合物的晶体类型为___________ 。
(2)比较第一电离能的大小:I1(B)___________ (填“>”、“<”或“=”)I1(D),原因是___________ 。
(3)晶体熔点:
___________ (填“高于”、“低于”或“等于”)DCA。
(4)基态G原子的价层电子排布式为___________ ,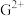 与
与 的未成对电子数之比为
的未成对电子数之比为___________ 。
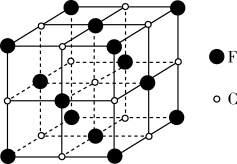
(5)基态F原子含有___________ 种空间运动状态不同的电子。C和F形成的一种化合物的立方晶胞如图所示,则该化合物的化学式为___________ 。
 与F元素的基态原子均有5个未成对电子。请回答下列问题:
与F元素的基态原子均有5个未成对电子。请回答下列问题:(1)若A离子与B离子的电子层结构相同,半径较大的是
(2)比较第一电离能的大小:I1(B)
(3)晶体熔点:

(4)基态G原子的价层电子排布式为
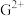 与
与 的未成对电子数之比为
的未成对电子数之比为(5)基态F原子含有

您最近一年使用:0次



