生产钛的方法之一是将金红石(TiO2)转化为 ,再进一步还原得到钛。
,再进一步还原得到钛。 转化为
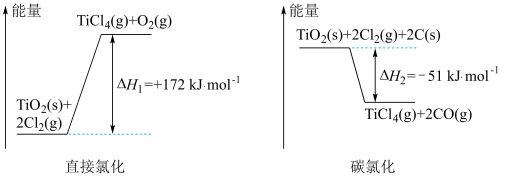
转化为 有直接氯化法和碳氯化法,相关能量示意图如图所示。下列说法不正确的是
有直接氯化法和碳氯化法,相关能量示意图如图所示。下列说法不正确的是
 ,再进一步还原得到钛。
,再进一步还原得到钛。 转化为
转化为 有直接氯化法和碳氯化法,相关能量示意图如图所示。下列说法不正确的是
有直接氯化法和碳氯化法,相关能量示意图如图所示。下列说法不正确的是
| A.将反应物固体粉碎可以加快直接氯化的反应速率 |
B.可推知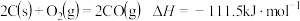 |
| C.判断直接氯化反应能否自发进行需要综合考虑体系的焓变和熵变 |
D.对于碳氯化反应,温度升高,平衡时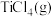 的产率变小 的产率变小 |
更新时间:2024-03-25 16:20:27
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】用 催化还原
催化还原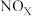 可以消除氮氧化物的污染,例如:
可以消除氮氧化物的污染,例如:
①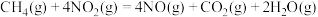
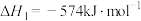
②

已知NO、 混合气体的密度是相同条件下氢气密度的17倍,16g甲烷和该混合气完全反应生成
混合气体的密度是相同条件下氢气密度的17倍,16g甲烷和该混合气完全反应生成 、
、 、
、 放出1042.8kJ的热量,则
放出1042.8kJ的热量,则 等于
等于
 催化还原
催化还原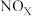 可以消除氮氧化物的污染,例如:
可以消除氮氧化物的污染,例如:①
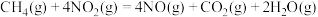
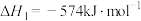
②


已知NO、
 混合气体的密度是相同条件下氢气密度的17倍,16g甲烷和该混合气完全反应生成
混合气体的密度是相同条件下氢气密度的17倍,16g甲烷和该混合气完全反应生成 、
、 、
、 放出1042.8kJ的热量,则
放出1042.8kJ的热量,则 等于
等于A.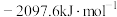 | B.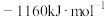 |
C.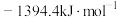 | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知氢气和碳燃烧的热化学方程式为:
①2H2(g)+O2(g)=2H2O(l)ΔH1=-akJ•mol-1
②H2(g)+ O2(g)=H2O(g)ΔH2=-bkJ•mol-1
O2(g)=H2O(g)ΔH2=-bkJ•mol-1
③C(s)+ O2(g)=CO(g)ΔH3=-ckJ•mol-1
O2(g)=CO(g)ΔH3=-ckJ•mol-1
④C(s)+O2(g)=CO2(g)ΔH4=-dkJ•mol-1
下列说法正确的是( )
①2H2(g)+O2(g)=2H2O(l)ΔH1=-akJ•mol-1
②H2(g)+
 O2(g)=H2O(g)ΔH2=-bkJ•mol-1
O2(g)=H2O(g)ΔH2=-bkJ•mol-1③C(s)+
 O2(g)=CO(g)ΔH3=-ckJ•mol-1
O2(g)=CO(g)ΔH3=-ckJ•mol-1④C(s)+O2(g)=CO2(g)ΔH4=-dkJ•mol-1
下列说法正确的是( )
| A.氢气的摩尔燃烧焓为-bkJ•mol-1 | B.碳的摩尔燃烧焓为-ckJ•mol-1 |
| C.一氧化碳的摩尔燃烧焓为(d-c)kJ•mol-1 | D. a>b a>b |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】已知以下的热化学反应方程式:
Fe2O3(s)+ CO(g)=2/3Fe3O4(s)+
CO(g)=2/3Fe3O4(s)+ CO2(g) ΔH=-15.73kJ/mol
CO2(g) ΔH=-15.73kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH=+640.4kJ/mol
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-24.8kJ/mol
则56gCO气体还原足量FeO固体得到Fe固体和CO2气体时对应的ΔH约为( )
Fe2O3(s)+
 CO(g)=2/3Fe3O4(s)+
CO(g)=2/3Fe3O4(s)+ CO2(g) ΔH=-15.73kJ/mol
CO2(g) ΔH=-15.73kJ/molFe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH=+640.4kJ/mol
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-24.8kJ/mol
则56gCO气体还原足量FeO固体得到Fe固体和CO2气体时对应的ΔH约为( )
| A.-327kJ/mol | B.+327kJ/mol |
| C.+436kJ/mol | D.-436kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】某MOFs多孔材料孔径大小和形状恰好将N2O4“固定”,能高选择性吸附NO2.废气中的NO2被吸附后,经处理能全部转化为HNO3.原理示意图如下。
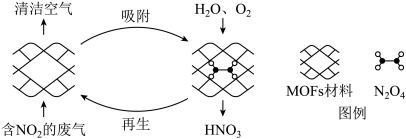
已知:N2O4(g) 2NO2(g)△H>0
2NO2(g)△H>0
下列说法不正确的是

已知:N2O4(g)
 2NO2(g)△H>0
2NO2(g)△H>0下列说法不正确的是
| A.温度升高时利于NO2吸附 |
B.多孔材料“固定”N2O4,促进2NO2(g) N2O4(g)平衡正向移动 N2O4(g)平衡正向移动 |
| C.转化为HNO3的反应是2N2O4+O2+2H2O=4HNO3 |
| D.每获得0.lmol HNO3时,转移电子的数目为6.02×1022 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
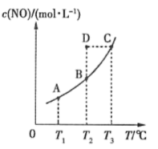
【推荐2】在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应: ,平衡时
,平衡时 与温度T的关系如图所示,则下列说法不正确的是
与温度T的关系如图所示,则下列说法不正确的是
 ,平衡时
,平衡时 与温度T的关系如图所示,则下列说法不正确的是
与温度T的关系如图所示,则下列说法不正确的是
A.该反应的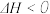 |
B.若该反应在T1、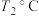 时的平衡常数分别为K1、K2,则K1>K2 时的平衡常数分别为K1、K2,则K1>K2 |
C.在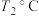 时,若反应体系处于状态D,则此时 时,若反应体系处于状态D,则此时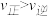 |
D.若状态B、C、D的压强分别为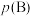 、 、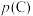 、 、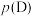 ,则 ,则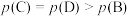 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】常温下,某密闭容器中反应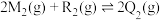 能自发进行。下列有关该反应的说法正确的是
能自发进行。下列有关该反应的说法正确的是
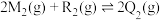 能自发进行。下列有关该反应的说法正确的是
能自发进行。下列有关该反应的说法正确的是| A.化学键断裂时放出热量 |
B.催化剂使正反应的 降低 降低 |
| C.该反应为放热反应 |
| D.若平衡常数不变,则平衡不移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列有关化学反应方向及判据的说法中不正确的是
| A.ΔH>0、ΔS<0的反应在任何温度下都不能自发进行 |
| B.2NaHCO3(s)=Na2CO3+H2O(g)+CO2(g) ΔH>0,该反应加热时能自发进行,原因反应的熵增大 |
| C.焓变和熵变都与反应的自发性有关,但焓变或熵变不可以单独作为反应自发性的判据 |
| D.自发反应就是能较快进行的反应,非自发反应就是无法进行的反应 |
您最近一年使用:0次

 CO(g)+H2(g)
CO(g)+H2(g) 

