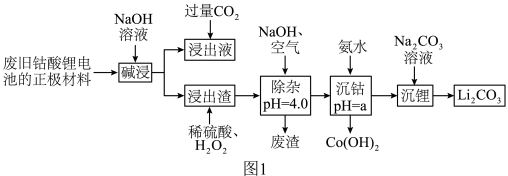
废旧钴酸锂电池的正极材料主要含有难溶于水的LiCoO2及少量Al、Fe、炭黑等,常用如图1所示的一种工艺分离并回收其中的金属钴和锂。
已知:①Ksp[Co(OH)2]=1.0×10-15;
②相关金属离子形成氢氧化物沉淀的pH如下表:
回答下列问题:
(1)LiCoO2中元素Co的化合价为___________ 。
(2)为提高碱浸率,可采取的措施有___________ (答出一条即可)。
(3)碱浸时的离子反应方程式为___________ 。
(4)沉钴的离子方程式为___________ 。
(5)加氨水控制沉钴的pH,当a≥___________ 时,此时溶液中c(Co2+)≤10-5mol⋅L-1,即认为“沉钴”完全。
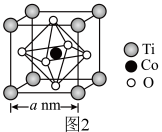
(6)钴的氢氧化物加热至290℃时可以完全脱水,所得产物可用于合成钛酸钴。钛酸钴的晶胞结构如图2所示,则该晶体化学式为___________ 。
(7)[Co(NH3)4(H2O)Cl]Cl2是钴的一种配合物,含1mol该配合物的溶液与足量AgNO3溶液能生成___________ molAgCl,该配合物中Co3+的配位数为___________ 。

已知:①Ksp[Co(OH)2]=1.0×10-15;
②相关金属离子形成氢氧化物沉淀的pH如下表:
| 金属阳离子 | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀的pH | 4.2 | 2.7 | 7.6 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.6 |
(1)LiCoO2中元素Co的化合价为
(2)为提高碱浸率,可采取的措施有
(3)碱浸时的离子反应方程式为
(4)沉钴的离子方程式为
(5)加氨水控制沉钴的pH,当a≥
(6)钴的氢氧化物加热至290℃时可以完全脱水,所得产物可用于合成钛酸钴。钛酸钴的晶胞结构如图2所示,则该晶体化学式为

(7)[Co(NH3)4(H2O)Cl]Cl2是钴的一种配合物,含1mol该配合物的溶液与足量AgNO3溶液能生成
更新时间:2024-03-28 16:19:19
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
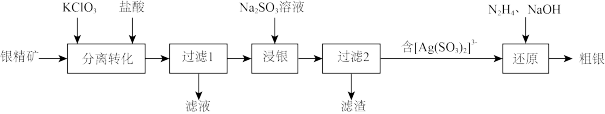
【推荐1】以银精矿(主要成分为Ag2S)为原料采用“预氧化湿法提银”工艺流程如下:
(1)N2H4的电子式为________________________ 。
(2)“分离转化”时,Ag2S转化为AgCl和S的化学方程式为______________ (ClO3-还原为Cl- );为提高Ag2S的转化率可采取的措施是_____________ (列举2条)。已知:Ksp(Ag2S)=1. 6×10-49 ,Ksp(AgCl)=2. 0×10-10 ,若不加KClO3,直接加氯化物,依据反应Ag2S+2Cl- 2AgCl+S2- ,能否实现其较完全转化?并说明理由:
2AgCl+S2- ,能否实现其较完全转化?并说明理由:________________
(3)“浸银”时,发生反应的离子方程式为________________________ 。
(4)“还原”时,2[ Ag(SO3)2]3- +N2H4+2OH -=2Ag↓+4SO32- +N2↑+H2↑+ 2H2O,该反应每生成1 mol Ag转移电子的物质的量为___________ 。

(1)N2H4的电子式为
(2)“分离转化”时,Ag2S转化为AgCl和S的化学方程式为
 2AgCl+S2- ,能否实现其较完全转化?并说明理由:
2AgCl+S2- ,能否实现其较完全转化?并说明理由:(3)“浸银”时,发生反应的离子方程式为
(4)“还原”时,2[ Ag(SO3)2]3- +N2H4+2OH -=2Ag↓+4SO32- +N2↑+H2↑+ 2H2O,该反应每生成1 mol Ag转移电子的物质的量为
您最近半年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】某湿法炼锌的萃余液中含有 、
、 、
、 、
、 、
、 、
、 及30~60
及30~60
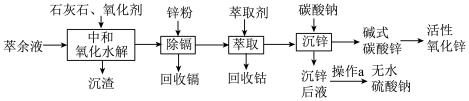
 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
已知:
回答下列问题:
(1)“中和氧化水解”时,先加入适量的石灰石调节溶液的pH为1.0;加入一定量的 ;再加入石灰石调节溶液的pH为4.0。
;再加入石灰石调节溶液的pH为4.0。
①“氧化”时, 转化为
转化为 除去,反应的离子方程式为
除去,反应的离子方程式为________ ,为提高反应速率可采取的措施_______ (举1例)。
②“沉渣”的主要成分除 、
、 外还有
外还有______ 。
③“氧化”时,若加入过量的 ,钴元素将会进入“沉渣”中,则氧化水解后的溶液中含钴微粒浓度为
,钴元素将会进入“沉渣”中,则氧化水解后的溶液中含钴微粒浓度为______  。
。
(2)“除镉”时,主要反应的离子方程式为________ 。
(3)“沉锌”时,在近中性条件下加入 可得碱式碳酸锌[
可得碱式碳酸锌[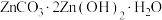 ]固体,同时产生大量的气体。
]固体,同时产生大量的气体。
①产生大量气体的原因是________ 。
②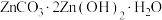 需洗涤,检验是否洗净的试剂是
需洗涤,检验是否洗净的试剂是________ 。
(4)不同质量分数的 溶液在不同温度下析出
溶液在不同温度下析出 晶体的物种如图所示。欲从含20%
晶体的物种如图所示。欲从含20%  及微量杂质的“沉锌后液”中直接析出无水
及微量杂质的“沉锌后液”中直接析出无水 ,“操作a”步骤为
,“操作a”步骤为________ 。

 、
、 、
、 、
、 、
、 、
、 及30~60
及30~60
 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
已知:
| 沉淀物 |  |  |  |  | 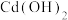 |
 | 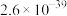 |  | 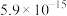 |  | 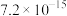 |
(1)“中和氧化水解”时,先加入适量的石灰石调节溶液的pH为1.0;加入一定量的
 ;再加入石灰石调节溶液的pH为4.0。
;再加入石灰石调节溶液的pH为4.0。①“氧化”时,
 转化为
转化为 除去,反应的离子方程式为
除去,反应的离子方程式为②“沉渣”的主要成分除
 、
、 外还有
外还有③“氧化”时,若加入过量的
 ,钴元素将会进入“沉渣”中,则氧化水解后的溶液中含钴微粒浓度为
,钴元素将会进入“沉渣”中,则氧化水解后的溶液中含钴微粒浓度为 。
。(2)“除镉”时,主要反应的离子方程式为
(3)“沉锌”时,在近中性条件下加入
 可得碱式碳酸锌[
可得碱式碳酸锌[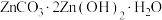 ]固体,同时产生大量的气体。
]固体,同时产生大量的气体。①产生大量气体的原因是
②
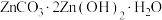 需洗涤,检验是否洗净的试剂是
需洗涤,检验是否洗净的试剂是(4)不同质量分数的
 溶液在不同温度下析出
溶液在不同温度下析出 晶体的物种如图所示。欲从含20%
晶体的物种如图所示。欲从含20%  及微量杂质的“沉锌后液”中直接析出无水
及微量杂质的“沉锌后液”中直接析出无水 ,“操作a”步骤为
,“操作a”步骤为
您最近半年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】我国的钴(Co)资源非常贫乏,一种利用湿法炼锌净化渣回收钴的工艺如下图所示。已知净化渣含有较高的锌、铜、铅、钴元素以及一定量的铁和锰元素,它们大多以金属单质和氧化物的形式存在。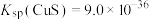 ,
, ,
, 。
。
② 在酸性溶液中有强氧化性
在酸性溶液中有强氧化性
(1)“常压浸出”需加热至70℃左右,宜采用___________ (填序号;①盐酸②硫酸③硝酸)进行酸浸,浸出渣主要成分为___________ 。
(2)大多数金属硫化物都难溶于水,能选择 除铜的原因是
除铜的原因是___________ ,若加入 后溶液中
后溶液中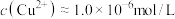 ,
,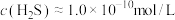 ,则溶液的pH约为
,则溶液的pH约为___________ 。
(3)过二硫酸钠( )氧化Mn2+生成MnO2沉淀,同时生成
)氧化Mn2+生成MnO2沉淀,同时生成 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:___________ 。
(4)根据流程可知:在“沉淀分离”步骤中,还原性Co2+___________ Mn2+(填“强于”或“弱于”);氧化沉淀所得产物为Co(OH)3,最终钴产品是Co(OH)3脱水后的产物,脱水前后质量比为55:46,则钴产品的化学式为___________ 。

 ,
, ,
, 。
。②
 在酸性溶液中有强氧化性
在酸性溶液中有强氧化性(1)“常压浸出”需加热至70℃左右,宜采用
(2)大多数金属硫化物都难溶于水,能选择
 除铜的原因是
除铜的原因是 后溶液中
后溶液中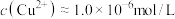 ,
,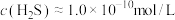 ,则溶液的pH约为
,则溶液的pH约为(3)过二硫酸钠(
 )氧化Mn2+生成MnO2沉淀,同时生成
)氧化Mn2+生成MnO2沉淀,同时生成 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:(4)根据流程可知:在“沉淀分离”步骤中,还原性Co2+
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】铁、钴及其化合物在生活、生产中用途广泛。请回答下列问题:
(1)基态Fe2+的核外电子排布式为_______ ;第四周期元素中,基态原子未成对电子数与Co相等的有_______ (填元素符号)。
(2)CoCl3在氨水中能形成多种配合物。取1molCoCl3·4NH3,加入足量硝酸银溶液,得到1mol白色沉淀。该物质在溶液中形成的配合离子化学式为_______ 。
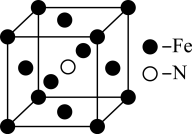
(3)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为_______ 。
(4)钴蓝晶体的立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其结构如下图,设NA为阿伏加德罗常数的值,钴蓝晶体的密度为_______ g/cm3(列计算式)。

(1)基态Fe2+的核外电子排布式为
(2)CoCl3在氨水中能形成多种配合物。取1molCoCl3·4NH3,加入足量硝酸银溶液,得到1mol白色沉淀。该物质在溶液中形成的配合离子化学式为
(3)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为

(4)钴蓝晶体的立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其结构如下图,设NA为阿伏加德罗常数的值,钴蓝晶体的密度为

您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】锰单质及其化合物应用十分广泛。回答下列问题:
(1)基态锰原子的核外电子排布式为_______
(2)MnO和MnS的熔点分别为1650℃和1610℃,前者熔点较高的原因是_______ 。
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。

①THF中与Mn2+形成配位键的原子为_______ (填元素符号)。
②写出一种与BH 互为等电子体的分子
互为等电子体的分子_______ 。
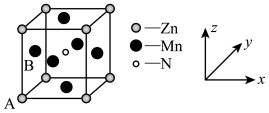
(4)某种含锰特殊材料的晶胞结构如图所示,该晶体的化学式为_______ ;其中原子坐标参数A为(0,0,0),B为(0, ,
, ),则晶胞中氮原子的坐标参数为
),则晶胞中氮原子的坐标参数为_______ 。
(5)金属锰有多种晶型,其中δ−Mn的结构为体心立方堆积,晶胞参数为apm,δ−Mn中锰的原子半径为_______ pm。已知阿伏加德罗常数的值为NA,δ−Mn的理论密度ρ=_______ g∙cm−3 (列出计算式)。
(1)基态锰原子的核外电子排布式为
(2)MnO和MnS的熔点分别为1650℃和1610℃,前者熔点较高的原因是
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。

①THF中与Mn2+形成配位键的原子为
②写出一种与BH
 互为等电子体的分子
互为等电子体的分子(4)某种含锰特殊材料的晶胞结构如图所示,该晶体的化学式为
 ,
, ),则晶胞中氮原子的坐标参数为
),则晶胞中氮原子的坐标参数为
(5)金属锰有多种晶型,其中δ−Mn的结构为体心立方堆积,晶胞参数为apm,δ−Mn中锰的原子半径为
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】有A、B、C、D、E五种元素。其相关信息如下:
回答下列问题:
(1)写出元素符号B:_______ ,C:_______ ,E:_______ 。
(2)F元素可形成F2+和F3+,其中较稳定的是F3+,原因是_______ 。
(3)A和C形成的18电子分子的结构式_______ 。
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有_______ (填序号)。
①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键
[E(CA3)4]2+具有对称的空间构型,若[E(CA3)4]2+中的两个CA3被两个其他基团取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为_______ (填字母)。
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)早在西汉时期的《淮南万毕术》中就记载“曾青得铁则化为铜”,这是有关“湿法炼铜”的最早文献记录。若向盛装有硫酸铜水溶液的试管里加入氨水,首先生成蓝色沉淀,继续滴加氨水,得到深蓝色的透明溶液。请写出蓝色沉淀溶解的离子反应方程式:_______ 。
| 元素 | 相关信息 |
| A | A原子的1s轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道中有三个未成对电子 |
| D | D是主族元素且与E同周期,其最外能层上有两个运动状态不同的电子 |
| E | E能与氧形成砖红色E2O和黑色的EO两种氧化物 |
| F | 基态原子3d能级上有6个电子 |
(1)写出元素符号B:
(2)F元素可形成F2+和F3+,其中较稳定的是F3+,原因是
(3)A和C形成的18电子分子的结构式
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有
①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键
[E(CA3)4]2+具有对称的空间构型,若[E(CA3)4]2+中的两个CA3被两个其他基团取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)早在西汉时期的《淮南万毕术》中就记载“曾青得铁则化为铜”,这是有关“湿法炼铜”的最早文献记录。若向盛装有硫酸铜水溶液的试管里加入氨水,首先生成蓝色沉淀,继续滴加氨水,得到深蓝色的透明溶液。请写出蓝色沉淀溶解的离子反应方程式:
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】铁、钴及其化合物在生活、生产中用途广泛。请回答下列问题:
(1)基态Fe2+的核外电子排布式为_______ ;第四周期元素中,基态原子未成对电子数与Co相等的有_______ (填元素符号)。
(2)CoCl3在氨水中能形成多种配合物。取1molCoCl3·4NH3,加入足量硝酸银溶液,得到1mol白色沉淀。该物质在溶液中形成的配合离子化学式为_______ 。
(3)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为_______ 。

(4)钴蓝晶体的立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其结构如下图,设NA为阿伏加德罗常数的值,钴蓝晶体的密度为_______ g/cm3(列计算式)。

(1)基态Fe2+的核外电子排布式为
(2)CoCl3在氨水中能形成多种配合物。取1molCoCl3·4NH3,加入足量硝酸银溶液,得到1mol白色沉淀。该物质在溶液中形成的配合离子化学式为
(3)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为

(4)钴蓝晶体的立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其结构如下图,设NA为阿伏加德罗常数的值,钴蓝晶体的密度为

您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(-NO2)还原为氨基(-NH2);在苯的溴代反应中用溴化铁作催化剂。
(1)Fe基态原子核外电子排布式为________________________ 。
(2)H、N、O的电负性从小到大的顺序是_________________ 。
(3)与NO 互为等电子体的一种分子为
互为等电子体的一种分子为__________ (填化学式)。氨基(-NH2)中氮原子的杂化类型为_____________ 。
(4)1mol苯胺分子中含有σ键的数目为_____________________ 。
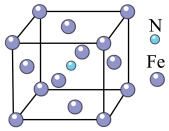
(5)Fe与N形成的某化合物晶胞如图所示,则该晶体的化学式为______________ 。
(1)Fe基态原子核外电子排布式为
(2)H、N、O的电负性从小到大的顺序是
(3)与NO
 互为等电子体的一种分子为
互为等电子体的一种分子为(4)1mol苯胺分子中含有σ键的数目为
(5)Fe与N形成的某化合物晶胞如图所示,则该晶体的化学式为

您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】镍的合金及其配合物用途非常广泛。回答下列问题:
(1)Ni与Ca均位于第四周期,最外层电子数也相同,但Ni的熔点和沸点均比Ca的高,这是因为_______ 。
(2)Ni2 MnGa晶体的立方晶胞结构如图a所示。

①已知Ni2MnGa的晶胞参数为0.5822nm,设NA为阿伏加德罗常数的数值,则Ni2MnGa晶体的密度为_______ (列出计算式)g· cm-3。
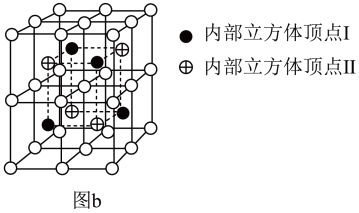
②Ni2MnGa晶体的晶胞结构还可以用图b表示,若●表示的是Mn,则 表示的是
表示的是_______ ,⊕表示的是_______ 。
(1)Ni与Ca均位于第四周期,最外层电子数也相同,但Ni的熔点和沸点均比Ca的高,这是因为
(2)Ni2 MnGa晶体的立方晶胞结构如图a所示。

①已知Ni2MnGa的晶胞参数为0.5822nm,设NA为阿伏加德罗常数的数值,则Ni2MnGa晶体的密度为
②Ni2MnGa晶体的晶胞结构还可以用图b表示,若●表示的是Mn,则
 表示的是
表示的是
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】对羟基苯甲酸乙酯广泛用于食品、化妆品、医药等领域。某化学兴趣小组通过查阅文献制备对羟基苯甲酸乙酯。回答下列问题:
Ⅰ.对羟基苯甲酸乙酯的合成
实验原理: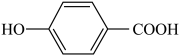 +CH3CH2OH
+CH3CH2OH
 +H2O;对羟基苯甲酸摩尔质量为138g/mol,对羟基苯甲酸乙酯的摩尔质量为166g/mol;
+H2O;对羟基苯甲酸摩尔质量为138g/mol,对羟基苯甲酸乙酯的摩尔质量为166g/mol;
实验步骤:取 乙醇和催化剂置于干燥的仪器A中,
乙醇和催化剂置于干燥的仪器A中, 对羟基苯甲酸置于恒压滴液漏斗C中,实验装置如图所示(加热和夹持装置省略)。加热回流,充分反应。
对羟基苯甲酸置于恒压滴液漏斗C中,实验装置如图所示(加热和夹持装置省略)。加热回流,充分反应。
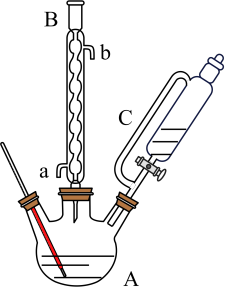
(1)仪器C的名称是____________________ ,仪器B的名称是____________________ 。
(2)某同学对实验装置做出了改进,在仪器A和B之间加一个脱水装置(如图),并在油水分离器(分水器)中预先加水至略低于支管口,加热回流,反应一段时间将水逐渐分去,至反应完毕。
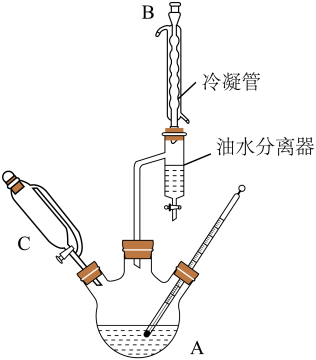
反应中利用分水器将水分去,该操作的目的是:____________________ 。
Ⅱ.对羟基苯甲酸乙酯的精制
实验方法:①反应完毕后趁热滤出催化剂,滤液倒入冷水中,析出固体,过滤。
②固体先后用5%的 溶液和水洗涤,干燥后得到粗产品。
溶液和水洗涤,干燥后得到粗产品。
③在装有冷凝管的圆底烧瓶中,按照一定比例加入粗品酯、乙醇、水和活性炭,加热回流0.5小时,趁热抽滤,滤液冷却,析出白色晶体,于80℃烘干。
(1)在②中用5%的 溶液洗涤的目的是
溶液洗涤的目的是_______ ,能不能用NaOH溶液替代?__________ (填“能”或“不能”)。
(2)在③趁热抽滤主要除去的杂质为___________ ,‘‘趁热”的目的是_________ 。
Ⅲ.该小组同学按0.1mol对羟基苯甲酸、0.4mol乙醇和催化剂2g进行投料,最后得到对羟基苯甲酸乙酯13.9g,则该实验的产率为____________________ 。
Ⅰ.对羟基苯甲酸乙酯的合成
实验原理:
 +CH3CH2OH
+CH3CH2OH
 +H2O;对羟基苯甲酸摩尔质量为138g/mol,对羟基苯甲酸乙酯的摩尔质量为166g/mol;
+H2O;对羟基苯甲酸摩尔质量为138g/mol,对羟基苯甲酸乙酯的摩尔质量为166g/mol;实验步骤:取
 乙醇和催化剂置于干燥的仪器A中,
乙醇和催化剂置于干燥的仪器A中, 对羟基苯甲酸置于恒压滴液漏斗C中,实验装置如图所示(加热和夹持装置省略)。加热回流,充分反应。
对羟基苯甲酸置于恒压滴液漏斗C中,实验装置如图所示(加热和夹持装置省略)。加热回流,充分反应。
(1)仪器C的名称是
(2)某同学对实验装置做出了改进,在仪器A和B之间加一个脱水装置(如图),并在油水分离器(分水器)中预先加水至略低于支管口,加热回流,反应一段时间将水逐渐分去,至反应完毕。

反应中利用分水器将水分去,该操作的目的是:
Ⅱ.对羟基苯甲酸乙酯的精制
实验方法:①反应完毕后趁热滤出催化剂,滤液倒入冷水中,析出固体,过滤。
②固体先后用5%的
 溶液和水洗涤,干燥后得到粗产品。
溶液和水洗涤,干燥后得到粗产品。③在装有冷凝管的圆底烧瓶中,按照一定比例加入粗品酯、乙醇、水和活性炭,加热回流0.5小时,趁热抽滤,滤液冷却,析出白色晶体,于80℃烘干。
(1)在②中用5%的
 溶液洗涤的目的是
溶液洗涤的目的是(2)在③趁热抽滤主要除去的杂质为
Ⅲ.该小组同学按0.1mol对羟基苯甲酸、0.4mol乙醇和催化剂2g进行投料,最后得到对羟基苯甲酸乙酯13.9g,则该实验的产率为
您最近半年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】硫酸氧钒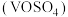 广泛用于媒染剂、催化剂、着色剂等方面。制备方法如下,回答下列问题:
广泛用于媒染剂、催化剂、着色剂等方面。制备方法如下,回答下列问题:
方法一:还原法制备

已知:在溶液中,钒主要以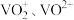 的形式存在。
的形式存在。
(1)基态 原子价层电子的轨道表示式为
原子价层电子的轨道表示式为_____________________
(2)真空干燥时需通入 的作用是
的作用是_____________________________ 。
(3)溶液 转化为
转化为 需要加入还原剂,最佳的还原剂为
需要加入还原剂,最佳的还原剂为_________ (填字母),写出相对应的离子方程式__________________________________________________
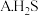
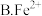

方法二:电解法制备
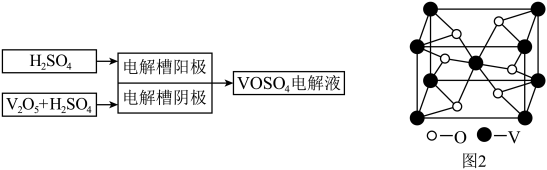
(4)写出电解槽中阴极反应式_________________________________________________________ 。
(5)与“电解法”相比,“还原法”的主要不足之处有_____________________ (写出一点)。
(6)钒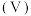 的某种氧化物的晶胞结构如图2所示。已知该晶体的密度为
的某种氧化物的晶胞结构如图2所示。已知该晶体的密度为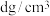 ,
, 表示阿伏加德罗常数的值,则晶胞的体积为
表示阿伏加德罗常数的值,则晶胞的体积为_____________________ 。
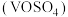 广泛用于媒染剂、催化剂、着色剂等方面。制备方法如下,回答下列问题:
广泛用于媒染剂、催化剂、着色剂等方面。制备方法如下,回答下列问题:方法一:还原法制备


已知:在溶液中,钒主要以
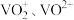 的形式存在。
的形式存在。(1)基态
 原子价层电子的轨道表示式为
原子价层电子的轨道表示式为(2)真空干燥时需通入
 的作用是
的作用是(3)溶液
 转化为
转化为 需要加入还原剂,最佳的还原剂为
需要加入还原剂,最佳的还原剂为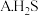
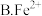

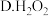
方法二:电解法制备


(4)写出电解槽中阴极反应式
(5)与“电解法”相比,“还原法”的主要不足之处有
(6)钒
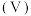 的某种氧化物的晶胞结构如图2所示。已知该晶体的密度为
的某种氧化物的晶胞结构如图2所示。已知该晶体的密度为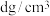 ,
, 表示阿伏加德罗常数的值,则晶胞的体积为
表示阿伏加德罗常数的值,则晶胞的体积为
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】氯气是一种重要的化工原料,下图为实验室制取氯气的装置。
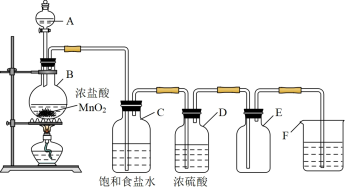
请回答下列问题:
(1)仪器E中收集的 颜色是
颜色是_______ 。
(2)仪器A的名称是_______ ,仪器B的名称是_______ 。
(3)仪器C中的饱和食盐水可以除去 中混有的杂质气体是
中混有的杂质气体是_______ (填化学式)。
(4)装置D的作用是_______ ,装置F中加入的溶液是_______ 。
(5)自来水厂使用 给自来水进行消毒,
给自来水进行消毒, 中氯元素的化合价是
中氯元素的化合价是_______ ,消毒时利用了 的
的_______ 性质。
(6)在新冠疫情防控期间,公共场所要求勤通风勤消毒,其中84消毒液经常用于公共场所消毒,制取84消毒液(含NaClO)发生化学反应的离子方程式是_______ 。

请回答下列问题:
(1)仪器E中收集的
 颜色是
颜色是(2)仪器A的名称是
(3)仪器C中的饱和食盐水可以除去
 中混有的杂质气体是
中混有的杂质气体是(4)装置D的作用是
(5)自来水厂使用
 给自来水进行消毒,
给自来水进行消毒, 中氯元素的化合价是
中氯元素的化合价是 的
的(6)在新冠疫情防控期间,公共场所要求勤通风勤消毒,其中84消毒液经常用于公共场所消毒,制取84消毒液(含NaClO)发生化学反应的离子方程式是
您最近半年使用:0次



