凉山州是矿产资源“聚宝盆”,下辖的会东、金阳、雷波等县磷矿资源丰富,磷化工产业比较发达。请回答下列问题:
(1)基态磷原子的价电子排布图为:___________ ;其基态原子核外有___________ 种不同能量的电子。
(2)含磷药物磷酸氯喹对治疗新冠肺炎有一定效果,其结构如下图。
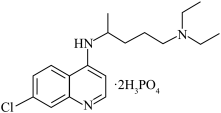
磷酸氯喹中所含第二周期元素第一电离能由大到小的顺序为:___________ ,其中碳原子的轨道杂化类型为:___________ 。
(3)卤化磷通常有三卤化磷和五卤化磷。三卤化磷的熔点见下表,试解释PF3、PCl3、PBr3、PI3熔点逐渐升高的原因是___________ 。
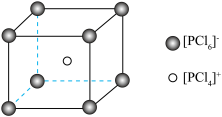
(4)已知PCl5晶体中含有等量的[PCl4]+和[PCl6]-。
①PCl5晶体中的化学键有___________ ,其中[PCl4]+的空间构型为___________ 。
②PCl5晶胞结构如下图,晶胞中含有的P原子的个数为___________ ,已知晶胞边长为apm,阿伏加德罗常数为NA,则该晶体密度为___________ g/cm3(列出计算式即可)。
(1)基态磷原子的价电子排布图为:
(2)含磷药物磷酸氯喹对治疗新冠肺炎有一定效果,其结构如下图。

磷酸氯喹中所含第二周期元素第一电离能由大到小的顺序为:
(3)卤化磷通常有三卤化磷和五卤化磷。三卤化磷的熔点见下表,试解释PF3、PCl3、PBr3、PI3熔点逐渐升高的原因是
| 三卤化磷 | PF3 | PCl3 | PBr3 | PI3 |
| 熔点/℃ | -151.5 | -93.6 | -41.5 | 61.2 |
①PCl5晶体中的化学键有
②PCl5晶胞结构如下图,晶胞中含有的P原子的个数为

更新时间:2024-03-28 11:27:51
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、M、Q、R是元素周期表前四周期的元素,且原子序数依次增大,其相关信息如表所示:
请回答下列问题。
(1)请写出元素R在元素周期表中位置:_______ 。
(2)X、Y、Z、M四种元素的原子半径由小到大的顺序是_______ (用元素符号表示)。
(3)元素R可形成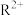 和
和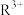 ,其中较稳定的是
,其中较稳定的是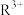 ,原因是
,原因是_______ 。
(4)短周期元素T与元素M在周期表中的位置呈现对角线关系,则元素T为_______ (填元素符号);已知元素T、Q的电负性分别为1.5和3.0,则它们形成的化合物是_______ (填“离子化合物”或“共价化合物”)。
| 元素代号 | 相关信息 |
| X | 原子核外有6种不同运动状态的电子 |
| Y | 基态原子中s电子总数与p电子总数相等 |
| Z | 原子半径在同周期元素中最大 |
| M | 第一至第六电离能(kJ/mol)依次为578、1817、2745、11575、14830、18376 |
| Q | 基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反 |
| R | 基态原子核外有7个能级上有电子且能量最高的能级上有6个电子 |
(1)请写出元素R在元素周期表中位置:
(2)X、Y、Z、M四种元素的原子半径由小到大的顺序是
(3)元素R可形成
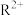 和
和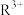 ,其中较稳定的是
,其中较稳定的是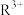 ,原因是
,原因是(4)短周期元素T与元素M在周期表中的位置呈现对角线关系,则元素T为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】2019年1月3日上午,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答下列问题:
(1)基态Ga原子价电子排布式_____ 。
(2)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为_____ ,As右边相邻元素X为_____ (填元素符号),与X同周期的p区元素中第一电离能大于X的元素有_____ 种;XO3的空间构型是_____ 。
(3)相同压强下,AsH3的沸点_____ SbH3(填“<”或“>”),原因为_____ 。
(4)现有Ti3+的配合物[TiCl(H2O)5]Cl2•H2O,其中配离子是_____ ,配位数为_____ ,在0.2mol该配合物溶液中滴加足量的AgNO3溶液,产生沉淀的物质的量为_____ 。
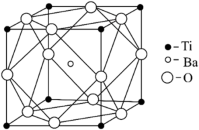
(5)偏钛酸钡晶体中晶胞的结构如图所示,晶胞边长为apm,阿伏伽德罗常数为NA,则该晶体的密度为______ g•cm-3。
(1)基态Ga原子价电子排布式
(2)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为
(3)相同压强下,AsH3的沸点
(4)现有Ti3+的配合物[TiCl(H2O)5]Cl2•H2O,其中配离子是
(5)偏钛酸钡晶体中晶胞的结构如图所示,晶胞边长为apm,阿伏伽德罗常数为NA,则该晶体的密度为

您最近半年使用:0次
【推荐3】氟及其化合物用途非常广泛。回答下列问题:
(1)基态氟原子的价层电子排布图为___________ 。
(2)制备NSF3的反应为FCONSF2+2AgF2 NSF3+2AgF+COF2。
NSF3+2AgF+COF2。
①F、O、N、S的第一电离能从小到大的顺序是___________ 。
②COF2分子的空间构型为___________ 。
③NSF3、COF2的沸点依次为-27.1°C、-84.6°C,前者沸点较高的原因是___________ 。
(3)NHF2的一种制备方法是CO(NH2)2+2F2+H2O=NHF2+CO2+NH4HF2。
①CO(NH2)2中C的杂化方式是___________ 。
②CO(NH2)2的熔沸点比CH3CONH2的高,其原因是___________ 。
③下列说法正确的是___________ (填标号)。
A.NHF2、CO2均是极性分子
B.CO2与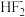 互为等电子体
互为等电子体
C.H2O与NHF2中心原子的价层电子对数相同
D.NH4HF2中存在离子键、配位键和氢键
(4)由Cs、Ag及F三种元素组成的一种超导材料的晶体结构如下图所示(Ag不是+1价):
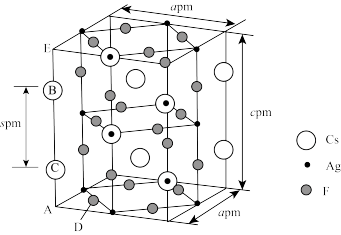
已知AC=BE,则C、D(Cs与F)间的距离为___________ pm(用含a、c、s的代数式表示,列出计算式,下同);设NA为阿伏加德罗常数的值,则晶体的密度为___________ g·cm-3。
(1)基态氟原子的价层电子排布图为
(2)制备NSF3的反应为FCONSF2+2AgF2
 NSF3+2AgF+COF2。
NSF3+2AgF+COF2。①F、O、N、S的第一电离能从小到大的顺序是
②COF2分子的空间构型为
③NSF3、COF2的沸点依次为-27.1°C、-84.6°C,前者沸点较高的原因是
(3)NHF2的一种制备方法是CO(NH2)2+2F2+H2O=NHF2+CO2+NH4HF2。
①CO(NH2)2中C的杂化方式是
②CO(NH2)2的熔沸点比CH3CONH2的高,其原因是
③下列说法正确的是
A.NHF2、CO2均是极性分子
B.CO2与
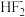 互为等电子体
互为等电子体C.H2O与NHF2中心原子的价层电子对数相同
D.NH4HF2中存在离子键、配位键和氢键
(4)由Cs、Ag及F三种元素组成的一种超导材料的晶体结构如下图所示(Ag不是+1价):

已知AC=BE,则C、D(Cs与F)间的距离为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】氮原子可以形成σ键、π键、大π键和配位键,成键的多样性使其形成了多种具有独特组成的物质。回答下列问题:
(1)基态氮原子价电子排布图不是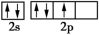 ,是因为该排布方式违背了
,是因为该排布方式违背了___________ 。
(2)肼(N2H4)的相对分子质量与乙烯接近,但沸点远高于乙烯的原因是___________ 。
(3)正硝酸钠(Na3NO4)为白色晶体,是一种重要的化工原料。
①Na3NO4阴离子的空间构型为___________ 。
②写出一种与Na3NO4的阴离子互为等电子体的化学式___________ 。
(4) ①吡啶分子(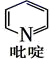 )是大体积平面配体,其结构简式如图所示,该配体的配位原子是
)是大体积平面配体,其结构简式如图所示,该配体的配位原子是___________ 。吡啶分子中,各元素的电负性由大到小的顺序为___________ ,其中碳、氮原子的轨道杂化方式分别是___________ 、___________ 。
②反式二氯二吡啶合铂分子结构如图所示,该分子是___________ 分子 选填“极性”、“非极性”
选填“极性”、“非极性”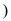 。
。
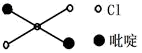
(5)某种磁性氮化铁的结构如图所示,N随机排列在Fe构成的正四面体空隙中,该晶体中铁、氮的微粒个数之比为___________ 。

(1)基态氮原子价电子排布图不是
 ,是因为该排布方式违背了
,是因为该排布方式违背了(2)肼(N2H4)的相对分子质量与乙烯接近,但沸点远高于乙烯的原因是
(3)正硝酸钠(Na3NO4)为白色晶体,是一种重要的化工原料。
①Na3NO4阴离子的空间构型为
②写出一种与Na3NO4的阴离子互为等电子体的化学式
(4) ①吡啶分子(
 )是大体积平面配体,其结构简式如图所示,该配体的配位原子是
)是大体积平面配体,其结构简式如图所示,该配体的配位原子是②反式二氯二吡啶合铂分子结构如图所示,该分子是
 选填“极性”、“非极性”
选填“极性”、“非极性”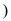 。
。
(5)某种磁性氮化铁的结构如图所示,N随机排列在Fe构成的正四面体空隙中,该晶体中铁、氮的微粒个数之比为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】金属钛(Ti)及化合物在化工、医药、材料等领域具有广泛应用。回答下列问题:
(1)Li4Ti5O12是电池的电极材料。与Li不同族但性质相似的元素是___________ (填元素符号),其电子占据最高能级的电子云轮廓图是___________
(2)K与Ti位于同一周期,K和Ti的第一电离能(I1)较大的是___________ ,它们的第二电离能(I2)分别为3051kJ/mol、1310kJ/mol,其原因是___________ 。
(3)钛与卤素形成的化合物TiX4熔点如下表
它们熔点差异的原因___________
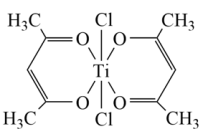
(4)Ti(IV)的某配合物可用于催化环烯烃聚合,其结构如图所示,该配合物中:Ti的配位数为___________ ,与Ti形成配位键的元素是___________ ,碳原子的杂化类型为___________ ;所含非金属元素的含氧酸根离子的立体构型是V形的是___________ (填离子符号)。
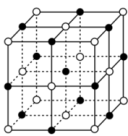
(5)已知N与Ti形成的化合物的晶胞结构如图所示,晶胞中Ti原子与N原子的最近距离为apm;晶胞的密度为p=___________ g/cm3(阿伏加德罗常数值为NA,用含NA的式子表示)
(1)Li4Ti5O12是电池的电极材料。与Li不同族但性质相似的元素是
(2)K与Ti位于同一周期,K和Ti的第一电离能(I1)较大的是
(3)钛与卤素形成的化合物TiX4熔点如下表
| TiX4 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点℃ | 377 | -24 | 38.3 | 153 |
它们熔点差异的原因
(4)Ti(IV)的某配合物可用于催化环烯烃聚合,其结构如图所示,该配合物中:Ti的配位数为

(5)已知N与Ti形成的化合物的晶胞结构如图所示,晶胞中Ti原子与N原子的最近距离为apm;晶胞的密度为p=

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】开发新型储氢材料是氢能利用的重要研究方向。
(1) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。
①基态原子Ti有_______ 种能量不同的电子,基态 的未成对电子有
的未成对电子有_______ 个。
② 由
由 和
和 构成,
构成, 的立体构型是
的立体构型是_______ 。
③Li、B、H元素的电负性由大到小排列顺序为_______ 。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径
_______ (填“ ”、“
”、“ ”或:“
”或:“ ”)
”) 。
。
②某储氢材料是短周期金属元素M的氢化物,M的部分电离能如下表所示:
该储氢材料的化学式为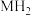 ,其晶胞结构如图所示。已知该晶体的密度
,其晶胞结构如图所示。已知该晶体的密度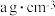 ,则该晶胞的体积为
,则该晶胞的体积为_______  [用a、
[用a、 表示(
表示( 为阿伏加德罗常数的值)]。
为阿伏加德罗常数的值)]。
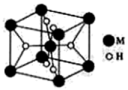
(3)氨硼烷与镧镍合金( )都是优良的储氢材料。
)都是优良的储氢材料。
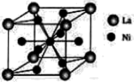
①镧镍合金的晶胞结构示意图如下图所示(只有1个原子位于晶胞内部),则
_______ 。
②氦硼烷(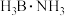 )在高温下释放氢后生成的立方氮化硼晶体,具有类似金刚石的结构,硬度略小于金刚石。则在下列各项中,立方氮化硼晶体不可用作
)在高温下释放氢后生成的立方氮化硼晶体,具有类似金刚石的结构,硬度略小于金刚石。则在下列各项中,立方氮化硼晶体不可用作_______ (填字母)。
a.耐磨材料 b.切削工具 c.导电材料 d.钻探钻头
(1)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。①基态原子Ti有
 的未成对电子有
的未成对电子有②
 由
由 和
和 构成,
构成, 的立体构型是
的立体构型是③Li、B、H元素的电负性由大到小排列顺序为
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径

 ”、“
”、“ ”或:“
”或:“ ”)
”) 。
。②某储氢材料是短周期金属元素M的氢化物,M的部分电离能如下表所示:
 |  |  |  | 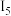 | |
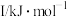 | 738 | 1451 | 7733 | 10540 | 13630 |
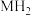 ,其晶胞结构如图所示。已知该晶体的密度
,其晶胞结构如图所示。已知该晶体的密度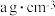 ,则该晶胞的体积为
,则该晶胞的体积为 [用a、
[用a、 表示(
表示( 为阿伏加德罗常数的值)]。
为阿伏加德罗常数的值)]。
(3)氨硼烷与镧镍合金(
 )都是优良的储氢材料。
)都是优良的储氢材料。①镧镍合金的晶胞结构示意图如下图所示(只有1个原子位于晶胞内部),则


②氦硼烷(
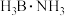 )在高温下释放氢后生成的立方氮化硼晶体,具有类似金刚石的结构,硬度略小于金刚石。则在下列各项中,立方氮化硼晶体不可用作
)在高温下释放氢后生成的立方氮化硼晶体,具有类似金刚石的结构,硬度略小于金刚石。则在下列各项中,立方氮化硼晶体不可用作a.耐磨材料 b.切削工具 c.导电材料 d.钻探钻头
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】I.含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
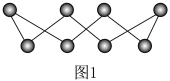
(1)S单质的常见形式为S8,其环状结构如图1所示,S原子采用的轨道杂化方式是_____ 。
(2)H2SeO4比H2SeO3酸性强的原因:_________ 。
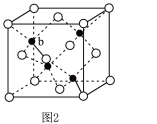
(3)ZnS在光导体材料、荧光体、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图2所示,其晶胞边长为a pm,密度为______ g⋅cm−3。(用含a和NA的表达式填空)
II.氮及其化合物与人类生产、生活息息相关。化肥(NH4)2SO4中会含有N4H4(SO4)2,该物质在水中电离出SO42-和N4H44+,N4H44+遇到碱性溶液会生成一种形似白磷(P4)的N4分子。请回答下列问题:
(4)N4分子中的氮氮键的键角为____ ,1molN4分子中含有的氮氮键的数目为____ 。
(5)N4比P4的沸点____ (填“高”或“低”),原因为________ 。
(1)S单质的常见形式为S8,其环状结构如图1所示,S原子采用的轨道杂化方式是

(2)H2SeO4比H2SeO3酸性强的原因:
(3)ZnS在光导体材料、荧光体、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图2所示,其晶胞边长为a pm,密度为

II.氮及其化合物与人类生产、生活息息相关。化肥(NH4)2SO4中会含有N4H4(SO4)2,该物质在水中电离出SO42-和N4H44+,N4H44+遇到碱性溶液会生成一种形似白磷(P4)的N4分子。请回答下列问题:
(4)N4分子中的氮氮键的键角为
(5)N4比P4的沸点
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)基态O原子的电子排布图为_______ ,基态O原子电子占据最高能级的电子云轮廓图为____ 形,O原子最外层电子的运动状态有_____ 种。
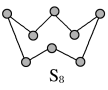
(2)下图为S8的结构,该分子中S原子的杂化轨道类型为______________ 。其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为_____________ 。
(3)气态三氧化硫以单分子形式存在,其分子的立体构型为_____ 形;固体三氧化硫中存在如下图所示的三聚分子,该分子中S原子的价层电子数___________ 。
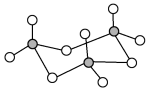
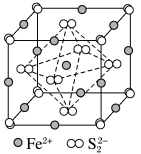
(4)FeS2晶体的晶胞如图所示。晶胞中有Fe2+_____ 个,有S22-_____ 个,晶胞中Fe2+位于S22-所形成的____ (填空隙名称)的体心。晶胞边长为a nm、FeS2相对分子质量为M,阿伏伽德罗常数的值为NA,其晶体密度的计算表达式为___________ g•cm﹣3。
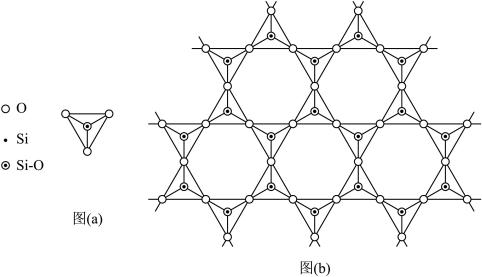
(5)在硅酸盐中,SiO44﹣四面体(如下图(a)通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长层状结构的多硅酸根;其中Si原子的杂化形式为____ 。该多硅酸根的化学式为_____ 。
| H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | −85.5 | 115.2 | >600(分解) | −75.5 | 16.8 | 10.3 |
| 沸点/℃ | −60.3 | 444.6 | −10.0 | 45.0 | 337.0 |
(1)基态O原子的电子排布图为
(2)下图为S8的结构,该分子中S原子的杂化轨道类型为

(3)气态三氧化硫以单分子形式存在,其分子的立体构型为

(4)FeS2晶体的晶胞如图所示。晶胞中有Fe2+

(5)在硅酸盐中,SiO44﹣四面体(如下图(a)通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长层状结构的多硅酸根;其中Si原子的杂化形式为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】填空。
(1)常压下,苯和甲苯的熔、沸点如下表;
晶体中分子间的作用力不仅取决于分子的大小,还取决于晶体中碳链的空间排列情况。请解释:
①苯的沸点比甲苯的沸点更低,主要原因是_______ 。
②苯晶体的熔点比甲苯的熔点更高,主要原因是_______ 。
(2)白磷晶体是由 分子(
分子(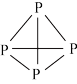 )组成的分子晶体,白磷以
)组成的分子晶体,白磷以 形式存在,而氮以
形式存在,而氮以 形式存在的原因
形式存在的原因_______ 。已知有关氮、磷的单键和叁键的键能( )如下表:
)如下表:
(1)常压下,苯和甲苯的熔、沸点如下表;
| 苯的模型 |  | 熔点:5.5℃ | 甲苯模型 |  | 熔点;-94.9℃ |
| 沸点:80.1℃ | 沸点:100.4℃ |
①苯的沸点比甲苯的沸点更低,主要原因是
②苯晶体的熔点比甲苯的熔点更高,主要原因是
(2)白磷晶体是由
 分子(
分子( )组成的分子晶体,白磷以
)组成的分子晶体,白磷以 形式存在,而氮以
形式存在,而氮以 形式存在的原因
形式存在的原因 )如下表:
)如下表:| N-N | N≡N | P-P | P≡P |
| 193 | 946 | 197 | 489 |
您最近半年使用:0次
【推荐1】电气石是一种具有保健作用的天然石材,其中主要含有B、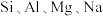 、O等元素。
、O等元素。
(1)灼烧钠的化合物,产生黄色火焰,是由于钠元素原子的电子由__ (“激发态”或“基态”)跃迁到另一个状态时产生的光谱。
(2)熔点:晶体
___ (“高于”或“低于”)晶体 ,其原因是
,其原因是___ 。
(3)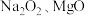 晶体中所含的化学键类型
晶体中所含的化学键类型___ (填“相同”或“不同”,下同),熔化时克服的粒子间作用力____ 。
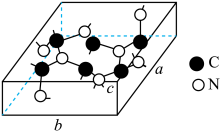
(4)金属铝的晶胞如下图所示,图中a、b、c、d四个铝原子形成正四面体,其内部空隙中可以填充其他原子。
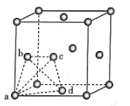
①晶胞中所有的正四面体内部空隙中都填充氢原子,那么形成的化合物的化学式为___ 。
②若晶胞参数为 ,则铝的原子半径为
,则铝的原子半径为___  。
。
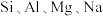 、O等元素。
、O等元素。(1)灼烧钠的化合物,产生黄色火焰,是由于钠元素原子的电子由
(2)熔点:晶体

 ,其原因是
,其原因是(3)
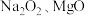 晶体中所含的化学键类型
晶体中所含的化学键类型(4)金属铝的晶胞如下图所示,图中a、b、c、d四个铝原子形成正四面体,其内部空隙中可以填充其他原子。

①晶胞中所有的正四面体内部空隙中都填充氢原子,那么形成的化合物的化学式为
②若晶胞参数为
 ,则铝的原子半径为
,则铝的原子半径为 。
。
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】央视报道《王者归“铼”》:中国发现超级金属“铼”,飞机火箭上天全靠它,有望打破美国垄断。
(1)铼(Re)被称为类锰元素,与锰的外围电子结构数相同,已知Mn的外围电子排布式为3d54s2,写出75Re的外围电子排布式:______ ,其最高价氧化物的化学式为_______ 。
(2)铢合金可作为醇脱氢反应的催化剂:CH3OH HCHO+H2↑,上述反应两种有机物中碳原子的杂化形式分别是
HCHO+H2↑,上述反应两种有机物中碳原子的杂化形式分别是______ 和_______ 。C、H、O三种元素中,电负性最大的是______ (填元素符号)。
(3)实验中常用过硫酸盐氧化法测定钢铁中锰的含量,反应原理为2Mn2++5S2O82-+8H2O 2MnO4-+10SO42-+16H+。已知H2S2O8的结构简式如图所示。
2MnO4-+10SO42-+16H+。已知H2S2O8的结构简式如图所示。

上述反应中S2O82-断裂的共价键类型为___ (填“σ键”或“π键”),每生成0.3molMnO4-,过硫酸根中断裂的共价键数目为_____ NA。
(4)科学家研制出一种新型的超硬材料,类似于金刚石的结构,但硬度比金刚石大,该晶体元素组成为C和N,其晶胞如图所示(图示原子都包含在晶胞内),则该晶胞所含氮原子的个数为____ 。已知晶胞参数分别为a nm、b nm、c nm,,该晶体的摩尔质量为Mg·mol-1,密度为ρg·cm-3,则阿伏加 德罗常数的数值为___ (用含a、b、c、ρ、M的代数式表示)。
(1)铼(Re)被称为类锰元素,与锰的外围电子结构数相同,已知Mn的外围电子排布式为3d54s2,写出75Re的外围电子排布式:
(2)铢合金可作为醇脱氢反应的催化剂:CH3OH
 HCHO+H2↑,上述反应两种有机物中碳原子的杂化形式分别是
HCHO+H2↑,上述反应两种有机物中碳原子的杂化形式分别是(3)实验中常用过硫酸盐氧化法测定钢铁中锰的含量,反应原理为2Mn2++5S2O82-+8H2O
 2MnO4-+10SO42-+16H+。已知H2S2O8的结构简式如图所示。
2MnO4-+10SO42-+16H+。已知H2S2O8的结构简式如图所示。
上述反应中S2O82-断裂的共价键类型为
(4)科学家研制出一种新型的超硬材料,类似于金刚石的结构,但硬度比金刚石大,该晶体元素组成为C和N,其晶胞如图所示(图示原子都包含在晶胞内),则该晶胞所含氮原子的个数为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】2023年杭州亚运会开幕式首次使用“零碳甲醇”作为主火炬塔燃料,实现废碳再生、循环内零碳排放。
已知某些共价键的键能:
(1) 的电子式为
的电子式为___________ 。
(2) 分子结构如图。
分子结构如图。 分子中O的杂化轨道类型
分子中O的杂化轨道类型___________ 。
②键长a、b、c从长到短的顺序为:___________ 。
③乙醇的沸点(78℃)高于甲醇(65℃)。解释原因:___________ 。
(3)在350℃、 催化下用
催化下用 制备
制备 的反应原理如图。
的反应原理如图。___________ 。
②下列说法正确的是___________ (填序号)。
a.电负性由大到小的顺序:O>C>H
b.步骤a涉及s—s 键的断裂和
键的断裂和
 键的生成
键的生成
c.步骤d、e的反应热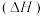 相等
相等
d.升高温度可以提高反应速率和 的平衡产率
的平衡产率
(4)干冰 的晶胞结构如图所示,若该晶胞边长为
的晶胞结构如图所示,若该晶胞边长为 ,干冰晶体的密度为
,干冰晶体的密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 的值为
的值为___________ 。
已知某些共价键的键能:
| 化学键 | H—H | C—H | O—H | C—O | C=O |
键能/ | 436 | 413 | 463 | 351 | 745 |
(1)
 的电子式为
的电子式为(2)
 分子结构如图。
分子结构如图。
 分子中O的杂化轨道类型
分子中O的杂化轨道类型②键长a、b、c从长到短的顺序为:
③乙醇的沸点(78℃)高于甲醇(65℃)。解释原因:
(3)在350℃、
 催化下用
催化下用 制备
制备 的反应原理如图。
的反应原理如图。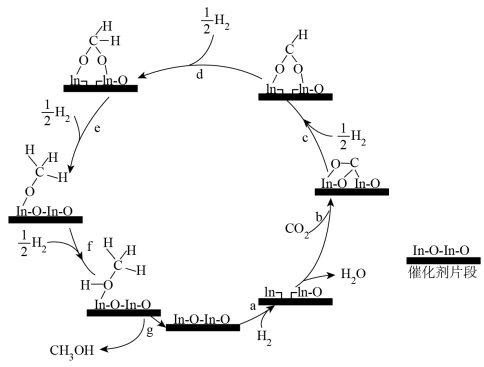
②下列说法正确的是
a.电负性由大到小的顺序:O>C>H
b.步骤a涉及s—s
 键的断裂和
键的断裂和
 键的生成
键的生成c.步骤d、e的反应热
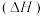 相等
相等d.升高温度可以提高反应速率和
 的平衡产率
的平衡产率(4)干冰
 的晶胞结构如图所示,若该晶胞边长为
的晶胞结构如图所示,若该晶胞边长为 ,干冰晶体的密度为
,干冰晶体的密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 的值为
的值为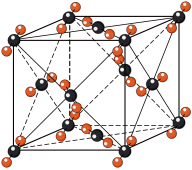
您最近半年使用:0次



