由铁及其化合物可制得FeSO4·7H2O、FeCl3、K2FeO4等化工产品,它们在生产、生活中具有 广泛应用。高炉炼铁的反应为 Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH=-23.5 kJ·mol-1,对于该反应下列有关说法正确的是
2Fe(s)+3CO2(g) ΔH=-23.5 kJ·mol-1,对于该反应下列有关说法正确的是
 2Fe(s)+3CO2(g) ΔH=-23.5 kJ·mol-1,对于该反应下列有关说法正确的是
2Fe(s)+3CO2(g) ΔH=-23.5 kJ·mol-1,对于该反应下列有关说法正确的是| A.若该反应一定能自发进行,则该反应的ΔS>0 |
| B.升高温度使反应物活化分子数增多,能提高反应速率和CO平衡转化率 |
| C.增加炼铁炉高度,延长CO和铁矿石接触时间,能降低平衡时尾气中CO的体积分数 |
| D.制备的生铁中含少量FexC,相同条件下与酸反应放出氢气的速率比纯铁快 |
更新时间:2024-04-08 17:38:41
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】将一定量的氨基甲酸铵置于恒容密闭容器中,发生反应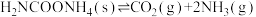 ,下列不能说明反应达到平衡的是
,下列不能说明反应达到平衡的是
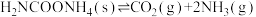 ,下列不能说明反应达到平衡的是
,下列不能说明反应达到平衡的是| A.混合气体的密度保持不变 | B.混合气体的平均摩尔质量保持不变 |
| C.二氧化碳体积分数保持不变 | D.混合气体的压强保持不变 |
您最近一年使用:0次
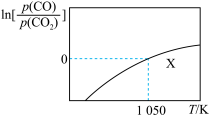
【推荐2】在一体积可变的密闭容器加入足量的Mn3C固体,并充入0.1 mol CO2,发生反应Mn3C(s)+CO2(g)⇌3Mn(s)+2CO(g)。已知:CO与CO2平衡分压比的自然对数值[ln ]与温度的关系如图所示(已知:平衡分压=总压×物质的量分数,Kp是用平衡分压代替浓度计算所得的平衡常数)。下列说法正确的是( )
]与温度的关系如图所示(已知:平衡分压=总压×物质的量分数,Kp是用平衡分压代替浓度计算所得的平衡常数)。下列说法正确的是( )
 ]与温度的关系如图所示(已知:平衡分压=总压×物质的量分数,Kp是用平衡分压代替浓度计算所得的平衡常数)。下列说法正确的是( )
]与温度的关系如图所示(已知:平衡分压=总压×物质的量分数,Kp是用平衡分压代替浓度计算所得的平衡常数)。下列说法正确的是( )
| A.该反应ΔH<0 |
| B.缩小容器体积有利于提高CO2的平衡转化率 |
| C.X点反应达到平衡时,则CO2的转化率为33.3% |
| D.假设1050 K时,X点反应达到平衡时容器的总压强为a kPa,则该温度下Kp为0.5a kPa |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.常温下2NH4Cl+Ba(OH)2·8H2O=BaCl2+2NH3↑+10H2O可自发进行,则该反应的ΔH﹤0 |
| B.用牺牲阳极的阴极保护法来保护钢闸门时,可用锌板作为牺牲阳极 |
C.常温下,向0.1mol·L-1CH3COONa溶液中加入少量水,溶液中 ·c(OH-)值不变 ·c(OH-)值不变 |
| D.Na2O2与足量的水反应生成2.24LO2,转移的电子数目为0.2×6.02×1023 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】下列内容与结论不对应的是
| 选项 | 内容 | 结论 |
| A |  变成 变成 | 该过程的 |
| B | 硝酸铵溶于水可自发进行 | 因为 |
| C | 一个反应的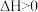 、 、 | 该反应一定不能自发进行 |
| D | 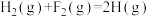 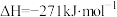  | 该反应在任何温度下均能自发进行 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】下列叙述中正确的是
| A.100℃时,纯水的pH约为6, 此时纯水呈酸性 |
| B.4 mol H2与1 mol N2混合反应生成NH3,转移电子数目小于6×6.02×1023 |
| C.反应Al2O3(s)+3Cl2(g)+3C(s)=2AlCl3(g)+3CO(g)室温下不能自发进行,则△H>0 |
| D.HCl和NaOH反应的中和热为-57.3kJ·mol-1,则H2SO4和Ba(OH)2反应的中和热为-114.6 kJ·mol-1 |
您最近一年使用:0次

 ,下列说法
,下列说法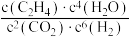
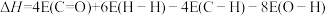 (E表示键能)
(E表示键能) ,转移电子的数目约为
,转移电子的数目约为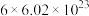
 越大越有利于提高
越大越有利于提高 的平衡转化率
的平衡转化率

