2017年5月海底天然气水合物(俗称可燃冰)试采成功,这是我国能源开发的一次历史性突破。一定条件下,CH4和CO2都能与H2O形成如图所示的笼状结构(表面的小球是水分子,内部的大球是CH4分子或CO2分子;“可燃冰”是CH4与H2O形成的水合物),其相关参数见下表。
(1)CH4和CO2所含的三种元素电负性从大到小的顺序为___________ ;碳原子的最高能级的符号是___________ ,其电子云形状是___________ 。
(2) 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为___________ ,分子的空间结构为___________ 。
(3)为开采海底的“可燃冰”,有科学家提出用 置换
置换 的设想。已知图中笼状结构的空腔直径为
的设想。已知图中笼状结构的空腔直径为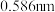 ,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________ 。
(4)“可燃冰”中分子间存在的作用力是氢键和___________ ,上图中最小的环中连接的原子总数是___________ 。
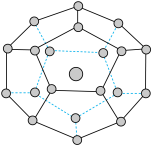
| 参数分子 | 分子直径/nm | 分子与H2O的结合能E(kJ·mol-1) |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
(1)CH4和CO2所含的三种元素电负性从大到小的顺序为
(2)
 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为(3)为开采海底的“可燃冰”,有科学家提出用
 置换
置换 的设想。已知图中笼状结构的空腔直径为
的设想。已知图中笼状结构的空腔直径为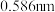 ,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
,根据上述图表,从物质结构及性质的角度分析,该设想的依据是(4)“可燃冰”中分子间存在的作用力是氢键和
更新时间:2024-04-15 15:06:40
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
【推荐1】2020年12月17日我国月球探测器“嫦娥五号”成功携带月壤,返回地球。月壤主要由氧(O)、硅(Si)、铝(Al)、铁(Fe)、铜(Cu)、镍(Ni)等多种元素组成。回答下列问题:
(1) 是“嫦娥五号”中用到的一种耐火材料,其熔点高、硬度大。工业上电解熔融
是“嫦娥五号”中用到的一种耐火材料,其熔点高、硬度大。工业上电解熔融 冶炼Al,
冶炼Al, 属于
属于___________ 晶体,第一电离能Ⅰ1 (Mg)与Ⅰ1 (Al)的关系是Ⅰ1 (Mg)___________ Ⅰ1 (Al)(填“>”、“<”或“=”)。
(2) 可与邻二氮菲(
可与邻二氮菲(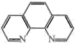 )中N原子通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定
)中N原子通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定 浓度,基态
浓度,基态 离子的价层电子排布式为
离子的价层电子排布式为___________ ,价层电子占据的原子轨道数为___________ ,邻二氮菲中N原子的杂化类型为___________ 。
(3)将金属铜投入氨水与 的混合溶液中,铜片溶解,溶液呈深蓝色,该反应的离子方程式为
的混合溶液中,铜片溶解,溶液呈深蓝色,该反应的离子方程式为___________ 。
(4)月壤中含有丰富的珍贵的 ,中国科学家在2017年成功合成钠氦化合物,使这个最稳定的元素“脱单”。该化合物晶胞中
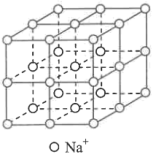
,中国科学家在2017年成功合成钠氦化合物,使这个最稳定的元素“脱单”。该化合物晶胞中 的排布如图所示,电子对(
的排布如图所示,电子对(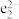 )和
)和 原子交替分布填充在小立方体的中心,晶胞中距
原子交替分布填充在小立方体的中心,晶胞中距 最近的He原子数目为
最近的He原子数目为___________ ,该化合物的化学式可表示为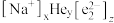 ,则x=
,则x=___________ (用z表达),晶胞参数为a pm,该晶体密度为___________  (写出表达式)。
(写出表达式)。
(1)
 是“嫦娥五号”中用到的一种耐火材料,其熔点高、硬度大。工业上电解熔融
是“嫦娥五号”中用到的一种耐火材料,其熔点高、硬度大。工业上电解熔融 冶炼Al,
冶炼Al, 属于
属于(2)
 可与邻二氮菲(
可与邻二氮菲( )中N原子通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定
)中N原子通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定 浓度,基态
浓度,基态 离子的价层电子排布式为
离子的价层电子排布式为(3)将金属铜投入氨水与
 的混合溶液中,铜片溶解,溶液呈深蓝色,该反应的离子方程式为
的混合溶液中,铜片溶解,溶液呈深蓝色,该反应的离子方程式为(4)月壤中含有丰富的珍贵的
 ,中国科学家在2017年成功合成钠氦化合物,使这个最稳定的元素“脱单”。该化合物晶胞中
,中国科学家在2017年成功合成钠氦化合物,使这个最稳定的元素“脱单”。该化合物晶胞中 的排布如图所示,电子对(
的排布如图所示,电子对(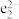 )和
)和 原子交替分布填充在小立方体的中心,晶胞中距
原子交替分布填充在小立方体的中心,晶胞中距 最近的He原子数目为
最近的He原子数目为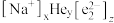 ,则x=
,则x= (写出表达式)。
(写出表达式)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】氟及其化合物用途十分广泛,回答下列问题:
(1)基态氟原子核外电子运动状态有___________ 种;
(2)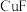 的熔点为
的熔点为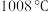 ,熔化呈液态时能导电;
,熔化呈液态时能导电; 的熔点为
的熔点为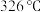 ,能升华,熔化呈液态时不导电。铜元素在元素周期表的位置
,能升华,熔化呈液态时不导电。铜元素在元素周期表的位置___________ ; 的基态价电子排布图为:
的基态价电子排布图为:___________ ;由信息可知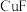 晶体类型是
晶体类型是___________ (填“离子晶体”、“共价晶体”或“分子晶体”)。
(3)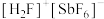 (氟锑酸)是一种超强酸,阳离子
(氟锑酸)是一种超强酸,阳离子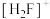 的杂化类型为
的杂化类型为___________ ,其离子空间构型为___________ 。
(4) 的晶胞如图所示,密度为
的晶胞如图所示,密度为 ,相邻的两个
,相邻的两个 的最近核间距为
的最近核间距为 ,则
,则 的摩尔质量为
的摩尔质量为___________  (列出代数式,设
(列出代数式,设 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,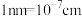 )。
)。

(1)基态氟原子核外电子运动状态有
(2)
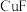 的熔点为
的熔点为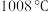 ,熔化呈液态时能导电;
,熔化呈液态时能导电; 的熔点为
的熔点为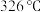 ,能升华,熔化呈液态时不导电。铜元素在元素周期表的位置
,能升华,熔化呈液态时不导电。铜元素在元素周期表的位置 的基态价电子排布图为:
的基态价电子排布图为: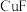 晶体类型是
晶体类型是(3)
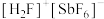 (氟锑酸)是一种超强酸,阳离子
(氟锑酸)是一种超强酸,阳离子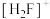 的杂化类型为
的杂化类型为(4)
 的晶胞如图所示,密度为
的晶胞如图所示,密度为 ,相邻的两个
,相邻的两个 的最近核间距为
的最近核间距为 ,则
,则 的摩尔质量为
的摩尔质量为 (列出代数式,设
(列出代数式,设 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,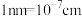 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】丁二酮肟( )是检验
)是检验 的灵敏试剂,在稀氨水介质中,
的灵敏试剂,在稀氨水介质中, 与丁二酮肟反应可生成鲜红色沉淀丁二酮肟镍,其分子结构如图所示。
与丁二酮肟反应可生成鲜红色沉淀丁二酮肟镍,其分子结构如图所示。

回答下列问题:
(1)Ni在元素周期表中的位置为_______ ;基态Ni中最外层电子所占据的原子轨道有_______ 个伸展方向。
(2)Ni与Ca位于同一周期且最外层电子数相同,单质Ni的熔点明显高于Ca,其原因是____ 。
(3)1mol丁二酮肟分子含有σ键数目为_______ ( 是阿伏加德罗常数的值)。
是阿伏加德罗常数的值)。
(4)丁二酮肟镍分子中C原子的杂化轨道类型有_______ ;元素N和O在周期表中相邻,元第一电离能 的原因是
的原因是_______ 。
(5)丁二酮肟镍分子内不存在的作用力有_______ (填序号)。
A.金属键 B.氢键 C.π键 D.配位键 E.范德华力
 )是检验
)是检验 的灵敏试剂,在稀氨水介质中,
的灵敏试剂,在稀氨水介质中, 与丁二酮肟反应可生成鲜红色沉淀丁二酮肟镍,其分子结构如图所示。
与丁二酮肟反应可生成鲜红色沉淀丁二酮肟镍,其分子结构如图所示。
回答下列问题:
(1)Ni在元素周期表中的位置为
(2)Ni与Ca位于同一周期且最外层电子数相同,单质Ni的熔点明显高于Ca,其原因是
(3)1mol丁二酮肟分子含有σ键数目为
 是阿伏加德罗常数的值)。
是阿伏加德罗常数的值)。(4)丁二酮肟镍分子中C原子的杂化轨道类型有
 的原因是
的原因是(5)丁二酮肟镍分子内不存在的作用力有
A.金属键 B.氢键 C.π键 D.配位键 E.范德华力
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为65,中子数为35.请回答下列问题:
(1)AY2是一种常用的溶剂,为_____________ 分子(填“极性”或“非极性”),分子中存在___________ 个σ键。
(2)X形成的单质与NaOH溶液反应的离子方程式为______________________________ ,超高导热绝缘耐高温纳米XB在绝缘材料中应用广泛,其晶体与金刚石类似,属于____ 晶体。
(3)X、氧、B元素的电负性由大到小的顺序为_______________ (用元素符号作答)。
(4)Z的基态原子核外电子排布式为___________________________ 。
(1)AY2是一种常用的溶剂,为
(2)X形成的单质与NaOH溶液反应的离子方程式为
(3)X、氧、B元素的电负性由大到小的顺序为
(4)Z的基态原子核外电子排布式为
您最近一年使用:0次
【推荐2】钙钛矿型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,如图所示为钙钛矿晶体结构,该结构是其晶体中具有代表性的最小重复单位。
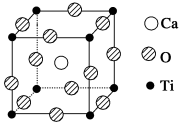
回答下列问题:
(1)在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钛离子、钙离子各有___________ 个、___________ 个。该物质的化学式可表示为___________ 。
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是___________ 。
(3)钙钛矿的组成元素中电负性大小顺序是___________ ;金属离子与氧离子间的作用力为___________ 。

回答下列问题:
(1)在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钛离子、钙离子各有
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)钙钛矿的组成元素中电负性大小顺序是
您最近一年使用:0次
【推荐3】我国科学家利用碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料成功地验证了三维两字霍尔效应,并发现了金属—绝缘体的转换。回答下列问题:
(1)基态砷原子的价电子排布式为____ 。
(2)As与Ge、Se同周期且相邻,它们的第一电离能由大到小的顺序为____ (用元素符号表示)。
(3)与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3>PH3原因是____ 。
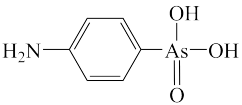
(4)含砷有机物“对氨基苯砷酸”的结构简式如图,砷原子轨道杂化类型为____ 。
(5)Cd2+与NH3形成的配离子[Cd(NH3)4]2+中,2个NH3被2个Cl-替代只得到1种结构,[Cd(NH3)4]2+的立体构型是____ ,1mol[Cd(NH3)4]2+含____ molσ键。
(1)基态砷原子的价电子排布式为
(2)As与Ge、Se同周期且相邻,它们的第一电离能由大到小的顺序为
(3)与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3>PH3原因是
(4)含砷有机物“对氨基苯砷酸”的结构简式如图,砷原子轨道杂化类型为

(5)Cd2+与NH3形成的配离子[Cd(NH3)4]2+中,2个NH3被2个Cl-替代只得到1种结构,[Cd(NH3)4]2+的立体构型是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】2023年春节,各地爆竹烟花有限开禁,年味增加。爆竹的主要成分是黑火药,含有硫黄、木炭和硝酸钾,其反应原理为S+ 2KNO3+3C=K2S+N2↑+3CO2↑。回答下列问题:
(1)氮原子的价电子排布图为________ , 爆竹燃放过程中,钾元素中的电子跃迁的方式是_________ 。
(2)上述反应涉及的元素中电负性最大的是_______ (填元素符号),K、S、N、O四种元素的第一电离能由大到小的顺序为_________ ,N2中π键与σ键的个数比为_______ , KNO3晶体中  的空间结构是
的空间结构是______________ 。
(3)硫单质的一种结构(如图所示)被称为王冠结构,分子中S原子的杂化方式为_______ ,该物质_______ (填“可溶”或“难溶”)于水。

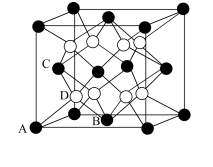
(4)硫化钾的晶胞结构如图。硫离子的配位数为_______________ ;若晶胞中A点坐标参数为(0,0,0),B点坐标参数为(  ,
, ,0),C点坐标参数为(0,
,0),C点坐标参数为(0,  ,
, ),则D点坐标参数为
),则D点坐标参数为_______ 。
(1)氮原子的价电子排布图为
(2)上述反应涉及的元素中电负性最大的是
 的空间结构是
的空间结构是(3)硫单质的一种结构(如图所示)被称为王冠结构,分子中S原子的杂化方式为

(4)硫化钾的晶胞结构如图。硫离子的配位数为
 ,
, ,0),C点坐标参数为(0,
,0),C点坐标参数为(0,  ,
, ),则D点坐标参数为
),则D点坐标参数为
您最近一年使用:0次
【推荐2】研究发现,在CO2低压合成甲醇反应CO23H2CH3OHH2O中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为________ 。元素Mn与O中,第一电离能较大的是________ ,基态原子核外未成对电子数较多的是________ 。
(2)CO2和CH3OH分子中C原子的杂化形式分别为________ 和________ 。
(3)比较CO2和H2O沸点________ ,原因是________ 。
(4)MnNO3中的化学键除了σ键外,还存在________ 。
(1)Co基态原子核外电子排布式为
(2)CO2和CH3OH分子中C原子的杂化形式分别为
(3)比较CO2和H2O沸点
(4)MnNO3中的化学键除了σ键外,还存在
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】稀土元素是指钪(Sc)、钇(Y)和镧系元素,共17种,位于元素周期表中第III B族,均为金属元素,在工业生产中有重要的作用。回答下列问题:
(1)基态钪( Sc)元素的原子核外电子占据的轨道数目共___________ 个 , 钇(Y)位于元素周期表中钪(Sc)的下一周期,钇( Y)的价电子排布式为___________ 。
(2)稀土元素常常能和许多配位体形成配合物。若一个配位体含有两个或两个以上的能提供孤电子对的原子,这种配位体就叫多齿配位体,有一个能提供孤电子对的原子为一齿,(羰基中的氧原子不能提供孤对电子),EDTA(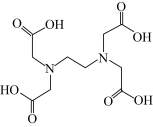 )是
)是___________ 齿配位体,它的配位原子为___________ ,其中 C原子的杂化方式为___________ 。
(3)钪(Sc)离子在水中以稳定对称的[ Sc(H2O)6]3+存在,其中O−Sc−O的键角只有90度和180度两种,其空间构型为___________ 。
(4)铈(Ce)属于镧系元素,氧化铈是一种重要的光催化材料。
①铈具有三价和四价两种价态,三价和四价间的可逆转换会造成氧空位的生成和消除。其光催化的基本原理如下图所示,当光照能量( hv )等于或大于氧化铈催化剂的能量时,氧化铈VB上的电子(e-)会受到激发跃迁至CB,留下带正电荷的空穴(h+ ) ,形成光生电子−空穴对,与所吸附的物质发生氧化还原反应。则在氧化还原反应中,空穴可视为___________ (填“氧化剂”或“还原剂”),图中A发生___________ (填“氧化”或“还原”)反应。
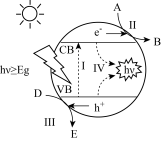
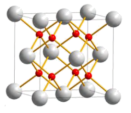
②氧化铈的晶体结构如下图所示,其中铈原子和氧原子的数量之比为___________ ,若 晶体密度为d g∙cm−3,阿伏加德罗常数为NA,晶胞参数a=___________ cm( 写出表达式)。
(1)基态钪( Sc)元素的原子核外电子占据的轨道数目共
(2)稀土元素常常能和许多配位体形成配合物。若一个配位体含有两个或两个以上的能提供孤电子对的原子,这种配位体就叫多齿配位体,有一个能提供孤电子对的原子为一齿,(羰基中的氧原子不能提供孤对电子),EDTA(
 )是
)是(3)钪(Sc)离子在水中以稳定对称的[ Sc(H2O)6]3+存在,其中O−Sc−O的键角只有90度和180度两种,其空间构型为
(4)铈(Ce)属于镧系元素,氧化铈是一种重要的光催化材料。
①铈具有三价和四价两种价态,三价和四价间的可逆转换会造成氧空位的生成和消除。其光催化的基本原理如下图所示,当光照能量( hv )等于或大于氧化铈催化剂的能量时,氧化铈VB上的电子(e-)会受到激发跃迁至CB,留下带正电荷的空穴(h+ ) ,形成光生电子−空穴对,与所吸附的物质发生氧化还原反应。则在氧化还原反应中,空穴可视为

②氧化铈的晶体结构如下图所示,其中铈原子和氧原子的数量之比为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为____________ 。
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为________ 。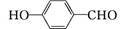 的沸点比
的沸点比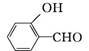 高,原因是
高,原因是__________ 。
(3)甲醛(H2C O)在Ni催化作用下,加氢可得甲醇(CH3OH)。甲醇分子内C原子的杂化方式为
O)在Ni催化作用下,加氢可得甲醇(CH3OH)。甲醇分子内C原子的杂化方式为__________ ,甲醇分子内的O—C—H键角____________ (填“大于”或“小于”)甲醛分子内的O—C—H键角。
(1)氧元素基态原子核外未成对电子数为
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为
 的沸点比
的沸点比 高,原因是
高,原因是(3)甲醛(H2C
 O)在Ni催化作用下,加氢可得甲醇(CH3OH)。甲醇分子内C原子的杂化方式为
O)在Ni催化作用下,加氢可得甲醇(CH3OH)。甲醇分子内C原子的杂化方式为
您最近一年使用:0次
【推荐2】硼酸( )为白色晶体,晶体结构为层状,其二维平面结构如图所示。
)为白色晶体,晶体结构为层状,其二维平面结构如图所示。
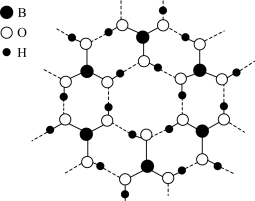
(1)关于 ,下列说法错误的是_______。
,下列说法错误的是_______。
(2)硼有两种天然同位素 和
和 ,硼元素的近似相对原子质量为10.80,则硼元素中
,硼元素的近似相对原子质量为10.80,则硼元素中 的质量分数为_______。
的质量分数为_______。
(3)B与其同周期的相邻元素,第一电离能由大到小的顺序为_______ (用元素符号表示)。
(4) 与足量的
与足量的 反应,生成
反应,生成 ,则
,则 属于
属于_______ 元弱酸。B和 的某些性质相似,类比
的某些性质相似,类比 的酸式电离写出硼酸的电离方程式:
的酸式电离写出硼酸的电离方程式:_______ 。
 )为白色晶体,晶体结构为层状,其二维平面结构如图所示。
)为白色晶体,晶体结构为层状,其二维平面结构如图所示。
(1)关于
 ,下列说法错误的是_______。
,下列说法错误的是_______。A.分子中B原子采用 杂化 杂化 | B.硼酸晶体中层与层之间存在范德华力 |
C.1  晶体中含有6 晶体中含有6 氢键 氢键 | D. 水溶性较好 水溶性较好 |
(2)硼有两种天然同位素
 和
和 ,硼元素的近似相对原子质量为10.80,则硼元素中
,硼元素的近似相对原子质量为10.80,则硼元素中 的质量分数为_______。
的质量分数为_______。| A.80% | B.20% | C.略大于20% | D.略小于20% |
(3)B与其同周期的相邻元素,第一电离能由大到小的顺序为
(4)
 与足量的
与足量的 反应,生成
反应,生成 ,则
,则 属于
属于 的某些性质相似,类比
的某些性质相似,类比 的酸式电离写出硼酸的电离方程式:
的酸式电离写出硼酸的电离方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】已知A、B、C、D、E、F都是元素周期表中前36号的元素,它们的原子序数依次增大。A单质是密度最小的气体。B是周期表已知元素中非金属性最强的元素,且和C属同一主族。D、E、F属同一周期,D、F为主族元素,又知E、F的原子序数分别是29、33。D跟B可形成离子化合物,其晶胞结构如图:

(1)比C元素质子数少1的原子的价层电子的轨道表示式为__________ 。
(2)E元素在周期表中第_____ 周期,第_____ 族的元素,它的+2价离子的电子排布式为________ 。写出E的单质与稀硝酸反应的离子方程式___________ 。
(3)F元素的名称是_____ 。与F同一主族的第二、三周期元素与A形成的化合物沸点的高低为___________ >__________ (用化学式表示),判断的理由____________ 。
(4)写出D跟A形成的化合物的电子式为________ 。

(1)比C元素质子数少1的原子的价层电子的轨道表示式为
(2)E元素在周期表中第
(3)F元素的名称是
(4)写出D跟A形成的化合物的电子式为
您最近一年使用:0次



