设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是A.在适宜条件下, 和 和 充分反应后,所得的气体分子总数目为 充分反应后,所得的气体分子总数目为 |
B. 溶液中阴离子数目大于 溶液中阴离子数目大于 |
C.室温下,向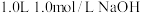 溶液中加入醋酸至溶液显中性,此时醋酸根离子的数目为 溶液中加入醋酸至溶液显中性,此时醋酸根离子的数目为 |
D. 质量分数为34%的 质量分数为34%的 溶液中极性键的数目为 溶液中极性键的数目为 |
更新时间:2024-04-19 09:05:16
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏加 德罗常数的值,下列说法正确的是( )
| A.100 g46%的乙醇水溶液中含有氧原子数目为4 NA |
| B.等质量的CO和N2含有的原子数目均为2 NA |
| C.在0.1mol•L-1的NH4Cl溶液中通入NH3 使溶液呈中性,含有NH4+数目为0.1NA |
| D.常温常压下,水蒸气通过过量的Na2O2使其增重2 g时,反应中转移的电子数为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】NA为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,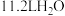 含有的分子数为0.5NA 含有的分子数为0.5NA |
B.常温常压下,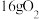 中含有的氧原子数为NA 中含有的氧原子数为NA |
C.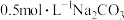 溶液中含有的钠离子数为NA 溶液中含有的钠离子数为NA |
D.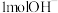 含有的电子数为9NA 含有的电子数为9NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】25℃时,将 0.10 mol•L-1的NaOH溶液逐滴滴入到20.00 mL 0.10 mol• L-1醋酸溶液中,溶液中的pH曲线与NaOH溶液体积的关系如图所示:

下列有关判断错误的是

下列有关判断错误的是
| A.该温度下,醋酸的Ka的数量级为l0-5 | B.N点对应的NaOH溶液体积可能为20.0mL |
| C.溶液中,水的电离程度N点比Q点大 | D.R点所示溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
您最近一年使用:0次
【推荐2】下列实验操作得到的现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向滴有酚酞的 溶液中多次少量加入 溶液中多次少量加入 固体 固体 | 溶液红色逐渐消失,有白色沉淀产生 |  水解显碱性 水解显碱性 |
| B | 用pH传感器分别测定等浓度的NaClO溶液和 溶液的pH 溶液的pH | NaClO溶液的pH较大 | 酸性: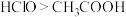 |
| C | 向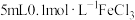 稀溶液中滴加5滴等浓度的KI溶液,振荡,将混合液分为2份,分别滴加KSCN溶液和淀粉溶液 稀溶液中滴加5滴等浓度的KI溶液,振荡,将混合液分为2份,分别滴加KSCN溶液和淀粉溶液 | 溶液分别出现红色和蓝色 | 说明 的反应是有限度的 的反应是有限度的 |
| D | 向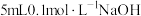 稀溶液中滴加5滴 稀溶液中滴加5滴 的 的 溶液,再滴加5滴 溶液,再滴加5滴 的 的 溶液 溶液 | 先出现白色沉淀,后出现蓝色沉淀 | 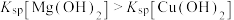 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,下列有关说法错误的是
A. 的醋酸溶液稀释至100mL,稀释后溶液的 的醋酸溶液稀释至100mL,稀释后溶液的 |
B.在稀释 溶液的过程中, 溶液的过程中, 的值不变 的值不变 |
C. 溶液中存在的离子浓度关系 溶液中存在的离子浓度关系 |
D.反应 的平衡常数 的平衡常数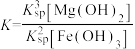 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】分析化学中“滴定分数”的定义为:所加滴定剂与被滴定组分的物质的量之比。常温下以 的HCl溶液滴定同浓度某一元碱MOH溶液并绘制滴定曲线如下图所示。下列说法
的HCl溶液滴定同浓度某一元碱MOH溶液并绘制滴定曲线如下图所示。下列说法不正确 的是

 的HCl溶液滴定同浓度某一元碱MOH溶液并绘制滴定曲线如下图所示。下列说法
的HCl溶液滴定同浓度某一元碱MOH溶液并绘制滴定曲线如下图所示。下列说法
| A.该酸碱中和滴定过程应该选用甲基橙做指示剂 |
B.x点处的溶液中满足: |
C.根据y点坐标可以算得 |
| D.从x点到z点,溶液中水的电离程度逐渐增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室使用 pH 传感器来测定某 Na2A 和 NaHA 混合溶液中 NaHA 的含量,用 0.1mol/L 盐酸滴定该混合溶液,得到如图曲线。滴定过程中,当滴入标准溶液的物质的量与待测组分的物质的量恰好符合化学反应式所表示的计量关系时,称反应达到了化学计量点,简称计量点。以下说法错误的是


| A.未滴定时该混合溶液中:2c(Na+)=3c(A2‒)+3c(HA‒)+3c(H2A) |
| B.滴定过程中始终有 c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(Cl-)+c(OH-)成立 |
| C.滴加 10mL 盐酸时,溶液中:c(Na+)>c(A2‒)>c(HA‒)>c(H2A)>c(H+) |
| D.滴加 30mL 盐酸时,溶液中:c(Na+)=c(Cl‒)>c(H2A>c(H+)>c(OH‒) |
您最近一年使用:0次

 Fe(SCN)3(红色)+3KCl,在平衡后,加入少量KCl固体,因为平衡不移动,体系颜色不变
Fe(SCN)3(红色)+3KCl,在平衡后,加入少量KCl固体,因为平衡不移动,体系颜色不变

