某小组进行“反应物浓度对反应速率影响”实验研究。分别取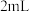 不同浓度的葡萄糖溶液和
不同浓度的葡萄糖溶液和 溶液于试管中,再依次向试管中滴加
溶液于试管中,再依次向试管中滴加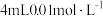 酸性
酸性 溶液,通过色度计监测溶液透光率随时间的变化关系。实验结果如图所示。
溶液,通过色度计监测溶液透光率随时间的变化关系。实验结果如图所示。
(2)酸性 溶液与
溶液与 溶液反应时,某种历程可表示如图。
溶液反应时,某种历程可表示如图。不合理 的是
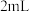 不同浓度的葡萄糖溶液和
不同浓度的葡萄糖溶液和 溶液于试管中,再依次向试管中滴加
溶液于试管中,再依次向试管中滴加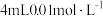 酸性
酸性 溶液,通过色度计监测溶液透光率随时间的变化关系。实验结果如图所示。
溶液,通过色度计监测溶液透光率随时间的变化关系。实验结果如图所示。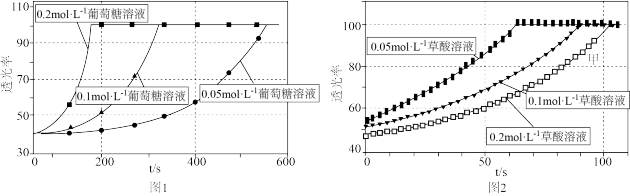
(2)酸性
 溶液与
溶液与 溶液反应时,某种历程可表示如图。
溶液反应时,某种历程可表示如图。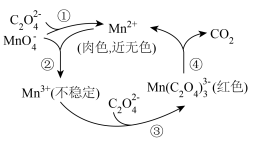
| A.从图1可知,该实验条件下,葡萄糖溶液浓度越大,反应速率越大 |
B.理论上, 和 和 的反应中参与反应的 的反应中参与反应的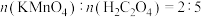 |
| C.图2中曲线甲反应速率加快的原因可能与反应生成有催化作用的物质有关 |
D.图2中 溶液浓度不同时,数据呈现的原因是:随 溶液浓度不同时,数据呈现的原因是:随 浓度增大,反应历程中①、②、③、④速率均减小 浓度增大,反应历程中①、②、③、④速率均减小 |
更新时间:2024-05-28 21:00:28
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】对于Cu+2H2SO4(浓)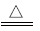 CuSO4+SO2↑+2H2O反应,下列说法正确的是( )
CuSO4+SO2↑+2H2O反应,下列说法正确的是( )
 CuSO4+SO2↑+2H2O反应,下列说法正确的是( )
CuSO4+SO2↑+2H2O反应,下列说法正确的是( )| A.Cu作还原剂,发生还原反应 |
| B.被还原的H2SO4与参加反应的H2SO4的物质的量比为1∶2 |
| C.当生成2.24 L(标准状况下)SO2时,转移的电子为2mol |
| D.当Cu足量时,H2SO4可完全反应 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】做实验时不小心使皮肤上粘了一些高锰酸钾,形成的黑斑很久才能消除,如果用乙二酸的稀溶液洗涤,黑斑可以迅速褪去,其离子方程式为MnO4—+H2C2O4+H+→CO2↑+Mn2++ 。下列有关叙述正确的是
| A.发生还原反应的是H2C2O4 | B.该离子方程式右侧方框内的产物是OH— |
| C.10mol CO2生成时,电子转移5 mol | D.1 mol乙二酸分子中含有7molσ键 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】在化学工业中,氮是非常重要的非金属元素。氨、铵盐、硝酸都是在化工生产中广泛使用的物质,水合肼(N2H4·H2O)是重要的氢能源稳定剂,其制备的反应原理为NaClO+2NH3=N2H4·H2O+NaCl。与此同时,氮的化合物如果处理不当也会造成环境污染。硝酸厂的烟气中含有大量的氮氧化物(NOx),将烟气与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中实现无害化处理,其转化过程如图所示。下列说法错误的是
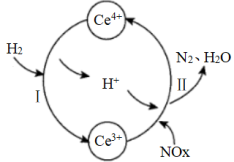

| A.该转化过程的实质为NOx被H2还原 |
| B.该处理过程中,混合溶液中Ce4+起催化作用 |
| C.过程Ⅰ发生反应的离子方程式:H2+Ce4+=2H++Ce3+ |
| D.x=2时,过程Ⅱ中还原剂与氧化剂的物质的量之比为4:1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为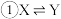 ;
;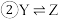 。反应
。反应 的速率
的速率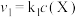 ,反应
,反应 的速率
的速率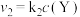 ,式中
,式中 、
、 为速率常数。图甲为该体系中
为速率常数。图甲为该体系中 、
、 、
、 浓度随时间变化的曲线,图乙为反应
浓度随时间变化的曲线,图乙为反应 和
和 的
的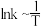 曲线。下列说法正确的是
曲线。下列说法正确的是

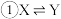 ;
;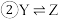 。反应
。反应 的速率
的速率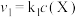 ,反应
,反应 的速率
的速率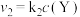 ,式中
,式中 、
、 为速率常数。图甲为该体系中
为速率常数。图甲为该体系中 、
、 、
、 浓度随时间变化的曲线,图乙为反应
浓度随时间变化的曲线,图乙为反应 和
和 的
的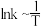 曲线。下列说法正确的是
曲线。下列说法正确的是 
A.随 的减小,反应 的减小,反应 的速率不断下降,而反应 的速率不断下降,而反应 的速率不断增大 的速率不断增大 |
B.由图甲可知,某时间段体系中可能存在如下关系: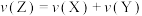 |
C.欲提高 的产率,需降低反应温度且控制反应时间 的产率,需降低反应温度且控制反应时间 |
D.温度高于 时,总反应速率由反应 时,总反应速率由反应 决定 决定 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】 捕获和转化可减少
捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应①完成之后,以
排放并实现资源利用,原理如图1所示。反应①完成之后,以 为载气,以恒定组成的
为载气,以恒定组成的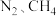 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到
混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上检测到有积碳。
,在催化剂上检测到有积碳。
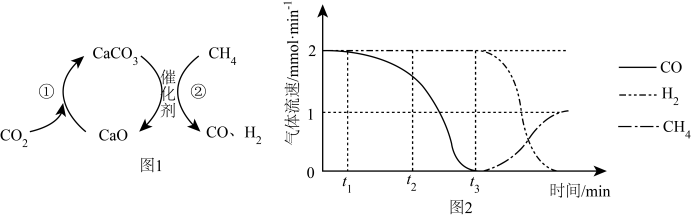
下列说法不正确 的是
 捕获和转化可减少
捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应①完成之后,以
排放并实现资源利用,原理如图1所示。反应①完成之后,以 为载气,以恒定组成的
为载气,以恒定组成的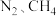 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到
混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上检测到有积碳。
,在催化剂上检测到有积碳。
下列说法
A.反应①为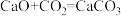 ;反应②为 ;反应②为 |
B.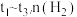 比 比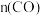 多,且生成 多,且生成 速率不变,可能有副反应 速率不变,可能有副反应 |
C. 时刻,反应②生成 时刻,反应②生成 速率小于副反应生成 速率小于副反应生成 的速率 的速率 |
D. 之后,反应②不再发生,随后副反应也逐渐停止 之后,反应②不再发生,随后副反应也逐渐停止 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】化学中常用图象直观的描述化学反应的进程或结果。下列图象描述正确的是:
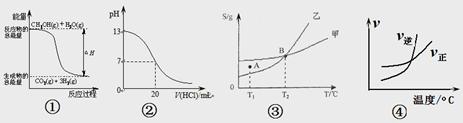

| A.根据图①可判断反应CH3OH(g)+H2O(g)=CO2(g)+3H2(g)的ΔH<0 |
| B.图②表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液的pH随加入酸体积的变化 |
| C.根据图③(S表示溶解度),A点表示T1℃时甲为饱和溶液,乙溶液未饱和。 |
D.根据图④可判断可逆反应A2(g)+3B2(g) 2AB3(g)的ΔH>0 2AB3(g)的ΔH>0 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】某温度下,H2 + CO2 CO+ H2O(g)的平衡常数K=9/4。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的
CO+ H2O(g)的平衡常数K=9/4。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的
 CO+ H2O(g)的平衡常数K=9/4。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的
CO+ H2O(g)的平衡常数K=9/4。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的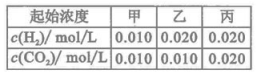
| A.平衡时,甲中和丙中H2的转化率是60% |
| B.平衡时,乙中CO2的转化率小于60% |
| C.反应开始时,丙中的反应速率最快,甲中的反应速率最慢 |
| D.平衡时,丙中c(CO2)是甲中的2倍,是0.008mol/L |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】一定条件下,恒容的密闭容器中,加入一定量的A与B发生反应:A(s)+2B(g) C(g)+2D(g) △H<0,平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法正确的是:
C(g)+2D(g) △H<0,平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法正确的是:

 C(g)+2D(g) △H<0,平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法正确的是:
C(g)+2D(g) △H<0,平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法正确的是:
| A.增加A的物质的量,正反应速率加快 |
| B.平衡时,其他条件不变,当温度升高时,转化率变大 |
| C.图中曲线的斜率表示反应的化学平衡常数 |
| D.平衡时,其他条件不变,再通入B,则反应混合物的温度升高 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】某课外兴趣小组利用硫代硫酸钠( )与稀硫酸反应,探究影响化学反应速率的因素(反应方程式为
)与稀硫酸反应,探究影响化学反应速率的因素(反应方程式为 ),设计了如表系列实验。下列说法
),设计了如表系列实验。下列说法不正确 的是
 )与稀硫酸反应,探究影响化学反应速率的因素(反应方程式为
)与稀硫酸反应,探究影响化学反应速率的因素(反应方程式为 ),设计了如表系列实验。下列说法
),设计了如表系列实验。下列说法| 实验序号 | 反应温度/℃ |  | 稀硫酸 |  | ||
| V/mL |  | V/mL |  | V/mL | ||
| 1 | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| 2 | 40 |  | 0.10 |  | 0.50 |  |
| 3 | 20 |  | 0.10 | 4.0 | 0.50 | 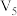 |
A.若用实验1和2探究温度对反应速率的影响,则需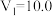 , , |
| B.设计该实验的基本原理为控制变量法 |
| C.实验1和3可探究稀硫酸浓度对该反应速率的影响 |
D.将水更换为 溶液,对实验结果无影响 溶液,对实验结果无影响 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】根据下列实验操作和现象所得到的结论不 正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向AgNO3溶液中加入过量的0.1mol•L-1的NaCl溶液,产生白色沉淀。再滴加几滴NaBr溶液,出现浅黄色沉淀 | Ksp(AgBr)<Ksp(AgCl) |
| B | 向a、b两试管中均加入4mL0.01mol•L-1KMnO4溶液和2mL0.01mol•L-1H2C2O4溶液。再向a试管内加入少量MnSO4固体,a中溶液褪色较快 | MnSO4可能是KMnO4和H2C2O4溶反应的催化剂 |
| C | 向饱和NaHCO3溶液中滴加饱和CaCl2溶液,先有白色沉淀产生,后放出无色气泡 | Ca2+与CO 结合促进HCO 结合促进HCO 的电离,溶液中H+浓度增大,与HCO 的电离,溶液中H+浓度增大,与HCO 反应产生CO2 反应产生CO2 |
| D | 向滴加有酚酞的氨水中加入蒸馏水,溶液的红色变浅 | 溶液中c(H+)、c(OH-)浓度均减小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】硅铝酸盐沸石离子交换分子筛M-ZSM-5(M为Fe、Co、Ni、Cu)催化N2O氧化CH4制甲醇的反应机理如图所示,下列说法错误的是
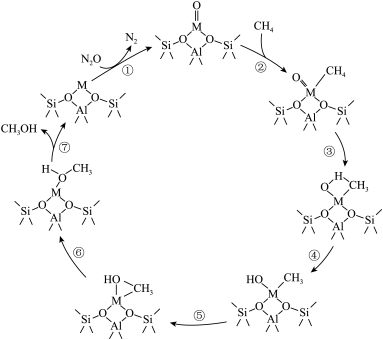
A.反应②的原子利用率为 |
B.反应①、②、③、⑥、⑦中, 的化合价发生了改变 的化合价发生了改变 |
C.M-ZSM-5能降低 氧化 氧化 制甲醇反应的活化能,改变反应的 制甲醇反应的活化能,改变反应的 |
D.总反应为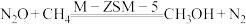 |
您最近一年使用:0次
【推荐3】利用CO2与CH4制备合成气(CO、H2),可能的反应历程如图所示:
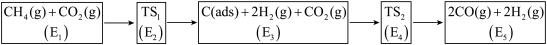
已知:
①C(ads)为吸附性活性炭,E表示方框中物质总能量(单位:kJ/mol),TS表示过渡态;
②部分键能数据如表:
下列说法错误的是
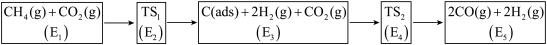
已知:
①C(ads)为吸附性活性炭,E表示方框中物质总能量(单位:kJ/mol),TS表示过渡态;
②部分键能数据如表:
| 化学键 | C-H | C=O | C≡O | H-H |
| 键能(kJ/mol) | a | x | b | c |
| A.若E3+E2>E4+E1,则决定速率步骤的化学方程式为CH4(g)=C(ads)+2H2(g) |
| B.总反应的热化学方程式可表示为CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=(E5-E1)kJ•mol-1 |
C.若总反应的△H=ekJ•mol-1,则C=O的键能为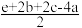 kJ•mol-1 kJ•mol-1 |
| D.使用催化剂后,过渡态能量(E2、E4)会降低 |
您最近一年使用:0次



