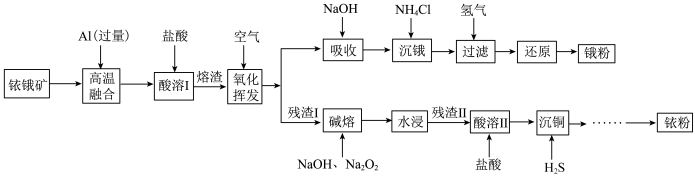
铱(77Ir)和锇(76Os)属于铂族金属,与金、银合称贵重金属,可以用于电气、精密仪表、催化剂等领域。铱锇矿的主要成分有Ir、Os、Ir2O3、OsO2,还含有CuO和SiO2等杂质,从铱锇矿中提取铱和锇的流程如下:
回答下列问题:
(1)“酸溶I”的目的是___________ ;酸溶I后溶渣的主要成分除Ir、Os外,还有___________ (填化学式)。
(2)“氧化挥发”是将溶渣置于300~800℃的管式炉内,通入空气氧化。再用NaOH溶液吸收OsO4生成Na2OsO4,该反应的离子方程式为___________ 。
(3)“沉锇”时,NH4Cl与Na2OsO4发生反应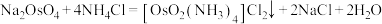 ,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是
,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是___________ 。
(4)“碱熔”时,“残渣I”中的Ir与Na2O2反应生成IrO2·nNa2O和O2,该反应的化学方程式为___________ 。
(5)“沉铜”过程中,当通入H2S达到饱和时测得溶液的pH=1,此时溶液中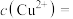
___________ mol/L。[已知:25℃,H2S溶于水形成饱和溶液时, ;H2S的电离常数
;H2S的电离常数 ,
, ;
;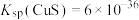 ]
]
(6)化合物 IrO2的四方晶格结构如图所示,其棱边夹角均为90°。已知IrO2晶体密度为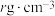 ,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为
,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为___________ (用代数式表示)g/mol。
回答下列问题:
(1)“酸溶I”的目的是
(2)“氧化挥发”是将溶渣置于300~800℃的管式炉内,通入空气氧化。再用NaOH溶液吸收OsO4生成Na2OsO4,该反应的离子方程式为
(3)“沉锇”时,NH4Cl与Na2OsO4发生反应
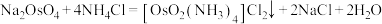 ,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是
,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是(4)“碱熔”时,“残渣I”中的Ir与Na2O2反应生成IrO2·nNa2O和O2,该反应的化学方程式为
(5)“沉铜”过程中,当通入H2S达到饱和时测得溶液的pH=1,此时溶液中
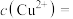
 ;H2S的电离常数
;H2S的电离常数 ,
, ;
;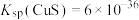 ]
](6)化合物 IrO2的四方晶格结构如图所示,其棱边夹角均为90°。已知IrO2晶体密度为
 ,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为
,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为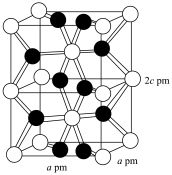
更新时间:2024-05-21 09:10:38
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】铬是不锈钢中一种重要的元素,铬的毒性与其存在的价态有关,低价铬对人体基本无害,六价铬比三价铬毒性高100倍,并易被人体吸收且在体内蓄积,有关含铬化合物的相互转化关系如图甲。
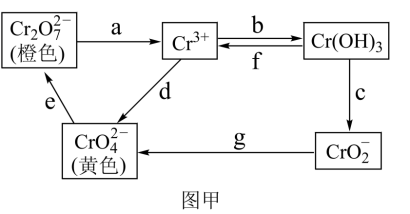
回答下列问题:
(1)从图甲中信息判断,Cr(OH)3是___________ 氢氧化物(填“酸性”、“碱性”或“两性”),相关反应的离子方程式为___________ 。
(2)图甲中所示转化过程中需要加入氧化剂的是___________ (填写表示转化过程的小写字母)。
(3)在水溶液中橙色的 与黄色的
与黄色的 有下列平衡关系:
有下列平衡关系: +H2O
+H2O 2
2 +2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是
+2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是___________ 。
(4)CrO3具有强氧化性,热稳定性较差,加热时逐步分解,其固体残留率( )随温度的变化如图乙所示。
)随温度的变化如图乙所示。
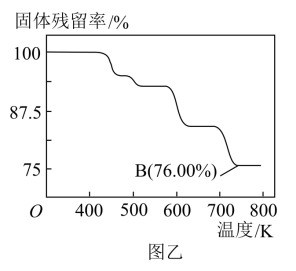
①三氧化铬在稀硫酸环境中氧化乙醇,CrO3变为绿色的Cr2(SO4)3,乙醇被完全氧化为CO2,则其化学方程式是___________ 。
②图乙中B点所示固体的化学式是___________ 。

回答下列问题:
(1)从图甲中信息判断,Cr(OH)3是
(2)图甲中所示转化过程中需要加入氧化剂的是
(3)在水溶液中橙色的
 与黄色的
与黄色的 有下列平衡关系:
有下列平衡关系: +H2O
+H2O 2
2 +2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是
+2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是(4)CrO3具有强氧化性,热稳定性较差,加热时逐步分解,其固体残留率(
 )随温度的变化如图乙所示。
)随温度的变化如图乙所示。
①三氧化铬在稀硫酸环境中氧化乙醇,CrO3变为绿色的Cr2(SO4)3,乙醇被完全氧化为CO2,则其化学方程式是
②图乙中B点所示固体的化学式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
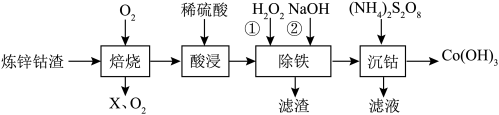
【推荐2】某校化学研究小组以炼锌钴渣(主要含有Co、Zn、Fe、Ni的金属硫化物)为原料制备Co(OH)3(氢氧化高钴)的流程如图,以实现“变废为宝”。 )时的
)时的 如表所示。
如表所示。
回答下列问题:
(1)在“焙烧”前,将炼锌钴渣磨成细粉,目的是_______ ,“ ”是
”是_______ (写化学式)。
(2)加入硫酸“酸浸”时发生的反应有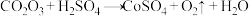 (未配平),该反应中的氧化产物与还原产物的物质的量之比为
(未配平),该反应中的氧化产物与还原产物的物质的量之比为_______ 。
(3)“除铁”时 与先加入的
与先加入的 发生反应的化学方程式为
发生反应的化学方程式为_______ ,反应温度不宜超过55℃的原因是_______ 。
(4)“沉钴”时,使用 调节溶液
调节溶液 ,
, 可将
可将 转化为
转化为 ,自身被还原为
,自身被还原为 ,发生该反应的离子方程式为
,发生该反应的离子方程式为___ ,得到的 经过滤、洗涤、干燥得到较纯产品,检验沉淀是否洗涤干净的操作及现象为
经过滤、洗涤、干燥得到较纯产品,检验沉淀是否洗涤干净的操作及现象为_______ 。
(5)若调节“沉钴”后滤液的 ,同时出现
,同时出现 和
和 沉淀,此时溶液中
沉淀,此时溶液中
_______ 。
 )时的
)时的 如表所示。
如表所示。| 离子 |  |  |  |  |  |  |
开始沉淀时的 | 1.5 | 6.3 | 7.0 | — | 6.4 | 7.2 |
完全沉淀时的 | 2.8 | 8.3 | 9.0 | 1.0 | 8.4 | 9.2 |
(1)在“焙烧”前,将炼锌钴渣磨成细粉,目的是
 ”是
”是(2)加入硫酸“酸浸”时发生的反应有
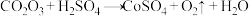 (未配平),该反应中的氧化产物与还原产物的物质的量之比为
(未配平),该反应中的氧化产物与还原产物的物质的量之比为(3)“除铁”时
 与先加入的
与先加入的 发生反应的化学方程式为
发生反应的化学方程式为(4)“沉钴”时,使用
 调节溶液
调节溶液 ,
, 可将
可将 转化为
转化为 ,自身被还原为
,自身被还原为 ,发生该反应的离子方程式为
,发生该反应的离子方程式为 经过滤、洗涤、干燥得到较纯产品,检验沉淀是否洗涤干净的操作及现象为
经过滤、洗涤、干燥得到较纯产品,检验沉淀是否洗涤干净的操作及现象为(5)若调节“沉钴”后滤液的
 ,同时出现
,同时出现 和
和 沉淀,此时溶液中
沉淀,此时溶液中
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”。以钛铁矿(主要成分钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如下。
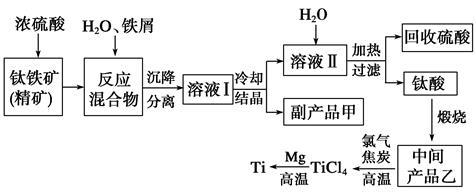
请回答下列问题。
(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为2R+C===2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为______ ;钛酸亚铁和浓H2SO4反应的产物之一是TiOSO4,反应中无气体生成,该反应的化学方程式为_________ 。
(2)上述生产流程中加入铁屑的目的是___________ 。此时溶液中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
①常温下,若所得溶液中Mg2+的物质的量浓度为0.001 8 mol/L,当溶液的pH等于________ 时,Mg(OH)2开始沉淀。
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方程式为____________ 。
(3)中间产品乙与焦炭、氯气在高温下发生反应制取TiCl4的方程式为_______ 。Mg还原TiCl4过程中必须在1070 K的温度下进行,你认为还应该控制的反应条件是_______ 。除去所得金属钛中少量的金属镁可用的试剂是______ 。
(4)在800~1 000 ℃时电解TiO2也可制得海绵钛,装置如下图所示。
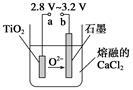
图中b是电源的________ 极,阴极的电极反应式为________ 。

请回答下列问题。
(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为2R+C===2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为
(2)上述生产流程中加入铁屑的目的是
| 氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
①常温下,若所得溶液中Mg2+的物质的量浓度为0.001 8 mol/L,当溶液的pH等于
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方程式为
(3)中间产品乙与焦炭、氯气在高温下发生反应制取TiCl4的方程式为
(4)在800~1 000 ℃时电解TiO2也可制得海绵钛,装置如下图所示。

图中b是电源的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某小组同学进行如下实验比较 和
和 的溶度积(
的溶度积( )大小。
)大小。
【实验Ⅰ】
①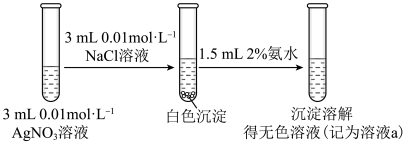
②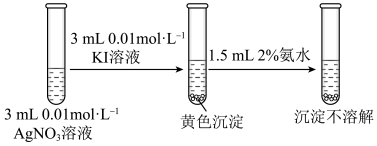
已知:
(1) 中阴离子的VSEPR模型名称是
中阴离子的VSEPR模型名称是___________ , 中
中 的配位数为
的配位数为___________ 。
(2)由上述实验可以得出结论: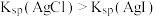 。依据的实验现象是
。依据的实验现象是___________ 。
为进一步证明上述结论,甲同学设计如下实验。
【实验Ⅱ】将(1)中溶液a分成3等份,并向其中逐滴加入试剂X。
(3)结合③和④,从平衡移动的角度解释③中产生白色沉淀的可能原因:___________ 。
(4)对比④和⑤,证实了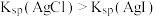 。利用
。利用 、
、 的关系解释上述结论成立的理由:
的关系解释上述结论成立的理由:___________ 。
(5)利用
 溶液、
溶液、
 溶液和
溶液和
 溶液,参照实验Ⅰ呈现形式,设计实验Ⅲ,证明
溶液,参照实验Ⅰ呈现形式,设计实验Ⅲ,证明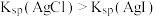
_________ 。
【实验Ⅲ】

(6)查阅资料可知,影响物质溶解性的因素之一是晶体中共价键成分的百分数。推测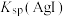 比
比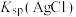 小的可能原因是:
小的可能原因是: 的电负性比
的电负性比
___________ (填“大”或“小”,下同), 晶体共价键成分的百分数比
晶体共价键成分的百分数比 晶体中的
晶体中的___________ 。
 和
和 的溶度积(
的溶度积( )大小。
)大小。【实验Ⅰ】
①

②

已知:

(1)
 中阴离子的VSEPR模型名称是
中阴离子的VSEPR模型名称是 中
中 的配位数为
的配位数为(2)由上述实验可以得出结论:
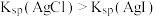 。依据的实验现象是
。依据的实验现象是为进一步证明上述结论,甲同学设计如下实验。
【实验Ⅱ】将(1)中溶液a分成3等份,并向其中逐滴加入试剂X。
| 装置 | 实验编号 | 试剂X | 现象 |
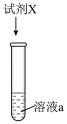 | ③ | 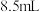 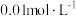 盐酸 盐酸 | 有白色沉淀产生 |
| ④ | 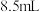 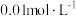  溶液 溶液 | 无明显现象 | |
| ⑤ | 4滴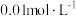  溶液 溶液 | 有黄色沉淀产生 |
(4)对比④和⑤,证实了
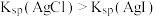 。利用
。利用 、
、 的关系解释上述结论成立的理由:
的关系解释上述结论成立的理由:(5)利用

 溶液、
溶液、
 溶液和
溶液和
 溶液,参照实验Ⅰ呈现形式,设计实验Ⅲ,证明
溶液,参照实验Ⅰ呈现形式,设计实验Ⅲ,证明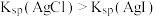
【实验Ⅲ】

(6)查阅资料可知,影响物质溶解性的因素之一是晶体中共价键成分的百分数。推测
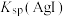 比
比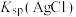 小的可能原因是:
小的可能原因是: 的电负性比
的电负性比
 晶体共价键成分的百分数比
晶体共价键成分的百分数比 晶体中的
晶体中的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】“低碳经济”是建设美丽中国的发展方向,对废气中的CO综合利用可以变废为宝。
(1)许多含碳燃料在不完全燃烧时会产生大量CO。
已知:①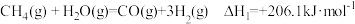
②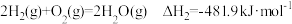
写出 和
和 不完全燃烧生成CO和
不完全燃烧生成CO和 的热化学方程式:
的热化学方程式:_______ 。
(2)二甲醚( )是清洁能源。利用CO合成二甲醚的原理是
)是清洁能源。利用CO合成二甲醚的原理是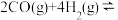
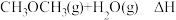 。在一定条件下,该反应中CO的平衡转化率
。在一定条件下,该反应中CO的平衡转化率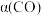 与温度(T)及压强的关系如图1所示。
与温度(T)及压强的关系如图1所示。

①图1中,p1_______ p2(填“>”“<”或“=”,下同),
_______ 0。
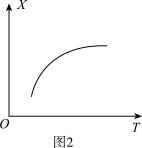
②若某物理量随温度(T)的变化如图2所示,则X表示的物理量可能为_______ (填一种)。
(3)利用CO也可以合成 。一定温度下,在1L恒容密闭容器中充入
。一定温度下,在1L恒容密闭容器中充入 和
和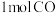 ,起始压强为
,起始压强为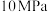 ,在一定条件下合成甲醇:
,在一定条件下合成甲醇: ,经过
,经过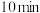 达到平衡,此时容器中压强为
达到平衡,此时容器中压强为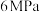 。
。
①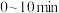 内,
内,
_______  。
。
②下列情况表明该反应达到平衡状态的是_______ (填序号)。
A.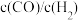 不再改变
不再改变
B.相同时间内CO的生成速率等于 的生成速率
的生成速率
C.一段时间后容器内混合气体的总压强不再改变
D.一段时间后容器内混合气体的平均摩尔质量不再改变
③在该温度下,此反应的平衡常数
_______ 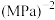 (结果保留小数点后两位)。
(结果保留小数点后两位)。
(4)工业上常用CO制备 ,进一步制得
,进一步制得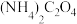 ,
,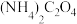 常用于钙镁离子的测定。将某样品灼烧并用酸处理成溶液,使钙离子溶解在溶液中。向溶液中加入足量
常用于钙镁离子的测定。将某样品灼烧并用酸处理成溶液,使钙离子溶解在溶液中。向溶液中加入足量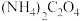 ,使
,使 完全形成
完全形成 白色沉淀。将白色沉淀过滤洗涤后溶于一定量的稀硫酸中,再用高锰酸钾溶液滴定。已知:常温下,
白色沉淀。将白色沉淀过滤洗涤后溶于一定量的稀硫酸中,再用高锰酸钾溶液滴定。已知:常温下, 的
的 ,取
,取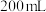 酸溶后的溶液,向其中加入
酸溶后的溶液,向其中加入 时,
时, 开始沉淀,则溶液中
开始沉淀,则溶液中 的浓度为
的浓度为_______ 。洗涤沉淀时经常先用稀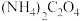 溶液洗涤后,再用水洗原因是
溶液洗涤后,再用水洗原因是_______ 。
(1)许多含碳燃料在不完全燃烧时会产生大量CO。
已知:①
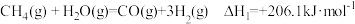
②
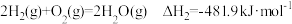
写出
 和
和 不完全燃烧生成CO和
不完全燃烧生成CO和 的热化学方程式:
的热化学方程式:(2)二甲醚(
 )是清洁能源。利用CO合成二甲醚的原理是
)是清洁能源。利用CO合成二甲醚的原理是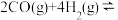
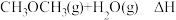 。在一定条件下,该反应中CO的平衡转化率
。在一定条件下,该反应中CO的平衡转化率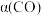 与温度(T)及压强的关系如图1所示。
与温度(T)及压强的关系如图1所示。
①图1中,p1

②若某物理量随温度(T)的变化如图2所示,则X表示的物理量可能为

(3)利用CO也可以合成
 。一定温度下,在1L恒容密闭容器中充入
。一定温度下,在1L恒容密闭容器中充入 和
和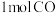 ,起始压强为
,起始压强为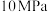 ,在一定条件下合成甲醇:
,在一定条件下合成甲醇: ,经过
,经过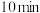 达到平衡,此时容器中压强为
达到平衡,此时容器中压强为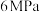 。
。①
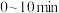 内,
内,
 。
。②下列情况表明该反应达到平衡状态的是
A.
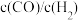 不再改变
不再改变B.相同时间内CO的生成速率等于
 的生成速率
的生成速率C.一段时间后容器内混合气体的总压强不再改变
D.一段时间后容器内混合气体的平均摩尔质量不再改变
③在该温度下,此反应的平衡常数

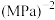 (结果保留小数点后两位)。
(结果保留小数点后两位)。(4)工业上常用CO制备
 ,进一步制得
,进一步制得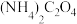 ,
,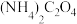 常用于钙镁离子的测定。将某样品灼烧并用酸处理成溶液,使钙离子溶解在溶液中。向溶液中加入足量
常用于钙镁离子的测定。将某样品灼烧并用酸处理成溶液,使钙离子溶解在溶液中。向溶液中加入足量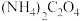 ,使
,使 完全形成
完全形成 白色沉淀。将白色沉淀过滤洗涤后溶于一定量的稀硫酸中,再用高锰酸钾溶液滴定。已知:常温下,
白色沉淀。将白色沉淀过滤洗涤后溶于一定量的稀硫酸中,再用高锰酸钾溶液滴定。已知:常温下, 的
的 ,取
,取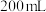 酸溶后的溶液,向其中加入
酸溶后的溶液,向其中加入 时,
时, 开始沉淀,则溶液中
开始沉淀,则溶液中 的浓度为
的浓度为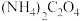 溶液洗涤后,再用水洗原因是
溶液洗涤后,再用水洗原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】稀土是一种重要的战略资源,元素铈(Ce)就是其中一种。铈的合金耐高温,可以用来制造喷气推进器零件等。
(1)铈元素在自然界中主要以氟碳铈矿形式存在,其主要化学成分为CeFCO3。工业上利用氟碳铈矿提取CeCl3的一种工艺流程如图所示:________ (填标号)。
焙烧过程中发生的主要反应化学方程式为________ 。
②酸浸过程中有同学认为用稀硫酸和H2O2替换盐酸更好,可能理由是________ 。
③常温下,当溶液中的某离子浓度≤1.0×10−5mol·L–1时,可认为该离子沉淀完全。据此,在生成Ce(OH)3的反应中,加入NaOH溶液至pH至少达到________ 时,即可视为Ce3+已完全沉淀。已知:Ksp(Ce(OH)3)=1.0×10−20。
④加热CeCl3·6H2O和NH4Cl的固体混合物可得到无水CeCl3,其中NH4Cl的作用是________ 。
(2)雾霾中含有大量的污染物NO,可以被Ce4+溶液吸收,生成NO 、NO
、NO (二者物质的量之比为1∶1),该反应氧化剂与还原剂的物质的量之比为
(二者物质的量之比为1∶1),该反应氧化剂与还原剂的物质的量之比为________ 。
(3)用电解的方法可将上述吸收液中的NO 转化为稳定的无毒气体,同时再生Ce4+,其原理如图所示。写出阴极的电极反应式
转化为稳定的无毒气体,同时再生Ce4+,其原理如图所示。写出阴极的电极反应式________ 。
(1)铈元素在自然界中主要以氟碳铈矿形式存在,其主要化学成分为CeFCO3。工业上利用氟碳铈矿提取CeCl3的一种工艺流程如图所示:
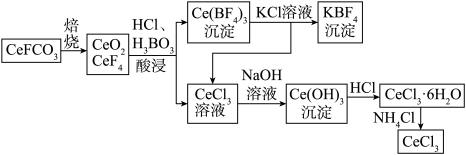
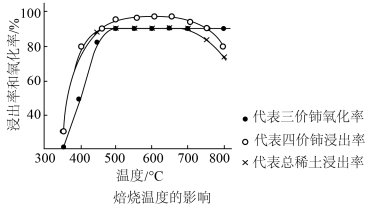
焙烧过程中发生的主要反应化学方程式为
②酸浸过程中有同学认为用稀硫酸和H2O2替换盐酸更好,可能理由是
③常温下,当溶液中的某离子浓度≤1.0×10−5mol·L–1时,可认为该离子沉淀完全。据此,在生成Ce(OH)3的反应中,加入NaOH溶液至pH至少达到
④加热CeCl3·6H2O和NH4Cl的固体混合物可得到无水CeCl3,其中NH4Cl的作用是
(2)雾霾中含有大量的污染物NO,可以被Ce4+溶液吸收,生成NO
 、NO
、NO (二者物质的量之比为1∶1),该反应氧化剂与还原剂的物质的量之比为
(二者物质的量之比为1∶1),该反应氧化剂与还原剂的物质的量之比为(3)用电解的方法可将上述吸收液中的NO
 转化为稳定的无毒气体,同时再生Ce4+,其原理如图所示。写出阴极的电极反应式
转化为稳定的无毒气体,同时再生Ce4+,其原理如图所示。写出阴极的电极反应式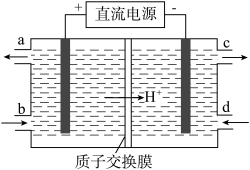
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】现今世界,新药物、新材料层出不穷。
(1)香料材料苯丙烯醇(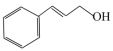 )中可能共面的碳原子数最多有
)中可能共面的碳原子数最多有______ 个。苯丙酮(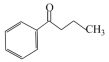 )不溶于水,苯丙烯醇(
)不溶于水,苯丙烯醇( )溶于水,二者溶解度相差较大的主要原因是
)溶于水,二者溶解度相差较大的主要原因是______ 。
(2)纳米二氧化钛 是一种光催化剂,常用于污水处理。其中一个实例如图所示。
是一种光催化剂,常用于污水处理。其中一个实例如图所示。
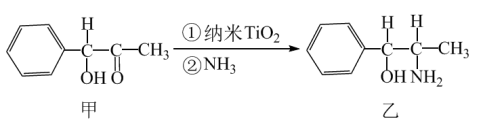
①化合物乙的分子中采取 杂化方式的原子有C和
杂化方式的原子有C和______ 。(填元素符号)
②碳原子连接4个不同的原子或原子团时,称为手性碳原子。一个化合物乙分子中含有______ 个手性碳原子。
③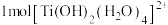 中
中 键的数目为
键的数目为______ 。
(3)砷化镓属于第三代半导体,晶胞结构与金刚石相似,如图所示。
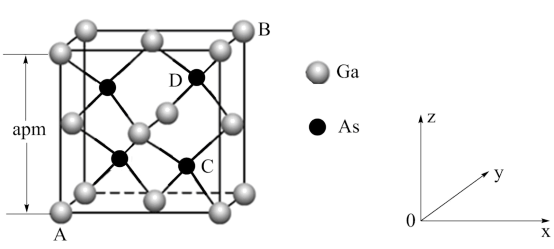
①砷化镓晶胞中镓原子的配位数为______ 。
② 原子占据的是
原子占据的是 原子围成的
原子围成的______ 空隙(填几何空间构型)。
③晶胞中原子坐标参数A为 ,B为
,B为 ,C
,C ,则D为
,则D为______ 。
④阿伏加 德罗常数的值为 ,砷化镓的密度为
,砷化镓的密度为______ 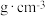 (列出计算式)
(列出计算式)
(1)香料材料苯丙烯醇(
 )中可能共面的碳原子数最多有
)中可能共面的碳原子数最多有 )不溶于水,苯丙烯醇(
)不溶于水,苯丙烯醇( )溶于水,二者溶解度相差较大的主要原因是
)溶于水,二者溶解度相差较大的主要原因是(2)纳米二氧化钛
 是一种光催化剂,常用于污水处理。其中一个实例如图所示。
是一种光催化剂,常用于污水处理。其中一个实例如图所示。
①化合物乙的分子中采取
 杂化方式的原子有C和
杂化方式的原子有C和②碳原子连接4个不同的原子或原子团时,称为手性碳原子。一个化合物乙分子中含有
③
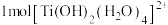 中
中 键的数目为
键的数目为(3)砷化镓属于第三代半导体,晶胞结构与金刚石相似,如图所示。

①砷化镓晶胞中镓原子的配位数为
②
 原子占据的是
原子占据的是 原子围成的
原子围成的③晶胞中原子坐标参数A为
 ,B为
,B为 ,C
,C ,则D为
,则D为④阿伏加 德罗常数的值为
 ,砷化镓的密度为
,砷化镓的密度为 (列出计算式)
(列出计算式)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】Li、Fe、As、Zn等均为重要的合金材料,回答下列问题
(1)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因是_______
(2)KSCN和K4[Fe(CN)6]常用于检验Fe3+,SCN-的立体构型为_______ ,K4[Fe(CN)6]中所含元素电负性由大到小的顺序为_______ 。
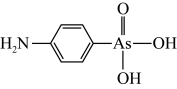
(3)H3AsO3的酸性弱于H3AsO4的原因为_______ 。 含砷有机物“对氨基苯胂酸”的结构简式如图,As原子轨道杂化类型为_______ ,lmol对氨基苯胂酸含 键数目为
键数目为_______ 。
(4)锌和镉位于同一副族,而锌与铜相邻。现有4种铜、锌元素的相应状态,
①锌:[Ar]3dl04s2、②锌:[Ar]3dl04s1、③铜:[Ar]3d104s1、 ④铜: [Ar]3d10失去1个电子需要的能量由大到小排序是_______(填字母)。
(5)Li2O为离子晶体,具有反萤石结构,晶胞如下图所示。则O2-配位数为_______ ,若晶胞参数为bnm,阿伏加德罗常数的值为NA,则Li2O的密度为_______ g·cm-3(列出计算式即可)。

(1)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因是
(2)KSCN和K4[Fe(CN)6]常用于检验Fe3+,SCN-的立体构型为
(3)H3AsO3的酸性弱于H3AsO4的原因为
 键数目为
键数目为
(4)锌和镉位于同一副族,而锌与铜相邻。现有4种铜、锌元素的相应状态,
①锌:[Ar]3dl04s2、②锌:[Ar]3dl04s1、③铜:[Ar]3d104s1、 ④铜: [Ar]3d10失去1个电子需要的能量由大到小排序是_______(填字母)。
| A.④②①③ | B.④②③① | C.①②④③ | D.①④③② |

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】自然界中存在大量的碳、氮、铜及其它们形成的化合物。请结合物质的结构与性质的知识,回答下列问题:
(1)下列表示处于激发态C原子的电子排布图是
A. B.
B.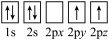 C.
C. D.
D.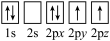
(2)N元素可以形成叠氮酸根离子( ),
), 的空间构型为
的空间构型为
(3)Cu(NH3)2Cl2有两种同分异构体,其中一种可溶于水,则此种化合物是
(4)①基态Cu2+的价电子轨道表达式为
②铜可以与氧气形成Cu2O晶体,其立方晶胞参数为a pm,设阿伏加德罗常数值为NA,该晶胞中部分O原子的坐标参数为:(0,0,0)、( ,
, ,
, )、(1,0,0)、(0,1,0);全部Cu原子的坐标参数为:(
)、(1,0,0)、(0,1,0);全部Cu原子的坐标参数为:( ,
, ,
, )、(
)、( ,
, ,
, )、(
)、( ,
, ,
, )、(
)、( ,
, ,
, )。该立方晶胞中Cu原子构成的空间构型为
)。该立方晶胞中Cu原子构成的空间构型为
您最近一年使用:0次
【推荐1】中科院张涛院士的研究团队研究发现纳米ZnO可作为一些催化剂的载体。下图是通过锌精矿(主要成分为ZnS)与软锰矿(主要成分为MnO2)酸性共融法制备纳米ZnO及MnO2的工艺流程。回答下列问题:
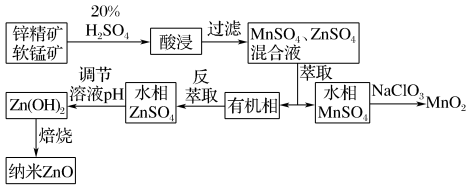
(1)“酸浸”时,锌、锰离子浸出率与溶液温度的关系如图所示。当锌、锰离子浸出效果最佳时,所采用的最适宜温度为___________ 。

(2)写出酸浸时ZnS与MnO2发生的主要反应的化学方程式(无单质硫生成)___________ 。
(3)(NH4)2S2O8是一种强氧化剂,能与Mn2+反应生成SO 和紫色MnO
和紫色MnO 。用(NH4)2S2O8检验水相中的Mn2+时发生反应的离子方程式为
。用(NH4)2S2O8检验水相中的Mn2+时发生反应的离子方程式为___________ 。
(4)二氧化锰广泛用于电池。一种海水中的“水”电池的电池总反应可表示为5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。电池放电时,负极的电极反应式为___________ 。
(5)电解尿素的碱性溶液制取N2和H2的装置如图所示。(电解池中的隔膜仅阻止气体通过,两电极都是惰性电极)
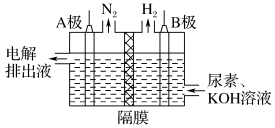
A电极的名称为___________ ,若起始时加入电解池的原料配比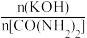 =3,完全反应后,电解排出液中
=3,完全反应后,电解排出液中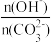 =
=___________ 。

(1)“酸浸”时,锌、锰离子浸出率与溶液温度的关系如图所示。当锌、锰离子浸出效果最佳时,所采用的最适宜温度为

(2)写出酸浸时ZnS与MnO2发生的主要反应的化学方程式(无单质硫生成)
(3)(NH4)2S2O8是一种强氧化剂,能与Mn2+反应生成SO
 和紫色MnO
和紫色MnO 。用(NH4)2S2O8检验水相中的Mn2+时发生反应的离子方程式为
。用(NH4)2S2O8检验水相中的Mn2+时发生反应的离子方程式为(4)二氧化锰广泛用于电池。一种海水中的“水”电池的电池总反应可表示为5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。电池放电时,负极的电极反应式为
(5)电解尿素的碱性溶液制取N2和H2的装置如图所示。(电解池中的隔膜仅阻止气体通过,两电极都是惰性电极)

A电极的名称为
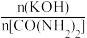 =3,完全反应后,电解排出液中
=3,完全反应后,电解排出液中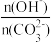 =
=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
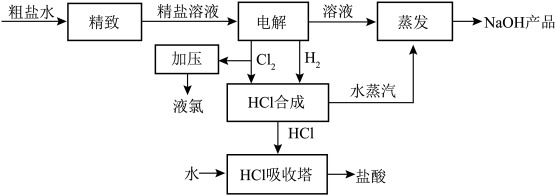
【推荐2】氯碱厂用电解饱和食盐水制取烧碱,同时制盐酸的工艺流程如下:
(1)氯气加压能得到液氯,这利用了氯气______________ 的物理性质。
(2)在HCl合成塔中是_______ 气过量。
(3)按照图示流程,为了制得100吨36.5%的盐酸,理论上需氯化钠_______ 吨。
(4)实验室制备HCl气体的化学方程式:_________ 。
(5)利用HCl合成时放出的热量来产生水蒸气,用于NaOH溶液的蒸发,这样做的优点是_______ 。
(6)氯化氢气体可做美丽的喷泉实验。标准状况下,用容积为V升的圆底烧瓶,采用排空气法收集干燥的氯化氢,所得气体的平均式量是34.625。喷泉实验后,烧瓶中的溶液的体积为____ ,物质的量浓度为___ 。
(7)某化学兴趣小组进行粗盐(含有少量氯化钙和硫酸镁杂质)提纯实验,请结合实验过程回答下列问题。
步骤一:称取10g粗盐,倒入烧杯中后加入30mL水溶解。为加快溶解速率,可采取的方法是______ (任写1种)。步骤二:依次加入稍过量的沉淀剂,充分反应后得到大量沉淀。沉淀剂加入顺序依次为(用化学式表示):__________ 。步骤三:将混合物进行过滤,取滤液进行下一步操作。步骤四:往滤液中加入适量的____ (填试剂名称),调节pH到7(用pH试纸测定),若该试剂不小心加过量,对所得到氯化钠的纯度____ (填“有”或“没有”)影响。步骤五:将滤液倒入______ 中进行加热,等到______ 时,停止加热,利用余热蒸干。步骤六:晶体转入试剂瓶中待用。在步骤三和五中,玻璃棒的作用依次是____ 、____ 。若最终得到的氯化钠固体中还含有微量的NaBr和KCl,更简单的除杂方法是______ 。已知氯元素的近似相对原子质量为35.5,由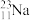 、
、 、
、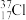 构成的11.7gNaCl中含有
构成的11.7gNaCl中含有
___ 克。
(1)氯气加压能得到液氯,这利用了氯气
(2)在HCl合成塔中是
(3)按照图示流程,为了制得100吨36.5%的盐酸,理论上需氯化钠
(4)实验室制备HCl气体的化学方程式:
(5)利用HCl合成时放出的热量来产生水蒸气,用于NaOH溶液的蒸发,这样做的优点是
(6)氯化氢气体可做美丽的喷泉实验。标准状况下,用容积为V升的圆底烧瓶,采用排空气法收集干燥的氯化氢,所得气体的平均式量是34.625。喷泉实验后,烧瓶中的溶液的体积为
(7)某化学兴趣小组进行粗盐(含有少量氯化钙和硫酸镁杂质)提纯实验,请结合实验过程回答下列问题。
步骤一:称取10g粗盐,倒入烧杯中后加入30mL水溶解。为加快溶解速率,可采取的方法是
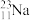 、
、 、
、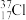 构成的11.7gNaCl中含有
构成的11.7gNaCl中含有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】试分析回答下列有关实验与计算问题:
(1)利用反应Ca2++H2O2+2NH3+8H2O=CaO2∙8H2O↓+2 ,在碱性环境下制取CaO2∙8H2O的装置如图:
,在碱性环境下制取CaO2∙8H2O的装置如图:
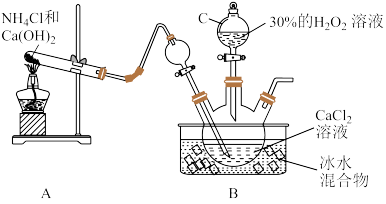
①仪器C的名称为_______ ;反应结束后,经_______ (填操作名称)、洗涤、低温烘干可获得CaO2∙8H2O。
②装置B中用冰水浴控制温度,其可能的原因是_______ 。
(2)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如图所示实验方案来测定该混合气体中SO2的体积分数。
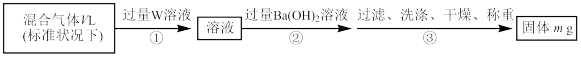
①W溶液可以是_______ (填序号)。
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为_______ (用含V、m的式子表示)。
(1)利用反应Ca2++H2O2+2NH3+8H2O=CaO2∙8H2O↓+2
 ,在碱性环境下制取CaO2∙8H2O的装置如图:
,在碱性环境下制取CaO2∙8H2O的装置如图:
①仪器C的名称为
②装置B中用冰水浴控制温度,其可能的原因是
(2)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如图所示实验方案来测定该混合气体中SO2的体积分数。
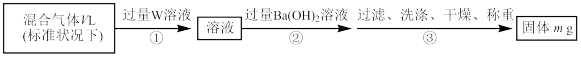
①W溶液可以是
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为
您最近一年使用:0次



