从衣食住行到探索浩瀚宇宙,都有氮及其化合物的参与,但同时有毒含氮化合物的排放,也对环境产生污染。如何实现环境保护与资源利用的和谐统一,已成为我们的重要研究课题。回答下列问题:
(1)在25℃,101 kPa时,利用NH3的还原性可以消除氮氧化物的污染,其中除去NO的主要反应如下:
ⅰ.
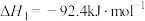
ⅱ.

ⅲ.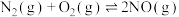

根据信息,写出NO(g)与NH3(g)反应生成N2(g)和H2O(l)的热化学方程式:__________ ;该反应自发进行的条件是__________ (填“高温”或“低温”)。
(2)活性炭还原法是消除氮氧化物污染的有效方法。在三个反应器中分别加入C、CaO/C、La2O3/C,通入NO使其浓度达到0.1 mol/L,不同温度下,测得反应2小时NO去除率如图所示:__________ (填“C”“ CaO/C”或“La2O3/C”),该情况下,A点__________ (填“是”或“不是”)平衡点。
②400℃时,CaO/C催化下反应速率v(NO)=__________ mol/(L·h)。
(3)臭氧脱硝存在如下两个反应:
a. ;
;
b. 。
。
T℃时,将2 mol NO2和1 mol O3混合气体充入一个1 L恒容密闭容器中发生上述反应,测得NO2的物质的量浓度随时间变化关系如下表:
若起始压强为p0,T℃下反应达到平衡时,N2O4的分压与N2O5的分压相等,则O3的体积分数=__________ (保留两位有效数字),反应b平衡常数Kp=__________ (用含p0式子表示,Kp为用平衡分压表示的平衡常数,即用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
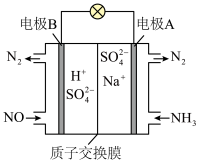
(4)工业上还可以利用原电池原理处理氮氧化合物,工作原理如图所示,则正极的电极反应式为__________ 。
(1)在25℃,101 kPa时,利用NH3的还原性可以消除氮氧化物的污染,其中除去NO的主要反应如下:
ⅰ.

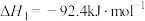
ⅱ.


ⅲ.
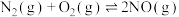

根据信息,写出NO(g)与NH3(g)反应生成N2(g)和H2O(l)的热化学方程式:
(2)活性炭还原法是消除氮氧化物污染的有效方法。在三个反应器中分别加入C、CaO/C、La2O3/C,通入NO使其浓度达到0.1 mol/L,不同温度下,测得反应2小时NO去除率如图所示:

②400℃时,CaO/C催化下反应速率v(NO)=
(3)臭氧脱硝存在如下两个反应:
a.
 ;
;b.
 。
。T℃时,将2 mol NO2和1 mol O3混合气体充入一个1 L恒容密闭容器中发生上述反应,测得NO2的物质的量浓度随时间变化关系如下表:
| t/h | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
| c(NO2)/(mol/L) | 2.0 | 1.4 | 1.0 | 0.70 | 0.50 | 0.40 | 0.40 |
(4)工业上还可以利用原电池原理处理氮氧化合物,工作原理如图所示,则正极的电极反应式为
更新时间:2024-05-17 17:02:02
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】硫是中学化学重要的非金属元素之一,请回答下列有关问题。
已知:2SO2(g)+O2(g) 2SO3(g) △H=-196.6kJ/mol
2SO3(g) △H=-196.6kJ/mol
2NO(g)+O2(g) 2NO2(g) △H=-113.0kJ/mol
2NO2(g) △H=-113.0kJ/mol
(1)反应NO2(g)+ SO2(g) SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH= ______ kJ/mol 。
(2)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是_________ 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO2的同时消耗1 molNO
(3)S2Cl2和SCl2均为重要的工业化合物。已知:
a.S2(l)+Cl2(g) S2Cl2(g) △H1
S2Cl2(g) △H1
b.S2Cl2(g)+ Cl2(g) 2SCl2(g) △H2
2SCl2(g) △H2
—定压强下,向10 L密闭容器中充入1 molS2Cl2和1 mol Cl2,发生反应b。Cl2与SCl2的消耗速率(υ)与温度(T)的关系如图所示:
① A、B、C、D四点对应状态下,达到平衡状态的有______ (填字母),理由是_______ 。
②—定温度下,在恒容密闭容器中发生反应a和反应b,达到平衡后缩小容器容积,重新达到平衡后,Cl2的平衡转化率_________ (填“增大”或“减小”或“不变”),理由是________ 。
II.氮有不同价态的化合物,如氨、氮气、亚硝酸钠、乙二胺等。
图(I)和图(II)分别为二元酸H2A和乙二胺(H2NCH2CH2NH2)溶液中各微粒的百分含量δ(即物质的量百分数)随溶液pH的变化曲线(25℃)。
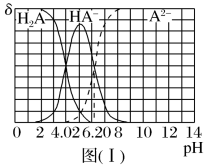
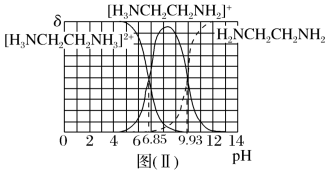
(1)H3NCH2CH2NH3A溶液显____ (填“酸”或“碱”)性。
(2)乙二胺在水溶液中发生第二步电离的方程式:____________________ ,其平衡常数Kb2= _______________________ 。
(3)向20 mL 0.1 mol/L的H2A溶液加入10 mL 0.1 mol/L H2NCH2CH2NH2溶液后,溶液中各离子浓度大小的关系为____________________________________ 。
已知:2SO2(g)+O2(g)
 2SO3(g) △H=-196.6kJ/mol
2SO3(g) △H=-196.6kJ/mol2NO(g)+O2(g)
 2NO2(g) △H=-113.0kJ/mol
2NO2(g) △H=-113.0kJ/mol(1)反应NO2(g)+ SO2(g)
 SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH= (2)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO2的同时消耗1 molNO
(3)S2Cl2和SCl2均为重要的工业化合物。已知:
a.S2(l)+Cl2(g)
 S2Cl2(g) △H1
S2Cl2(g) △H1b.S2Cl2(g)+ Cl2(g)
 2SCl2(g) △H2
2SCl2(g) △H2—定压强下,向10 L密闭容器中充入1 molS2Cl2和1 mol Cl2,发生反应b。Cl2与SCl2的消耗速率(υ)与温度(T)的关系如图所示:
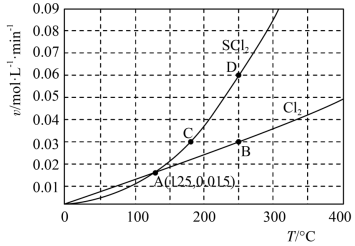
已知B点时,c(Cl2)=0.07 mol/L
① A、B、C、D四点对应状态下,达到平衡状态的有
②—定温度下,在恒容密闭容器中发生反应a和反应b,达到平衡后缩小容器容积,重新达到平衡后,Cl2的平衡转化率
II.氮有不同价态的化合物,如氨、氮气、亚硝酸钠、乙二胺等。
图(I)和图(II)分别为二元酸H2A和乙二胺(H2NCH2CH2NH2)溶液中各微粒的百分含量δ(即物质的量百分数)随溶液pH的变化曲线(25℃)。


(1)H3NCH2CH2NH3A溶液显
(2)乙二胺在水溶液中发生第二步电离的方程式:
(3)向20 mL 0.1 mol/L的H2A溶液加入10 mL 0.1 mol/L H2NCH2CH2NH2溶液后,溶液中各离子浓度大小的关系为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】综合利用 、
、 对构建低碳社会有重要意义。
对构建低碳社会有重要意义。
(1)利用 与
与 制备合成气CO、
制备合成气CO、 ,可能的反应历程如图所示:
,可能的反应历程如图所示:
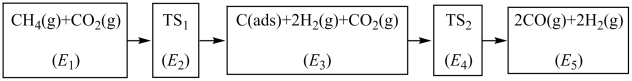
说明: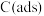 为吸附性活性炭,E表示方框中物质的总能量(单位:
为吸附性活性炭,E表示方框中物质的总能量(单位: ),
), 表示过渡态。
表示过渡态。
①制备合成气 、
、 总反应的热化学方程式为
总反应的热化学方程式为_______ 。
②若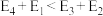 ,则决定制备“合成气”反应速率的化学方程式
,则决定制备“合成气”反应速率的化学方程式_______ 。
(2)工业上常采用 和
和 为原料合成乙醇,反应方程式为:
为原料合成乙醇,反应方程式为: .一定温度下,向容积均为
.一定温度下,向容积均为 的恒容密闭容器中分别通入
的恒容密闭容器中分别通入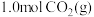 和
和 ,在不同催化剂X、Y的催化下发生反应.测得
,在不同催化剂X、Y的催化下发生反应.测得 时,
时, 转化率与温度的变化关系如图所示。
转化率与温度的变化关系如图所示。
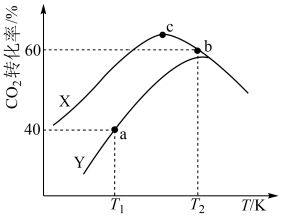
①该反应适宜选用的催化剂为_______ (填“X”或“Y”)。
② 时,a点对应容器在
时,a点对应容器在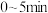 内的平均反应速率
内的平均反应速率
_______ ;b、c点对应状态下反应物的有效碰撞几率b_______ c(填“>”“<”或“=”),原因为_______ 。
③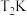 时,保持温度不变向容器中再充入
时,保持温度不变向容器中再充入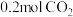 、
、 ,平衡将
,平衡将_______ 移动(填“向正反应方向”、“向逆反应方向”或“不”)。
(3)随着科学技术的发展, 的捕集利用技术成为研究重点,
的捕集利用技术成为研究重点, 可以被
可以被 溶液捕获,所得溶液
溶液捕获,所得溶液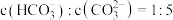 ,该溶液的
,该溶液的
_______ 。[已知室温下, ,
,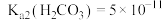 ]
]
 、
、 对构建低碳社会有重要意义。
对构建低碳社会有重要意义。(1)利用
 与
与 制备合成气CO、
制备合成气CO、 ,可能的反应历程如图所示:
,可能的反应历程如图所示: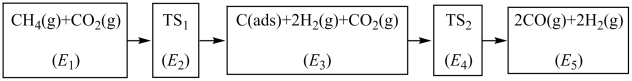
说明:
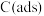 为吸附性活性炭,E表示方框中物质的总能量(单位:
为吸附性活性炭,E表示方框中物质的总能量(单位: ),
), 表示过渡态。
表示过渡态。①制备合成气
 、
、 总反应的热化学方程式为
总反应的热化学方程式为②若
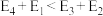 ,则决定制备“合成气”反应速率的化学方程式
,则决定制备“合成气”反应速率的化学方程式(2)工业上常采用
 和
和 为原料合成乙醇,反应方程式为:
为原料合成乙醇,反应方程式为: .一定温度下,向容积均为
.一定温度下,向容积均为 的恒容密闭容器中分别通入
的恒容密闭容器中分别通入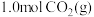 和
和 ,在不同催化剂X、Y的催化下发生反应.测得
,在不同催化剂X、Y的催化下发生反应.测得 时,
时, 转化率与温度的变化关系如图所示。
转化率与温度的变化关系如图所示。
①该反应适宜选用的催化剂为
②
 时,a点对应容器在
时,a点对应容器在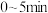 内的平均反应速率
内的平均反应速率
③
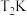 时,保持温度不变向容器中再充入
时,保持温度不变向容器中再充入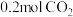 、
、 ,平衡将
,平衡将(3)随着科学技术的发展,
 的捕集利用技术成为研究重点,
的捕集利用技术成为研究重点, 可以被
可以被 溶液捕获,所得溶液
溶液捕获,所得溶液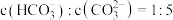 ,该溶液的
,该溶液的
 ,
,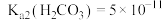 ]
]
您最近一年使用:0次
【推荐3】直接排放含 的烟气会形成酸雨,危害环境。工业上常采用催化还原法和碱吸收法处理SO2气体。
的烟气会形成酸雨,危害环境。工业上常采用催化还原法和碱吸收法处理SO2气体。
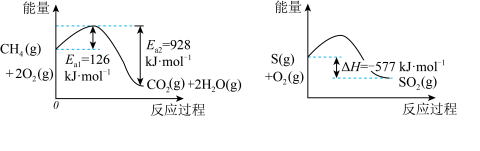
(1)1 mol (g)完全燃烧生成气态水的能量变化和1 mol S(g)燃烧的能量变化如图所示。在催化剂作用下,
(g)完全燃烧生成气态水的能量变化和1 mol S(g)燃烧的能量变化如图所示。在催化剂作用下, 可以还原
可以还原 生成单质S(g)、
生成单质S(g)、 (g)和
(g)和 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:____________ 。
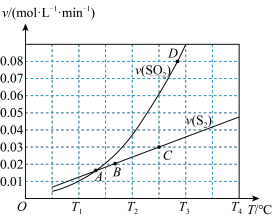
(2)焦炭催化还原二氧化硫的化学方程式为 。一定压强下,向1 L密闭容器中加入足量的焦炭和1 mol
。一定压强下,向1 L密闭容器中加入足量的焦炭和1 mol  发生反应,测得
发生反应,测得 的生成速率与
的生成速率与 (g)的生成速率随温度变化的关系如图所示:
(g)的生成速率随温度变化的关系如图所示:
① A、B、C、D四点对应的状态中,达到平衡状态的是_______ (填字母)。
②该反应的
_____ 0(填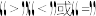 )。
)。
③下列措施能够增大 平衡转化率的是
平衡转化率的是______ 。
A 降低温度 B 增加C的量
C 减小容器体积 D 添加高效催化剂
(3)当吸收液失去吸收能力后通入 可得到
可得到 溶液,用如图所示装置电解
溶液,用如图所示装置电解 溶液可制得强氧化剂
溶液可制得强氧化剂 。
。

①写出电解 溶液的化学方程式:
溶液的化学方程式:________ 。
②若用9.65 A的恒定电流电解饱和 溶液1小时,理论上生成的
溶液1小时,理论上生成的 的物质的量为
的物质的量为________ (F=96500 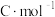 )。
)。
 的烟气会形成酸雨,危害环境。工业上常采用催化还原法和碱吸收法处理SO2气体。
的烟气会形成酸雨,危害环境。工业上常采用催化还原法和碱吸收法处理SO2气体。
(1)1 mol
 (g)完全燃烧生成气态水的能量变化和1 mol S(g)燃烧的能量变化如图所示。在催化剂作用下,
(g)完全燃烧生成气态水的能量变化和1 mol S(g)燃烧的能量变化如图所示。在催化剂作用下, 可以还原
可以还原 生成单质S(g)、
生成单质S(g)、 (g)和
(g)和 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:
(2)焦炭催化还原二氧化硫的化学方程式为
 。一定压强下,向1 L密闭容器中加入足量的焦炭和1 mol
。一定压强下,向1 L密闭容器中加入足量的焦炭和1 mol  发生反应,测得
发生反应,测得 的生成速率与
的生成速率与 (g)的生成速率随温度变化的关系如图所示:
(g)的生成速率随温度变化的关系如图所示:① A、B、C、D四点对应的状态中,达到平衡状态的是
②该反应的

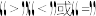 )。
)。③下列措施能够增大
 平衡转化率的是
平衡转化率的是A 降低温度 B 增加C的量
C 减小容器体积 D 添加高效催化剂
(3)当吸收液失去吸收能力后通入
 可得到
可得到 溶液,用如图所示装置电解
溶液,用如图所示装置电解 溶液可制得强氧化剂
溶液可制得强氧化剂 。
。
①写出电解
 溶液的化学方程式:
溶液的化学方程式:②若用9.65 A的恒定电流电解饱和
 溶液1小时,理论上生成的
溶液1小时,理论上生成的 的物质的量为
的物质的量为 )。
)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】铁、钴(Co)是同族元素,都是较活泼的金属,它们的化合物在工业上有重要的应用。
(1)草酸钴(CoC2O4)是一种难溶于水的浅粉红色粉末,通常用CoSO4溶液和(NH4)2C2O4溶液反应制得,写出该反应的离子方程式:______________
(2)现将含0.5mol FeCl3的溶液和含1.5mol KSCN的溶液混合,混合后溶液体积为1L,已知溶液存在平衡:Fe3++ 3SCN-=Fe(SCN)3(忽略其它过程)。平衡浓度 c[Fe(SCN)3]与温度T的关系如图1所示:则该反应△H____ 0(填“>”或“<”),温度为T1时,反应在5秒钟时达到平衡,则达到平衡时的平均反应速率v(SCN-)=____ ,该温度下的Fe3+的平衡转化率为____ 。
(3)工业上用电解浓NaOH溶液制备Na2FeO4,其工作原理如图2所示,则Cu电极连接电源的___ 极,阳极的电极反应式为________________

(1)草酸钴(CoC2O4)是一种难溶于水的浅粉红色粉末,通常用CoSO4溶液和(NH4)2C2O4溶液反应制得,写出该反应的离子方程式:
(2)现将含0.5mol FeCl3的溶液和含1.5mol KSCN的溶液混合,混合后溶液体积为1L,已知溶液存在平衡:Fe3++ 3SCN-=Fe(SCN)3(忽略其它过程)。平衡浓度 c[Fe(SCN)3]与温度T的关系如图1所示:则该反应△H
(3)工业上用电解浓NaOH溶液制备Na2FeO4,其工作原理如图2所示,则Cu电极连接电源的

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某研究性学习小组利用草酸溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验设计如下:(假设溶液混合时体积可以加和)
(1)写出草酸与酸性 KMnO4溶液反应的离子方程式:_________________ 。
(2)甲同学利用实验①来绘制反应过程中生成 CO2的物质的量 n(CO2)随反应时间 t 的变化曲线。反应在 t = t1时完成。试在下图中画出 n(CO2)随反应时间 t 变化的曲线____ ,并确定m =______________ mol。

(3)乙同学欲通过实验①、②探究反应物浓度对该反应速率的影响,则a =________ ,T = ____________ 。若 t1 < 8 s,可以得出的结论是: _____________________ 。
(4)在实验②的条件下,可以计算,从反应开始到结束,KMnO4 消耗的平均反应速率是____________ mol/(L·s)(保留两位有效数字)。
(5)通过比较实验②、③的结果,可以探究_____________ 变化对化学反应速率的影响。
(6)丙同学在实验④条件下进行该反应,结果却发现反应产生了二组分混合气体。元素分析测得该混合气体的含氧质量分数低于 CO2。溶液完全褪色后发现体系中残余的草酸浓度明显低于其他三组实验。丙同学猜测在实验④中出现了草酸分解的副反应。试写出实验④中草酸分解的化学方程式:______________________________________________ 。
实验序号 | 实验温度 (K) | 酸性 KMnO4溶液 | 草酸溶液 | 去离子水 | 溶液褪色 时间 | ||
| c (mol/L) | V (mL) | c (mol/L) | V (mL) | V (mL) | t (s) | ||
| ① | 298 | 0.02 | 2.0 | 0.10 | 4.0 | 0 | t1 |
| ② | T | 0.02 | 2.0 | 0.10 | 3.0 | a | 8.0 |
| ③ | 343 | 0.02 | 2.0 | 0.10 | 3.0 | a | t2 |
| ④ | 373 | 0.02 | 2.0 | 0.10 | 3.0 | a | t3 |
(2)甲同学利用实验①来绘制反应过程中生成 CO2的物质的量 n(CO2)随反应时间 t 的变化曲线。反应在 t = t1时完成。试在下图中画出 n(CO2)随反应时间 t 变化的曲线

(3)乙同学欲通过实验①、②探究反应物浓度对该反应速率的影响,则a =
(4)在实验②的条件下,可以计算,从反应开始到结束,KMnO4 消耗的平均反应速率是
(5)通过比较实验②、③的结果,可以探究
(6)丙同学在实验④条件下进行该反应,结果却发现反应产生了二组分混合气体。元素分析测得该混合气体的含氧质量分数低于 CO2。溶液完全褪色后发现体系中残余的草酸浓度明显低于其他三组实验。丙同学猜测在实验④中出现了草酸分解的副反应。试写出实验④中草酸分解的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】天然气是一种清洁的化石燃料,也是引起温室效应的一种物质。天然气的综合利用对节能减排、高效利用能源、减少二氧化碳排放有重大意义。作为化工原料,合成甲醇是天然气综合利用的重要途径。
CH4(g)+ CO2(g) 2CO(g)+ 2H2(g)△H=+247.3 kJ·mol—1 ①
2CO(g)+ 2H2(g)△H=+247.3 kJ·mol—1 ①
CH4(g)+H2O(g) CO(g)+3H2(g) △H=+206.2 kJ·mol—1 ②
CO(g)+3H2(g) △H=+206.2 kJ·mol—1 ②
Ⅰ、合成甲醇的主要反应为:2H2(g)+ CO(g) CH3OH(g) △H=-90.8 kJ·mol—1
CH3OH(g) △H=-90.8 kJ·mol—1
(1)该反应熵变△S________ 0(填“>、=或<”),该反应在______ (填“高温”或“低温”)条件下能自发进行。
(2)生产过程中,合成气要循环,其目的是:________________________________ 。
(3)T℃下此反应的平衡常数为160。某时刻测得各组分的浓度如下,比较此时正、逆反应速率的大小:υ(正)________ υ(逆)(填“>”“<”或“=”)
(4)在恒温恒容条件下,充入一定量的H2和CO,发生上述反应,则该反应达到平衡状态的标志有( )
A.混合气体的密度保持不变 B.混合气体的总压强保持不变
C.甲醇的浓度保持不变 D.υ正(H2)= υ逆(CH3OH)
(5)在恒温恒容条件下,要提高反应2H2(g)+ CO(g) CH3OH(g)中CO的转化率,可以采取的措施是
CH3OH(g)中CO的转化率,可以采取的措施是( )
A.升温 B.加入催化剂 C.增加CO的浓度
D.增加H2的浓度 E.充入惰性气体 F.分离出甲醇
Ⅱ、合成甲醇的另一反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-akJ·mol-1(a>0)。
CH3OH(g)+H2O(g) △H=-akJ·mol-1(a>0)。
在一定温度下的2L固定容积的密闭容器中,通入2 molCO2和3mol H2,发生上述反应,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。

(6)下列措施中能使n(CH3OH )/n(CO2 )增大的是______ (填编号)。
A.升高温度
B.恒温恒容下充入He(g)
C.将H2O(g)从体系中分离
D.恒温恒容再充入2 mol CO2和3 mol H2
(7)经计算该温度下此反应的平衡常数K=0.20 L2·mol—2。若改变条件_________ (填选项),可使K=1。
A.增大压强 B.增大反应物浓度 C.降低温度
D.升高温度 E.加入催化剂
(8)10min内,用H2表示的该反应的化学反应速率为=_________ mol·L—1·min—1
CH4(g)+ CO2(g)
 2CO(g)+ 2H2(g)△H=+247.3 kJ·mol—1 ①
2CO(g)+ 2H2(g)△H=+247.3 kJ·mol—1 ①CH4(g)+H2O(g)
 CO(g)+3H2(g) △H=+206.2 kJ·mol—1 ②
CO(g)+3H2(g) △H=+206.2 kJ·mol—1 ②Ⅰ、合成甲醇的主要反应为:2H2(g)+ CO(g)
 CH3OH(g) △H=-90.8 kJ·mol—1
CH3OH(g) △H=-90.8 kJ·mol—1 (1)该反应熵变△S
(2)生产过程中,合成气要循环,其目的是:
(3)T℃下此反应的平衡常数为160。某时刻测得各组分的浓度如下,比较此时正、逆反应速率的大小:υ(正)
| 物质 | H2 | CO | CH3OH |
| 浓度/(mol·L—1) | 0.20 | 0.10 | 0.40 |
(4)在恒温恒容条件下,充入一定量的H2和CO,发生上述反应,则该反应达到平衡状态的标志有
A.混合气体的密度保持不变 B.混合气体的总压强保持不变
C.甲醇的浓度保持不变 D.υ正(H2)= υ逆(CH3OH)
(5)在恒温恒容条件下,要提高反应2H2(g)+ CO(g)
 CH3OH(g)中CO的转化率,可以采取的措施是
CH3OH(g)中CO的转化率,可以采取的措施是A.升温 B.加入催化剂 C.增加CO的浓度
D.增加H2的浓度 E.充入惰性气体 F.分离出甲醇
Ⅱ、合成甲醇的另一反应为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-akJ·mol-1(a>0)。
CH3OH(g)+H2O(g) △H=-akJ·mol-1(a>0)。在一定温度下的2L固定容积的密闭容器中,通入2 molCO2和3mol H2,发生上述反应,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。

(6)下列措施中能使n(CH3OH )/n(CO2 )增大的是
A.升高温度
B.恒温恒容下充入He(g)
C.将H2O(g)从体系中分离
D.恒温恒容再充入2 mol CO2和3 mol H2
(7)经计算该温度下此反应的平衡常数K=0.20 L2·mol—2。若改变条件
A.增大压强 B.增大反应物浓度 C.降低温度
D.升高温度 E.加入催化剂
(8)10min内,用H2表示的该反应的化学反应速率为=
您最近一年使用:0次
【推荐1】甲醇是重要的化工基础原料和清洁液体燃料,在CO2加氢合成CH3OH的体系中,同时发生下列竞争反应:
(ⅰ)CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.3 kJ/mol
CH3OH(g)+H2O(g) △H1=-49.3 kJ/mol
(ⅱ)CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.1 kJ/mol
CO(g)+H2O(g) △H2=+41.1 kJ/mol
由CO也能直接加氢合成甲醇:(iii) 2H2(g)+CO(g) CH3OH(g) △H
CH3OH(g) △H
(1)△H =_______ kJ/mol。
(2)反应(ⅱ) CO2(g)+H2(g) CO(g)+H2O(g)的正、逆反应平衡常数随温度变化曲线如图所示。
CO(g)+H2O(g)的正、逆反应平衡常数随温度变化曲线如图所示。
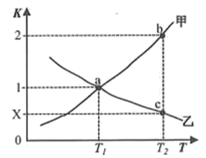
下列分析正确的是_______ 。
A.曲线甲为K(逆),曲线乙为K(正)
B.a点时,一定有v正=v逆
C.c点时,x=0.5
(3)催化剂M、N对CO2(g)+3H2(g) CH3OH(g)+H2O(g)反应进程的能量影响如下图(a)所示,两种催化剂对应的1nk~
CH3OH(g)+H2O(g)反应进程的能量影响如下图(a)所示,两种催化剂对应的1nk~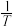 关系如下图(b)所示(已知;lnk=-
关系如下图(b)所示(已知;lnk=-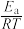 +C,其中Ea为活化能,k为速率常数,R和C为常数)。
+C,其中Ea为活化能,k为速率常数,R和C为常数)。
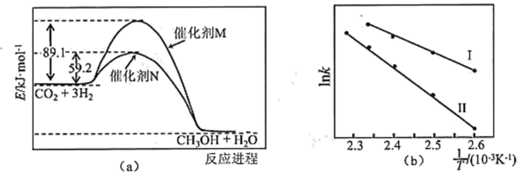
①使用催化剂M时,逆反应的活化能为_______ kJ/mol。
②催化剂N对应曲线是图(b)中的_______ (填“Ⅰ”或“Ⅱ”)
(4)为进一步研究CO2与H2反应制CH3OH的过程中原料气组成对反应速率的影响,分别向三个压强恒定为P的密闭容器(装有等量催化剂,且在实验温度范围内催化剂活性变化不大)中通入相同碳氢比的三种混合气,相同时间内,测得甲醇生成速率与温度的关系如图所示。
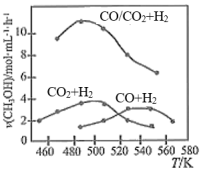
①三个容器中,甲醇的生成速率达峰值后均随温度升高而下降的原因是_______ 。
②结合研究目的,参照图中三条曲线,你可得出的结论是_______ (写一条)。
(5)恒温下,在压强恒定为P的装置中,按n(CO2):n(H2)=1:3加入反应物,发生反应(ⅰ)、(ⅱ)。达到平衡时,若CO2转化率为20%,甲醇的选择性为50%。列出反应(ⅰ)CO2(g)+3H2(g) CH3OH(g)+H2O(g)的平衡常数计算式:Kp=
CH3OH(g)+H2O(g)的平衡常数计算式:Kp=_______ (不必化简)。(已知: 的选择性x=
的选择性x=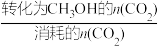 ×100%;Kp为用分压代替浓度的平衡常数。)
×100%;Kp为用分压代替浓度的平衡常数。)
(ⅰ)CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49.3 kJ/mol
CH3OH(g)+H2O(g) △H1=-49.3 kJ/mol(ⅱ)CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.1 kJ/mol
CO(g)+H2O(g) △H2=+41.1 kJ/mol由CO也能直接加氢合成甲醇:(iii) 2H2(g)+CO(g)
 CH3OH(g) △H
CH3OH(g) △H(1)△H =
(2)反应(ⅱ) CO2(g)+H2(g)
 CO(g)+H2O(g)的正、逆反应平衡常数随温度变化曲线如图所示。
CO(g)+H2O(g)的正、逆反应平衡常数随温度变化曲线如图所示。
下列分析正确的是
A.曲线甲为K(逆),曲线乙为K(正)
B.a点时,一定有v正=v逆
C.c点时,x=0.5
(3)催化剂M、N对CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)反应进程的能量影响如下图(a)所示,两种催化剂对应的1nk~
CH3OH(g)+H2O(g)反应进程的能量影响如下图(a)所示,两种催化剂对应的1nk~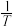 关系如下图(b)所示(已知;lnk=-
关系如下图(b)所示(已知;lnk=-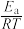 +C,其中Ea为活化能,k为速率常数,R和C为常数)。
+C,其中Ea为活化能,k为速率常数,R和C为常数)。
①使用催化剂M时,逆反应的活化能为
②催化剂N对应曲线是图(b)中的
(4)为进一步研究CO2与H2反应制CH3OH的过程中原料气组成对反应速率的影响,分别向三个压强恒定为P的密闭容器(装有等量催化剂,且在实验温度范围内催化剂活性变化不大)中通入相同碳氢比的三种混合气,相同时间内,测得甲醇生成速率与温度的关系如图所示。

①三个容器中,甲醇的生成速率达峰值后均随温度升高而下降的原因是
②结合研究目的,参照图中三条曲线,你可得出的结论是
(5)恒温下,在压强恒定为P的装置中,按n(CO2):n(H2)=1:3加入反应物,发生反应(ⅰ)、(ⅱ)。达到平衡时,若CO2转化率为20%,甲醇的选择性为50%。列出反应(ⅰ)CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)的平衡常数计算式:Kp=
CH3OH(g)+H2O(g)的平衡常数计算式:Kp= 的选择性x=
的选择性x=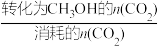 ×100%;Kp为用分压代替浓度的平衡常数。)
×100%;Kp为用分压代替浓度的平衡常数。)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】研究CO、CO2的回收利用既可变废为宝,又可减少碳的排放。请回答下列问题:
(1)二甲醚(CH3OCH3)被誉为“21世纪的清洁燃料”,由CO和H2制备二甲醚的反应原理如下:
CO(g)+2H2(g)⇌CH3OH(g) △H=-90.1kJ/mol
2CH3OH(g)⇌CH3OCH3(g)+H2O(g) △H=-24.5kJ/mol
已知:CO(g)+H2O(g)⇌CO2(g)+H2(g) △H=-41.0kJ/mol
则2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)的△H=________
(2)T1K时,将1mol二甲醚引入一个抽真空的150L恒容密闭容器中,发生分解反应CH3OCH3(g)⇌CH4(g)+H2(g)+CO(g)。
在不同时间测定容器内的总压,所得数据见下表,
①由表中数据计算,0~6.5min内的平均反应速率)(CH3OCH3)=___
mol⋅L-1⋅min-1(结果保留两位有效数字)反应达平衡时,二甲醚的分解率为___ ,该温度下平衡常数K=___ 。
②反应达到平衡后,若升高温度,CH3OCH3的浓度增大,则该反应为___ 反应(填“放热”或“吸热”)。
在T2K、1.0×104 kPa下,等物质的量的CO与CH4混合气体发生如下反应:CO(g)+CH4(g)=CH3CHO(g)
反应速率v=v正-v逆=k正p(CO)⋅p(CH4)-k逆p(CH3HO),k正、k逆分别为k正、k逆向反应速率常数,p为气体的分压(气体分压p=气体总压p总×体积分数)。用气体分压表示的平衡常数KP=4.5×10-5kPa-1,则CO的转化率为20%时, =
=___ 。
(1)二甲醚(CH3OCH3)被誉为“21世纪的清洁燃料”,由CO和H2制备二甲醚的反应原理如下:
CO(g)+2H2(g)⇌CH3OH(g) △H=-90.1kJ/mol
2CH3OH(g)⇌CH3OCH3(g)+H2O(g) △H=-24.5kJ/mol
已知:CO(g)+H2O(g)⇌CO2(g)+H2(g) △H=-41.0kJ/mol
则2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)的△H=
(2)T1K时,将1mol二甲醚引入一个抽真空的150L恒容密闭容器中,发生分解反应CH3OCH3(g)⇌CH4(g)+H2(g)+CO(g)。
在不同时间测定容器内的总压,所得数据见下表,
| 反应时间t/min | 0 | 6.5 | 13.0 | 26.5 | 52.6 | ∞ |
| 气体总压p总/kPa | 50.0 | 55.0 | 65.0 | 83.2 | 103.8 | 125.0 |
①由表中数据计算,0~6.5min内的平均反应速率)(CH3OCH3)=
mol⋅L-1⋅min-1(结果保留两位有效数字)反应达平衡时,二甲醚的分解率为
②反应达到平衡后,若升高温度,CH3OCH3的浓度增大,则该反应为
在T2K、1.0×104 kPa下,等物质的量的CO与CH4混合气体发生如下反应:CO(g)+CH4(g)=CH3CHO(g)
反应速率v=v正-v逆=k正p(CO)⋅p(CH4)-k逆p(CH3HO),k正、k逆分别为k正、k逆向反应速率常数,p为气体的分压(气体分压p=气体总压p总×体积分数)。用气体分压表示的平衡常数KP=4.5×10-5kPa-1,则CO的转化率为20%时,
 =
=
您最近一年使用:0次
【推荐3】CO、CO2气体的综合利用,是化学工业重要研究方向之一。工业上用CO、CO2、H2来合成甲醇(CH3OH),有关信息如下:
(1)反应Ⅲ的△H___ 0(填“>”或“<”)。
(2)反应Ⅲ:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。最近采用真空封管法制备的磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:
CH3OH(g)+H2O(g)。最近采用真空封管法制备的磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:

容易得到的副产物有CO和CH2O,其中相对较少的副产物为___ ;上述合成甲醇的反应速率较慢,要使反应速率加只快,主要降低下列变化中___ (填字母)的能量变化。
A.*OCH3→*CH3OH B. *CO→*COH
C. *OCH2→*OCH3 D. *CO+*OH→*CO+*H2O
(3)一定温度下,在某恒容密闭容器中充入6molH2和2molCO2,测得初始压强为16MPa,在催化剂条件下发生CO2(g) +3H2(g) CH3OH(g)+H2O(g),平衡后压强减少了6MPa。反应后CH3OH的压强为
CH3OH(g)+H2O(g),平衡后压强减少了6MPa。反应后CH3OH的压强为___ ;用压强代替物质的量浓度来表示K值,则反应的Kp=___ 。
(4)已知水煤气变换反应:CO(g)+H2O(g) CO2(g)+H2(g)。将等体积CO、H2O充入恒容密闭容器中,反应速率v=v正-v逆=k正c(CO)c(H2O)-k逆c(CO2)c(H2),其中正、逆反应的速率常数只与温度有关。在T1和T2时,CO的转化率与时间变化如图所示。
CO2(g)+H2(g)。将等体积CO、H2O充入恒容密闭容器中,反应速率v=v正-v逆=k正c(CO)c(H2O)-k逆c(CO2)c(H2),其中正、逆反应的速率常数只与温度有关。在T1和T2时,CO的转化率与时间变化如图所示。

①M点与N点对应的 的大小关系:M
的大小关系:M___ N(填“>”“=”或“<”)。
②N点时 =
=___ 。
| 化学反应 | 平衡常数 | 温度/℃ | ||
| 500 | 700 | 800 | ||
Ⅰ.2H2(g)+CO(g) CH3OH(g) △H1 CH3OH(g) △H1 | K1 | 2.5 | 0.34 | 0.015 |
Ⅱ.H2(g)+CO2(g) H2O(g)+CO(g) △H2 H2O(g)+CO(g) △H2 | K2 | 1.0 | 1.70 | 2.52 |
Ⅲ.3H2(g)+CO2(g) CH3OH(g)+H2O(g) △H CH3OH(g)+H2O(g) △H | K3 | |||
(2)反应Ⅲ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。最近采用真空封管法制备的磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:
CH3OH(g)+H2O(g)。最近采用真空封管法制备的磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:
容易得到的副产物有CO和CH2O,其中相对较少的副产物为
A.*OCH3→*CH3OH B. *CO→*COH
C. *OCH2→*OCH3 D. *CO+*OH→*CO+*H2O
(3)一定温度下,在某恒容密闭容器中充入6molH2和2molCO2,测得初始压强为16MPa,在催化剂条件下发生CO2(g) +3H2(g)
 CH3OH(g)+H2O(g),平衡后压强减少了6MPa。反应后CH3OH的压强为
CH3OH(g)+H2O(g),平衡后压强减少了6MPa。反应后CH3OH的压强为(4)已知水煤气变换反应:CO(g)+H2O(g)
 CO2(g)+H2(g)。将等体积CO、H2O充入恒容密闭容器中,反应速率v=v正-v逆=k正c(CO)c(H2O)-k逆c(CO2)c(H2),其中正、逆反应的速率常数只与温度有关。在T1和T2时,CO的转化率与时间变化如图所示。
CO2(g)+H2(g)。将等体积CO、H2O充入恒容密闭容器中,反应速率v=v正-v逆=k正c(CO)c(H2O)-k逆c(CO2)c(H2),其中正、逆反应的速率常数只与温度有关。在T1和T2时,CO的转化率与时间变化如图所示。
①M点与N点对应的
 的大小关系:M
的大小关系:M②N点时
 =
=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】完成下列问题
(1)燃料电池是一种将燃料(如氢气、甲烷、乙醇、肼等)和氧化剂(如氧气)的化学能直接转化为电能的电化学反应装置,具有清洁、安全、高效等特点。燃料电池的能量转化率可以达到80%以上。如以反应 为原理设计成燃料电池,其利用率高,装置如图所示。
为原理设计成燃料电池,其利用率高,装置如图所示。___________ ,a处的电极反应式是___________ 。
②当消耗标准状况下
 时,导线上转移的电子的物质的量是
时,导线上转移的电子的物质的量是___________ mol。
(2)将一定量纯净的氨基甲酸铵置于恒容密闭真空容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡: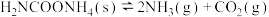 。
。不能 判断该反应已经达到化学平衡的是___________ 。
①
②密闭容器中总压强不变
③密闭容器中混合气体的密度不变
④混合气体总质量不变
⑤密闭容器混合气体的总物质的量不变
⑥密闭容器中 的体积分数不变
的体积分数不变
⑦密闭容器中混合气体的平均相对分子质量不变
(3)一定条件下,在5L密闭容器内,反应 ,
, 的物质的量随时间变化如表:
的物质的量随时间变化如表:
用 表示
表示 内该反应的平均速率为
内该反应的平均速率为___________ 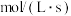 。在第5s时,
。在第5s时, 的转化率为
的转化率为___________ ,在第2s时 的体积分数为
的体积分数为___________ 。
(4)已知: ,不同温度(T)下,
,不同温度(T)下, 分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度 消耗一半时所需的相应时间),则
消耗一半时所需的相应时间),则
___________  (填“>”、“=”或“<”)。当温度为
(填“>”、“=”或“<”)。当温度为 、起始压强为
、起始压强为 ,反应至
,反应至 时,此时体系压强
时,此时体系压强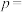
___________ (用 表示)。
表示)。
(1)燃料电池是一种将燃料(如氢气、甲烷、乙醇、肼等)和氧化剂(如氧气)的化学能直接转化为电能的电化学反应装置,具有清洁、安全、高效等特点。燃料电池的能量转化率可以达到80%以上。如以反应
 为原理设计成燃料电池,其利用率高,装置如图所示。
为原理设计成燃料电池,其利用率高,装置如图所示。
②当消耗标准状况下

 时,导线上转移的电子的物质的量是
时,导线上转移的电子的物质的量是(2)将一定量纯净的氨基甲酸铵置于恒容密闭真空容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
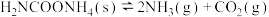 。
。①

②密闭容器中总压强不变
③密闭容器中混合气体的密度不变
④混合气体总质量不变
⑤密闭容器混合气体的总物质的量不变
⑥密闭容器中
 的体积分数不变
的体积分数不变⑦密闭容器中混合气体的平均相对分子质量不变
(3)一定条件下,在5L密闭容器内,反应
 ,
, 的物质的量随时间变化如表:
的物质的量随时间变化如表:时间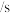 | 0 | 1 | 2 | 3 | 4 | 5 |
 | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
 表示
表示 内该反应的平均速率为
内该反应的平均速率为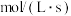 。在第5s时,
。在第5s时, 的转化率为
的转化率为 的体积分数为
的体积分数为(4)已知:
 ,不同温度(T)下,
,不同温度(T)下, 分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度 消耗一半时所需的相应时间),则
消耗一半时所需的相应时间),则
 (填“>”、“=”或“<”)。当温度为
(填“>”、“=”或“<”)。当温度为 、起始压强为
、起始压强为 ,反应至
,反应至 时,此时体系压强
时,此时体系压强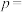
 表示)。
表示)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】 存在于天然气、沼气、煤矿坑井气中,它既是优质气体燃料,也是制造合成气和许多化工产品的重要原料。回答下列问题:
存在于天然气、沼气、煤矿坑井气中,它既是优质气体燃料,也是制造合成气和许多化工产品的重要原料。回答下列问题:
(1) 催化重整不仅可以得到合成气(
催化重整不仅可以得到合成气( 和
和 ),还对温室气体的减排具有重要意义。
),还对温室气体的减排具有重要意义。
已知:

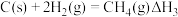
 催化重整反应:
催化重整反应: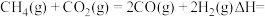
_______ (用 、
、 、
、 表示),若
表示),若 ,则
,则 催化重整反应为
催化重整反应为__________ (填“吸”或“放”)热反应。
(2)图中为甲烷燃烧过程的能量变化,该反应的活化能为_______  ,
,
_______  。
。

(3)图中是目前研究较多的一类 燃料电池的工作原理示意图。
燃料电池的工作原理示意图。
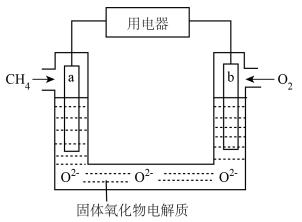
①a极为电池___________ (填“正”或“负”)极;b极的电极反应式为_________ 。
②电池中内电路的 移向
移向___________ (填“a”或“b”)极。
(4)用该燃料电池电解 溶液(电极材料为石墨),当电子转移
溶液(电极材料为石墨),当电子转移 时,阴极产物是
时,阴极产物是____________ (写化学式),阳极析出气体体积为________ L(标准状况)。
 存在于天然气、沼气、煤矿坑井气中,它既是优质气体燃料,也是制造合成气和许多化工产品的重要原料。回答下列问题:
存在于天然气、沼气、煤矿坑井气中,它既是优质气体燃料,也是制造合成气和许多化工产品的重要原料。回答下列问题:(1)
 催化重整不仅可以得到合成气(
催化重整不仅可以得到合成气( 和
和 ),还对温室气体的减排具有重要意义。
),还对温室气体的减排具有重要意义。已知:


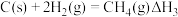
 催化重整反应:
催化重整反应: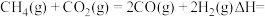
 、
、 、
、 表示),若
表示),若 ,则
,则 催化重整反应为
催化重整反应为(2)图中为甲烷燃烧过程的能量变化,该反应的活化能为
 ,
,
 。
。
(3)图中是目前研究较多的一类
 燃料电池的工作原理示意图。
燃料电池的工作原理示意图。
①a极为电池
②电池中内电路的
 移向
移向(4)用该燃料电池电解
 溶液(电极材料为石墨),当电子转移
溶液(电极材料为石墨),当电子转移 时,阴极产物是
时,阴极产物是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氮氧化物是主要大气污染物,可采用多种方法消除,其中氢气选择性催化还原(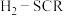 )是一种理想的方法,备受研究者关注,其相关反应如下:
)是一种理想的方法,备受研究者关注,其相关反应如下:
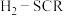 法的主反应:
法的主反应:

副反应: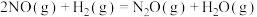

(1)已知: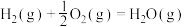
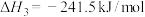
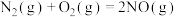
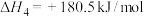
①
_____ 。
②副反应能自发进行的条件是_____ (填“低温”或“高温”)。
(2)恒温条件下,将NO、 充入某恒容密闭容器中,在催化剂作用下进行反应。在不同温度下,反应相同时间时测得混合气体中
充入某恒容密闭容器中,在催化剂作用下进行反应。在不同温度下,反应相同时间时测得混合气体中 、
、 的体积分数随温度的变化关系如图所示。
的体积分数随温度的变化关系如图所示。
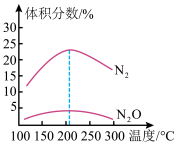
①提高主反应选择性的最佳措施是_____ (填序号)。
A降低温度 B.使用合适的催化剂 C.增大 D.增大压强
D.增大压强
②如图,温度高于205℃时, 的体积分数随温度的升高而减小的原因可能是
的体积分数随温度的升高而减小的原因可能是_____ 。
(3)T℃, 恒容密闭容器中发生上述反应,平衡体系中
恒容密闭容器中发生上述反应,平衡体系中 物质的量分数为10%,平衡压强与起始压强之比为3.6∶4,则NO的有效去除率(转化为
物质的量分数为10%,平衡压强与起始压强之比为3.6∶4,则NO的有效去除率(转化为 )为
)为_____ 。
(4)一定条件下,恒温恒容容器中充入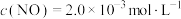 、
、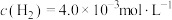 ,只发生
,只发生 反应,体系的总压强p随时间t的变化如下表所示:[已知该反应速率方程为
反应,体系的总压强p随时间t的变化如下表所示:[已知该反应速率方程为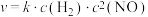 ]
]
当t=20min时,
_____  (速率常数
(速率常数 )
)
(5) 、
、 和熔融
和熔融 可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则石墨Ⅰ为原电池的
可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则石墨Ⅰ为原电池的_____ 极,正极反应式为_____ 。

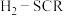 )是一种理想的方法,备受研究者关注,其相关反应如下:
)是一种理想的方法,备受研究者关注,其相关反应如下: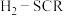 法的主反应:
法的主反应:

副反应:
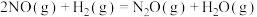

(1)已知:
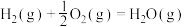
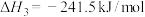
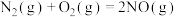
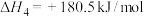
①

②副反应能自发进行的条件是
(2)恒温条件下,将NO、
 充入某恒容密闭容器中,在催化剂作用下进行反应。在不同温度下,反应相同时间时测得混合气体中
充入某恒容密闭容器中,在催化剂作用下进行反应。在不同温度下,反应相同时间时测得混合气体中 、
、 的体积分数随温度的变化关系如图所示。
的体积分数随温度的变化关系如图所示。
①提高主反应选择性的最佳措施是
A降低温度 B.使用合适的催化剂 C.增大
 D.增大压强
D.增大压强②如图,温度高于205℃时,
 的体积分数随温度的升高而减小的原因可能是
的体积分数随温度的升高而减小的原因可能是(3)T℃,
 恒容密闭容器中发生上述反应,平衡体系中
恒容密闭容器中发生上述反应,平衡体系中 物质的量分数为10%,平衡压强与起始压强之比为3.6∶4,则NO的有效去除率(转化为
物质的量分数为10%,平衡压强与起始压强之比为3.6∶4,则NO的有效去除率(转化为 )为
)为(4)一定条件下,恒温恒容容器中充入
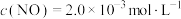 、
、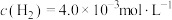 ,只发生
,只发生 反应,体系的总压强p随时间t的变化如下表所示:[已知该反应速率方程为
反应,体系的总压强p随时间t的变化如下表所示:[已知该反应速率方程为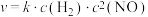 ]
]| t/min | 0 | 10 | 20 | 30 | 40 |
| p/kPa | 24 | 22.6 | 21.6 | 21 | 21 |

 (速率常数
(速率常数 )
)(5)
 、
、 和熔融
和熔融 可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则石墨Ⅰ为原电池的
可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则石墨Ⅰ为原电池的
您最近一年使用:0次



