硫酸亚铁铵[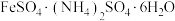 ,相对分子质量为M]为浅绿色晶体,在空气中能稳定存在,不易被氧化,溶于水,不溶于乙醇、实验室制备过程如下:
,相对分子质量为M]为浅绿色晶体,在空气中能稳定存在,不易被氧化,溶于水,不溶于乙醇、实验室制备过程如下:
第一步:在圆底烧瓶中称取mg铁屑,再用量筒量取15mL 的稀硫酸,实验装置如图所示,在80℃条件下电磁搅拌反应3min。
的稀硫酸,实验装置如图所示,在80℃条件下电磁搅拌反应3min。 溶液的蒸发皿中,水浴加热搅拌至硫酸铵全部溶解,停止搅拌,继续蒸发浓缩直至表面有晶膜出现。
溶液的蒸发皿中,水浴加热搅拌至硫酸铵全部溶解,停止搅拌,继续蒸发浓缩直至表面有晶膜出现。
第三步:冷却至室温,待有大量晶体析出时,减压过滤,用试剂N少量多次洗涤,干燥后,称得晶体质量为11.8g。计算产率。
回答下列问题:
(1)硫酸亚铁铵中组成元素的原子半径由大到小的顺序为___________ 。
(2)已知:Cr的3d比4p能量低得多,重铬酸钾具有二聚结构,它由两个通过氧原子键合在一起的铬原子组成,中心Cr为正四面体形,结构为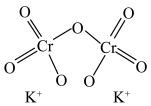 ,其中Cr原子的杂化方式为___________(填标号)。
,其中Cr原子的杂化方式为___________(填标号)。
(3)圆底烧瓶中生成 的离子方程式为
的离子方程式为___________ 。
(4)第二步中需要称量剩余铁屑质量的原因为___________ ,写出制备硫酸亚铁铵晶体的化学方程式:___________ 。
(5)试剂N是___________ 。
(6)准确称取0.8g硫酸亚铁铵晶体三份,分别放入三个250mL锥形瓶中,加入100mL水,20mL 的硫酸。1g氟化铵固体(不参与反应,有利于滴定终点的判断)。6~8滴二苯胺磺酸钠指示剂,用
的硫酸。1g氟化铵固体(不参与反应,有利于滴定终点的判断)。6~8滴二苯胺磺酸钠指示剂,用 重铬酸钾标准液进行滴定。
重铬酸钾标准液进行滴定。
①重铬酸钾在酸性条件下的还原产物为 ,写出该滴定反应的离子方程式:
,写出该滴定反应的离子方程式:___________ 。
②三次实验消耗标准液的体积分别是16.75mL、16.80mL、16.85mL,则硫酸亚铁铵晶体的纯度为___________ (写出含M的表达式)。
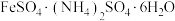 ,相对分子质量为M]为浅绿色晶体,在空气中能稳定存在,不易被氧化,溶于水,不溶于乙醇、实验室制备过程如下:
,相对分子质量为M]为浅绿色晶体,在空气中能稳定存在,不易被氧化,溶于水,不溶于乙醇、实验室制备过程如下:第一步:在圆底烧瓶中称取mg铁屑,再用量筒量取15mL
 的稀硫酸,实验装置如图所示,在80℃条件下电磁搅拌反应3min。
的稀硫酸,实验装置如图所示,在80℃条件下电磁搅拌反应3min。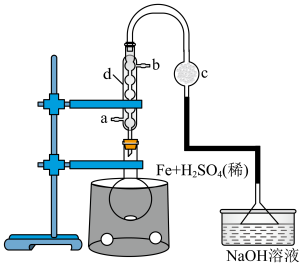
 溶液的蒸发皿中,水浴加热搅拌至硫酸铵全部溶解,停止搅拌,继续蒸发浓缩直至表面有晶膜出现。
溶液的蒸发皿中,水浴加热搅拌至硫酸铵全部溶解,停止搅拌,继续蒸发浓缩直至表面有晶膜出现。第三步:冷却至室温,待有大量晶体析出时,减压过滤,用试剂N少量多次洗涤,干燥后,称得晶体质量为11.8g。计算产率。
回答下列问题:
(1)硫酸亚铁铵中组成元素的原子半径由大到小的顺序为
(2)已知:Cr的3d比4p能量低得多,重铬酸钾具有二聚结构,它由两个通过氧原子键合在一起的铬原子组成,中心Cr为正四面体形,结构为
 ,其中Cr原子的杂化方式为___________(填标号)。
,其中Cr原子的杂化方式为___________(填标号)。A. | B. | C.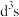 | D.sp |
(3)圆底烧瓶中生成
 的离子方程式为
的离子方程式为(4)第二步中需要称量剩余铁屑质量的原因为
(5)试剂N是
(6)准确称取0.8g硫酸亚铁铵晶体三份,分别放入三个250mL锥形瓶中,加入100mL水,20mL
 的硫酸。1g氟化铵固体(不参与反应,有利于滴定终点的判断)。6~8滴二苯胺磺酸钠指示剂,用
的硫酸。1g氟化铵固体(不参与反应,有利于滴定终点的判断)。6~8滴二苯胺磺酸钠指示剂,用 重铬酸钾标准液进行滴定。
重铬酸钾标准液进行滴定。①重铬酸钾在酸性条件下的还原产物为
 ,写出该滴定反应的离子方程式:
,写出该滴定反应的离子方程式:②三次实验消耗标准液的体积分别是16.75mL、16.80mL、16.85mL,则硫酸亚铁铵晶体的纯度为
更新时间:2024-05-26 09:35:11
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】化肥厂所产生的废水中,氮元素多以NH 和NH3·H2O的形式存在,直接排入水体中,不仅会引起水体富营养化,还会对人群及生物产生毒害作用。工业上,常用NaNO2来处理含NH
和NH3·H2O的形式存在,直接排入水体中,不仅会引起水体富营养化,还会对人群及生物产生毒害作用。工业上,常用NaNO2来处理含NH 或NH3·H2O的废水,其流程如图所示:
或NH3·H2O的废水,其流程如图所示:
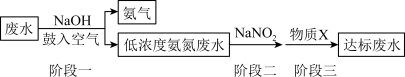
已知:二价硫可表示为S(II);NaNO2易被空气中的氧气氧化,其与稀硫酸反应会生成易分解的亚硝酸。
(1)NaNO2中N的化合价为_______ 价。
(2)NaNO2的外观、味道均与食盐相似,但具有剧毒,被严禁作为食盐食用。误食后,能将血液中的Fe(II)_______ (填“氧化”或“还原”)为Fe(III);服用维生素C能缓解NaNO2中毒,维生素C作_______ (填“氧化剂”或“还原剂”)。
(3)在“阶段一”中,加入NaOH的作用为_______ (用离子方程式表示);鼓入空气的目的是_______ 。
(4)“阶段二”中NH 与NaNO2反应生成无污染的物质,该反应的离子方程式为
与NaNO2反应生成无污染的物质,该反应的离子方程式为_______ 。
(5)某化学兴趣小组设计如下实验探究NaNO2溶液与KI溶液的反应,步骤及现象如下。
①2mL注射器,吸取1mL浓度均为0.2mol·L-1NaNO2和KI的混合溶液,针头朝上排出空气。
②吸入少量稀硫酸并迅速将针头插入橡皮塞,观察到有无色气泡产生,溶液变黑,黑色固体析出附着在壁上,轻轻摇动将黑色固体洗到溶液中。
③摘去橡皮塞,轻轻拉动注射器活塞,吸入少量空气,观察到无色气体变成红棕色。
④将注射器中少量溶液挤入淀粉溶液中,观察到淀粉溶液变为蓝色。
步骤①中排出空气的目的是_______ ;步骤③中红棕色气体的化学式为_______ ;实验中NaNO2溶液与KI溶液发生反应的离子方程式为_______ 。
 和NH3·H2O的形式存在,直接排入水体中,不仅会引起水体富营养化,还会对人群及生物产生毒害作用。工业上,常用NaNO2来处理含NH
和NH3·H2O的形式存在,直接排入水体中,不仅会引起水体富营养化,还会对人群及生物产生毒害作用。工业上,常用NaNO2来处理含NH 或NH3·H2O的废水,其流程如图所示:
或NH3·H2O的废水,其流程如图所示:
已知:二价硫可表示为S(II);NaNO2易被空气中的氧气氧化,其与稀硫酸反应会生成易分解的亚硝酸。
(1)NaNO2中N的化合价为
(2)NaNO2的外观、味道均与食盐相似,但具有剧毒,被严禁作为食盐食用。误食后,能将血液中的Fe(II)
(3)在“阶段一”中,加入NaOH的作用为
(4)“阶段二”中NH
 与NaNO2反应生成无污染的物质,该反应的离子方程式为
与NaNO2反应生成无污染的物质,该反应的离子方程式为(5)某化学兴趣小组设计如下实验探究NaNO2溶液与KI溶液的反应,步骤及现象如下。
①2mL注射器,吸取1mL浓度均为0.2mol·L-1NaNO2和KI的混合溶液,针头朝上排出空气。
②吸入少量稀硫酸并迅速将针头插入橡皮塞,观察到有无色气泡产生,溶液变黑,黑色固体析出附着在壁上,轻轻摇动将黑色固体洗到溶液中。
③摘去橡皮塞,轻轻拉动注射器活塞,吸入少量空气,观察到无色气体变成红棕色。
④将注射器中少量溶液挤入淀粉溶液中,观察到淀粉溶液变为蓝色。
步骤①中排出空气的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某实验小组以CoCl2·6H2O、过氧化氢、液氨、氯化铵固体为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,他们进行了如下实验:
①氨的测定:精确称取wgX,加适量水溶解,注入下图所示的蒸馏烧瓶中(夹持和加热仪器略去),然后逐滴加入足量10%NaOH溶液,加热烧瓶将氨蒸出,用V1mLc1mol·L-1的盐酸吸收蒸出的氨,然后取下锥形瓶,用c2 mol·L-1 NaOH标准溶液滴定过剩的HCl。.终点时消耗V2 mLNaOH溶液。
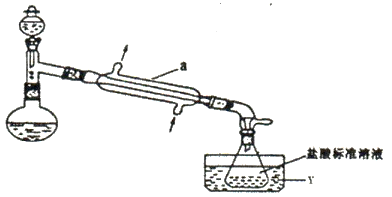
②氯的测定:准确称取样品X配成溶液,用K2CrO4溶液为指示剂,用AgNO3标准溶液滴定,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)
回答下列问题:
(1)X的制备过程中,温度不能过高,其原因是____________________________
(2)仪器a的名称是________________ ;测定氨前应该对装置进行气密性检验,若气密性不好则测定结果将________ (填“偏高”或“偏低”).该滴定过程中选择________ 做指示剂。
(3)样品中氨的质量分数表达式为_____________________________ 。
(4)测定氯的过程中,AgNO3标准溶液置于_________ (填“无色”或“棕色”)滴定管中;滴定终点时,溶液中已检测不到Cl-[c(Cl-)≤1.0×10-5 mol·L-1],则出现砖红色沉淀时,溶液中c(CrO42-)的最小值为_____________ mol·L-1。[已.知:Ksp(AgCl)=1.0×10-10,Ksp( Ag2CrO4)=1.12×10-12]
(5)经测定分析,样品X中钴、氨和氯的物质的量之比为1:6:3,则制备X的化学方程式为________________________________________ 。
(6)某同学向CoCl2溶液中加入足量(NH4)2C2O4得到CoC2O4沉淀,在空气中煅烧CoC2O4生成钻氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则所得钴氧化物的化学式为________________ 。
①氨的测定:精确称取wgX,加适量水溶解,注入下图所示的蒸馏烧瓶中(夹持和加热仪器略去),然后逐滴加入足量10%NaOH溶液,加热烧瓶将氨蒸出,用V1mLc1mol·L-1的盐酸吸收蒸出的氨,然后取下锥形瓶,用c2 mol·L-1 NaOH标准溶液滴定过剩的HCl。.终点时消耗V2 mLNaOH溶液。

②氯的测定:准确称取样品X配成溶液,用K2CrO4溶液为指示剂,用AgNO3标准溶液滴定,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)
回答下列问题:
(1)X的制备过程中,温度不能过高,其原因是
(2)仪器a的名称是
(3)样品中氨的质量分数表达式为
(4)测定氯的过程中,AgNO3标准溶液置于
(5)经测定分析,样品X中钴、氨和氯的物质的量之比为1:6:3,则制备X的化学方程式为
(6)某同学向CoCl2溶液中加入足量(NH4)2C2O4得到CoC2O4沉淀,在空气中煅烧CoC2O4生成钻氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则所得钴氧化物的化学式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】某处工厂排出的烟道气中含氮氧化物(主要为NO、NO2)、粉尘和少量水蒸气。课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
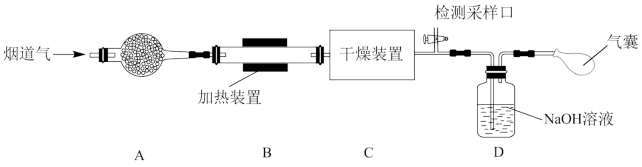
已知:①活泼金属易形成氧化膜②形成原电池能加快反应速率③HClO的氧化性比NaClO强;
(1)氮氧化物可用碱溶液吸收。装置D中NO和NO2混合气体按一定比例被NaOH溶液完全吸收生成NaNO2和H2O,写出该反应的化学方程式_______ ;若反应后尾气无残留,则参加反应的NO2、NO物质的量比值为_______ (填字母)。
a.≥1 b.≤1 c.任意值
(2)可使用适量酸性H2O2溶液,将溶液中的NO 全部氧化为NO
全部氧化为NO ,发生反应的离子方程式是
,发生反应的离子方程式是_______ 。
(3)溶液中NO 直接排放在水体中也会造成污染,现用活泼金属将溶液中NO
直接排放在水体中也会造成污染,现用活泼金属将溶液中NO 转化为N2,实现氮元素的脱除,具体步骤如下:
转化为N2,实现氮元素的脱除,具体步骤如下:
步骤一、取适量(2)中H2O2处理后的溶液,调节pH至中性,蒸发浓缩,得到c(NO )为0.100mol·L-1的溶液甲。
)为0.100mol·L-1的溶液甲。
步骤二、现量取50mL溶液甲,分别用金属铝、金属铁和铝铁合金在45℃、惰性气体氛围中对溶液乙进行氮脱除。
步骤三、重复实验2~3次,溶液中NO 的残留情况与反应时间的关系如图所示。
的残留情况与反应时间的关系如图所示。
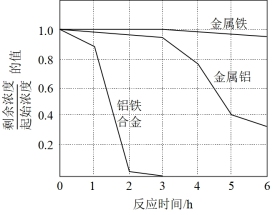
①金属铝和金属铁在0~3h内,NO 的脱除效率均很低,几乎没被脱除,其可能的原因是
的脱除效率均很低,几乎没被脱除,其可能的原因是_______ 。
②0~3h内铝铁合金的氮脱除效率比金属铝、金属铁大得多,其可能的原因_______ 。
(4)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性NaClO溶液来处理。HClO氧化NO生成NO 和Cl-,发生反应的离子方程式是
和Cl-,发生反应的离子方程式是_______ 。
(5)NaClO溶液能有效去除NO。25℃时,NO的去除率随pH的变化如图1所示(用盐酸调节pH);pH=4时,NO的去除率随温度的变化如图2所示。
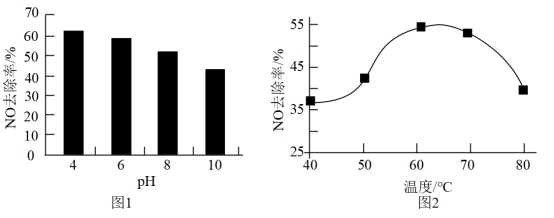
①25℃时,随着pH降低,NO脱除率增大的原因是_______ 。
②pH=4时,60~80℃间NO脱除率下降的原因是_______ 。

已知:①活泼金属易形成氧化膜②形成原电池能加快反应速率③HClO的氧化性比NaClO强;
(1)氮氧化物可用碱溶液吸收。装置D中NO和NO2混合气体按一定比例被NaOH溶液完全吸收生成NaNO2和H2O,写出该反应的化学方程式
a.≥1 b.≤1 c.任意值
(2)可使用适量酸性H2O2溶液,将溶液中的NO
 全部氧化为NO
全部氧化为NO ,发生反应的离子方程式是
,发生反应的离子方程式是(3)溶液中NO
 直接排放在水体中也会造成污染,现用活泼金属将溶液中NO
直接排放在水体中也会造成污染,现用活泼金属将溶液中NO 转化为N2,实现氮元素的脱除,具体步骤如下:
转化为N2,实现氮元素的脱除,具体步骤如下:步骤一、取适量(2)中H2O2处理后的溶液,调节pH至中性,蒸发浓缩,得到c(NO
 )为0.100mol·L-1的溶液甲。
)为0.100mol·L-1的溶液甲。步骤二、现量取50mL溶液甲,分别用金属铝、金属铁和铝铁合金在45℃、惰性气体氛围中对溶液乙进行氮脱除。
步骤三、重复实验2~3次,溶液中NO
 的残留情况与反应时间的关系如图所示。
的残留情况与反应时间的关系如图所示。
①金属铝和金属铁在0~3h内,NO
 的脱除效率均很低,几乎没被脱除,其可能的原因是
的脱除效率均很低,几乎没被脱除,其可能的原因是②0~3h内铝铁合金的氮脱除效率比金属铝、金属铁大得多,其可能的原因
(4)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性NaClO溶液来处理。HClO氧化NO生成NO
 和Cl-,发生反应的离子方程式是
和Cl-,发生反应的离子方程式是(5)NaClO溶液能有效去除NO。25℃时,NO的去除率随pH的变化如图1所示(用盐酸调节pH);pH=4时,NO的去除率随温度的变化如图2所示。

①25℃时,随着pH降低,NO脱除率增大的原因是
②pH=4时,60~80℃间NO脱除率下降的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】三氯氧磷( )可用作半导体掺杂剂及光导纤维原料,是能推进中国半导体产业链发展壮大的一种重要的化工原料。工业上可以直接氧化
)可用作半导体掺杂剂及光导纤维原料,是能推进中国半导体产业链发展壮大的一种重要的化工原料。工业上可以直接氧化 制备
制备 ,反应原理为:
,反应原理为: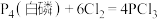 ,
,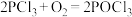 。
。
已知: 、
、 的部分性质如下:
的部分性质如下:
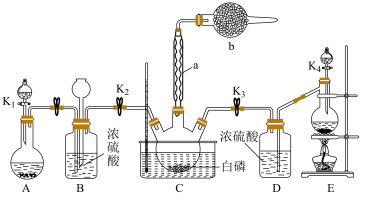
某化学兴趣小组模拟该工艺设计实验装置如图(某些夹持装置和加热装置已略去):__________ ,b中盛放的药品是__________ 。
(2)装置E反应的离子方程式为______________________________ 。
(3)C反应温度控制在60~65℃,温度不能过高的原因是______________________________ 。分离提纯获得 的实验操作名称为
的实验操作名称为__________ 。
(4) 与NaOH溶液反应的化学方程式为
与NaOH溶液反应的化学方程式为______________________________ 。
(5)通过测定三氯氧磷产品中氯元素含量,可进一步计算产品的纯度,实验步骤如下:
①取ag只含 杂质的产品置于盛50.00mL蒸馏水的水解瓶中,摇动至完全水解,将水解液配成100.00mL溶液,预处理排除含磷粒子的影响。
杂质的产品置于盛50.00mL蒸馏水的水解瓶中,摇动至完全水解,将水解液配成100.00mL溶液,预处理排除含磷粒子的影响。
②取10.00mL溶液于锥形瓶中,向其中加入 的
的 溶液
溶液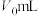 ,使
,使 完全沉淀,再加入20mL硝基苯,振荡,使沉淀表面被有机物覆盖;然后选择
完全沉淀,再加入20mL硝基苯,振荡,使沉淀表面被有机物覆盖;然后选择 指示剂,用
指示剂,用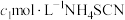 溶液滴定过量
溶液滴定过量 至终点,记下所用体积为
至终点,记下所用体积为 。
。
[已知: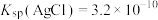 ,
,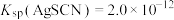 ]
]
实验过程中加入硝基苯的目的是__________ ,若无此操作,则所测 的含量将
的含量将__________ (填“偏高”、“偏低”或“不变”)。根据以上数据产品中 的质量分数为
的质量分数为__________ (用含a、 、
、 、
、 、
、 的代数式表示)。
的代数式表示)。
 )可用作半导体掺杂剂及光导纤维原料,是能推进中国半导体产业链发展壮大的一种重要的化工原料。工业上可以直接氧化
)可用作半导体掺杂剂及光导纤维原料,是能推进中国半导体产业链发展壮大的一种重要的化工原料。工业上可以直接氧化 制备
制备 ,反应原理为:
,反应原理为: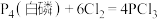 ,
,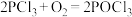 。
。已知:
 、
、 的部分性质如下:
的部分性质如下:熔点/℃ | 沸点/℃ | 相对分子质量 | 其它 | |
| -112 | 75.5 | 137.5 | 易水解得到两种酸 |
| 2 | 105.3 | 153.5 | 易水解得到两种酸 |
(2)装置E反应的离子方程式为
(3)C反应温度控制在60~65℃,温度不能过高的原因是
 的实验操作名称为
的实验操作名称为(4)
 与NaOH溶液反应的化学方程式为
与NaOH溶液反应的化学方程式为(5)通过测定三氯氧磷产品中氯元素含量,可进一步计算产品的纯度,实验步骤如下:
①取ag只含
 杂质的产品置于盛50.00mL蒸馏水的水解瓶中,摇动至完全水解,将水解液配成100.00mL溶液,预处理排除含磷粒子的影响。
杂质的产品置于盛50.00mL蒸馏水的水解瓶中,摇动至完全水解,将水解液配成100.00mL溶液,预处理排除含磷粒子的影响。②取10.00mL溶液于锥形瓶中,向其中加入
 的
的 溶液
溶液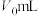 ,使
,使 完全沉淀,再加入20mL硝基苯,振荡,使沉淀表面被有机物覆盖;然后选择
完全沉淀,再加入20mL硝基苯,振荡,使沉淀表面被有机物覆盖;然后选择 指示剂,用
指示剂,用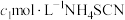 溶液滴定过量
溶液滴定过量 至终点,记下所用体积为
至终点,记下所用体积为 。
。[已知:
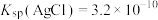 ,
,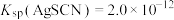 ]
]实验过程中加入硝基苯的目的是
 的含量将
的含量将 的质量分数为
的质量分数为 、
、 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】烟道气中的NOx是主要的大气污染物之一,为了监测其含量,选用如下采样和检测方法。回答下列问题:
I.采样
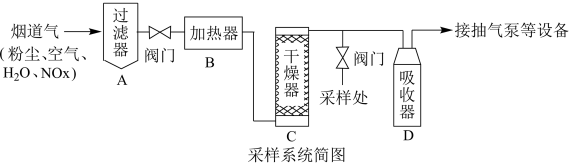
采样步骤:
①检验系统气密性;②加热器将烟道气加热至140。C;③打开抽气泵置换系统内空气;④采集无尘、干燥的气样;⑤关闭系统,停止采样。
II. NOx含量的测定
将VL气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3-,加水稀释至100.00 mL。量取20.00 mL该溶液,加入V1 mL c1 mol·L-1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L-1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗V2 mL。
(1)NO被H2O2氧化为NO3-的离子方程式是___________ 。
(2)滴定操作使用的玻璃仪器主要有___________ 。
(3)滴定过程中发生下列反应:
3Fe2+ +NO3-+4H+ = NO↑+3Fe3+ +2H2O
Cr2O72-+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O
则气样中NOx折合成NO2的含量为_________ mg·m-3。
(4)判断下列情况对NOx含量测定结果的影响(填“偏高” 、“偏低”或“无影响 ”)若缺少采样步骤③,会使测试结果___________ 。若FeSO4标准溶液部分变质,会使测定结果___________ 。
I.采样

采样步骤:
①检验系统气密性;②加热器将烟道气加热至140。C;③打开抽气泵置换系统内空气;④采集无尘、干燥的气样;⑤关闭系统,停止采样。
II. NOx含量的测定
将VL气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3-,加水稀释至100.00 mL。量取20.00 mL该溶液,加入V1 mL c1 mol·L-1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L-1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗V2 mL。
(1)NO被H2O2氧化为NO3-的离子方程式是
(2)滴定操作使用的玻璃仪器主要有
(3)滴定过程中发生下列反应:
3Fe2+ +NO3-+4H+ = NO↑+3Fe3+ +2H2O
Cr2O72-+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O
则气样中NOx折合成NO2的含量为
(4)判断下列情况对NOx含量测定结果的影响(填“偏高” 、“偏低”或“无影响 ”)若缺少采样步骤③,会使测试结果
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】摩尔盐[xFeSO4·y(NH4)2SO4·zH2O]是一种重要化工原料。其组成可通过下列实验测定:
①称取1.5680 g样品,准确配成100 mL溶液A。
②量取25.00mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固体0.4660g。
③再量取25.00 mL溶液A,滴加适量稀硫酸,用0.0200 mol·L-1KMnO4溶液滴定至终点,生成Mn2+,消耗KMnO4溶液10.00 mL。
(1)③中发生反应的离子方程式为___________ ,滴定终点的现象是___________ 。
(2)通过计算确定样品的组成(必须写出计算过程)。______
①称取1.5680 g样品,准确配成100 mL溶液A。
②量取25.00mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固体0.4660g。
③再量取25.00 mL溶液A,滴加适量稀硫酸,用0.0200 mol·L-1KMnO4溶液滴定至终点,生成Mn2+,消耗KMnO4溶液10.00 mL。
(1)③中发生反应的离子方程式为
(2)通过计算确定样品的组成(必须写出计算过程)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表列出了九种元素在元素周期表中的位置。
请回答下列问题。
(1)元素①用于制造氢弹的两种核素的中子数分别为1和2,两者互称为___________ ;当今考古工作者利用元素③的一种质量数为14的核素即___________ (填写符号)测定一些文物的年代,该核素的中子数为___________ 。
(2)在③和⑥两种元素中,原子半径较大的是___________ (填元素符号);元素④的原子结构示意图为___________ 。
(3)②和⑧两种元素最高价氧化物对应的水化物中,碱性较强的是___________ (填化学式)。⑤、⑦、⑨三种元素的简单气态氢化物中,稳定性最弱的是___________ (填化学式)。
(4)元素X是比元素⑧质子数小8的同主族元素,其过氧化物中阴阳离子个数比为___________ ;若将该过氧化物7.8 g加入足量水充分反应,则该反应中转移电子数目为___________ 。(设阿伏加德罗常数的数值为NA)
(5)写出证明元素⑦比元素⑨非金属性强的反应的离子方程式:_______ 。
周期 | IA | 0 | ||||||
一 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
二 | ② | ③ | ④ | ⑤ | ||||
三 | ⑥ | ⑦ | ||||||
四 | ⑧ | ⑨ |
(1)元素①用于制造氢弹的两种核素的中子数分别为1和2,两者互称为
(2)在③和⑥两种元素中,原子半径较大的是
(3)②和⑧两种元素最高价氧化物对应的水化物中,碱性较强的是
(4)元素X是比元素⑧质子数小8的同主族元素,其过氧化物中阴阳离子个数比为
(5)写出证明元素⑦比元素⑨非金属性强的反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,填写下列空白。
(1)写出元素符号,②_______ ⑨_______ 。
(2)写出⑤单质跟乙醇反应的化学方程式_______ 。
(3)①③④⑦可组成一化合物,其原子个数之比为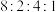 。写出该化合物的化学式
。写出该化合物的化学式_______ 。
(4)画出⑦的原子结构示意图_______ 。
(5)⑦⑧⑩的简单离子半径由大到小的顺序是_______ (用离子符号表示)
(6)④⑦的最简单氢化物的稳定性顺序是_______ (用化学式表示),这两种氢化物中沸点较高的是_______ (用化学式表示),原因是_______ 。
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 四 | ⑩ |
(2)写出⑤单质跟乙醇反应的化学方程式
(3)①③④⑦可组成一化合物,其原子个数之比为
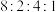 。写出该化合物的化学式
。写出该化合物的化学式(4)画出⑦的原子结构示意图
(5)⑦⑧⑩的简单离子半径由大到小的顺序是
(6)④⑦的最简单氢化物的稳定性顺序是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E、F、G是原子序数依次增大的前四周期元素,A元素原子核外电子只有一种自旋取向,A、B元素原子的最外层电子数相等;C元素原子核外s能级上的电子总数与p能级上的电子总数相等;D元素原子半径是短周期主族元素中最大的;E元素的价层电子在s和p能级的原子轨道中运动的电子数相等; 与F元素的基态原子均有5个未成对电子。请回答下列问题:
与F元素的基态原子均有5个未成对电子。请回答下列问题:
(1)若A离子与B离子的电子层结构相同,半径较大的是___________ (填离子符号),A与B形成的二元化合物的晶体类型为___________ 。
(2)比较第一电离能的大小:I1(B)___________ (填“>”、“<”或“=”)I1(D),原因是___________ 。
(3)晶体熔点:
___________ (填“高于”、“低于”或“等于”)DCA。
(4)基态G原子的价层电子排布式为___________ ,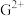 与
与 的未成对电子数之比为
的未成对电子数之比为___________ 。
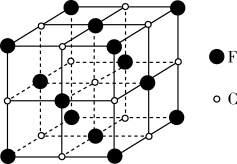
(5)基态F原子含有___________ 种空间运动状态不同的电子。C和F形成的一种化合物的立方晶胞如图所示,则该化合物的化学式为___________ 。
 与F元素的基态原子均有5个未成对电子。请回答下列问题:
与F元素的基态原子均有5个未成对电子。请回答下列问题:(1)若A离子与B离子的电子层结构相同,半径较大的是
(2)比较第一电离能的大小:I1(B)
(3)晶体熔点:

(4)基态G原子的价层电子排布式为
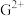 与
与 的未成对电子数之比为
的未成对电子数之比为(5)基态F原子含有

您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐1】丹参酸具有潜在的抗肿瘤和抗血栓生成的效果,可用于药理实验、活性筛选等,合成丹参酸的路线如图所示:

已知: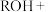
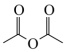

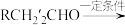
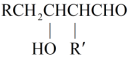
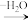
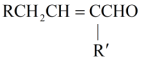
回答下列问题:
(1)A中官能团的名称是___________ ,化合物B中采取 和
和 杂化的碳原子个数比为
杂化的碳原子个数比为___________ 。
(2)碳原子上连有4个不同的原子或基团时,该碳原子称为手性碳原子,上述有机物中含有手性碳原子的有机物为___________ (填“A”“B”“C”“D”或“E”)。
(3)A→B的反应类型是___________ 。
(4)B→C的化学方程式为___________ 。
(5)X与D互为同分异构体,请写出满足下列条件的X的结构简式:___________ 。
①1mol X能与5mol NaOH发生反应;
②有5个碳原子在同一条直线上;
③与 溶液可以发生显色反应。
溶液可以发生显色反应。
(6)设计以 、
、 为原料制取
为原料制取 的合成路线
的合成路线___________ (其他无机试剂任选)。

已知:
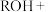


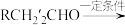
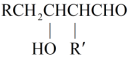
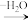
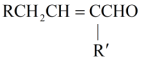
回答下列问题:
(1)A中官能团的名称是
 和
和 杂化的碳原子个数比为
杂化的碳原子个数比为(2)碳原子上连有4个不同的原子或基团时,该碳原子称为手性碳原子,上述有机物中含有手性碳原子的有机物为
(3)A→B的反应类型是
(4)B→C的化学方程式为
(5)X与D互为同分异构体,请写出满足下列条件的X的结构简式:
①1mol X能与5mol NaOH发生反应;
②有5个碳原子在同一条直线上;
③与
 溶液可以发生显色反应。
溶液可以发生显色反应。(6)设计以
 、
、 为原料制取
为原料制取 的合成路线
的合成路线
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】中国疾控中心成功研发出两种含氯低温消毒剂,解决了低温消毒难题。“-40℃低温消毒剂”的主要成分之一是二氯异氰尿酸钠,其合成方法如图所示。
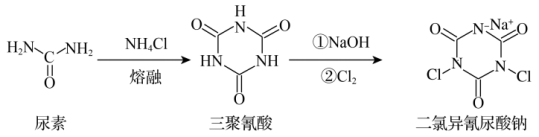
回答下列问题:
(1)碳元素位于元素周期表的_______ 区,基态原子与基态碳原子具有相同未成对电子数的同周期元素是_______ (填元素符号)。
(2)尿素中C、N原子的杂化方式分别为_______ ,尿素可与多种金属形成配合物,其配位原子可以是_______ 。尿素易溶于水,除尿素和水都是极性分子外,其原因还有_______ 。
(3)三聚氰酸分子中σ键与π键的数目之比为_______ 。
(4)下列说法正确的是_______。
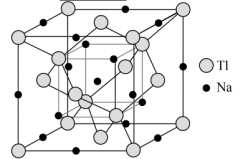
(5)铊化钠的晶胞结构如图所示,若晶胞参数为a pm,该物质的摩尔质量为M g/mol,阿伏加德罗常数的值为NA,则晶胞密度为_______ g/cm3;Tl原子间的最近距离为_______ pm。

回答下列问题:
(1)碳元素位于元素周期表的
(2)尿素中C、N原子的杂化方式分别为
(3)三聚氰酸分子中σ键与π键的数目之比为
(4)下列说法正确的是_______。
| A.氯化铵中阳离子的空间构型是正四面体形 |
| B.二氯异氰尿酸钠所含元素中电负性最大的是氯 |
| C.二氯异氰尿酸钠晶体中存在离子键、共价键和配位键 |
| D.三聚氰酸具有与苯环类似的结构,可推知三聚氰酸分子中存在大π键 |

您最近一年使用:0次
【推荐3】氮元素可形成许多结构和性质特殊的化合物。回答下列问题:
(1)基态N原子的核外电子运动状态有________ 种;由氮元素形成的三种微粒:①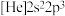 ②
②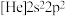 ③
③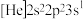 。下列叙述正确的是
。下列叙述正确的是________ (填标号)。
A.微粒半径: B.失去一个电子所需最低能量:
B.失去一个电子所需最低能量: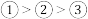
C.电子排布属于激发态的是:③ D.得电子能力: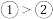
(2) 的空间结构为
的空间结构为________ ,中心原子的杂化方式为________ , 分子的键角
分子的键角________  (填“>”“<”或“=”);
(填“>”“<”或“=”); 水解生成具有强烈杀菌作用的物质,已知电负性
水解生成具有强烈杀菌作用的物质,已知电负性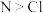 ,其水解的化学方程式为
,其水解的化学方程式为________ 。
(3) 的熔点
的熔点________ (填“高于”或“低于”)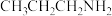 ,主要原因是
,主要原因是________________ ;已知烷基的推电子效应强于H,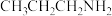 与
与 结合
结合 能力更强的是
能力更强的是________ 。
(1)基态N原子的核外电子运动状态有
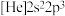 ②
②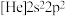 ③
③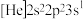 。下列叙述正确的是
。下列叙述正确的是A.微粒半径:
 B.失去一个电子所需最低能量:
B.失去一个电子所需最低能量: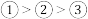
C.电子排布属于激发态的是:③ D.得电子能力:
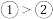
(2)
 的空间结构为
的空间结构为 分子的键角
分子的键角 (填“>”“<”或“=”);
(填“>”“<”或“=”); 水解生成具有强烈杀菌作用的物质,已知电负性
水解生成具有强烈杀菌作用的物质,已知电负性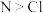 ,其水解的化学方程式为
,其水解的化学方程式为(3)
 的熔点
的熔点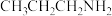 ,主要原因是
,主要原因是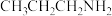 与
与 结合
结合 能力更强的是
能力更强的是
您最近一年使用:0次



