金属钼在工业和国防建设中有重要的作用,其化合物钼酸钠晶体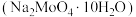 可制造金属缓释剂。由钼精矿(主要成分为
可制造金属缓释剂。由钼精矿(主要成分为 ,含有少量不反应的杂质)制备钼及钼酸钠晶体的工艺流程如图所示,回答下列问题:
,含有少量不反应的杂质)制备钼及钼酸钠晶体的工艺流程如图所示,回答下列问题:____________ 。
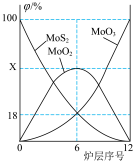
(2)焙烧过程中采用“多层逆流(空气从炉底进入,钼精矿经粉碎后从炉顶进入)焙烧”,下图为焙烧时各炉层固体物料的物质的量百分数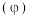 。
。____________ ;“多层逆流焙烧”的优点是_______________ ;
②某些生产工艺在焙烧时加入碳酸钙会更环保,其原因是________ (用化学方程式表示);
(3)碱浸时发生反应的离子方程式为_____________________ ;
(4)已知钼酸钠的溶解度曲线如图所示,要获得钼酸钠晶体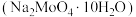 的操作2为
的操作2为________ 、_________ 、过滤、洗涤、干燥; 生成,用固体
生成,用固体 除去.在除
除去.在除 前测定碱浸液中
前测定碱浸液中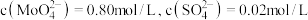 ,当
,当 开始沉淀时,
开始沉淀时, 的去除率为
的去除率为_____ %(保留整数)[已知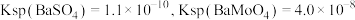 ,溶液体积变化忽略不计]。
,溶液体积变化忽略不计]。
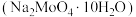 可制造金属缓释剂。由钼精矿(主要成分为
可制造金属缓释剂。由钼精矿(主要成分为 ,含有少量不反应的杂质)制备钼及钼酸钠晶体的工艺流程如图所示,回答下列问题:
,含有少量不反应的杂质)制备钼及钼酸钠晶体的工艺流程如图所示,回答下列问题: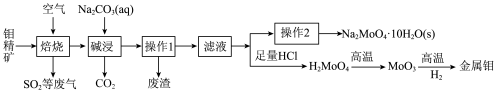
(2)焙烧过程中采用“多层逆流(空气从炉底进入,钼精矿经粉碎后从炉顶进入)焙烧”,下图为焙烧时各炉层固体物料的物质的量百分数
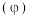 。
。
②某些生产工艺在焙烧时加入碳酸钙会更环保,其原因是
(3)碱浸时发生反应的离子方程式为
(4)已知钼酸钠的溶解度曲线如图所示,要获得钼酸钠晶体
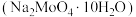 的操作2为
的操作2为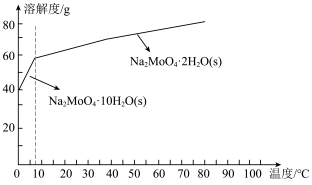
 生成,用固体
生成,用固体 除去.在除
除去.在除 前测定碱浸液中
前测定碱浸液中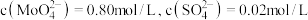 ,当
,当 开始沉淀时,
开始沉淀时, 的去除率为
的去除率为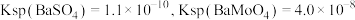 ,溶液体积变化忽略不计]。
,溶液体积变化忽略不计]。
更新时间:2024-05-24 16:24:27
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】钾离子电池以其优异的性能成为替代理离子电池的一种选择,该电池的负极是由钾嵌入石墨中构成,正极主要含 、铝箔、醚类有机物等。从某废旧钾离子电池中回收部分材料的流程如下:
、铝箔、醚类有机物等。从某废旧钾离子电池中回收部分材料的流程如下:

已知:I.放电时负极的电极反应式为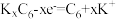 ;
;
II.常温下, ,当溶液中某离子浓度低于
,当溶液中某离子浓度低于 时,认为该离子已沉淀完全。
时,认为该离子已沉淀完全。
回答下列问题:
(1)废旧电池放电处理的原因为___________ 。
(2)“碱浸”时发生的化学反应方程式为___________ 。
(3)已知 中的铁为+3价,则“酸溶”时主要反应的离子方程式为
中的铁为+3价,则“酸溶”时主要反应的离子方程式为___________ ;该工序中温度需控制在40℃的原因为___________ 。
(4)若最终调节pH=3,则所得母液中的
___________ (填“已”或“未”)沉淀完全。
(5)实验室中从“反萃取”所得混合液中分离出 溶液的操作名称为
溶液的操作名称为___________ 。
(6)废旧钾离子电池放电处理并拆解后,从负极得到石墨,其结构如图。石墨两层之间最近碳原子间距远大于层内最近碳原子间距的原因为___________ ;设阿伏加德罗常数的值为 ,则石墨晶体密度为
,则石墨晶体密度为___________  (列式即可)。
(列式即可)。

 、铝箔、醚类有机物等。从某废旧钾离子电池中回收部分材料的流程如下:
、铝箔、醚类有机物等。从某废旧钾离子电池中回收部分材料的流程如下:
已知:I.放电时负极的电极反应式为
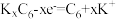 ;
;II.常温下,
 ,当溶液中某离子浓度低于
,当溶液中某离子浓度低于 时,认为该离子已沉淀完全。
时,认为该离子已沉淀完全。回答下列问题:
(1)废旧电池放电处理的原因为
(2)“碱浸”时发生的化学反应方程式为
(3)已知
 中的铁为+3价,则“酸溶”时主要反应的离子方程式为
中的铁为+3价,则“酸溶”时主要反应的离子方程式为(4)若最终调节pH=3,则所得母液中的

(5)实验室中从“反萃取”所得混合液中分离出
 溶液的操作名称为
溶液的操作名称为(6)废旧钾离子电池放电处理并拆解后,从负极得到石墨,其结构如图。石墨两层之间最近碳原子间距远大于层内最近碳原子间距的原因为
 ,则石墨晶体密度为
,则石墨晶体密度为 (列式即可)。
(列式即可)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】钛酸钡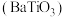 是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。用高钛渣(主要成分为
是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。用高钛渣(主要成分为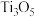 ,含
,含 、
、 等杂质)为原料制备
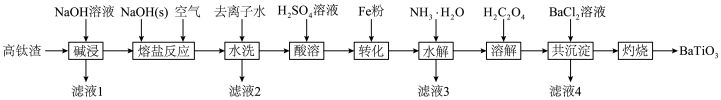
等杂质)为原料制备 的工业流程如下:
的工业流程如下:
已知:① 在溶液中呈绿色;
在溶液中呈绿色; 是强电解质;
是强电解质;
②部分金属离子开始沉淀的 如下表:
如下表:
回答下列问题:
(1)“碱浸”操作过程中除去的杂质为_______ 。
(2)“水洗”过程中 与水发生离子交换反应:
与水发生离子交换反应: ,滤液2呈绿色,经除杂处理后可在
,滤液2呈绿色,经除杂处理后可在_______ (操作单元名称)循环利用,“熔盐反应”过程中 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
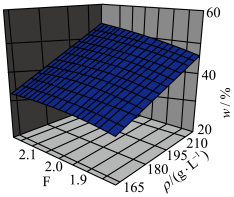
(3)“酸溶”过程中 (
( 溶液质量浓度)及F(
溶液质量浓度)及F( 溶液酸度)与w(
溶液酸度)与w( 质量分数)之间的关系如图所示。当
质量分数)之间的关系如图所示。当 值恒定时,随
值恒定时,随 溶液质量浓度增大,所需硫酸的质量分数
溶液质量浓度增大,所需硫酸的质量分数_______ (填“增大”“减小”或“不变”)。
(4)“水解”操作加入 目的是调节溶液
目的是调节溶液 ,可适当提高水解速率。已知:
,可适当提高水解速率。已知: ,水解反应
,水解反应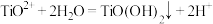 的平衡常数
的平衡常数
_______ ;“转化”过程加入铁粉的目的是_______ ,滤液3中含有的金属阳离子有_______ 。
(5)“共沉淀”过程发生反应: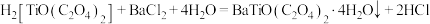 ,“灼烧”时隔绝空气,发生反应的化学方程式为
,“灼烧”时隔绝空气,发生反应的化学方程式为_______ 。
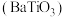 是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。用高钛渣(主要成分为
是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。用高钛渣(主要成分为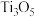 ,含
,含 、
、 等杂质)为原料制备
等杂质)为原料制备 的工业流程如下:
的工业流程如下:
已知:①
 在溶液中呈绿色;
在溶液中呈绿色; 是强电解质;
是强电解质;②部分金属离子开始沉淀的
 如下表:
如下表:| 金属离子 |  |  |  |
开始沉淀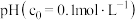 | 1.9 | 7.0 | 9.1 |
(1)“碱浸”操作过程中除去的杂质为
(2)“水洗”过程中
 与水发生离子交换反应:
与水发生离子交换反应: ,滤液2呈绿色,经除杂处理后可在
,滤液2呈绿色,经除杂处理后可在 发生反应的离子方程式为
发生反应的离子方程式为(3)“酸溶”过程中
 (
( 溶液质量浓度)及F(
溶液质量浓度)及F( 溶液酸度)与w(
溶液酸度)与w( 质量分数)之间的关系如图所示。当
质量分数)之间的关系如图所示。当 值恒定时,随
值恒定时,随 溶液质量浓度增大,所需硫酸的质量分数
溶液质量浓度增大,所需硫酸的质量分数
(4)“水解”操作加入
 目的是调节溶液
目的是调节溶液 ,可适当提高水解速率。已知:
,可适当提高水解速率。已知: ,水解反应
,水解反应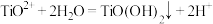 的平衡常数
的平衡常数
(5)“共沉淀”过程发生反应:
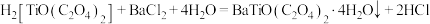 ,“灼烧”时隔绝空气,发生反应的化学方程式为
,“灼烧”时隔绝空气,发生反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】碲(Te)为第VIA元素,其单质凭借优良的性能成为制作合金添加剂、半导体、光电元件的主体材料,并被广泛应用于冶金、航空航天、电子等领域。可从精炼铜的阳极泥(主要成分为Cu2Te)中回收碲,
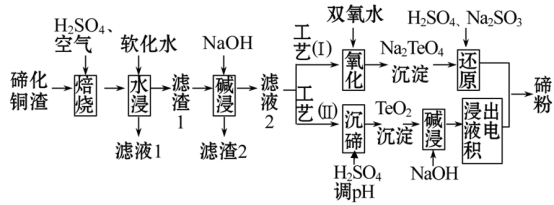
(1)“培烧”后,确主要以TeO2 形式存在,写出相应反应的离子方程式:______ 。
(2)为了选择最佳的培烧工艺进行了温度和硫酸加入量的条件试验,结果如下表所示:
则实验中应选择的条件为___________ ,原因为________________ 。
(3)滤渣1在碱浸时发生的化学方程式为___________ 。
(4)工艺(I)中,“还原”时发生的总的化学方程式为_____ 。
(5)由于工艺(I)中“氧化”对溶液和物料条件要求高。有研究者采用工艺(II)获得磅.则“电积”过程中,阴极的电极反应式为___________ 。
(6)工业生产中,滤渣2经硫酸酸浸后得滤液3和滤渣3。
①滤液3 与滤液1合井。进入铜电积系统。该处理措施的优点为______ 。
②滤渣3中若含Au和Ag,可用_____ 将二者分离。(填字母)
A.王水 B.稀硝酸 C.浓氢氧化钠溶液 D.浓盐酸

(1)“培烧”后,确主要以TeO2 形式存在,写出相应反应的离子方程式:
(2)为了选择最佳的培烧工艺进行了温度和硫酸加入量的条件试验,结果如下表所示:
温度/℃ | 硫酸加入量(理论量倍数) | 浸出率/% | |
Cu | Te | ||
450 | 1.25 | 77.3 | 2.63 |
460 | 1.00 | 80.29 | 2.81 |
1.25 | 89.86 | 2.87 | |
1.50 | 92.31 | 7.70 | |
500 | 1.25 | 59.83 | 5.48 |
550 | 1.25 | 11.65 | 10.63 |
则实验中应选择的条件为
(3)滤渣1在碱浸时发生的化学方程式为
(4)工艺(I)中,“还原”时发生的总的化学方程式为
(5)由于工艺(I)中“氧化”对溶液和物料条件要求高。有研究者采用工艺(II)获得磅.则“电积”过程中,阴极的电极反应式为
(6)工业生产中,滤渣2经硫酸酸浸后得滤液3和滤渣3。
①滤液3 与滤液1合井。进入铜电积系统。该处理措施的优点为
②滤渣3中若含Au和Ag,可用
A.王水 B.稀硝酸 C.浓氢氧化钠溶液 D.浓盐酸
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其制取如下:
已知:①2KOH +Cl2→KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2→5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+2KClO3+10KOH→2K2FeO4+6KNO3+3KCl+5H2O
回答下列问题:
(1)高铁酸钾(K2FeO4)应在_______ (填“温度较高”或“温度较低”)情况下进行;
(2)0.1 mol/LKClO溶液中c (ClO-) +c (HClO)_______ 0.1 mol/L (填>、<、=)
(3)K2FeO4具有强氧化性的原因____________________________ ;
(4)配制KOH溶液时,是在每100mL水中溶解56 gKOH固体(该溶液的密度为1.56g/mL),它的物质的量浓度为_________________ ;
(5)在“反应液Ⅰ”中加KOH固体的目的是_______________ ;
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为KClO
(6)从“反应液Ⅱ”中分离出K2FeO4后,会有副产品__________ (写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途_____________________ 。
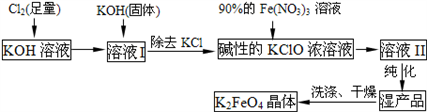
已知:①2KOH +Cl2→KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2→5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+2KClO3+10KOH→2K2FeO4+6KNO3+3KCl+5H2O
回答下列问题:
(1)高铁酸钾(K2FeO4)应在
(2)0.1 mol/LKClO溶液中c (ClO-) +c (HClO)
(3)K2FeO4具有强氧化性的原因
(4)配制KOH溶液时,是在每100mL水中溶解56 gKOH固体(该溶液的密度为1.56g/mL),它的物质的量浓度为
(5)在“反应液Ⅰ”中加KOH固体的目的是
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为KClO
(6)从“反应液Ⅱ”中分离出K2FeO4后,会有副产品
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】燃煤烟气的脱硫脱硝是目前研究的热点。回答下列问题:
(1)用 CH4 催化还原氮氧化物可以消除氮氧化物污染,涉及反应如下:
I.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ∆H=-574kJ/mol
II.CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ∆H=-1160kJ/mol
III.H2O(g)=H2O(l) ∆H=-44kJ/mol
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) ∆H=_________ kJ/mol
(2)某科研小组研究臭氧氧化-碱吸收法同时脱除 SO2 和 NO工艺,氧化过程反应原理及反应热、活化能数据如表:
其他条件不变,每次向容积为2L的反应器中充入含1.0molNO、1.0molSO2 的混合气和 2.0molO3,改变温度,反应相同时间t 后,体系中NO 和 SO2 的转化率如图所示。
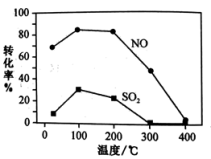
①由图可知相同温度下 NO 的转化率远高于 SO2,结合题中数据分析其可能原因:_______
②温度高于200℃后,NO和SO2的转化率随温度升高显著下降的可能原因是_______
③若其他条件不变,缩小反应器的容积,NO 和 SO2的平衡转化率_______ (填“增大”“减小”或“不变”)
(3)在一定条件下,焦炭催化还原SO2的化学方程式为:2C(s)+2SO2(g)⇌S2(g)+2CO2(g)
①该反应的逆反应速率表达式:v逆=k逆·c(S2)·c2(CO2),k逆为速率常数(仅与温度有关)。表为某温度下,测得的实验数据:
由表中数据可知,该温度下,上述反应的逆反应速率常数 k逆=_______ L2·mol-2·min-1
②一定压强下,向1L 密闭容器中加入足量的焦炭和 1molSO2 发生上述反应,反应 10min 时,测得SO2的生成速率与S2(g)的生成速率随温度变化的关系如图所示:
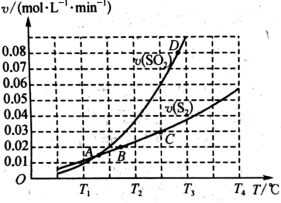
根据图象,判断反应2C(s)+2SO2(g)⇌S2(g)+2CO2(g)的∆H_______ (填“>”“<”“=”)0 A、B、C、D 四点对应的状态中,达到平衡状态的有_______ (填字母),该点对应的温度下的化学平衡常数K=_______
(1)用 CH4 催化还原氮氧化物可以消除氮氧化物污染,涉及反应如下:
I.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ∆H=-574kJ/mol
II.CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ∆H=-1160kJ/mol
III.H2O(g)=H2O(l) ∆H=-44kJ/mol
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) ∆H=
(2)某科研小组研究臭氧氧化-碱吸收法同时脱除 SO2 和 NO工艺,氧化过程反应原理及反应热、活化能数据如表:
| 反应 | 反应热(∆H1)/kJ mol-1 mol-1 | 活化能(Ea1)//kJ mol-1 mol-1 |
| NO(g)+O3(g)⇌NO2(g)+O2(g) | -200.9 | 3.2 |
SO2(g)+O3(g) SO3(g)+O2(g) SO3(g)+O2(g) | -241.6 | 58 |
| 臭氧分解:2O3(g)⇌3O2(g) |

①由图可知相同温度下 NO 的转化率远高于 SO2,结合题中数据分析其可能原因:
②温度高于200℃后,NO和SO2的转化率随温度升高显著下降的可能原因是
③若其他条件不变,缩小反应器的容积,NO 和 SO2的平衡转化率
(3)在一定条件下,焦炭催化还原SO2的化学方程式为:2C(s)+2SO2(g)⇌S2(g)+2CO2(g)
①该反应的逆反应速率表达式:v逆=k逆·c(S2)·c2(CO2),k逆为速率常数(仅与温度有关)。表为某温度下,测得的实验数据:
| S2的浓度/(mol/L) | CO2的浓度/(mol/L) | 逆反应速率/(mol L-1 L-1 min-1) min-1) |
| 0.1 | c1 | 9.6 |
| c2 | c1 | 19.2 |
| c2 | 0.3 | 64.8 |
②一定压强下,向1L 密闭容器中加入足量的焦炭和 1molSO2 发生上述反应,反应 10min 时,测得SO2的生成速率与S2(g)的生成速率随温度变化的关系如图所示:

根据图象,判断反应2C(s)+2SO2(g)⇌S2(g)+2CO2(g)的∆H
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】乙烯的产量是衡量一个国家石油化工发展水平的标志,乙烯作为现代有机合成的重要原料,研究其合成方法受到科学家的青睐。回答下列问题:
(1)丙烯歧化法
反应原理为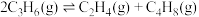
 ,向恒温恒容的密闭容器中通入一定量的
,向恒温恒容的密闭容器中通入一定量的 ,生成
,生成 的物质的量与时间的关系如表所示:
的物质的量与时间的关系如表所示:
①
___________ ;初始时总压强为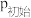 ,
, 时总压强为
时总压强为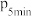 ,则
,则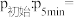
___________ 。
②其他条件不变,若缩小容器的体积,则 的转化率将
的转化率将___________ (填“增大”、“减小”或“不变”)。
(2) 催化加氢法
催化加氢法
反应原理为
 。向2L的恒容密闭容器中通入
。向2L的恒容密闭容器中通入
 和
和
 ,在催化剂作用下发生上述反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图所示:
,在催化剂作用下发生上述反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图所示:
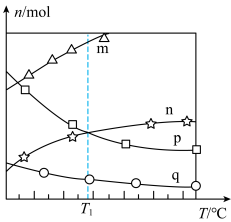
①图中曲线代表乙烯的物质的量随温度的变化关系的是___________ (填字母)。
②下列说法正确的是___________ (填标号)。
A.使用催化剂,可降低反应的活化能,加快反应速率,提高平衡产率
B.其他条件不变时,若扩大容器容积,则平衡逆向移动, 减小,
减小, 增大
增大
C.若容器内混合气体的密度不再随时间改变时,说明反应已达到平衡状态
D.保持其他条件不变,再通入
 ,达到平衡时
,达到平衡时 的转化率增大,平衡常数K保持不变
的转化率增大,平衡常数K保持不变
③ 时,反应的化学平衡常数
时,反应的化学平衡常数
___________ , 的平衡转化率为
的平衡转化率为___________ (保留三位有效数字)%。
(3)柴油裂解法
实验测得柴油裂解得到乙烯和丙烯的收率与温度、柴油在裂解设备内的停留时间的关系如图所示,工业上为获得较多的乙烯应选择较为适宜的温度和停留时间分别为___________ K和___________ s。

(1)丙烯歧化法
反应原理为
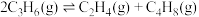
 ,向恒温恒容的密闭容器中通入一定量的
,向恒温恒容的密闭容器中通入一定量的 ,生成
,生成 的物质的量与时间的关系如表所示:
的物质的量与时间的关系如表所示:| 反应时间/min | 5 | 10 | 15 | 20 | 25 |
 的物质的量/mol 的物质的量/mol | 0.8 | 1.2 | 1.5 | a | 1.5 |

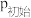 ,
, 时总压强为
时总压强为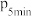 ,则
,则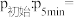
②其他条件不变,若缩小容器的体积,则
 的转化率将
的转化率将(2)
 催化加氢法
催化加氢法反应原理为

 。向2L的恒容密闭容器中通入
。向2L的恒容密闭容器中通入
 和
和
 ,在催化剂作用下发生上述反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图所示:
,在催化剂作用下发生上述反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图所示:
①图中曲线代表乙烯的物质的量随温度的变化关系的是
②下列说法正确的是
A.使用催化剂,可降低反应的活化能,加快反应速率,提高平衡产率
B.其他条件不变时,若扩大容器容积,则平衡逆向移动,
 减小,
减小, 增大
增大C.若容器内混合气体的密度不再随时间改变时,说明反应已达到平衡状态
D.保持其他条件不变,再通入

 ,达到平衡时
,达到平衡时 的转化率增大,平衡常数K保持不变
的转化率增大,平衡常数K保持不变③
 时,反应的化学平衡常数
时,反应的化学平衡常数
 的平衡转化率为
的平衡转化率为(3)柴油裂解法
实验测得柴油裂解得到乙烯和丙烯的收率与温度、柴油在裂解设备内的停留时间的关系如图所示,工业上为获得较多的乙烯应选择较为适宜的温度和停留时间分别为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】以菱镁矿(主要成分是 ,含少量
,含少量 、
、 、
、 和
和 等)为原料制备镁和铁红,流程如下,回答下列问题:
等)为原料制备镁和铁红,流程如下,回答下列问题:
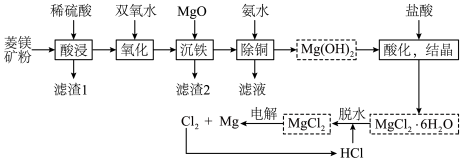
(1)写出“氧化”的离子方程式___________ ;以石墨为电极,“电解”中阳极的电极反应式为___________ 。
(2)“脱水”中 的作用是
的作用是___________ 。
(3)已知: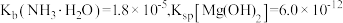 。“除铜”中,
。“除铜”中,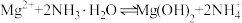 的平衡常数
的平衡常数
___________ 。
(4)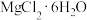 的热重曲线如图所示。
的热重曲线如图所示。
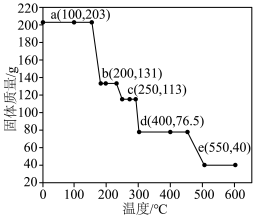
①200℃时固体产物的化学式为___________ 。
②写出400℃时生成固体产物(一种碱式盐)的化学方程式___________ 。
(5)镁铁晶胞如图所示。已知:晶胞参数为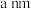 ,
, 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
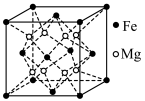
2个最近的Fe原子之间距离为________ nm,该晶体密度为_______ g/cm3(以上两空均用含字母的式子表示)。
 ,含少量
,含少量 、
、 、
、 和
和 等)为原料制备镁和铁红,流程如下,回答下列问题:
等)为原料制备镁和铁红,流程如下,回答下列问题:
(1)写出“氧化”的离子方程式
(2)“脱水”中
 的作用是
的作用是(3)已知:
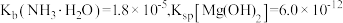 。“除铜”中,
。“除铜”中,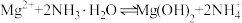 的平衡常数
的平衡常数
(4)
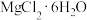 的热重曲线如图所示。
的热重曲线如图所示。
①200℃时固体产物的化学式为
②写出400℃时生成固体产物(一种碱式盐)的化学方程式
(5)镁铁晶胞如图所示。已知:晶胞参数为
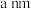 ,
, 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
2个最近的Fe原子之间距离为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】镓是制作高性能半导体的重要原料。在工业上经常从锌矿冶炼的废渣中回收镓。已知锌矿渣中含有Zn、Fe、Pb、Ga以及二氧化硅等,目前综合利用锌矿渣的流程如下:

已知:①Ga性质与铝相似。
②lg2=0.3,lg3=0.48。
③如下表所示。
(1)写出Ga的原子结构示意图______________________________ 。
(2)滤渣1的成分为________________________ 。
(3)加入H2O2的目的( 用离子方程式和适当语言回答)____________________________________ 。
(4)室温条件下,若浸出液中各种阳离子的浓度均为0.01mo/L且某种离子浓度小于1×10-5 mol/L即认为该离子已完全除去,问操作B调节pH的范围是________________________ 。
(5)操作C中,需要加入氢氧化钠溶液,其目的是_____________________ (用离子方程式解释);能否用氨水代替NaOH溶液,为什么? ________________________ ;如何检测Fe(OH)3洗涤干净? ________________________ 。
(6)在工业上,经常用电解NaGaO2溶液的方法生产Ga,写出阴极的电极反应方程式:____________________________________ 。

已知:①Ga性质与铝相似。
②lg2=0.3,lg3=0.48。
③如下表所示。
| Zn(OH)2 | Ga(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| Ksp | 1.6×10-17 | 2.7×10-31 | 8×10-16 | 2.8×10-39 |
(2)滤渣1的成分为
(3)加入H2O2的目的( 用离子方程式和适当语言回答)
(4)室温条件下,若浸出液中各种阳离子的浓度均为0.01mo/L且某种离子浓度小于1×10-5 mol/L即认为该离子已完全除去,问操作B调节pH的范围是
(5)操作C中,需要加入氢氧化钠溶液,其目的是
(6)在工业上,经常用电解NaGaO2溶液的方法生产Ga,写出阴极的电极反应方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
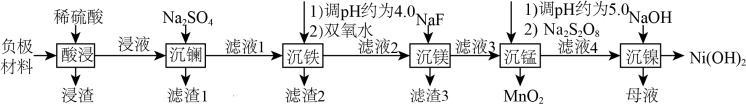
【推荐3】氢镍电池是目前使用最广的含镍电池,废旧电池的处理对环境保护和资源的再利用意义重大。一种对废旧氢镍电池负极材料(含有NiO、Ni和少量La、Fe、Mg、MnO2、石墨粉等)进行湿法处理的流程如图所示:
②Ksp(MgF2)=6.4 ;
;
③H2SO4第一步完全电离,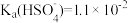 。
。
回答下列问题:
(1)Ni2+的价层电子排布式为_____________ 。
(2)能提高“酸浸”效率的措施有_____________ (任写一种)。
(3)若滤渣1的成分为 ,已知“沉镧”过程中溶液的pH与沉镧率的变化关系如图所示。试分析pH<2.0时沉镧率降低的原因
,已知“沉镧”过程中溶液的pH与沉镧率的变化关系如图所示。试分析pH<2.0时沉镧率降低的原因_________________ 。
(5)“沉镁”后滤液3中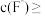
__________  (溶液中离子浓度
(溶液中离子浓度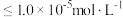 时认为该离子沉淀完全)。
时认为该离子沉淀完全)。
(6) 中存在过氧键(-O-O-),“沉锰”反应的离子方程式为
中存在过氧键(-O-O-),“沉锰”反应的离子方程式为_________________ 。
(7)“沉镍”所用试剂不宜选用氨水的原因为_________________ ,母液中可提取出的循环利用的物质为_____________ (填化学式)。
②Ksp(MgF2)=6.4
 ;
;③H2SO4第一步完全电离,
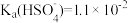 。
。回答下列问题:
(1)Ni2+的价层电子排布式为
(2)能提高“酸浸”效率的措施有
(3)若滤渣1的成分为
 ,已知“沉镧”过程中溶液的pH与沉镧率的变化关系如图所示。试分析pH<2.0时沉镧率降低的原因
,已知“沉镧”过程中溶液的pH与沉镧率的变化关系如图所示。试分析pH<2.0时沉镧率降低的原因 
| A.KSCN溶液 |
| B.K3[Fe(CN)6]溶液 |
| C.NaOH溶液 |
| D.KSCN溶液和氯水 |
(5)“沉镁”后滤液3中
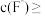
 (溶液中离子浓度
(溶液中离子浓度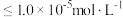 时认为该离子沉淀完全)。
时认为该离子沉淀完全)。(6)
 中存在过氧键(-O-O-),“沉锰”反应的离子方程式为
中存在过氧键(-O-O-),“沉锰”反应的离子方程式为(7)“沉镍”所用试剂不宜选用氨水的原因为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】用含有Al2O3、SiO2和少量FeO·xFe2O3的铝灰制备Al2(SO4)3·18H2O,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ..再经过一系列操作,分离得到产品。
(1)步骤Ⅰ中过滤所得滤渣主要成分为:______________________ ,
H2SO4溶解Al2O3的离子方程式为:_____________________ 。
(2)步骤Ⅱ中加入KMnO4时发生反应的离子方程式为:______________ 。
(3)已知:生成氢氧化物沉淀的pH
注:金属离子的起始浓度均为0.1 mol·L-1
①根据表中数据解释步骤Ⅱ的目的:________________________ ,
②当Al3+开始沉淀时,Fe3+的浓度约为:_______________________ 。
(4)已知:一定条件下,MnO 可与Mn2+反应生成MnO2。
可与Mn2+反应生成MnO2。
①向Ⅲ的沉淀中加入浓盐酸并加热,能说明沉淀中存在MnO2的现象是:___________________ 。
②步骤Ⅳ中加入MnSO4的目的是:__________________________ 。
(5)步骤Ⅴ中“一系列操作”是__________________ 、_________________ 。
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ..再经过一系列操作,分离得到产品。
(1)步骤Ⅰ中过滤所得滤渣主要成分为:
H2SO4溶解Al2O3的离子方程式为:
(2)步骤Ⅱ中加入KMnO4时发生反应的离子方程式为:
(3)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度均为0.1 mol·L-1
①根据表中数据解释步骤Ⅱ的目的:
②当Al3+开始沉淀时,Fe3+的浓度约为:
(4)已知:一定条件下,MnO
 可与Mn2+反应生成MnO2。
可与Mn2+反应生成MnO2。①向Ⅲ的沉淀中加入浓盐酸并加热,能说明沉淀中存在MnO2的现象是:
②步骤Ⅳ中加入MnSO4的目的是:
(5)步骤Ⅴ中“一系列操作”是
您最近一年使用:0次
【推荐2】镁及其化合物是实验设计的热点载体,查阅资料。
某学习小组设计实验探究镁与二氧化氮反应的产物,提供的实验装置如图所示。
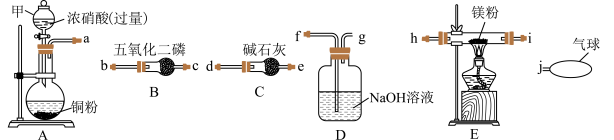
(1)仪器甲名称为_______ ,仪器接口顺序为a→______ ,______ →______ ,______ →______ ,______ →______ ,______ →j。
(2)装置A中的主要现象为_______ ,C装置的作用是_____ 。
(3)确定有N2生成的实验现象是________ 。
(4)经测定,Mg与NO2反应生成MgO、Mg3N2和N2,其中Mg3N2和N2的物质的量相等。E中发生反应的化学方程式为______ 。
(5)实验完毕后,设计实验确认产物中有Mg3N2,取少量C中残留固体于试管中滴加蒸馏水,_________ ,则产物中有氮化镁。
| ⅰ | 2NO2+2NaOH=NaNO2+NaNO3+H2O |
| ⅱ | Mg3N2与水反应 |

(1)仪器甲名称为
(2)装置A中的主要现象为
(3)确定有N2生成的实验现象是
(4)经测定,Mg与NO2反应生成MgO、Mg3N2和N2,其中Mg3N2和N2的物质的量相等。E中发生反应的化学方程式为
(5)实验完毕后,设计实验确认产物中有Mg3N2,取少量C中残留固体于试管中滴加蒸馏水,
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。

回答下列问题:
(1)盛放MnO2粉末的仪器名称是___ ,a中的试剂为____ ,b中采用的加热方式是___ ,c中化学反应的离子方程式是___ 。
(2)反应结束后,取出b中试管,经冷却结晶,__ ,__ ,干燥,得到 晶体。d的作用是
晶体。d的作用是__ ,可选用试剂__ (填编号)。
a. b.
b. c.
c. d.
d.
(3)取少量 和
和 溶液分别置于1号和2号试管中,滴加中性
溶液分别置于1号和2号试管中,滴加中性 溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 显
显__ 色。可知该条件下 的氧化能力
的氧化能力__  (填“大于”或“小于”)。
(填“大于”或“小于”)。
(4)制备 时,温度过高会生成
时,温度过高会生成 。当
。当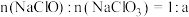 时,该反应中
时,该反应中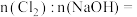
__ 。
 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
回答下列问题:
(1)盛放MnO2粉末的仪器名称是
(2)反应结束后,取出b中试管,经冷却结晶,
 晶体。d的作用是
晶体。d的作用是a.
 b.
b. c.
c. d.
d.
(3)取少量
 和
和 溶液分别置于1号和2号试管中,滴加中性
溶液分别置于1号和2号试管中,滴加中性 溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 显
显 的氧化能力
的氧化能力 (填“大于”或“小于”)。
(填“大于”或“小于”)。(4)制备
 时,温度过高会生成
时,温度过高会生成 。当
。当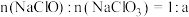 时,该反应中
时,该反应中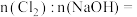
您最近一年使用:0次



