利用铜萃取剂M,通过如下反应实现铜离子的富集:
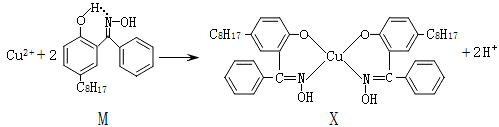
(1)X难溶于水、易溶于有机溶剂,其晶体类型为________ 。
(2)M所含元素的电负性由大到小顺序为_______ ,N原子以_____ 轨道与O原子形成σ键。
(3)上述反应中断裂和生成的化学键有______ (填序号)。
a.离子键
b.配位键
c.金属键
d.范德华力
e.共价键
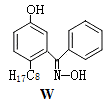
(4)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是_____ 。
(5)基态Cu2+的外围电子排布式为________ ,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律。判断Sc3+、Zn2+的水合离子为无色的依据是___________ 。

(1)X难溶于水、易溶于有机溶剂,其晶体类型为
(2)M所含元素的电负性由大到小顺序为
(3)上述反应中断裂和生成的化学键有
a.离子键
b.配位键
c.金属键
d.范德华力
e.共价键
(4)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是

(5)基态Cu2+的外围电子排布式为
| 离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
| 颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
更新时间:2016-12-09 07:39:50
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】硼元素为绿色植物或藻类生长的必需元素。回答下列问题:
(1)基态硼原子核外电子排布式可表示为__________________ 。
(2)晶体硼单质的基本结构单元为正二十面体,其能自发地呈现多面体外形,这种性质称为晶体的__________________ 。
(3)将少量BF3通入水中时,得到四氟硼酸(HBF4)溶液,同时有硼酸生成。四氟硼酸为无色透明液体,呈强酸性,用于金属表面氧化物、硅酸盐膜的清洁和腐蚀剂。
①BF 离子中B原子的杂化方式为
离子中B原子的杂化方式为___________ 。
②硼酸晶体[H3BO3或B(OH)3]的片层结构如下图所示,其在冷水中溶解度低,而在热水中增加,原因是______________________ 。
③硼酸溶液中,存在[B(OH)4]-离子,该离子中含有的化学键为_____________ 。
A.离子键 B.共价键 C.金属键 D.配位键

(4)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,结构之一为立方氮化硼,如图所示。
①图中氮原子的配位数为________ ,离硼原子最近且等距离的硼原子有______ 个。
②已知立方氮化硼晶胞中B与N之间的距离为a nm,则晶胞边长___________ pm。
(1)基态硼原子核外电子排布式可表示为
(2)晶体硼单质的基本结构单元为正二十面体,其能自发地呈现多面体外形,这种性质称为晶体的
(3)将少量BF3通入水中时,得到四氟硼酸(HBF4)溶液,同时有硼酸生成。四氟硼酸为无色透明液体,呈强酸性,用于金属表面氧化物、硅酸盐膜的清洁和腐蚀剂。
①BF
 离子中B原子的杂化方式为
离子中B原子的杂化方式为②硼酸晶体[H3BO3或B(OH)3]的片层结构如下图所示,其在冷水中溶解度低,而在热水中增加,原因是
③硼酸溶液中,存在[B(OH)4]-离子,该离子中含有的化学键为
A.离子键 B.共价键 C.金属键 D.配位键

(4)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,结构之一为立方氮化硼,如图所示。
①图中氮原子的配位数为
②已知立方氮化硼晶胞中B与N之间的距离为a nm,则晶胞边长
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】GaN是制造5G芯片的材料,氮化镓铝和氮化铝LED可发出紫外光。回答下列问题:
(1)基态As原子核外电子排布式为[Ar]________ ,下列状态的铝中,电离最外层的一个电子所需能量最小的是_____________ (填标号)。
A. B.
B. 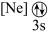 C.[Ne] D.
C.[Ne] D. 
(2)8—羟基喹啉铝(分子式C27H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH4与 (8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为
(8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为_______ ; 所含元素中电负性最大的是
所含元素中电负性最大的是___ (填元素符号),C、N、O的杂化方式依次为 _____ 、_________ 和____________ 。
(3)已知下列化合物的熔点:
①表中卤化物的熔点产生差异的原因是____________ 。
②熔融AlCl3时可生成具有挥发性的二聚体Al2Cl6,二聚体Al2Cl6的结构式为_______ ;其中Al的配位数为_________ 。
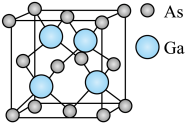
(4)GaAs的晶胞结构如图所示,紧邻的As原子之间的距离为x,紧邻的As、Ga原子之间的距离为y,则 =
=________ 。
(1)基态As原子核外电子排布式为[Ar]
A.
 B.
B. 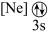 C.[Ne] D.
C.[Ne] D. 
(2)8—羟基喹啉铝(分子式C27H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH4与
 (8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为
(8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为 所含元素中电负性最大的是
所含元素中电负性最大的是(3)已知下列化合物的熔点:
| 化合物 | AlF3 | GaF3 | AlCl3 |
| 熔点/℃ | 1040 | 1000 | 194 |
①表中卤化物的熔点产生差异的原因是
②熔融AlCl3时可生成具有挥发性的二聚体Al2Cl6,二聚体Al2Cl6的结构式为
(4)GaAs的晶胞结构如图所示,紧邻的As原子之间的距离为x,紧邻的As、Ga原子之间的距离为y,则
 =
=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】铜及其化合物在生产生活中有着重要应用。回答下列问题:
(1)基态 离子核外电子有
离子核外电子有_______ 种不同的空间运动状态。
(2)向硫酸铜溶液中滴加氨水,首先出现蓝色沉淀,氨水过量后沉淀逐渐溶解,加入乙醇后析出深蓝色晶体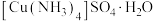 。
。
①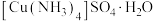 中,配位原子是
中,配位原子是_______ ,与 是等电子体的一种分子为
是等电子体的一种分子为_______ (填化学式)。
② 具有对称的空间构型,若其中两个
具有对称的空间构型,若其中两个 被两个
被两个 取代,能得到两种不同结构的产物,请推测
取代,能得到两种不同结构的产物,请推测 的空间构型最可能为
的空间构型最可能为_______ 。
③当氨分子得到一个 ,变成铵根离子时,下列描述合理的是
,变成铵根离子时,下列描述合理的是_______ 。
A.氮原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角变小了
④请写出氨水过量后沉淀逐渐溶解的离子方程式:_______ 。
⑤加入乙醇后会有深蓝色的晶体析出的原因为_______ 。
(3)科学家推测胆矾结构示意图可简单表示如图,则胆矾中含有的化学键类型是_______ (填字母代号)。
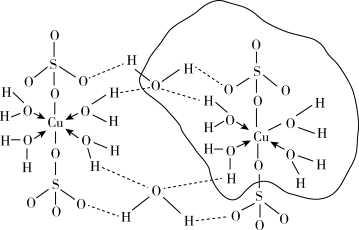
a.配位键 b.极性键 c.离子键 d.非极性键 e.氢键
(1)基态
 离子核外电子有
离子核外电子有(2)向硫酸铜溶液中滴加氨水,首先出现蓝色沉淀,氨水过量后沉淀逐渐溶解,加入乙醇后析出深蓝色晶体
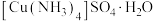 。
。①
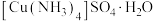 中,配位原子是
中,配位原子是 是等电子体的一种分子为
是等电子体的一种分子为②
 具有对称的空间构型,若其中两个
具有对称的空间构型,若其中两个 被两个
被两个 取代,能得到两种不同结构的产物,请推测
取代,能得到两种不同结构的产物,请推测 的空间构型最可能为
的空间构型最可能为③当氨分子得到一个
 ,变成铵根离子时,下列描述合理的是
,变成铵根离子时,下列描述合理的是A.氮原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角变小了
④请写出氨水过量后沉淀逐渐溶解的离子方程式:
⑤加入乙醇后会有深蓝色的晶体析出的原因为
(3)科学家推测胆矾结构示意图可简单表示如图,则胆矾中含有的化学键类型是

a.配位键 b.极性键 c.离子键 d.非极性键 e.氢键
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】Be被主要用于原子能反应堆材料、宇航工程材料等,有“超级金属、尖端金属、空间金属”之称。硫酸法是现代工业用绿柱石(主要成分为 ,还含有铁等杂质)生产氧化铍的方法之一,其简化的工艺流程如下:
,还含有铁等杂质)生产氧化铍的方法之一,其简化的工艺流程如下:

已知几种金属阳离子的氢氧化物沉淀时的pH如下表:
(1)步骤②中还可以采取什么措施提高反应速率___________ (除粉碎外,任写一点)。
(2)滤渣1成分的化学式为___________ 。
(3)步骤③中加入 的目的是
的目的是___________ 。
(4)步骤④不宜使用 溶液来沉淀
溶液来沉淀 ,原因是
,原因是___________ (用必要的文字和离子方程式说明);已知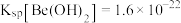 ,则
,则 沉淀完全时,溶液中
沉淀完全时,溶液中
___________  (通常认为溶液中离子浓度小于
(通常认为溶液中离子浓度小于 时为沉淀完全)。
时为沉淀完全)。
(5)绿柱石因含有不同杂质而产生不同的颜色。各种绿柱石中最名贵的是祖母绿,这是由铬、钒元素的存在造成的。
①基态 的最高能层中成对电子与未成对电子的数目之比为
的最高能层中成对电子与未成对电子的数目之比为___________ 。
②重铬酸铵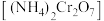 常用作有机合成催化剂,
常用作有机合成催化剂, 的结构如图。
的结构如图。
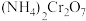 中
中 键数目为
键数目为___________  。
。

 ,还含有铁等杂质)生产氧化铍的方法之一,其简化的工艺流程如下:
,还含有铁等杂质)生产氧化铍的方法之一,其简化的工艺流程如下:
已知几种金属阳离子的氢氧化物沉淀时的pH如下表:
| 金属阳离子 |  |  |  |  |
| 开始沉淀时pH | 1.5 | 3.3 | 6.5 | 5.2 |
| 沉淀完全时pH | 3.7 | 5.0 | 9.7 | — |
(1)步骤②中还可以采取什么措施提高反应速率
(2)滤渣1成分的化学式为
(3)步骤③中加入
 的目的是
的目的是(4)步骤④不宜使用
 溶液来沉淀
溶液来沉淀 ,原因是
,原因是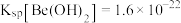 ,则
,则 沉淀完全时,溶液中
沉淀完全时,溶液中
 (通常认为溶液中离子浓度小于
(通常认为溶液中离子浓度小于 时为沉淀完全)。
时为沉淀完全)。(5)绿柱石因含有不同杂质而产生不同的颜色。各种绿柱石中最名贵的是祖母绿,这是由铬、钒元素的存在造成的。
①基态
 的最高能层中成对电子与未成对电子的数目之比为
的最高能层中成对电子与未成对电子的数目之比为②重铬酸铵
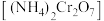 常用作有机合成催化剂,
常用作有机合成催化剂, 的结构如图。
的结构如图。
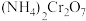 中
中 键数目为
键数目为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】(1)火箭使用的推进剂燃料由N、H两种元素组成,且原子个数N:H=1:2,其水溶液显碱性,则该物质中N原子的杂化方式为_______ 。
(2)笑气(N2O)曾被用作麻醉剂,但过度吸食会导致身体机能紊乱。预测N2O的结构式为_ 。
(3)元素的基态气态原子得到一个电子形成气态-1价离子时所放出的能量称作第一电子亲和能(E),-1价阴离子再获得一个电子的能量变化叫做第二电子亲和能,部分元素或离子的电子亲和能数据如表所示。
下列说法正确的是__ 。
A.电子亲和能越大,说明越难得到电子
B.一个基态的气态氧原子得到一个电子成为O2-时放出141 kJ的能量
C.氧元素的第二电子亲和能是-780 kJ/mol
D.基态的气态氧原子得到两个电子成为O2-需要吸收能量
(4)在电解炼铝过程中加入冰晶石(用“A”代替),可起到降低Al2O3熔点的作用。冰晶石的生产原理为:2Al(OH)3+12HF+3Na2CO3=2A+3CO2↑+9H2O。根据题意完成下列填空:
①冰晶石的化学式为__ 。
②冰晶石由两种微粒构成,冰晶石的晶胞结构如图甲所示,●位于大立方体的顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是__ (填微粒符号)。
③冰晶石溶液中不存在的微粒间作用力有__ (填选项字母)。
A.离子键 B.共价键 C.配位键 D.金属键 E.范德华力 F.氢键
④Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示:
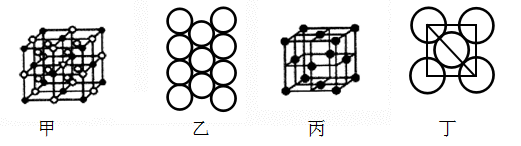
若已知A1的原子半径为d cm,NA代表阿伏加德罗常数,Al的相对原子质量为M,则Al晶体的密度为______ g•cm-3(用字母表示)。
(5)配合物Fe(CO)5的熔点-20℃,沸点103 ℃,可用于制备纯铁。Fe(CO)5的结构如图所示。

①Fe(CO)5晶体类型属于_______ 晶体。
②关于Fe(CO)5,下列说法正确的是______ 。
A.Fe(CO)5是非极性分子,CO是极性分子
B.Fe(CO)5中Fe原子以sp3杂化方式与CO成键
C.1 mol Fe(CO)5含有10 mol配位键
D.反应Fe(CO)5=Fe+5CO没有新化学键生成
(2)笑气(N2O)曾被用作麻醉剂,但过度吸食会导致身体机能紊乱。预测N2O的结构式为
(3)元素的基态气态原子得到一个电子形成气态-1价离子时所放出的能量称作第一电子亲和能(E),-1价阴离子再获得一个电子的能量变化叫做第二电子亲和能,部分元素或离子的电子亲和能数据如表所示。
| 元素 | C1 | Br | I | O | O- |
| 电子亲和能(kJ/mol) | 349 | 343 | 295 | 141 | -780 |
下列说法正确的是
A.电子亲和能越大,说明越难得到电子
B.一个基态的气态氧原子得到一个电子成为O2-时放出141 kJ的能量
C.氧元素的第二电子亲和能是-780 kJ/mol
D.基态的气态氧原子得到两个电子成为O2-需要吸收能量
(4)在电解炼铝过程中加入冰晶石(用“A”代替),可起到降低Al2O3熔点的作用。冰晶石的生产原理为:2Al(OH)3+12HF+3Na2CO3=2A+3CO2↑+9H2O。根据题意完成下列填空:
①冰晶石的化学式为
②冰晶石由两种微粒构成,冰晶石的晶胞结构如图甲所示,●位于大立方体的顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是
③冰晶石溶液中不存在的微粒间作用力有
A.离子键 B.共价键 C.配位键 D.金属键 E.范德华力 F.氢键
④Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示:

若已知A1的原子半径为d cm,NA代表阿伏加德罗常数,Al的相对原子质量为M,则Al晶体的密度为
(5)配合物Fe(CO)5的熔点-20℃,沸点103 ℃,可用于制备纯铁。Fe(CO)5的结构如图所示。

①Fe(CO)5晶体类型属于
②关于Fe(CO)5,下列说法正确的是
A.Fe(CO)5是非极性分子,CO是极性分子
B.Fe(CO)5中Fe原子以sp3杂化方式与CO成键
C.1 mol Fe(CO)5含有10 mol配位键
D.反应Fe(CO)5=Fe+5CO没有新化学键生成
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】以 、
、 等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
(1)基态 原子的末成对电子有
原子的末成对电子有_______ 个。
(2) 、
、 等金属具有良好的导电性,从金属键的理论看,原因是
等金属具有良好的导电性,从金属键的理论看,原因是_______ 。
(3)邻苯二甲酸酐(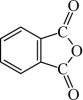 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺(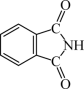 )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是_______ 。
(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为_______ 。
(5) 晶体中部分
晶体中部分 原子被
原子被 原子替代后可以改善半导体的性能,
原子替代后可以改善半导体的性能, 键中离子键成分的百分数小于
键中离子键成分的百分数小于 键,原因是
键,原因是_______ 。
(6)氧化亚铜的晶胞结构如下图所示,若最近的 与
与 的核间距为
的核间距为 ,则氧化亚铜晶体的密度是
,则氧化亚铜晶体的密度是_______  (
( 代表阿伏加德罗常数的值,列式即可)。
代表阿伏加德罗常数的值,列式即可)。

 、
、 等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:(1)基态
 原子的末成对电子有
原子的末成对电子有(2)
 、
、 等金属具有良好的导电性,从金属键的理论看,原因是
等金属具有良好的导电性,从金属键的理论看,原因是(3)邻苯二甲酸酐(
 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺( )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为
(5)
 晶体中部分
晶体中部分 原子被
原子被 原子替代后可以改善半导体的性能,
原子替代后可以改善半导体的性能, 键中离子键成分的百分数小于
键中离子键成分的百分数小于 键,原因是
键,原因是(6)氧化亚铜的晶胞结构如下图所示,若最近的
 与
与 的核间距为
的核间距为 ,则氧化亚铜晶体的密度是
,则氧化亚铜晶体的密度是 (
( 代表阿伏加德罗常数的值,列式即可)。
代表阿伏加德罗常数的值,列式即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】 是一种高迁移率的新型热电材料,回答下列问题:
是一种高迁移率的新型热电材料,回答下列问题:
(1) 为
为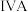 族元素,单质
族元素,单质 与干燥
与干燥 反应生成
反应生成 。常温常压下
。常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为___________ ,其固体的晶体类型为___________ 。
(2) 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为___________ (填化学式,下同),键角由大到小的顺序为___________
(3)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系CdSnAs2的晶胞结构如图所示,晶胞棱边夹角均为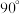 ,晶胞中部分原子的分数坐标如下表所示。
,晶胞中部分原子的分数坐标如下表所示。
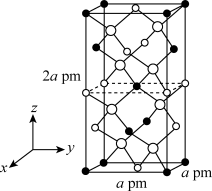
找出距离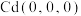 最近的Sn
最近的Sn_____ (用分数坐标表示)。CdSnAs2晶体中与单个Sn键合的As有______ 个。
 是一种高迁移率的新型热电材料,回答下列问题:
是一种高迁移率的新型热电材料,回答下列问题:(1)
 为
为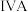 族元素,单质
族元素,单质 与干燥
与干燥 反应生成
反应生成 。常温常压下
。常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为(2)
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为(3)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系CdSnAs2的晶胞结构如图所示,晶胞棱边夹角均为
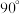 ,晶胞中部分原子的分数坐标如下表所示。
,晶胞中部分原子的分数坐标如下表所示。| 坐标原子 | X | y | Z |
| Cd | 0 | 0 | 0 |
| Sn | 0 | 0 | 0.5 |
| As | 0.25 | 0.25 | 0.125 |

找出距离
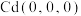 最近的Sn
最近的Sn
您最近一年使用:0次
【推荐2】完成填空。
(1)下列书写方式可正确表示原子轨道的是_______ 。
A.2s B.2d C.3px D.3f
(2)写出基态镓(Ga)的价电子排布式:_______ 。
(3)碳元素、氧元素分别与氢元素形成的最简单化合物中,沸点较高的为_______ (写化学式),原因是_______ 。
(4)R为铬元素,R的一种配合物的化学式为RCl3·6H2O。已知0.01molRCl3·6H2O在水溶液中用过量硝酸银溶液处理,产生0.02molAgCl沉淀。此配合物最可能是_______ 。
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2·H2O
C.[R(H2O)4Cl2]Cl·2H2O D.[R(H2O)3Cl3]·3H2O
(5)NF3可由NH3和F2在Cu催化剂存在下反应直接得到:4NH3+3F2 NF3+3NH4F。上述化学方程式中的5种物质所属的晶体类型有
NF3+3NH4F。上述化学方程式中的5种物质所属的晶体类型有_______ (填序号)。
A.离子晶体 B.分子晶体 C.共价晶体 D.金属晶体
(6)向含少量CuSO4的水溶液中逐滴滴入氨水,生成蓝色沉淀,继续滴加氨水至过量,沉淀溶解,得到深蓝色溶液,写出沉淀溶解过程中涉及的离子方程式_______ 。
(1)下列书写方式可正确表示原子轨道的是
A.2s B.2d C.3px D.3f
(2)写出基态镓(Ga)的价电子排布式:
(3)碳元素、氧元素分别与氢元素形成的最简单化合物中,沸点较高的为
(4)R为铬元素,R的一种配合物的化学式为RCl3·6H2O。已知0.01molRCl3·6H2O在水溶液中用过量硝酸银溶液处理,产生0.02molAgCl沉淀。此配合物最可能是
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2·H2O
C.[R(H2O)4Cl2]Cl·2H2O D.[R(H2O)3Cl3]·3H2O
(5)NF3可由NH3和F2在Cu催化剂存在下反应直接得到:4NH3+3F2
 NF3+3NH4F。上述化学方程式中的5种物质所属的晶体类型有
NF3+3NH4F。上述化学方程式中的5种物质所属的晶体类型有A.离子晶体 B.分子晶体 C.共价晶体 D.金属晶体
(6)向含少量CuSO4的水溶液中逐滴滴入氨水,生成蓝色沉淀,继续滴加氨水至过量,沉淀溶解,得到深蓝色溶液,写出沉淀溶解过程中涉及的离子方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分。表中所列的字母分别代表一种元素。
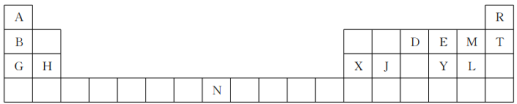
回答下列问题:
(1)请写出H的单质与二氧化碳反应的方程式:_______ 。
(2)D的简单气态氢化物的VSEPR模型为_______ ,分子的空间结构为_______ 。
(3)第一电离能H_______ X(填“>”“<”或“=”),其原因是_______ 。
(4)电负性E_______ M(填“>”“<”或“=”)。
(5)D2E的沸点比DA3的沸点低,其原因是_______ 。

回答下列问题:
(1)请写出H的单质与二氧化碳反应的方程式:
(2)D的简单气态氢化物的VSEPR模型为
(3)第一电离能H
(4)电负性E
(5)D2E的沸点比DA3的沸点低,其原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下:

回答下列问题:
(1)基态钛原子的价电子排布图为______________ ,其原子核外共有________ 种运动状态不相同的电子。金属钛晶胞如下图1所示,为_______________ 堆积(填堆积方式)。
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l-l >> l-b > b-b(l为孤对电子对,b为键合电子对),则关于H2O中的H-O-H键角可得出的结论是________ 。
(3)已知TiCl4在通常情况下是无色液体,熔点为–37℃,沸点为136℃,可知TiCl4为________ 晶体。
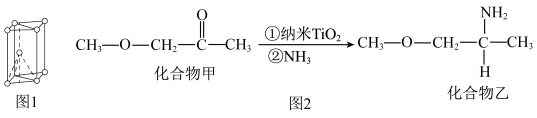
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2。化合物乙的沸点明显高于化合物甲,主要原因是____________ 。化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为___________ 。
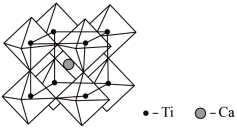
(5)钙钛矿晶体的结构如右图所示。钛离子位于立方晶胞的角顶,被________ 个氧离子包围成配位八面体;钙离子位于立方晶胞的体心,被________ 个氧离子包围。钙钛矿晶体的化学式为________________ 。若该晶胞的边长为a pm,则钙钛矿晶体的密度为______ g.cm-3(只要求列算式,不必计算出数值)。

回答下列问题:
(1)基态钛原子的价电子排布图为
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l-l >> l-b > b-b(l为孤对电子对,b为键合电子对),则关于H2O中的H-O-H键角可得出的结论是
| A.180° | B.接近120°,但小于120° |
| C.接近120°,但大于120° | D.接近109°28’,但小于109°28’ |
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2。化合物乙的沸点明显高于化合物甲,主要原因是

(5)钙钛矿晶体的结构如右图所示。钛离子位于立方晶胞的角顶,被

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】(1)氯酸钾熔化,粒子间克服了________ ;(填“离子键”“共价键”或“分子间作用力”,下同);二氧化硅熔化,粒子间克服了______ ;碘升华,粒子间克服了______ 。三种晶体的熔点由高到低的顺序是______ 。
(2)下列六种晶体:①CO2、②NaCl、③Na、④Si、⑤CS2、⑥金刚石,它们的熔点由低到高的顺序为_______ (用序号表示)。
(3)A、B、C、D为四种不同类型的晶体,性质如下:A固态时能导电,能溶于盐酸;B能溶于CS2,不溶于水;C固态时不导电,液态时能导电,可溶于水;D固态、液态时均不导电,熔点为3500℃。
试推断它们的晶体类型:A.____________ ;B.____________ ;C.____________ ;D.____________ 。
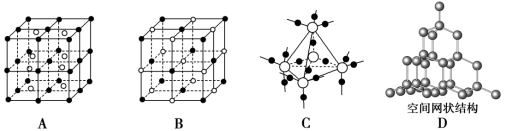
(4)A~D是化学教材中常见的几种晶体结构模型,请填写相应物质的名称:A.____________ ;B.____________ ;C.____________ ;D.____________ 。
(2)下列六种晶体:①CO2、②NaCl、③Na、④Si、⑤CS2、⑥金刚石,它们的熔点由低到高的顺序为
(3)A、B、C、D为四种不同类型的晶体,性质如下:A固态时能导电,能溶于盐酸;B能溶于CS2,不溶于水;C固态时不导电,液态时能导电,可溶于水;D固态、液态时均不导电,熔点为3500℃。
试推断它们的晶体类型:A.
(4)A~D是化学教材中常见的几种晶体结构模型,请填写相应物质的名称:A.

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】(现有几组物质的熔点(℃)数据:
据此回答下列问题:
(1)由表格可知,A组熔点普遍偏高,据此回答:
①A组属于__________ 晶体,其熔化时克服的粒子间的作用力是__________ ;
②硼晶体的硬度________ 硅晶体的硬度(填“大于”“小于”)。
(2)B组中 熔点反常是由于
熔点反常是由于__________ 。
(3)C组晶体中 、
、 、
、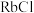 的熔点由高到低的顺序为
的熔点由高到低的顺序为_________ , 晶体的熔点高于三者,其原因是
晶体的熔点高于三者,其原因是________________ 。
(4)氢化铝钠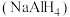 是一种新型轻质储氢材料,掺入少量
是一种新型轻质储氢材料,掺入少量 的
的 在150℃时释氢,在170℃、
在150℃时释氢,在170℃、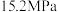 条件下又重复吸氢。
条件下又重复吸氢。 的晶胞结构如图所示:
的晶胞结构如图所示:
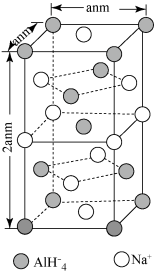
 晶体中,与
晶体中,与 紧邻且等距的
紧邻且等距的 有
有___________ 个; 晶体的密度为
晶体的密度为________  (用含a的代数式表示)。若
(用含a的代数式表示)。若 晶胞底心处的
晶胞底心处的 被
被 取代,得到的晶体为
取代,得到的晶体为_________ (填化学式)。
| A组 | B组 | C组 |
| 金刚石:3550 |  : :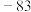 |  |
| 硅晶体:1410 |  : :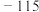 |  |
| 硼晶体:2300 |  : :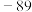 | 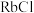 |
| 二氧化硅:1732 |  : :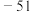 |  :2800℃ :2800℃ |
(1)由表格可知,A组熔点普遍偏高,据此回答:
①A组属于
②硼晶体的硬度
(2)B组中
 熔点反常是由于
熔点反常是由于(3)C组晶体中
 、
、 、
、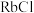 的熔点由高到低的顺序为
的熔点由高到低的顺序为 晶体的熔点高于三者,其原因是
晶体的熔点高于三者,其原因是(4)氢化铝钠
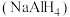 是一种新型轻质储氢材料,掺入少量
是一种新型轻质储氢材料,掺入少量 的
的 在150℃时释氢,在170℃、
在150℃时释氢,在170℃、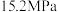 条件下又重复吸氢。
条件下又重复吸氢。 的晶胞结构如图所示:
的晶胞结构如图所示:
 晶体中,与
晶体中,与 紧邻且等距的
紧邻且等距的 有
有 晶体的密度为
晶体的密度为 (用含a的代数式表示)。若
(用含a的代数式表示)。若 晶胞底心处的
晶胞底心处的 被
被 取代,得到的晶体为
取代,得到的晶体为
您最近一年使用:0次



