【化学一化学与技术】下图是某企业设计的硫酸—磷肥—水泥联产、海水—淡水多用、盐—热—电联产的三大生态产业链流程图。
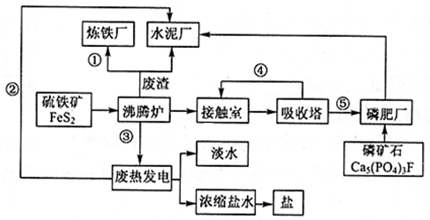
根据上述产业流程回答下列问题:
(1)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出③、④输送的主要物质的化学式或能量形式:③_____________________ ④_____________________ 。
(2)沸腾炉发生反应的化学方程式:_____________________ 。磷肥厂的主要产品是普钙(磷酸二氢钙和硫酸钙),写出由磷矿石和硫酸反应制普钙的化学方程式_____________________ 。
(3)在接触室中设置热交换器的目的是_______________ 、提高SO2转化率,从而充分利用能源。
(4)热电厂的冷却水是_____________________ ,该流程中浓缩盐水除提取盐以外还可提取的物质有_____________________ (写出一种即可)。
(5)根据现代化工厂设计理念请提出高炉炼铁厂废气、废渣及多余热能利用的设想:_________________ (写出一点即可)。

根据上述产业流程回答下列问题:
(1)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出③、④输送的主要物质的化学式或能量形式:③
(2)沸腾炉发生反应的化学方程式:
(3)在接触室中设置热交换器的目的是
(4)热电厂的冷却水是
(5)根据现代化工厂设计理念请提出高炉炼铁厂废气、废渣及多余热能利用的设想:
2015·山东泰安·一模 查看更多[1]
更新时间:2016-12-08 23:43:38
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】我国有广阔的海岸线,海水的综合利用大有可为。海水中溴含量约为65mg·L-1,从海水中提取溴的工艺流程如图所示。
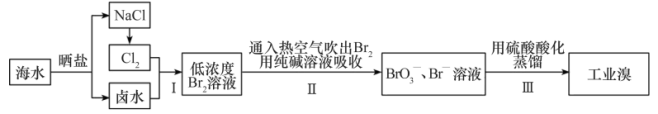
(1)步骤Ⅰ、步骤Ⅲ发生反应的离子反应方程式为___ 、___ 。
(2)步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是___ 。
(3)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的___ 。(填性质)
(4)步骤Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数:___ 。
 Br2+
Br2+ CO
CO =
= BrO
BrO +
+ Br-+
Br-+ CO2↑
CO2↑
(5)步骤Ⅱ中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。若从1000L海水中提取溴,理论上需要SO2的质量为___ 。

(1)步骤Ⅰ、步骤Ⅲ发生反应的离子反应方程式为
(2)步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是
(3)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的
(4)步骤Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数:
 Br2+
Br2+ CO
CO =
= BrO
BrO +
+ Br-+
Br-+ CO2↑
CO2↑(5)步骤Ⅱ中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。若从1000L海水中提取溴,理论上需要SO2的质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】一种以瓦斯泥(主要含ZnO、Bi2O3、Bi2S3、Bi、Fe2O3,还含少量PbO、CuO)为原料制备ZnO和BiOCl的工艺流程如图所示。回答下列问题:
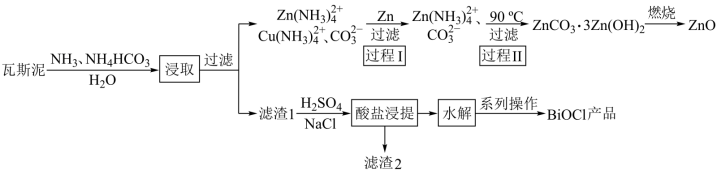
(1)“浸取”时,为避免瓦斯泥在反应器的底部沉淀、结块,可采取的措施为_____ 。
(2)“过程I”中发生反应的离子方程式为____ 。
(3)“过程II”产生的NH3可在流程的_____ 步骤中循环使用。
(4)“酸盐浸提”时,为使铋充分浸出,可将适量NaCl作助溶剂。单质铋在Fe3+的作用下被溶解。
①含铋物质发生反应的化学方程式为:
i.Bi2O3+3H2SO4+6NaCl=2BiCl3+3Na2SO4+3H2O;
ii.Bi2S3+3Fe2(SO4)3+6NaCl=2BiCl3+3Na2SO4+6FeSO4+3S;
iii.____ 。
②“滤渣2”的主要成分除S外还有____ (填化学式)。
(5)已知“水解”时,生成BiOCl沉淀的适宜pH范围为1.6~2.0;溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
①结合上述信息分析,“水解”时加入适量Zn粉的目的是____ 。
②“水解”后的“系列操作”为____ 。
(6)取mg活性氧化锌样品溶于盐酸,再配成待测液,加入3~4滴指示剂,再加入适量六亚甲基四胺,用amol•L-1的EDTA标准液进行滴定,消耗标准液VmL。样品中氧化锌的质量分数为____ (用代数式表示)。
已知:1.0mLEDTA标准液[c(EDTA)=1mol•L-1]相当于0.08139g氧化锌。

(1)“浸取”时,为避免瓦斯泥在反应器的底部沉淀、结块,可采取的措施为
(2)“过程I”中发生反应的离子方程式为
(3)“过程II”产生的NH3可在流程的
(4)“酸盐浸提”时,为使铋充分浸出,可将适量NaCl作助溶剂。单质铋在Fe3+的作用下被溶解。
①含铋物质发生反应的化学方程式为:
i.Bi2O3+3H2SO4+6NaCl=2BiCl3+3Na2SO4+3H2O;
ii.Bi2S3+3Fe2(SO4)3+6NaCl=2BiCl3+3Na2SO4+6FeSO4+3S;
iii.
②“滤渣2”的主要成分除S外还有
(5)已知“水解”时,生成BiOCl沉淀的适宜pH范围为1.6~2.0;溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 金属离子 | Fe2+ | Fe3+ | Zn2+ |
| 开始沉淀时的pH | 7.0 | 1.9 | 6.2 |
| 完全沉淀时的pH | 9.0 | 3.2 | 8.0 |
②“水解”后的“系列操作”为
(6)取mg活性氧化锌样品溶于盐酸,再配成待测液,加入3~4滴指示剂,再加入适量六亚甲基四胺,用amol•L-1的EDTA标准液进行滴定,消耗标准液VmL。样品中氧化锌的质量分数为
已知:1.0mLEDTA标准液[c(EDTA)=1mol•L-1]相当于0.08139g氧化锌。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】钼酸钠晶体( )可用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(主要成分为
)可用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(主要成分为 ,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。

请回答下列问题:
(1) 中Mo的化合价为
中Mo的化合价为___________
(2)“焙烧”时,有 生成,反应的化学方程式为
生成,反应的化学方程式为___________ ,氧化产物是___________
(3)“碱浸”生成 和另外一种物质,
和另外一种物质, 的电子式为
的电子式为___________ ,另外一种生成物的化学式为___________
(4)若“除重金属离子”时加入的沉淀剂为 ,则废渣的成分为
,则废渣的成分为___________  填化学式
填化学式
(5)测得“除重金属离子”中部分离子的浓度: “结晶”前应先除去
“结晶”前应先除去 ,方法是加入
,方法是加入 固体。假设加入
固体。假设加入 固体后溶液体积不变,当
固体后溶液体积不变,当 开始沉淀时,去除的
开始沉淀时,去除的 的质量分数为
的质量分数为___________  已知
已知
 )可用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(主要成分为
)可用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(主要成分为 ,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
请回答下列问题:
(1)
 中Mo的化合价为
中Mo的化合价为(2)“焙烧”时,有
 生成,反应的化学方程式为
生成,反应的化学方程式为(3)“碱浸”生成
 和另外一种物质,
和另外一种物质, 的电子式为
的电子式为(4)若“除重金属离子”时加入的沉淀剂为
 ,则废渣的成分为
,则废渣的成分为 填化学式
填化学式
(5)测得“除重金属离子”中部分离子的浓度:
 “结晶”前应先除去
“结晶”前应先除去 ,方法是加入
,方法是加入 固体。假设加入
固体。假设加入 固体后溶液体积不变,当
固体后溶液体积不变,当 开始沉淀时,去除的
开始沉淀时,去除的 的质量分数为
的质量分数为 已知
已知
您最近一年使用:0次
【推荐1】工厂烟气(主要污染物 、NO)直接排放会造成空气污染,需处理后才能排放。
、NO)直接排放会造成空气污染,需处理后才能排放。
(1)①用天然碱生产小苏打的母液(主要溶质为碳酸钠)吸收烟气中 的相关反应的热化学方程式如下:
的相关反应的热化学方程式如下:
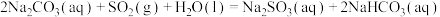
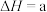 kJ·mol
kJ·mol
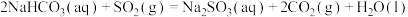
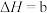 kJ·mol
kJ·mol
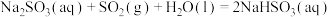
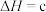 kJ·mol
kJ·mol
反应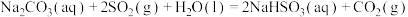 的
的
______ kJ·mol
②已知拆开1 mol 键,1 mol
键,1 mol  键,1 mol
键,1 mol  键分别需要的能量是436 kJ、391 kJ、946 kJ,则
键分别需要的能量是436 kJ、391 kJ、946 kJ,则 与
与 反应生成
反应生成 的热化学方程式为
的热化学方程式为______
(2) 氧化。
氧化。
40℃时向一定量 溶液中按一定流速持续通入工厂烟气,溶液的pH与ORP值(氧化还原电位)随时间变化如图所示。
溶液中按一定流速持续通入工厂烟气,溶液的pH与ORP值(氧化还原电位)随时间变化如图所示。
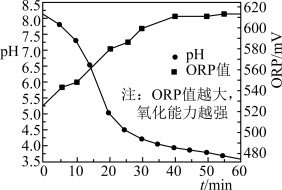
①写出溶液中NO与 反应生成
反应生成 和
和 的离子方程式:
的离子方程式:______ 。
②烟气中含有少量 ,NO的脱除率比不含
,NO的脱除率比不含 的烟气高,可能原因是
的烟气高,可能原因是______ 。
(3) 光催化。主要是利用
光催化。主要是利用 光催化剂在紫外线作用下产生的高活性自由基(
光催化剂在紫外线作用下产生的高活性自由基(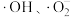 )和
)和 (
( 代表空位,空位有很强的得电子能力),将烟气中的
代表空位,空位有很强的得电子能力),将烟气中的 、NO等氧化除去。
、NO等氧化除去。 光催化剂粒子表面产生·OH的机理如图所示(图中部分产物略去)。已知
光催化剂粒子表面产生·OH的机理如图所示(图中部分产物略去)。已知 中电子跃迁的能量
中电子跃迁的能量 eV。
eV。
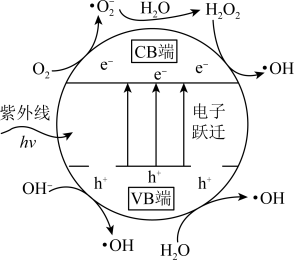
 光催化剂在紫外线作用下产生·OH的过程可描述为
光催化剂在紫外线作用下产生·OH的过程可描述为______ 。
 、NO)直接排放会造成空气污染,需处理后才能排放。
、NO)直接排放会造成空气污染,需处理后才能排放。(1)①用天然碱生产小苏打的母液(主要溶质为碳酸钠)吸收烟气中
 的相关反应的热化学方程式如下:
的相关反应的热化学方程式如下: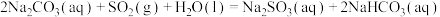
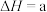 kJ·mol
kJ·mol
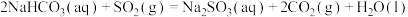
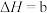 kJ·mol
kJ·mol
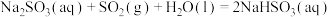
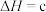 kJ·mol
kJ·mol
反应
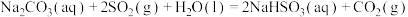 的
的

②已知拆开1 mol
 键,1 mol
键,1 mol  键,1 mol
键,1 mol  键分别需要的能量是436 kJ、391 kJ、946 kJ,则
键分别需要的能量是436 kJ、391 kJ、946 kJ,则 与
与 反应生成
反应生成 的热化学方程式为
的热化学方程式为(2)
 氧化。
氧化。40℃时向一定量
 溶液中按一定流速持续通入工厂烟气,溶液的pH与ORP值(氧化还原电位)随时间变化如图所示。
溶液中按一定流速持续通入工厂烟气,溶液的pH与ORP值(氧化还原电位)随时间变化如图所示。
①写出溶液中NO与
 反应生成
反应生成 和
和 的离子方程式:
的离子方程式:②烟气中含有少量
 ,NO的脱除率比不含
,NO的脱除率比不含 的烟气高,可能原因是
的烟气高,可能原因是(3)
 光催化。主要是利用
光催化。主要是利用 光催化剂在紫外线作用下产生的高活性自由基(
光催化剂在紫外线作用下产生的高活性自由基(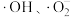 )和
)和 (
( 代表空位,空位有很强的得电子能力),将烟气中的
代表空位,空位有很强的得电子能力),将烟气中的 、NO等氧化除去。
、NO等氧化除去。 光催化剂粒子表面产生·OH的机理如图所示(图中部分产物略去)。已知
光催化剂粒子表面产生·OH的机理如图所示(图中部分产物略去)。已知 中电子跃迁的能量
中电子跃迁的能量 eV。
eV。
 光催化剂在紫外线作用下产生·OH的过程可描述为
光催化剂在紫外线作用下产生·OH的过程可描述为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】二甲醚(CH3OCH3)是清洁的燃料和重要的化工原料,具有广泛的应用前景。回答下列问题:
(1)工业上用甲醇制备二甲醚(2CH3OH→CH3OCH3+H2O)分为液相脱水法(已被逐步淘汰)和气相脱水法。液相脱水法是甲醇在浓硫酸作用下加热脱水,该法在实际生产中的主要缺点是_______ 。
(2)我国某科研团队通过计算机模拟技术提出在12-磷钨酸(固体强酸)催化作用下甲醇气相脱水合成二甲醚的反应机理:
CH3OH+H+→IM1(中间体1)→TS1(过渡态1)→IM3(中间体3)→CH +H2O,
+H2O,
CH +CH3OH→+IM2(中间体2)→TS2(过渡态2)→IM4(中间体4)→CH3OCH3+H+
+CH3OH→+IM2(中间体2)→TS2(过渡态2)→IM4(中间体4)→CH3OCH3+H+
反应过程和相对能量E(kJ•mol-1)如图所示。

①该反应机理中的最大能垒(活化能)E正=_______ kJ·mol-1;2CH3OH(g) CH3OCH3(g)+H2O(g)ΔH=
CH3OCH3(g)+H2O(g)ΔH=_______ 。
②IM1为CH2=OH++H2,CH3OH+H+→IM1是一个无垒(活化能为0)过程,可推测该过程_______ (填标号)。
A.从断键开始B.从成键开始C.断键时吸收的能量更多D.成键时释放的能量更多
类似地,IM2为CH2=OH++_______ 。
(3)一定条件下,密闭容器中充入甲醇发生气相脱水反应:2CH3OH(g) CH3OCH3(g)+H2O(g),甲醇的平衡转化率α与平衡常数的关系式为K=
CH3OCH3(g)+H2O(g),甲醇的平衡转化率α与平衡常数的关系式为K=_______ (填含α的代数式);若要进一步提高甲醇的平衡转化率但不改变平衡常数值,可以采取的措施有_______ (答出一条)。
(1)工业上用甲醇制备二甲醚(2CH3OH→CH3OCH3+H2O)分为液相脱水法(已被逐步淘汰)和气相脱水法。液相脱水法是甲醇在浓硫酸作用下加热脱水,该法在实际生产中的主要缺点是
(2)我国某科研团队通过计算机模拟技术提出在12-磷钨酸(固体强酸)催化作用下甲醇气相脱水合成二甲醚的反应机理:
CH3OH+H+→IM1(中间体1)→TS1(过渡态1)→IM3(中间体3)→CH
 +H2O,
+H2O,CH
 +CH3OH→+IM2(中间体2)→TS2(过渡态2)→IM4(中间体4)→CH3OCH3+H+
+CH3OH→+IM2(中间体2)→TS2(过渡态2)→IM4(中间体4)→CH3OCH3+H+反应过程和相对能量E(kJ•mol-1)如图所示。

①该反应机理中的最大能垒(活化能)E正=
 CH3OCH3(g)+H2O(g)ΔH=
CH3OCH3(g)+H2O(g)ΔH=②IM1为CH2=OH++H2,CH3OH+H+→IM1是一个无垒(活化能为0)过程,可推测该过程
A.从断键开始B.从成键开始C.断键时吸收的能量更多D.成键时释放的能量更多
类似地,IM2为CH2=OH++
(3)一定条件下,密闭容器中充入甲醇发生气相脱水反应:2CH3OH(g)
 CH3OCH3(g)+H2O(g),甲醇的平衡转化率α与平衡常数的关系式为K=
CH3OCH3(g)+H2O(g),甲醇的平衡转化率α与平衡常数的关系式为K=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】页岩气中含有CH4、CO2、H2S等气体,是蕴藏于页岩层可供开采的天然气资源。页岩气的有效利用需要处理其中所含的CO2和H2S。
Ⅰ.CO2的处理:
(1)CO2和CH4重整可制合成气(主要成分为CO、H2)。
已知下列热化学反应方程式:C(s)+2H2(g)=CH4(g);ΔH=-74.5kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g);ΔH=-40.0kJ·mol-1
C(s)+H2O(g)=CO(g)+H2(g);ΔH=+132.0kJ·mol-1
反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的ΔH=___________ kJ·mol-1。
(2)Ni催化CO2加H2形成CH4,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中CH4的百分含量及CO2的转化率随温度的变化如图2所示。
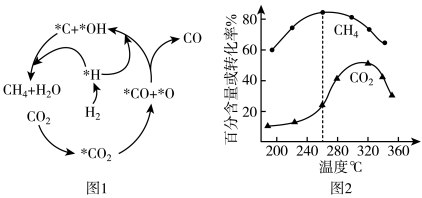
①260℃时生成主要产物所发生反应的化学方程式为___________ 。
②温度高于320℃,CO2的转化率下降的原因是___________ 。
Ⅱ.H2S的处理:Fe2O3可用作脱除H2S气体的脱硫剂。Fe2O3脱硫和Fe2O3再生的可能反应机理如图3所示。

(3)Fe2O3脱硫剂的脱硫和再生过程可以描述为___________ 。
(4)再生时需控制通入O2的浓度和温度。400℃条件下,氧气浓度较大时,会出现脱硫剂再生时质量增大,且所得再生脱硫剂脱硫效果差,原因是___________ 。
(5)脱硫剂再生时可以使用水汽代替O2。700℃条件下,用水汽代替O2再生时,生成Fe3O4、H2S和H2,Fe3O4也可作脱硫剂。
①写出水汽作用条件下脱硫剂再生反应的化学方程式:___________ 。
②用O2再生时会生成污染性气体SO2,用水汽再生时会排放出有毒的H2S,采用O2和水汽混合再生的方法,可以将产生的SO2和H2S转化为S单质。则为不排放出SO2和H2S,理论上O2和水汽的体积比应为___________ 。
Ⅰ.CO2的处理:
(1)CO2和CH4重整可制合成气(主要成分为CO、H2)。
已知下列热化学反应方程式:C(s)+2H2(g)=CH4(g);ΔH=-74.5kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g);ΔH=-40.0kJ·mol-1
C(s)+H2O(g)=CO(g)+H2(g);ΔH=+132.0kJ·mol-1
反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的ΔH=
(2)Ni催化CO2加H2形成CH4,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中CH4的百分含量及CO2的转化率随温度的变化如图2所示。

①260℃时生成主要产物所发生反应的化学方程式为
②温度高于320℃,CO2的转化率下降的原因是
Ⅱ.H2S的处理:Fe2O3可用作脱除H2S气体的脱硫剂。Fe2O3脱硫和Fe2O3再生的可能反应机理如图3所示。

(3)Fe2O3脱硫剂的脱硫和再生过程可以描述为
(4)再生时需控制通入O2的浓度和温度。400℃条件下,氧气浓度较大时,会出现脱硫剂再生时质量增大,且所得再生脱硫剂脱硫效果差,原因是
(5)脱硫剂再生时可以使用水汽代替O2。700℃条件下,用水汽代替O2再生时,生成Fe3O4、H2S和H2,Fe3O4也可作脱硫剂。
①写出水汽作用条件下脱硫剂再生反应的化学方程式:
②用O2再生时会生成污染性气体SO2,用水汽再生时会排放出有毒的H2S,采用O2和水汽混合再生的方法,可以将产生的SO2和H2S转化为S单质。则为不排放出SO2和H2S,理论上O2和水汽的体积比应为
您最近一年使用:0次
【推荐1】一种高硫锰矿的主要成分为 ,主要杂质为
,主要杂质为 ,还含有少量
,还含有少量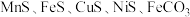 等,其中
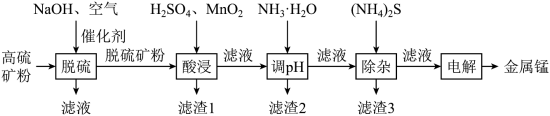
等,其中 含量较大。研究人员设计了如下流程,制得了金属锰。
含量较大。研究人员设计了如下流程,制得了金属锰。
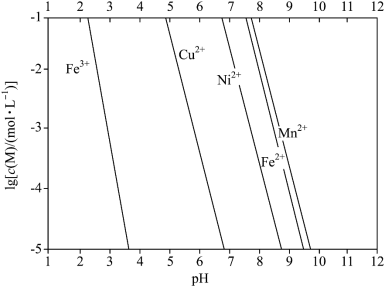
已知:①金属离子的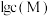 与溶液
与溶液 的关系如下图所示。
的关系如下图所示。
②金属硫化物的溶度积常数如下表。
回答下列问题。
(1)碱性溶液中,在催化剂存在下通空气氧化脱硫,硫化物中的硫元素被氧化为单质。写出硫化亚铁发生反应的化学方程式___________ 。
(2)根据矿物组成,脱硫时能被 部分溶解的物质是
部分溶解的物质是___________ 。若未经脱硫直接酸浸,会产生的污染物是___________ 。
(3)酸浸时,加入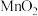 的作用是
的作用是___________ (用离子方程式表示)。
(4)调溶液 到5左右,滤渣2的主要成分是
到5左右,滤渣2的主要成分是___________ ;加入适量的 除去的主要离子是
除去的主要离子是___________ 。
(5)除杂后的 溶液通过电解制得金属锰,惰性阳极发生的电极反应为
溶液通过电解制得金属锰,惰性阳极发生的电极反应为___________ 。
(6)请写出基态Mn原子的价层电子排布式___________ ;锰的化合物 是一种锂电池材料,其晶胞中的氧原子以面心立方堆积(如图),若该晶胞参数为a pm,则晶体密度为
是一种锂电池材料,其晶胞中的氧原子以面心立方堆积(如图),若该晶胞参数为a pm,则晶体密度为___________  。
。

 ,主要杂质为
,主要杂质为 ,还含有少量
,还含有少量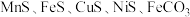 等,其中
等,其中 含量较大。研究人员设计了如下流程,制得了金属锰。
含量较大。研究人员设计了如下流程,制得了金属锰。
已知:①金属离子的
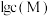 与溶液
与溶液 的关系如下图所示。
的关系如下图所示。
②金属硫化物的溶度积常数如下表。
| 金属硫化物 |  |  |  |  |
 |  | 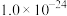 | 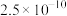 |  |
(1)碱性溶液中,在催化剂存在下通空气氧化脱硫,硫化物中的硫元素被氧化为单质。写出硫化亚铁发生反应的化学方程式
(2)根据矿物组成,脱硫时能被
 部分溶解的物质是
部分溶解的物质是(3)酸浸时,加入
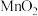 的作用是
的作用是(4)调溶液
 到5左右,滤渣2的主要成分是
到5左右,滤渣2的主要成分是 除去的主要离子是
除去的主要离子是(5)除杂后的
 溶液通过电解制得金属锰,惰性阳极发生的电极反应为
溶液通过电解制得金属锰,惰性阳极发生的电极反应为(6)请写出基态Mn原子的价层电子排布式
 是一种锂电池材料,其晶胞中的氧原子以面心立方堆积(如图),若该晶胞参数为a pm,则晶体密度为
是一种锂电池材料,其晶胞中的氧原子以面心立方堆积(如图),若该晶胞参数为a pm,则晶体密度为 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】CO2是引起“温室效应”的主要物质,CO2的甲烷化可以实现其循环利用。
(1)甲烷化过程中,可能发生如下反应:
I. CO2 (g)+4H2(g) CH4(g)+2H2O(g) △H1
CH4(g)+2H2O(g) △H1
II. CO2 (g)+H2(g) CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
已知反应II中相关的化学键键能数据如下:
由此计算△H2=_________________ 。
(2)在常压、催化剂条件下,将CO2和H2 (体积比为1:4,总物质的量为m mol)置于密闭容器中,发生反应I和II。测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)
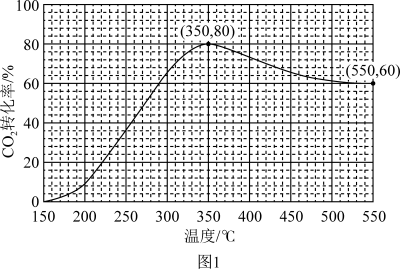
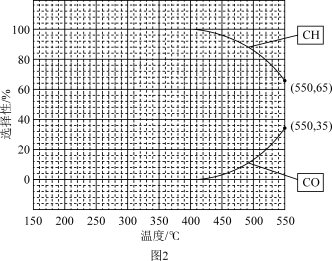
①由图1和图2可知,△H1___ 0(填“>”或“<”),____________ 可影响催化剂的选择性。
②由图1可知CO2的转化率呈现先升高后降低的变化趋势,其原因是_______________ 。
③下列措施能提高CO2平衡转化率的是__________ (填标号)
A.提高原料气中H2所占比例 B.适当增大压强 C.升高温度
D.增大催化剂的比表面积 E.前段加热,后段冷却
④350℃时,反应在t1时刻达到平衡,平衡时容器体积为VL,该温度下反应I的平衡常数为_____ (用m、V表示)。
⑤550℃时,反应在t2时刻达到平衡,此时容器中H2O(g)的物质的量为__ mol(用m表示)
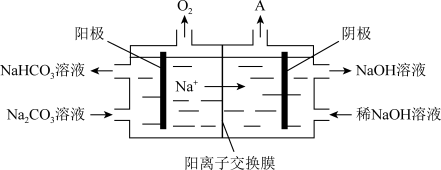
(3)CO2与NaOH溶液反应得到Na2CO3溶液。电解Na2CO3溶液的原理如图所示,阳极的电极反应式为______________________________________ 。
。
(1)甲烷化过程中,可能发生如下反应:
I. CO2 (g)+4H2(g)
 CH4(g)+2H2O(g) △H1
CH4(g)+2H2O(g) △H1II. CO2 (g)+H2(g)
 CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2已知反应II中相关的化学键键能数据如下:
| 化学键 | H—H | C=O | C O O | H—O |
| E/(kJ·mol-1) | 436 | 750 | 1076 | 463 |
由此计算△H2=
(2)在常压、催化剂条件下,将CO2和H2 (体积比为1:4,总物质的量为m mol)置于密闭容器中,发生反应I和II。测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)


①由图1和图2可知,△H1
②由图1可知CO2的转化率呈现先升高后降低的变化趋势,其原因是
③下列措施能提高CO2平衡转化率的是
A.提高原料气中H2所占比例 B.适当增大压强 C.升高温度
D.增大催化剂的比表面积 E.前段加热,后段冷却
④350℃时,反应在t1时刻达到平衡,平衡时容器体积为VL,该温度下反应I的平衡常数为
⑤550℃时,反应在t2时刻达到平衡,此时容器中H2O(g)的物质的量为
(3)CO2与NaOH溶液反应得到Na2CO3溶液。电解Na2CO3溶液的原理如图所示,阳极的电极反应式为
。

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氮和碳的化合物与人类生产、生活密切相关。
(1)已知:N2(g)+O2(g)===2NO(g) ΔH=+180.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1
则反应2H2(g)+2NO(g)===2H2O(g)+N2(g) ΔH=__________ 。
(2)在压强为0.1 MPa条件下,将CO和H2的混合气体在催化剂作用下转化为甲醇的反应为CO(g)+2H2(g) ⇌ CH3OH(g)ΔH<0。
①下列能说明该反应达到平衡状态的是( )
a.混合气体的密度不再变化 b.CO和H2的物质的量之比不再变化
c.v(CO)=v(CH3OH) d.CO在混合气中的质量分数保持不变
②T1℃时,在一个体积为5 L的恒压容器中充入1 mol CO、2 mol H2,经过5 min达到平衡,CO的转化率为0.75,则T1℃时,CO(g)+2H2(g) ⇌ CH3OH(g)的平衡常数K=_______________________ 。
③在T1℃时,在体积为5 L的恒容容器中充入一定量的H2和CO,反应达到平衡时CH3OH的体积分数与n(H2)/n(CO)的关系如图所示。温度不变,当n(H2)/n(CO) =2.5时,达到平衡状态,CH3OH的体积分数可能是图象中的___________ 点。
(3)用催化转化装置净化汽车尾气,装置中涉及的反应之一为:2NO(g)+2CO(g) ⇌ N2(g)+2CO2(g)。
①探究上述反应中NO的平衡转化率与压强、温度的关系,得到如图所示的曲线。催化装置比较适合的温度和压强是___________ 。
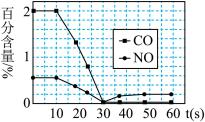
②测试某型号汽车在冷启动(冷启动指发动机水温低的情况下启动)时催化装置内CO和NO百分含量随时间变化曲线如图所示。则前10 s内,CO和NO百分含量没明显变化的原因是____________ 。
(4)右图所示的装置能吸收和转化NO2和SO2。
①阳极区的电极反应为__________________ 。
②阴极排出的溶液中含S2O42-离子,能将NO2气体转化为无污染气体,同时生成的SO32-可在阴极区再生。写出该反应的离子方程式:___ 。
(1)已知:N2(g)+O2(g)===2NO(g) ΔH=+180.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1
则反应2H2(g)+2NO(g)===2H2O(g)+N2(g) ΔH=
(2)在压强为0.1 MPa条件下,将CO和H2的混合气体在催化剂作用下转化为甲醇的反应为CO(g)+2H2(g) ⇌ CH3OH(g)ΔH<0。
①下列能说明该反应达到平衡状态的是
a.混合气体的密度不再变化 b.CO和H2的物质的量之比不再变化
c.v(CO)=v(CH3OH) d.CO在混合气中的质量分数保持不变
②T1℃时,在一个体积为5 L的恒压容器中充入1 mol CO、2 mol H2,经过5 min达到平衡,CO的转化率为0.75,则T1℃时,CO(g)+2H2(g) ⇌ CH3OH(g)的平衡常数K=
③在T1℃时,在体积为5 L的恒容容器中充入一定量的H2和CO,反应达到平衡时CH3OH的体积分数与n(H2)/n(CO)的关系如图所示。温度不变,当n(H2)/n(CO) =2.5时,达到平衡状态,CH3OH的体积分数可能是图象中的
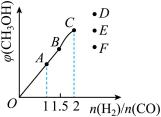
(3)用催化转化装置净化汽车尾气,装置中涉及的反应之一为:2NO(g)+2CO(g) ⇌ N2(g)+2CO2(g)。
①探究上述反应中NO的平衡转化率与压强、温度的关系,得到如图所示的曲线。催化装置比较适合的温度和压强是

②测试某型号汽车在冷启动(冷启动指发动机水温低的情况下启动)时催化装置内CO和NO百分含量随时间变化曲线如图所示。则前10 s内,CO和NO百分含量没明显变化的原因是
(4)右图所示的装置能吸收和转化NO2和SO2。

①阳极区的电极反应为
②阴极排出的溶液中含S2O42-离子,能将NO2气体转化为无污染气体,同时生成的SO32-可在阴极区再生。写出该反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】NaH2PO2有保鲜及抑菌作用,常用于蔬菜水果的保鲜。
已知:P4(白磷)+NaOH→NaH2PO2+PH3↑。PH3有强还原性,是无色、有毒且能自燃的气体。某同学用如图所示装置制取少量NaH2PO2。
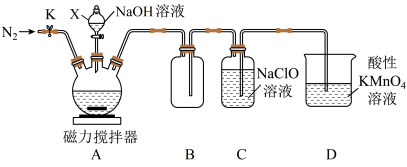
请回答下列问题:
(1)仪器X的名称为______ ,装置B的作用是______ 。
(2)该装置中有一处明显错误是______ 。
(3)实验操作有如下步骤:
①打开K,先通入一段时间的N2;
②在三颈烧瓶中加入丁醇和白磷;
③检查装置气密性;
④打开K,再通入一段时间的N2;
⑤关闭K,打开磁力加热搅拌器加热至50℃~60℃,滴加NaOH溶液;
则正确的操作顺序是______ (填序号)。
(4)先通入一段时间N2的目的是______ 。
(5)PH3在C、D中都被氧化成磷酸,C中反应的化学方程式为______ 。
(6)取产品mg溶于稀硫酸配成250mL溶液,取25.00mL溶液于锥形瓶中,然后用0.02000mol/LKMnO4标准溶液滴定,滴定终点的现象是______ ;达到滴定终点时消耗VmLKMnO4标准溶液(杂质不与KMnO4反应),则产品纯度为______ %(用含m、V的代数式表示)。
已知:P4(白磷)+NaOH→NaH2PO2+PH3↑。PH3有强还原性,是无色、有毒且能自燃的气体。某同学用如图所示装置制取少量NaH2PO2。

请回答下列问题:
(1)仪器X的名称为
(2)该装置中有一处明显错误是
(3)实验操作有如下步骤:
①打开K,先通入一段时间的N2;
②在三颈烧瓶中加入丁醇和白磷;
③检查装置气密性;
④打开K,再通入一段时间的N2;
⑤关闭K,打开磁力加热搅拌器加热至50℃~60℃,滴加NaOH溶液;
则正确的操作顺序是
(4)先通入一段时间N2的目的是
(5)PH3在C、D中都被氧化成磷酸,C中反应的化学方程式为
(6)取产品mg溶于稀硫酸配成250mL溶液,取25.00mL溶液于锥形瓶中,然后用0.02000mol/LKMnO4标准溶液滴定,滴定终点的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室中模拟工业上制取少量无水氯化铁的装置及操作如下。

已知:无水 遇水剧烈反应,加热易升华。请回答下列问题:
遇水剧烈反应,加热易升华。请回答下列问题:
(1)a管的作用是___________ ,装置A中反应的离子方程式为___________ 。
(2)装置C中硬质玻璃管内的实验现象为___________ 。
(3)反应后产物中常存在氯化亚铁杂质,对装置进行改进的方法是___________ 。
(4)下列有关说法正确的是___________。
(5)实验结束后,取硬质玻璃管中的固体适量,用一定浓度的盐酸溶解,再滴入 溶液,没有出现血红色,说明该固体中没有+3价的铁。判断结论是否正确并说明理由:
溶液,没有出现血红色,说明该固体中没有+3价的铁。判断结论是否正确并说明理由:___________ 。

已知:无水
 遇水剧烈反应,加热易升华。请回答下列问题:
遇水剧烈反应,加热易升华。请回答下列问题:(1)a管的作用是
(2)装置C中硬质玻璃管内的实验现象为
(3)反应后产物中常存在氯化亚铁杂质,对装置进行改进的方法是
(4)下列有关说法正确的是___________。
| A.实验开始前,应先在装置内装好所需药品,再检查装置气密性 |
| B.两处酒精灯加热的顺序为先加热A处,再加热C处 |
C.装置D中的水可用冷水或冰水,目的是更好地冷凝收集 |
D.E处虚线框内的装置可选用 或 或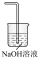 |
(5)实验结束后,取硬质玻璃管中的固体适量,用一定浓度的盐酸溶解,再滴入
 溶液,没有出现血红色,说明该固体中没有+3价的铁。判断结论是否正确并说明理由:
溶液,没有出现血红色,说明该固体中没有+3价的铁。判断结论是否正确并说明理由:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下:

已知:①硫酸浸取中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH值如下:
③Cr2O +H2O=CrO
+H2O=CrO +2H+
+2H+
(1)实验室用12.5mol/L的硫酸配制480ml 2mol/L的硫酸,需量取12.5mol/L的硫酸_______ ml。
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O ,写出此反应的离子方程式
,写出此反应的离子方程式_____ 。
(3)加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时又可以将Cr2O 转化为
转化为____________ (填微粒的化学式)。
(4)钠离子交换树脂的反应原理为:Mn++nNaR MR+nNa+则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有
MR+nNa+则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有 ___________ 。
(5)写出上述流程中用SO2进行还原时发生反应的离子方程式_______ 。
(6)沉淀滴定法是测定粒子浓度的方法之一。为了测定某废水中SCN-浓度,可用标准AgNO3溶液滴定待测液,已知:
滴定时下列试剂可选为滴定指示剂的是 ________ (填字母代号),滴定终点的现象是_____ 。
A NaCl B K2CrO4 C KI D NaCN

已知:①硫酸浸取中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH值如下:
| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 沉淀完全时的pH值 | 3.7 | 11.1 | 5.4(>8溶解) | 9(>溶解) |
 +H2O=CrO
+H2O=CrO +2H+
+2H+(1)实验室用12.5mol/L的硫酸配制480ml 2mol/L的硫酸,需量取12.5mol/L的硫酸
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O
 ,写出此反应的离子方程式
,写出此反应的离子方程式(3)加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时又可以将Cr2O
 转化为
转化为(4)钠离子交换树脂的反应原理为:Mn++nNaR
 MR+nNa+则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有
MR+nNa+则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有 (5)写出上述流程中用SO2进行还原时发生反应的离子方程式
(6)沉淀滴定法是测定粒子浓度的方法之一。为了测定某废水中SCN-浓度,可用标准AgNO3溶液滴定待测液,已知:
| 银盐性质 | AgCl | AgI | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 黄 | 白 | 砖红 | 白 |
| KW | 1.8×10﹣10 | 8.3×10﹣17 | 1.2×10﹣16 | 3.5×10﹣11 | 1.0×10﹣12 |
A NaCl B K2CrO4 C KI D NaCN
您最近一年使用:0次



