可以利用氧化锌粗品(含有Fe2O3、FeO、CuO)为原料制备纯净的氧化锌,其化学工艺流程如下:

按要求回答下列问题:
(1)加双氧水主要作用是氧化溶液中的Fe2+,该反应的离子方程式为___________ 。
(2)调节pH主要是使溶液中的Fe3+生成沉淀而被除去,溶液pH对除Fe效率影响如图所示。则除Fe3+时应控制溶液的pH为______ (填序号)。

a.3.5~4.0 b.2.5~3.5
c.1.5~2.5 d.0.5~1.5
(3)固体b为_________ (填化学式),固体c为碱式碳酸锌,煅烧固体c的化学方程式为__________ 。
(4)工业上也可以将氧化锌粗品采用碱溶的方法,将氧化锌转化为Na2[Zn(OH)4]溶液,然后电解该溶液制取锌,以石墨为电极电解时,阴极的电极反应式为___________ ,当生成1mol锌时,阳极上生成气体在标准状况下的体积为__________ L。“纸质电池”的纸片内充入的是水和氧化锌组成的电解液,纸的一边镀锌另一边镀二氧化锰,电池总反应为Zn+2MnO2+H2O=ZnO+2MnO(OH),该电池的负极反应式为_________ 。

按要求回答下列问题:
(1)加双氧水主要作用是氧化溶液中的Fe2+,该反应的离子方程式为
(2)调节pH主要是使溶液中的Fe3+生成沉淀而被除去,溶液pH对除Fe效率影响如图所示。则除Fe3+时应控制溶液的pH为

a.3.5~4.0 b.2.5~3.5
c.1.5~2.5 d.0.5~1.5
(3)固体b为
(4)工业上也可以将氧化锌粗品采用碱溶的方法,将氧化锌转化为Na2[Zn(OH)4]溶液,然后电解该溶液制取锌,以石墨为电极电解时,阴极的电极反应式为
更新时间:2016-12-09 08:03:35
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】Ⅰ.海水晒盐后所得的苦卤中含有较高浓度的MgCl2、KCl以及金属溴化物。以下是苦卤化学分离的过程。

回答下列问题:
(1)若试剂A是一种有色气体单质,则A是_______ (填化学式);
(2)“操作Ⅱ”是_______ ,“操作Ⅲ”是_______ 。(填字母)
a.蒸发 b.蒸馏 c.分液 d.重结晶
(3)试剂B可能是下列物质中的________ 。(填字母)
a.饱和NaCl溶液 b.CCl4 c.NaOH d.乙醇
Ⅱ.一种工业制备SrCl2·6H2O的生产流程如下图所示:

已知:①M(SrCl2·6H2O)=267g·mol-1;②Ksp(SrSO4)=3.3×10-7、Ksp(BaSO4)=1.1×10-10;③经盐酸浸取后,溶液中有Sr2+和Cl-及少量Ba2+。
(1)加入硫酸溶液的目的是______________ ;为了提高原料的利用率,滤液中Sr2+的浓度应不高于_________ mol·L−1 (注:此时滤液中Ba2+浓度为1×10−5 mol·L−1)。
(2)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×10−2 mol的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应的离子),待Cl-完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol·L−1的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_________________________________________ 。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为_______ (保留4位有效数字)。

回答下列问题:
(1)若试剂A是一种有色气体单质,则A是
(2)“操作Ⅱ”是
a.蒸发 b.蒸馏 c.分液 d.重结晶
(3)试剂B可能是下列物质中的
a.饱和NaCl溶液 b.CCl4 c.NaOH d.乙醇
Ⅱ.一种工业制备SrCl2·6H2O的生产流程如下图所示:

已知:①M(SrCl2·6H2O)=267g·mol-1;②Ksp(SrSO4)=3.3×10-7、Ksp(BaSO4)=1.1×10-10;③经盐酸浸取后,溶液中有Sr2+和Cl-及少量Ba2+。
(1)加入硫酸溶液的目的是
(2)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×10−2 mol的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应的离子),待Cl-完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol·L−1的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
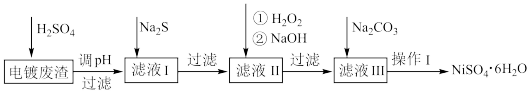
【推荐2】镍(Ni)及其化合物广泛应用于电池、电镀和催化剂等领域,一种以电镀废渣(除含镍外,还含有Cu2+、Zn2+、Fe2+等)为原料获得NiSO4·6H2O的流程如图:
(1)SO 的VSEPR模型为
的VSEPR模型为______ 。
(2)加入Na2S的目的是______ [已知:Ksp(FeS)=6.3×10-18,Ksp(CuS)=1.3×10-36,Ksp(ZnS)=1.3×10-21,Ksp(NiS)=1.1×10-21]
(3)H2O2为______ (填“极性”或“非极性”)分子,可用氯酸钠代替H2O2,写出氯酸钠与“滤液II”反应的离子方程式:______ 。
(4)向“滤液II”中加入NaOH调节pH在一定范围内可生成氢氧化铁沉淀。已知常温下Fe(OH)3的Ksp=1.0×10-39,若要使溶液中c(Fe3+)≤1.0×10-6mol•L-1,则应该控制溶液pH不小于_____ 。
(5)硫酸镍与硫酸铜类似,向硫酸镍中加入足量氨水可以形成[Ni(NH3)6]SO4蓝色溶液。
①在[Ni(NH3)6]SO4中,Ni2+与NH3之间形成的化学键是_____ ,该物质中配位数是_____ 。
②NH3分子的空间结构为_____ 。

(1)SO
 的VSEPR模型为
的VSEPR模型为(2)加入Na2S的目的是
(3)H2O2为
(4)向“滤液II”中加入NaOH调节pH在一定范围内可生成氢氧化铁沉淀。已知常温下Fe(OH)3的Ksp=1.0×10-39,若要使溶液中c(Fe3+)≤1.0×10-6mol•L-1,则应该控制溶液pH不小于
(5)硫酸镍与硫酸铜类似,向硫酸镍中加入足量氨水可以形成[Ni(NH3)6]SO4蓝色溶液。
①在[Ni(NH3)6]SO4中,Ni2+与NH3之间形成的化学键是
②NH3分子的空间结构为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量Al、Fe等)可通过下列实验方法回收钴,并制备金属锂。

已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
②Li2CO3在不同温度下的溶解度如下表:
(1)LiCoO2中,Co元素的化合价为_____ 。
(2)上述流程中为加快化学反应速率而采取的措施是_____ 。
(3)在上述溶解过程中,通入SO2的目的为_____ 。
(4)加NaOH调pH的目的是_____ 。
(5)写出“沉钴”过程中发生反应的离子方程式_____ 。
(6)洗涤所得Li2CO3沉淀要使用_____ (填“热水”或“冷水”),将氯化锂溶液蒸干的过程中还需不断通入HCl气体,其作用是_____ 。
(7)Co(OH)2在空气中加热时,固体残留率随温度的变化如图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为_____ (填化学式)。


已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
②Li2CO3在不同温度下的溶解度如下表:
| 温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
(1)LiCoO2中,Co元素的化合价为
(2)上述流程中为加快化学反应速率而采取的措施是
(3)在上述溶解过程中,通入SO2的目的为
(4)加NaOH调pH的目的是
(5)写出“沉钴”过程中发生反应的离子方程式
(6)洗涤所得Li2CO3沉淀要使用
(7)Co(OH)2在空气中加热时,固体残留率随温度的变化如图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】铁单质及其化合物的应用非常广泛。
(1)氢氧化铁胶体与硫酸铜溶液的本质区别是_______ 。
(2)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热化学方程式_______ 。从能量角度分析,铁触媒的作用是_______ 。

(3)给铁件镀铜时,铁件应作_______ 极;电解精炼铜时,粗铜作_______ 极,其电极反应方程式为_______ 。
(4)电解足量的硫酸铜溶液时,电解池的总反应方程式为_______ ,电解一段时间后,发现阴极析出铜的质量为 ,此时向电解液中加入
,此时向电解液中加入_______  的
的_______ (填物质的化学式)即可将电解液恢复电解前的状态。
(1)氢氧化铁胶体与硫酸铜溶液的本质区别是
(2)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热化学方程式

(3)给铁件镀铜时,铁件应作
(4)电解足量的硫酸铜溶液时,电解池的总反应方程式为
 ,此时向电解液中加入
,此时向电解液中加入 的
的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学兴趣小组进行有关点解食盐水的探究实验,点解装置如图所示。

实验一:电解饱和食盐水
(1)实验约需40mL饱和食盐水,配置450mL饱和食盐水所需的玻璃仪器有:烧杯、_____ 。
A.450mL容量瓶 B.500mL容量瓶 C.电子天平 D.玻璃棒 E.量筒 F.胶头滴管
(2)电解饱和食盐水的化学方程式为______ 。
(3)Y电极附近产物的检验方法:_______ 。
实验二:电解不饱和食盐水及产物分析。相同条件下,电解1mol/L NaCl溶液并收集两极产生的气体。在X处收集到V1 mL气体。同时,在Y处收集到V2 mL气体,停止电解。结果发现V2<V1,且与电解饱和食盐水相比,Y处收集到的气体颜色明显较浅。经讨论分析,导致上述现象的原因有:
i.有部分Cl2溶于NaCl溶液中;
ii.有O2生成。
(4)设计实验证明有部分Cl2溶于NaCl溶液中,实验方案为________ 。
(5)证明有O2生成并测定O2的体积。按如图所示装置进行实验,通过注射器缓缓地将在Y处收集到V2 mL气体全部推入装置A(盛有足量试剂NaOH溶液)中,最终,量气管中收集到V3 mL气体(设V1、V2、V3均在相同条件下测得)。

①装置A的作用是________ 。
②本实验中,观察到________ 的现象,说明石墨电极上有O2生成。
③实验中是否需要预先除尽装置中的空气?______ (填“是”或“否”)。
④实验二中,在石墨电极上产生的Cl2的总体积为______ mL(用代数式表示)。

实验一:电解饱和食盐水
(1)实验约需40mL饱和食盐水,配置450mL饱和食盐水所需的玻璃仪器有:烧杯、
A.450mL容量瓶 B.500mL容量瓶 C.电子天平 D.玻璃棒 E.量筒 F.胶头滴管
(2)电解饱和食盐水的化学方程式为
(3)Y电极附近产物的检验方法:
实验二:电解不饱和食盐水及产物分析。相同条件下,电解1mol/L NaCl溶液并收集两极产生的气体。在X处收集到V1 mL气体。同时,在Y处收集到V2 mL气体,停止电解。结果发现V2<V1,且与电解饱和食盐水相比,Y处收集到的气体颜色明显较浅。经讨论分析,导致上述现象的原因有:
i.有部分Cl2溶于NaCl溶液中;
ii.有O2生成。
(4)设计实验证明有部分Cl2溶于NaCl溶液中,实验方案为
(5)证明有O2生成并测定O2的体积。按如图所示装置进行实验,通过注射器缓缓地将在Y处收集到V2 mL气体全部推入装置A(盛有足量试剂NaOH溶液)中,最终,量气管中收集到V3 mL气体(设V1、V2、V3均在相同条件下测得)。

①装置A的作用是
②本实验中,观察到
③实验中是否需要预先除尽装置中的空气?
④实验二中,在石墨电极上产生的Cl2的总体积为
您最近一年使用:0次
【推荐3】当今世界多国相继规划了碳达烽、碳中和的时间节点,因此研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。
(1)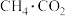 催化重整不仅对温室气体的减排有重要意义,还可以得到合成气(CO和H2)。
催化重整不仅对温室气体的减排有重要意义,还可以得到合成气(CO和H2)。
已知:①
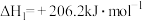
②
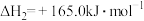
写出该催化重整反应的热化学方程式:___________ 。
(2)在恒容密闭容器中通入等物质的量的CO2和H2并发生反应 ,300℃下,CO2物质的量浓度c(CO2)随时间t变化的曲线如图所示:
,300℃下,CO2物质的量浓度c(CO2)随时间t变化的曲线如图所示:
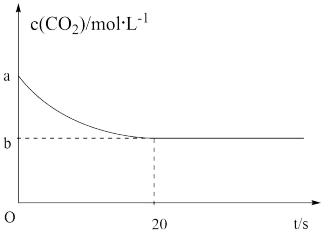
此条件下反应前20的平均速率v(H2)=___________ (用含a、b的代数式表示)。当混合气体的某项物理量保持不变时,可认为反应达到了平衡状态,该物理量可能是___________ (填序号)。
a.压强 b.密度 c.平均摩尔质量 d.颜色
(3)电催化合成甲酸因活化容易且能在常温常压下反应,因此具有广阔前景。某CO2电催化反应器示意图如图所示:

①阴极的电极反应式是___________ 。
②该电解反应得到的副产品除H2外,还可能有___________ (任写一个)。
(1)
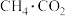 催化重整不仅对温室气体的减排有重要意义,还可以得到合成气(CO和H2)。
催化重整不仅对温室气体的减排有重要意义,还可以得到合成气(CO和H2)。已知:①

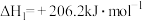
②

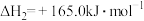
写出该催化重整反应的热化学方程式:
(2)在恒容密闭容器中通入等物质的量的CO2和H2并发生反应
 ,300℃下,CO2物质的量浓度c(CO2)随时间t变化的曲线如图所示:
,300℃下,CO2物质的量浓度c(CO2)随时间t变化的曲线如图所示:
此条件下反应前20的平均速率v(H2)=
a.压强 b.密度 c.平均摩尔质量 d.颜色
(3)电催化合成甲酸因活化容易且能在常温常压下反应,因此具有广阔前景。某CO2电催化反应器示意图如图所示:

①阴极的电极反应式是
②该电解反应得到的副产品除H2外,还可能有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铋及其化合物在工业生产中用途广泛,如氯氧化铋( )常用作电子设备、塑料助剂等。一种用铋精矿(
)常用作电子设备、塑料助剂等。一种用铋精矿( ,含有
,含有 、
、 、
、 及不溶性杂质)制备
及不溶性杂质)制备 的一种方法,其流程如图:
的一种方法,其流程如图:

已知:
① 开始沉淀(
开始沉淀( )的pH为1.9,沉淀完全(
)的pH为1.9,沉淀完全( )时的pH为3.2
)时的pH为3.2
② 开始沉淀(
开始沉淀( )的pH为7.0,沉淀完全(
)的pH为7.0,沉淀完全( )时的pH为9.0
)时的pH为9.0
③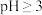 时,
时,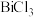 极易水解为
极易水解为 沉淀
沉淀
请回答以下问题:
(1)“加压浸取"过程中, 转化为
转化为 ,
, 转化为
转化为 ,而
,而 溶解进入浸出液且硫元素转化为
溶解进入浸出液且硫元素转化为 ,请写出
,请写出 在此过程中发生反应的离子方程式:
在此过程中发生反应的离子方程式:___________ 。
(2)“操作I”为___________ 、___________ 、过滤、洗涤、干燥。
(3)分析盐酸羟胺(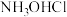 )在流程中的作用:
)在流程中的作用:___________ 。
(4)滤液3中 的浓度为
的浓度为 ,“调pH”步骤中pH的范围为
,“调pH”步骤中pH的范围为___________ 。
(5)写出流程中生成 的离子方程式:
的离子方程式:___________ 。
(6)铋化锂晶胞结构如图所示:

①晶胞可以看作是由Bi原子构成的面心立方晶格,Li原子填充在其中的四面体和八面体空隙处,图中铋原子坐标参数:A为(0,0,0)、B为___________ 。
②若晶胞的参数为apm,阿伏加德罗常数为 ,晶体的密度为
,晶体的密度为_______ 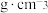 (填计算表达式)。
(填计算表达式)。
 )常用作电子设备、塑料助剂等。一种用铋精矿(
)常用作电子设备、塑料助剂等。一种用铋精矿( ,含有
,含有 、
、 、
、 及不溶性杂质)制备
及不溶性杂质)制备 的一种方法,其流程如图:
的一种方法,其流程如图:
已知:
①
 开始沉淀(
开始沉淀( )的pH为1.9,沉淀完全(
)的pH为1.9,沉淀完全( )时的pH为3.2
)时的pH为3.2②
 开始沉淀(
开始沉淀( )的pH为7.0,沉淀完全(
)的pH为7.0,沉淀完全( )时的pH为9.0
)时的pH为9.0③
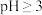 时,
时,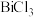 极易水解为
极易水解为 沉淀
沉淀请回答以下问题:
(1)“加压浸取"过程中,
 转化为
转化为 ,
, 转化为
转化为 ,而
,而 溶解进入浸出液且硫元素转化为
溶解进入浸出液且硫元素转化为 ,请写出
,请写出 在此过程中发生反应的离子方程式:
在此过程中发生反应的离子方程式:(2)“操作I”为
(3)分析盐酸羟胺(
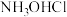 )在流程中的作用:
)在流程中的作用:(4)滤液3中
 的浓度为
的浓度为 ,“调pH”步骤中pH的范围为
,“调pH”步骤中pH的范围为(5)写出流程中生成
 的离子方程式:
的离子方程式:(6)铋化锂晶胞结构如图所示:

①晶胞可以看作是由Bi原子构成的面心立方晶格,Li原子填充在其中的四面体和八面体空隙处,图中铋原子坐标参数:A为(0,0,0)、B为
②若晶胞的参数为apm,阿伏加德罗常数为
 ,晶体的密度为
,晶体的密度为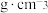 (填计算表达式)。
(填计算表达式)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】金属及其化合物在生产生活中占有极其重要的地位,请结合金属及其化合物的相关知识回答下列问题:
(1)某溶液有Mg2+、Fe2+、Al3+、Cu2+等,加入足量的Na2O2后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______。
(2)高铁酸钠(Na2FeO4)是一种新型水处理剂。某兴趣小组欲利用废金属屑(主要成分为Fe和Cu,含有少量Fe2O3)制取高铁酸钠并回收金属Cu,其工艺流程:_______ (填化学式,下同),滤渣II的主要成分为_______ 。
②检验滤液I中是否存在Fe3+的试剂是_______ 。
③制备 的反应原理是:
的反应原理是: 。当转移电子总数约为
。当转移电子总数约为 时,则生成Na2FeO4的物质的量为
时,则生成Na2FeO4的物质的量为_______ mol。
④FeSO4可以把酸性废水中Cr2O 还原为Cr3+,计算:还原0.1mol Cr2O
还原为Cr3+,计算:还原0.1mol Cr2O 需要FeSO4
需要FeSO4_______ mol
(3)纳米铁粉可用于处理废水中的NO 。酸性条件下,纳米铁粉与废水中NO
。酸性条件下,纳米铁粉与废水中NO 反应生成Fe3+与
反应生成Fe3+与 ,其反应的离子方程式是
,其反应的离子方程式是_______ 。
(1)某溶液有Mg2+、Fe2+、Al3+、Cu2+等,加入足量的Na2O2后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______。
| A.Mg2+ | B.Fe2+ | C.A13+ | D.Cu2+ |

②检验滤液I中是否存在Fe3+的试剂是
③制备
 的反应原理是:
的反应原理是: 。当转移电子总数约为
。当转移电子总数约为 时,则生成Na2FeO4的物质的量为
时,则生成Na2FeO4的物质的量为④FeSO4可以把酸性废水中Cr2O
 还原为Cr3+,计算:还原0.1mol Cr2O
还原为Cr3+,计算:还原0.1mol Cr2O 需要FeSO4
需要FeSO4(3)纳米铁粉可用于处理废水中的NO
 。酸性条件下,纳米铁粉与废水中NO
。酸性条件下,纳米铁粉与废水中NO 反应生成Fe3+与
反应生成Fe3+与 ,其反应的离子方程式是
,其反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某胶囊是一种常用的治疗胃酸过多的药品,其主要成分为一种两性氢氧化物。某同学欲对该胶囊内的白色固体的主要成分进行检验,设计了如下实验步骤:

(1) 操作Ⅱ所需要的玻璃仪器有_________ 、_________ 、________ 。
(2) 写出下列反应的方程式:
③的化学方程式:____________________________________________________ ,
④的离子方程式:______________________________________________________ 。
(3) 根据实验推测,该胃药的主要成分为_________________________________________ 。
(4) 该同学通过阅读课外读物了解到:常用胃药中除了上述实验已检出的物质外,还有NaHCO3,请你帮助该同学完成对滤液C中主要成分的探究实验(简要描述操作步骤):_____________________ 。

(1) 操作Ⅱ所需要的玻璃仪器有
(2) 写出下列反应的方程式:
③的化学方程式:
④的离子方程式:
(3) 根据实验推测,该胃药的主要成分为
(4) 该同学通过阅读课外读物了解到:常用胃药中除了上述实验已检出的物质外,还有NaHCO3,请你帮助该同学完成对滤液C中主要成分的探究实验(简要描述操作步骤):
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】工业上利用废镍催化剂(主要成分为Ni,还含有一定量的Zn、Fe、SiO2、CaO等)制备草酸镍晶体的流程如下:

(1)请写出一种能提高“酸浸”速率的措施:___________ ;滤渣I的成分是___________ (填化学式)。
(2)除铁时,控制不同的条件可以得到不同的滤渣II。已知滤渣II的成分与温度、pH关系如图所示:

①写出除铁步骤中次氯酸钠发生反应的离子方程式___________ 。
②若控制温度25℃、pH=4时除去铁,此时溶液中c(Fe3+)=___________ 。(已知25℃时,Fe(OH)3的Ksp[Fe(OH)3]=2.64×10-39)
(3)加入有机萃取剂除掉的金属阳离子主要是___________ 。
(4)某化学镀镍试剂的化学式为(NH4)xNi(SO4)y(Ni为+2价,,x、y均为正整数)。为测定该镀镍试剂的组成,进行如下实验:
I、称量28.7g镀镍试剂,配制100mL溶液A;
Ⅱ、准确量取10.00mL溶液A,用0.40mol·L-1的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),消耗EDTA标准溶液25.00mL;
Ⅲ、另取10.00mL溶液A,加入足量的BaCl2溶液,得到白色沉淀4.66g。
①配制100mL镀镍试剂时,需要的仪器除药匙、托盘天平、玻璃棒、烧杯、量筒、胶头滴管外,还需要___________ 。
②该镀镍试剂的化学式为___________ 。

(1)请写出一种能提高“酸浸”速率的措施:
(2)除铁时,控制不同的条件可以得到不同的滤渣II。已知滤渣II的成分与温度、pH关系如图所示:

①写出除铁步骤中次氯酸钠发生反应的离子方程式
②若控制温度25℃、pH=4时除去铁,此时溶液中c(Fe3+)=
(3)加入有机萃取剂除掉的金属阳离子主要是
(4)某化学镀镍试剂的化学式为(NH4)xNi(SO4)y(Ni为+2价,,x、y均为正整数)。为测定该镀镍试剂的组成,进行如下实验:
I、称量28.7g镀镍试剂,配制100mL溶液A;
Ⅱ、准确量取10.00mL溶液A,用0.40mol·L-1的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),消耗EDTA标准溶液25.00mL;
Ⅲ、另取10.00mL溶液A,加入足量的BaCl2溶液,得到白色沉淀4.66g。
①配制100mL镀镍试剂时,需要的仪器除药匙、托盘天平、玻璃棒、烧杯、量筒、胶头滴管外,还需要
②该镀镍试剂的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】镍及其化合物在工业上有广泛的应用。工业上用红土镍矿(主要成分为NiO,含CoO、FeO、 、
、 、MgO、CaO和
、MgO、CaO和 )制备
)制备 的工艺流程如图所示。
的工艺流程如图所示。

已知:①25℃时,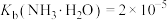 ,
,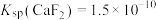 ,
,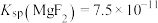 ,
,


②萃取的反应原理为
回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有_______ (答出一条即可),滤渣1的主要成分是_______ 。
(2)“氧化”过程中发生反应的离子方程式为_______ 。
(3)为探究 在氨水中能否溶解,计算反应
在氨水中能否溶解,计算反应 的平衡常数
的平衡常数
_______ ,“调pH”过程中氨水不能过量的主要原因是_______ 。
(4)若“除镁、钙”前 mol⋅L⁻¹,当
mol⋅L⁻¹,当 mol⋅L⁻¹时,除钙率为
mol⋅L⁻¹时,除钙率为_______ (忽略沉淀前后溶液的体积变化)。
(5)向“水相”中加入 可形成
可形成 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为_______ ,试剂X为_______ (填名称)。
 、
、 、MgO、CaO和
、MgO、CaO和 )制备
)制备 的工艺流程如图所示。
的工艺流程如图所示。
已知:①25℃时,
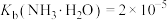 ,
,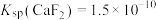 ,
,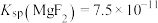 ,
,

②萃取的反应原理为

回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有
(2)“氧化”过程中发生反应的离子方程式为
(3)为探究
 在氨水中能否溶解,计算反应
在氨水中能否溶解,计算反应 的平衡常数
的平衡常数
(4)若“除镁、钙”前
 mol⋅L⁻¹,当
mol⋅L⁻¹,当 mol⋅L⁻¹时,除钙率为
mol⋅L⁻¹时,除钙率为(5)向“水相”中加入
 可形成
可形成 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】亚氯酸钠(NaClO2)与二氧化氯(ClO2)都具有强氧化性,可以用作新冠肺炎防疫的消毒剂。两者作漂白剂时,不伤害织物;作饮用水消毒剂时,不残留异味。某研究性学习小组利用如图装置由二氧化氯制备NaClO2·3H2O,并探究其性质。

查阅资料:
①ClO2易与碱溶液反应生成等物质的量的两种盐,其中一种为氯酸盐。
②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
(1)制备与分离:
①仪器a的名称是_______ 。
②装置A中发生的反应的化学方程式为_______ 。
③装置B的作用是_______ 。若要从装置C 反应后的溶液中获得无水NaClO2晶体的操作步骤如下,请完成下列操作中步骤Ⅱ的内容。
反应后的溶液中获得无水NaClO2晶体的操作步骤如下,请完成下列操作中步骤Ⅱ的内容。
Ⅰ.减压,55℃蒸发结晶;
Ⅱ._______ ;
Ⅲ.用38~60℃热水洗涤;
Ⅳ.在38~60℃间进行干燥,得到成品。
(2)装置D用来处理尾气,有关反应的离子方程式是_______ 。实验结束后,继续通入一段时间N2的目的是_______ 。
(3)测定与计算:利用题中原理制备出NaClO2·3H2O晶体的样品,可以用“间接碘量法”测定样品( 杂质与I-不发生反应)
杂质与I-不发生反应) 的纯度,过程如下:取样品1.4450g配制成250mL溶液,从中取出25.00mL,加入足量KI固体和适量稀H2SO4,充分反应后再加入0.1mol/LNa2S2O3标准溶液,Na2S2O3标准溶液与上述反应生成的I2刚好完全反应时消耗的体积为34.6mL。已知:ClO
的纯度,过程如下:取样品1.4450g配制成250mL溶液,从中取出25.00mL,加入足量KI固体和适量稀H2SO4,充分反应后再加入0.1mol/LNa2S2O3标准溶液,Na2S2O3标准溶液与上述反应生成的I2刚好完全反应时消耗的体积为34.6mL。已知:ClO +4I-+4H+=2H2O+2I2+Cl-,I2+2S2O
+4I-+4H+=2H2O+2I2+Cl-,I2+2S2O =S4O
=S4O +2I-。样品中NaClO2·3H2O的纯度为
+2I-。样品中NaClO2·3H2O的纯度为_______ %。

查阅资料:
①ClO2易与碱溶液反应生成等物质的量的两种盐,其中一种为氯酸盐。
②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
(1)制备与分离:
①仪器a的名称是
②装置A中发生的反应的化学方程式为
③装置B的作用是
 反应后的溶液中获得无水NaClO2晶体的操作步骤如下,请完成下列操作中步骤Ⅱ的内容。
反应后的溶液中获得无水NaClO2晶体的操作步骤如下,请完成下列操作中步骤Ⅱ的内容。Ⅰ.减压,55℃蒸发结晶;
Ⅱ.
Ⅲ.用38~60℃热水洗涤;
Ⅳ.在38~60℃间进行干燥,得到成品。
(2)装置D用来处理尾气,有关反应的离子方程式是
(3)测定与计算:利用题中原理制备出NaClO2·3H2O晶体的样品,可以用“间接碘量法”测定样品(
 杂质与I-不发生反应)
杂质与I-不发生反应) 的纯度,过程如下:取样品1.4450g配制成250mL溶液,从中取出25.00mL,加入足量KI固体和适量稀H2SO4,充分反应后再加入0.1mol/LNa2S2O3标准溶液,Na2S2O3标准溶液与上述反应生成的I2刚好完全反应时消耗的体积为34.6mL。已知:ClO
的纯度,过程如下:取样品1.4450g配制成250mL溶液,从中取出25.00mL,加入足量KI固体和适量稀H2SO4,充分反应后再加入0.1mol/LNa2S2O3标准溶液,Na2S2O3标准溶液与上述反应生成的I2刚好完全反应时消耗的体积为34.6mL。已知:ClO +4I-+4H+=2H2O+2I2+Cl-,I2+2S2O
+4I-+4H+=2H2O+2I2+Cl-,I2+2S2O =S4O
=S4O +2I-。样品中NaClO2·3H2O的纯度为
+2I-。样品中NaClO2·3H2O的纯度为
您最近一年使用:0次



