二氯化砜(SO2Cl2)是一种无色液体,主要用于有机物和无机物的氯化等。其熔点为-54.1℃.沸点为69.2℃;常温下比较稳定,受热易分解,遇水剧烈反应生成硫酸和盐酸。
(1)制备。实验室可利用SO2和Cl2按下列装置制取少量SO2Cl2(丙中放有樟脑液,起催化作用)。已知SO2(g)+Cl2(g) SO2Cl2(g) △H<0
SO2Cl2(g) △H<0
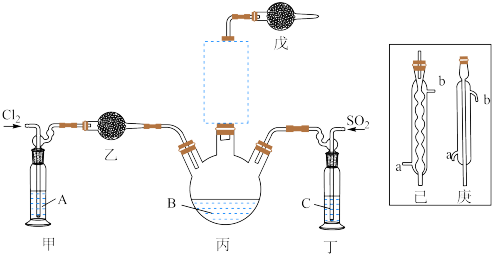
①可以用浓盐酸和酸性高锰酸钾制取氯气,该反应的化学方程式为_________ ;溶液A为____ 。
②上图实框中仪器己的名称为_____ ;反应装置图的虚框中未画出的仪器是____ (填“己”或“庚”)。
③如果将丙装置放入冰水中,会更有利于二氯化砜的生成,其原因是___________ 。
④下列有关说法错误的是________ (填编号)。
a.乙、戊装置相同,在实验中的作用也完全相同
b.甲、丁装置为洗气装置,可用于气体的除杂和干燥
c.组装仪器后首先要进行的操作是检查装置的气密性
d.为提高反应物的利用率,可控制甲、丁装置中产生气泡的速率相等
(2)提纯。将收集到的产物进行减压蒸馏,减压蒸馏的目的是____________________ 。
(3)测定。取1.00g蒸馏后液体,小心地完全溶于水,向所得的溶液中加入足量氯化钡溶液,测得生成沉淀的质量为1.60g,则所得蒸馏成分中二氯化砜的质量百分含量为_________ %。
(4)贮存。二氯化砜应储存于阴凉、干燥、通风良好的库房。但久置后微显黄色,其原因是______ 。
(1)制备。实验室可利用SO2和Cl2按下列装置制取少量SO2Cl2(丙中放有樟脑液,起催化作用)。已知SO2(g)+Cl2(g)
 SO2Cl2(g) △H<0
SO2Cl2(g) △H<0
①可以用浓盐酸和酸性高锰酸钾制取氯气,该反应的化学方程式为
②上图实框中仪器己的名称为
③如果将丙装置放入冰水中,会更有利于二氯化砜的生成,其原因是
④下列有关说法错误的是
a.乙、戊装置相同,在实验中的作用也完全相同
b.甲、丁装置为洗气装置,可用于气体的除杂和干燥
c.组装仪器后首先要进行的操作是检查装置的气密性
d.为提高反应物的利用率,可控制甲、丁装置中产生气泡的速率相等
(2)提纯。将收集到的产物进行减压蒸馏,减压蒸馏的目的是
(3)测定。取1.00g蒸馏后液体,小心地完全溶于水,向所得的溶液中加入足量氯化钡溶液,测得生成沉淀的质量为1.60g,则所得蒸馏成分中二氯化砜的质量百分含量为
(4)贮存。二氯化砜应储存于阴凉、干燥、通风良好的库房。但久置后微显黄色,其原因是
更新时间:2016-12-09 15:33:35
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图所示。
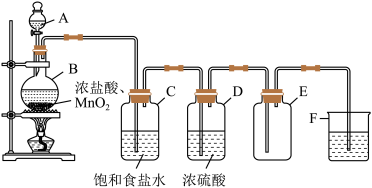
(1)装置中,饱和食盐水的作用是___________ ;浓硫酸的作用是___________ 。
(2)化学实验中常用湿润的KI淀粉试纸检验是否有Cl2产生。如果有Cl2产生,可观察到___________ ,反应的化学方程式为___________ 。
(3)写出下列反应的化学方程式:
①气体发生装置中进行的反应:___________ 。
②NaOH溶液中发生的反应:___________ 。

(1)装置中,饱和食盐水的作用是
(2)化学实验中常用湿润的KI淀粉试纸检验是否有Cl2产生。如果有Cl2产生,可观察到
(3)写出下列反应的化学方程式:
①气体发生装置中进行的反应:
②NaOH溶液中发生的反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某课外小组的同学拟用下图所示的装置从含碘废液(除H2O外,还有I2、I-等)中回收碘。回答下列问题:
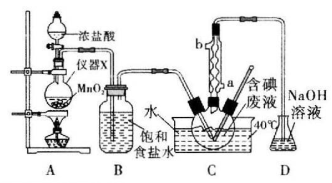
(1)装置A中发生反应的离子方程式为________ 。
(2)仪器X的名称为________ ;装置D的作用是________ 。
(3)装置C中球形冷凝管冷却水从________ (填“a”或“b”)进入,反应控制在较低温度下且保持溶液pH =2进行,其主要原因是________ 。
(4)三口烧瓶中液体经过滤得粗碘,粗碘可经________ (填操作名称)得到纯碘。
(5)为测定某含碘废水中I2的含量,取样l00mL,调节溶液pH后,滴加2滴淀粉溶液,然后用0.02500mol/LNa2S2O3标准溶液滴定,消耗标准液18.15mL。则滴定终点时的现象为________ ,含碘废水中I2的含量=________ mg/mL(结果保留小数点后三位,已知:I2 +2S2O32-=2I-+S4O62-)。

(1)装置A中发生反应的离子方程式为
(2)仪器X的名称为
(3)装置C中球形冷凝管冷却水从
(4)三口烧瓶中液体经过滤得粗碘,粗碘可经
(5)为测定某含碘废水中I2的含量,取样l00mL,调节溶液pH后,滴加2滴淀粉溶液,然后用0.02500mol/LNa2S2O3标准溶液滴定,消耗标准液18.15mL。则滴定终点时的现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】工厂里常用浓氨水检验氯气管道是否漏气,其反应方程式为: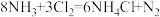 ,回答下列问题:
,回答下列问题:
(1)实验室用二氧化锰为原料制取Cl2,该反应的离子方程式为_____ ,干燥C12常用装有_____ 的洗气瓶。
(2)实验室用下列两种方法制氯气:①用含HCl146g的浓盐酸与足量的MnO2反应;②用87gMnO2与足量浓盐酸反应。所得的氯气_____。
(3)在 中
中
①还原剂是_____ ,还原产物是_____ (都填化学式)。
②氧化剂与还原剂的分子数之比为_____ ,当有4个NH3参加反应时,转移的电子个数为_____ 。
③当生成28gN2时,被氧化的物质为_____ g。
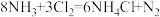 ,回答下列问题:
,回答下列问题:(1)实验室用二氧化锰为原料制取Cl2,该反应的离子方程式为
(2)实验室用下列两种方法制氯气:①用含HCl146g的浓盐酸与足量的MnO2反应;②用87gMnO2与足量浓盐酸反应。所得的氯气_____。
| A.①比②多 | B.②比①多 | C.一样多 | D.无法比较 |
 中
中①还原剂是
②氧化剂与还原剂的分子数之比为
③当生成28gN2时,被氧化的物质为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学计算在化学中占有重要地位,请回答下列问题。
(1)相同质量的SO2和SO3所含氧原子的个数比为___________ 。
(2)质量相同的A、B两种气体,在同温同压下,A的分子数比B多,则A的密度___________ B的密度(填“>”“=”或“<”)。
(3)焦亚硫酸钠(Na2S2O3)是常用食品抗氧化剂,常于葡萄酒、果脯等食品中。果脯中的Na2S2O5的使用量是以游离的SO2来计算的,我国规定每千克果脯中SO2的最高含量是0.35g。
①下列试剂可用于检测SO2的是___________ 。
A.I2 B.HCl C.H2SO4 D.CS2
②某500 g果脯样品经检测得知:含有SO2的物质的量为0.005mol,该产品是否合格?___________ (填“是”或“否”)。
(1)相同质量的SO2和SO3所含氧原子的个数比为
(2)质量相同的A、B两种气体,在同温同压下,A的分子数比B多,则A的密度
(3)焦亚硫酸钠(Na2S2O3)是常用食品抗氧化剂,常于葡萄酒、果脯等食品中。果脯中的Na2S2O5的使用量是以游离的SO2来计算的,我国规定每千克果脯中SO2的最高含量是0.35g。
①下列试剂可用于检测SO2的是
A.I2 B.HCl C.H2SO4 D.CS2
②某500 g果脯样品经检测得知:含有SO2的物质的量为0.005mol,该产品是否合格?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】正确书写下列反应的化学方程式或离子方程式。
(1)将少量的SO2气体通入足量澄清石灰水中的离子方程式:___ 。
(2)将过量的SO2气体通入少量氨水中的离子方程式:___ 。
(3)过量的铁与稀硝酸反应的离子方程式为___ ,该反应中稀硝酸体现___ 性。
(4)碳与浓硝酸反应的化学方程式为___ ,该反应中浓硝酸体现___ 性。
(1)将少量的SO2气体通入足量澄清石灰水中的离子方程式:
(2)将过量的SO2气体通入少量氨水中的离子方程式:
(3)过量的铁与稀硝酸反应的离子方程式为
(4)碳与浓硝酸反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】SO2在生产、生活中具有重要的作用,据所学知识回答相关问题。
(1) SO2通入Na2CO3溶液中有CO2生成,说明H2SO3具有___________ (填“酸性”、“氧化性”、“还原性”或“漂白性”,下同),SO2通入品红溶液中,品红溶液褪色,说明SO2具有___________ 。
(2)已知SO2通入FeCl3溶液会发生反应,该反应的现象为___________ ,请写出该反应的离子方程式___________ 。
(3)向含锌粉的悬浊液中通入SO2可制备ZnS2O4
①该反应的化学方程式为___________ ,若反应中有0.1mol电子转移,则生成ZnS2O4___________ g。
②向反应后的溶液中加入过量盐酸,溶液出现黄色浑浊,且有刺激性气体产生,反应的化学方程式为___________ 。
(1) SO2通入Na2CO3溶液中有CO2生成,说明H2SO3具有
(2)已知SO2通入FeCl3溶液会发生反应,该反应的现象为
(3)向含锌粉的悬浊液中通入SO2可制备ZnS2O4
①该反应的化学方程式为
②向反应后的溶液中加入过量盐酸,溶液出现黄色浑浊,且有刺激性气体产生,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】能源问题是现代社会发展的三大基本问题之一。
(1)焦炭可用于制取水煤气。实验测得1.2 g 碳与水蒸气完全反应生成水煤气时,吸收了13.16 kJ热量。该反应的热化学方程式为_________________________ ;该反应在________ 条件下能自发进行(选“高温”、“低温”或“任意温度”)。
(2)甲醇(CH3OH)广泛用作燃料电池的燃料,工业上可由CO和H2来合成,化学方程式为CO(g)+2H2(g)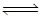 CH3OH(g)。如图是在不同温度下CO的转化率随时间变化的曲线。
CH3OH(g)。如图是在不同温度下CO的转化率随时间变化的曲线。
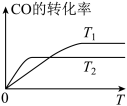
①T1________ T2(填“>”、“<”或“=”)。T1和T2温度下的平衡常数大小关系是K1________ (填“>”、“<”或“=”)K2。
②若容器容积不变,下列措施不能增加CO转化率的是________ (填字母)。
a.降低温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大
③生成甲醇的化学反应速率(v)与时间(t)的关系如图所示。则图中t2时采取的措施可能是___________________ ;
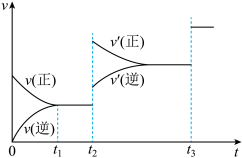
t3时采取的措施可能是_________________ 。
④若在T1℃时,往一密闭容器通入等物质的量CO和H2测得容器内总压强1MPa,40min达平衡时测得容器内总压强为0.6MPa,计算生成甲醇的压强平衡常数KP=________ (MPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)甲醇(CH3OH)燃料电池是以铂为电极,以KOH溶液为电解质溶液,在两极区分别加入CH3OH和O2即可产生电流。负极加入的物质是________ ;正极的电极反应为_______________________ 。
(1)焦炭可用于制取水煤气。实验测得1.2 g 碳与水蒸气完全反应生成水煤气时,吸收了13.16 kJ热量。该反应的热化学方程式为
(2)甲醇(CH3OH)广泛用作燃料电池的燃料,工业上可由CO和H2来合成,化学方程式为CO(g)+2H2(g)
 CH3OH(g)。如图是在不同温度下CO的转化率随时间变化的曲线。
CH3OH(g)。如图是在不同温度下CO的转化率随时间变化的曲线。
①T1
②若容器容积不变,下列措施不能增加CO转化率的是
a.降低温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大
③生成甲醇的化学反应速率(v)与时间(t)的关系如图所示。则图中t2时采取的措施可能是

t3时采取的措施可能是
④若在T1℃时,往一密闭容器通入等物质的量CO和H2测得容器内总压强1MPa,40min达平衡时测得容器内总压强为0.6MPa,计算生成甲醇的压强平衡常数KP=
(3)甲醇(CH3OH)燃料电池是以铂为电极,以KOH溶液为电解质溶液,在两极区分别加入CH3OH和O2即可产生电流。负极加入的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
Ⅰ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
(1)该反应的化学平衡常数表达式为K=________ 。
(2)该反应为________ 反应(填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是________ 。
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为_______ ℃。
Ⅱ.高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g) Fe(s)+CO2(g) △H>0,其平衡常数K=
Fe(s)+CO2(g) △H>0,其平衡常数K=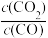 ,已知1100℃时,K=0.263。
,已知1100℃时,K=0.263。
(5)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO体积比值_______ (填“增大”、“减小”或“不变”):平衡常数K值________ (填“增大”、“减小”或“不变”)。
(6)1100℃时测得高炉中,c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下,该反应是否处于化学平衡状态______ (填“是”或“否”),此时v正______ v逆(填“>”或“=”或“<”)。
Ⅰ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(2)该反应为
(3)能判断该反应是否达到化学平衡状态的依据是
| A.容器中压强不变 | B.混合气体中c(CO)不变 |
| C.v正(H2)=v逆(H2O) | D.c(CO2)=c(CO) |
Ⅱ.高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g)
 Fe(s)+CO2(g) △H>0,其平衡常数K=
Fe(s)+CO2(g) △H>0,其平衡常数K=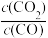 ,已知1100℃时,K=0.263。
,已知1100℃时,K=0.263。(5)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO体积比值
(6)1100℃时测得高炉中,c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下,该反应是否处于化学平衡状态
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】ZnO具有抗菌性,也是重要的轮胎添加剂。工业上由粗ZnO(含FeO、CuO)制备活性ZnO流程如下:

已知此溶液中Fe2+、 Fe3+、 Cu2+、 Zn2+形成氢氧化物的pH如下表
(1)实验室中用98%H2SO4来配制稀硫酸所需使用的玻璃仪器有:胶头滴管、_______ 、_______ 、_______ 。
(2)在A中加H2O2的目的之一是使溶液pH升高,使Fe3+沉淀完全。另外还有一个目的是______________________ ;在A中_______ (填”能”或”不能”)使Fe2+直接沉淀除去;
(3)要使A溶液顺利成为B溶液, 溶液的pH应控制在__________________ ; B中加入Zn,既能降低氢离子浓度又能____________________________ ;
(4)书写碱式碳酸锌焙烧制备活性ZnO的化学方程式__________________________ .

已知此溶液中Fe2+、 Fe3+、 Cu2+、 Zn2+形成氢氧化物的pH如下表
| 离子 | 开始沉沉淀的pH | 完全沉淀的pH |
| Fe2+ | 6.4 | 8.4 |
| Fe3+ | 2.4 | 3.1 |
| Cu2+ | 5.2 | 6.7 |
| Zn2+ | 6.8 | 9 |
(1)实验室中用98%H2SO4来配制稀硫酸所需使用的玻璃仪器有:胶头滴管、
(2)在A中加H2O2的目的之一是使溶液pH升高,使Fe3+沉淀完全。另外还有一个目的是
(3)要使A溶液顺利成为B溶液, 溶液的pH应控制在
(4)书写碱式碳酸锌焙烧制备活性ZnO的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】聚合硫酸铁[Fe2(OH)6-2n(SO4)n]m广泛用于水的净化。以FeSO4·7H2O为原料,经溶解、氧化、水解聚合等步骤,可制备聚合硫酸铁。
(1)将一定量的FeSO4·7H2O溶于稀硫酸,在约70℃下边搅拌边缓慢加入一定量的H2O2溶液,继续反应一段时间,得到红棕色黏稠液体。该过程中反应温度不宜过高,原因是_______ ;H2O2氧化Fe2+的离子方程式为________ 。
(2)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000g,置于250mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10−2mol·L−1K2Cr2O7溶液滴定至终点(滴定过程中 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。
①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将_______ (填“偏大”或“偏小”或“无影响”)。
②计算该样品中铁的质量分数(写出计算过程)_____________ 。
(1)将一定量的FeSO4·7H2O溶于稀硫酸,在约70℃下边搅拌边缓慢加入一定量的H2O2溶液,继续反应一段时间,得到红棕色黏稠液体。该过程中反应温度不宜过高,原因是
(2)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000g,置于250mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10−2mol·L−1K2Cr2O7溶液滴定至终点(滴定过程中
 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将
②计算该样品中铁的质量分数(写出计算过程)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】镁是很活泼的金属,常用作脱硫剂、脱氧剂。在电子工业中用镁制取硅的反应为:2Mg+SiO2 2MgO+Si,同时有副反应发生:2Mg+Si
2MgO+Si,同时有副反应发生:2Mg+Si Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4,SiH4在常温下是一种不稳定、易分解的气体(燃烧热约为1430
Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4,SiH4在常温下是一种不稳定、易分解的气体(燃烧热约为1430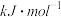 )。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
)。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
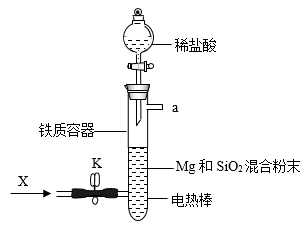
(1)由于O2的存在对该实验有较大影响,实验中应通入X气体作为保护气。X气体应选用①CO2、②N2、③H2中的____________ 。
(2)当接通电源引发反应后,切断电源,反应能继续进行,其原因是____________ 。证明了反应物Mg与SiO2具有的总能量_________ (填“大于”、“小于”或“等于”)生成物MgO和Si具有的总能量。
(3)反应结束时,待冷却至常温后,关闭K,从分液漏斗中加入稀盐酸,可观察到导管口a处有闪亮的火星。据此现象可推知_______ 在空气中能自燃。燃烧的热化学方程式为______ ,当产生等量的热量时,燃烧CH4和SiH4的物质的量之比为_______ (CH4的燃烧热是890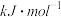 )
)
 2MgO+Si,同时有副反应发生:2Mg+Si
2MgO+Si,同时有副反应发生:2Mg+Si Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4,SiH4在常温下是一种不稳定、易分解的气体(燃烧热约为1430
Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4,SiH4在常温下是一种不稳定、易分解的气体(燃烧热约为1430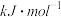 )。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
)。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
(1)由于O2的存在对该实验有较大影响,实验中应通入X气体作为保护气。X气体应选用①CO2、②N2、③H2中的
(2)当接通电源引发反应后,切断电源,反应能继续进行,其原因是
(3)反应结束时,待冷却至常温后,关闭K,从分液漏斗中加入稀盐酸,可观察到导管口a处有闪亮的火星。据此现象可推知
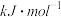 )
)
您最近一年使用:0次

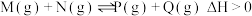 。在某温度下,反应物的起始浓度分别为
。在某温度下,反应物的起始浓度分别为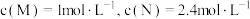 。达到平衡后,
。达到平衡后, 的转化率为
的转化率为 。请回答下列问题:
。请回答下列问题: 的转化率为
的转化率为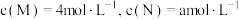 ;达到平衡后,
;达到平衡后,
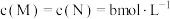 ,达到平衡后,
,达到平衡后,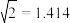 )。
)。


